Durchgreifende Keratoplastik (PKP)
Abstoßungsrate : etwa 4,9–28,9 % 7)
Hauptursache für Versagen : Abstoßung (früh) + Endothelversagen (spät) 3)
Merkmale : enthält Vollschicht-Spendergewebe, daher höchste Antigenität

Die Hornhauttransplantation ist eine der erfolgreichsten Organtransplantationen. Bei einer ersten perforierenden Keratoplastik (PKP) an einem Auge mit niedrigem Risiko erreicht die 5-Jahres-Überlebensrate 95 %. Diese hohe Erfolgsrate wird durch das Immunprivileg der Hornhaut unterstützt.
Die Faktoren, die das Immunprivileg der Hornhaut ausmachen, sind wie folgt:
Bei Hochrisikoaugen mit Hornhautneovaskularisation kann die Versagensrate nach 3 Jahren jedoch über 35 % betragen. Auch unter Immunprivileg ist die häufigste Ursache für Transplantatversagen die irreversible immunologische Abstoßung 1).
„Transplantatabstoßung“ bezeichnet die spezifische Immunantwort des Wirts gegen die Spenderhornhaut. Primäres Transplantatversagen (primary graft failure) ist ein Zustand, bei dem das Transplantat aufgrund eines Defekts des Spendergewebes, eines chirurgischen Traumas oder unsachgemäßer Konservierung innerhalb von 8 Wochen nach der Operation nicht klar wird und nicht immunvermittelt ist 3). Es tritt bei etwa 0,1 % der PKP auf.
Die Diagnose einer Abstoßung wird nur bei Transplantaten gestellt, die nach der Operation mindestens 2 Wochen lang klar geblieben sind. Mehr als die Hälfte der Fälle treten innerhalb des ersten Jahres nach der Operation auf, mit einem Höhepunkt zwischen 6 Monaten und 1 Jahr. Es kann jedoch auch mehr als 20 Jahre nach der Operation auftreten. Die Progressionsrate von Abstoßung zu Versagen wird mit etwa 49 % angegeben.
Die Hornhauttransplantation ist weltweit die am häufigsten durchgeführte Gewebetransplantation. Laut einer internationalen Umfrage aus dem Jahr 2012 machte die PKP etwa 70 % aller Hornhauttransplantationen aus 1). In den letzten Jahren haben sich DSAEK und DMEK bei Endothelerkrankungen schnell verbreitet, und DALK bei Keratokonus und Narben nach Keratitis ist zu einer Standardoption geworden, wodurch sich die Zusammensetzung der Operationsverfahren erheblich verändert hat. Die PKP bleibt jedoch für ausgedehnte Hornhauttrübungen und Anomalien unverzichtbar und birgt das höchste Abstoßungsrisiko 1).
Durchgreifende Keratoplastik (PKP)
Abstoßungsrate : etwa 4,9–28,9 % 7)
Hauptursache für Versagen : Abstoßung (früh) + Endothelversagen (spät) 3)
Merkmale : enthält Vollschicht-Spendergewebe, daher höchste Antigenität
Tiefe lamelläre Keratoplastik (DALK)
Abstoßungsrate : 1–24 % 4)
Vorteil : eliminiert das Risiko einer Endothelabstoßung
Herausforderung : Stromaabstoßung kann auftreten 4)
Hornhautendotheltransplantation (DSAEK)
Abstoßungsrate : Durchschnitt 10 % (Bereich 0–45 %)
Primäre Versagensrate: Durchschnitt 5 % (Spanne 0–29 %)
Merkmale: Einige Berichte zeigen keinen signifikanten Unterschied im Vergleich zur PKP3)
Descemet-Membran-Endothel-Keratoplastik (DMEK)
Abstoßungsrate: Durchschnitt 1,9 % (Spanne 0–5,9 %)7)
Primäre Versagensrate: 1,7 %
Merkmale: Geringste Antigenität, niedrigste Abstoßungsrate3)
In einer großen Kohortenstudie wurde gezeigt, dass DMEK im Vergleich zu PKP und DSAEK ein signifikant geringeres Abstoßungsrisiko aufweist3). Eine Metaanalyse zum Vergleich von UT-DSAEK und DMEK ergab keinen signifikanten Unterschied im Abstoßungsrisiko 12 Monate postoperativ2). In einer niederländischen multizentrischen randomisierten kontrollierten Studie mit 54 Augen war die Rate des Erreichens von 20/25 oder besser 12 Monate postoperativ in der DMEK-Gruppe signifikant höher als in der DSAEK-Gruppe (66 % vs. 33 %, P=0,02), während es keine signifikanten Unterschiede in der Endothelzelldichte oder den refraktiven Veränderungen gab11).
Mehr als die Hälfte der Fälle treten innerhalb des ersten Jahres nach der Operation auf, insbesondere zwischen 6 Monaten und 1 Jahr. Eine Abstoßung kann jedoch auch nach langer Zeit auftreten. Daher sollte bei Symptomen wie Rötung, verschwommenem Sehen oder Sehverschlechterung, selbst Jahre nach der Operation, umgehend ein Arzt aufgesucht werden. Es gibt Berichte über Abstoßungen, die durch eine Impfung mehr als 20 Jahre nach der Operation ausgelöst wurden10).
Die Abstoßungsrate der PKP liegt bei etwa 4,9–28,9 %, während die der DMEK im Durchschnitt 1,9 % (Spanne 0–5,9 %) beträgt, also deutlich niedriger ist. Dieser Unterschied ist hauptsächlich auf die Menge des transplantierten Spendergewebes zurückzuführen. Bei der PKP werden Epithel und Stroma mit dendritischen Zellen transplantiert, was die Antigenität erhöht. Im Gegensatz dazu werden bei der DMEK nur die Descemet-Membran und das Endothel transplantiert, mit geringerer Antigenität und ohne Notwendigkeit von Nähten, was das Risiko verringert. Allerdings tritt auch nach Absetzen von Steroiden bei etwa 6 % der DMEK-Patienten eine Abstoßung auf, was die Bedeutung einer langfristigen Steroidtherapie unterstreicht.
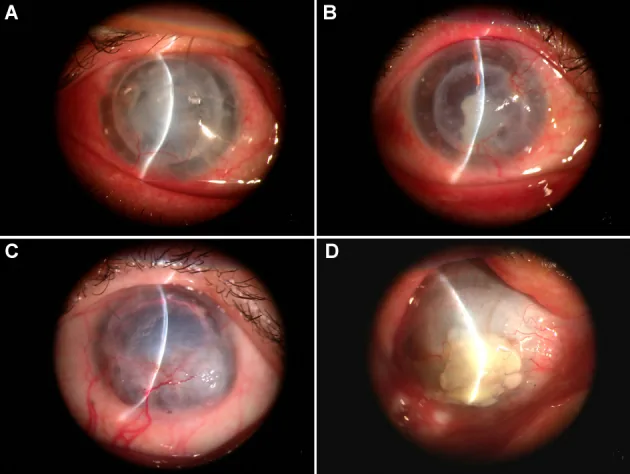
Es treten verschwommenes Sehen, Rötung, Augenschmerzen, Fremdkörpergefühl und verminderte Sehschärfe auf. Die Häufigkeitsgipfel liegen 3 Monate und 1 Jahr nach der Operation. Bei subjektiven Symptomen ist eine sofortige ärztliche Konsultation erforderlich.
Die Diagnosekriterien für eine Abstoßung umfassen Rötung, Photophobie, verminderte Sehschärfe, Zellen in der Vorderkammer, Hornhautpräzipitate (KP), eine endotheliale oder epitheliale Abstoßungslinie, subepitheliale Infiltrate und ein lokalisiertes Transplantatödem1).
Charakteristisch sind auf das Transplantat beschränkte KP; KP auf der Empfängerhornhaut werden nicht beobachtet. Die Khodadoust-Linie ist eine lineare Anordnung von Hornhautpräzipitaten, die die fortschreitende Front der endothelialen Abstoßung darstellt.
Die Abstoßung wird je nach betroffener Schicht in drei Typen eingeteilt: epithelial, stromal und endothelial. Der endotheliale Typ hat den stärksten Einfluss auf die Transplantatprognose; eine Verzögerung der Behandlung führt zu irreversibler endothelialer Insuffizienz und Sehverlust.
| Abstoßungstyp | Häufigkeit | Hauptbefunde |
|---|---|---|
| Epithelial | Etwa 2 % | Vom Limbus ausgehende lineare Erhebung (epithelial rejection line) |
| Stromal | — | Stromaödem als einziger Befund |
| Endothelial | Etwa 50 % | KP · Khodadoust-Linie · Ödem |
Epitheliale Abstoßung (epithelial rejection) ist mit etwa 2 % aller Abstoßungen selten. Als Vorläuferläsion werden 0,2–0,5 mm große runde subepitheliale Infiltrate direkt unter der Bowman-Membran beobachtet. Im Fortschreiten bilden sie eine ödematös erhabene lineare Läsion (epithelial rejection line). Sie beeinträchtigt die klare Heilung des Transplantats kaum, kann aber eine endotheliale Abstoßung auslösen.
Stromale Abstoßung (stromal rejection) zeigt als einzigen Befund ein Stromaödem. Bei DALK kann eine stromale Immunabstoßung als stromales Infiltrat oder Grenzflächenvaskularisation auftreten 4). Die Unterscheidung von einem Hornhautödem durch endotheliale Abstoßung bei PKP-Augen ist schwierig.
Endotheliale Abstoßung (endothelial rejection) macht etwa 50 % aller Abstoßungen aus und ist klinisch am bedeutendsten. Wichtiger Befund sind auf das Transplantat beschränkte retrokorneale Präzipitate (KP); bei Bildung einer Khodadoust-Linie tritt an dieser Stelle ein Stromaödem auf. Mischformen (epithelial + endothelial etc.) werden in etwa 30 % der Fälle beobachtet.
Die Khodadoust-Linie ist ein lineares retrokorneales Präzipitat, das für die endotheliale Abstoßung charakteristisch ist. Sie stellt die fortschreitende Front der Abstoßung dar, die sich allmählich über das Transplantatendothel bewegt; in den von der Linie durchzogenen Bereichen werden Endothelzellen geschädigt, was zu einem Stromaödem führt. Wird eine Khodadoust-Linie festgestellt, muss sofort eine intensive Steroidtherapie eingeleitet werden.
| Befund | Abstoßung | HSV/VZV-Endothelitis | CMV-Endothelitis |
|---|---|---|---|
| Verteilung der KP | Auf das Transplantat beschränkt | Auch außerhalb des Transplantats | Auch außerhalb des Transplantats |
| Farbe der KP | Weiß bis grauweiß | Braun | Braun bis weiß |
| Charakteristische Befunde | Khodadoust-Linie | Arlt-Dreieck | Coin-Läsion |
Die Abstoßungsreaktion ist am stärksten durch auf das Transplantat beschränkte KP gekennzeichnet, während die virale Endothelitis sich dadurch unterscheidet, dass KP auch außerhalb des Transplantats gefunden werden. Beachten Sie, dass Ablagerungen auf der hinteren Hornhautfläche manchmal bei der Hornhauttransplantation vom Spender stammen können, daher ist es für die Differenzialdiagnose nützlich, die Verteilung der KP bei der täglichen Untersuchung zu dokumentieren.
Fälle mit erhöhtem Abstoßungsrisiko bei PKP werden als Hochrisiko-Augen bezeichnet, und die folgenden Faktoren werden genannt.
Bei DMEK kann eine Abstoßung während der Steroidreduktion ausgelöst werden. In einem Fall trat 15 Monate nach DMEK bei Umstellung von Betamethason auf Fluorometholon eine Abstoßung auf7). Periphere anteriore Synechien (PAS) wurden ebenfalls als Risikofaktor für DMEK-Abstoßung berichtet7).
Bei Organtransplantationen ist der Nutzen des HLA-Matchings klar, bei Hornhauttransplantationen sind die Ergebnisse jedoch uneinheitlich1). Die im Vereinigten Königreich durchgeführte Corneal Transplant Follow-up Study II (CTFS II) ist eine große prospektive klinische Studie, die die Auswirkung des HLA-Klasse-II-Matchings (HLA-DR) bei Hochrisiko-PKP untersuchte1). Von 1998 bis 2011 wurden 1133 Transplantationen gesammelt und unter der Bedingung von ≤2 HLA-Klasse-I-Mismatches in Gruppen mit 0, 1 oder 2 HLA-DR-Mismatches stratifiziert1). Die Gewebetypisierung von Spender und Empfänger erfolgte mittels DNA-basierter Methoden (PCR-SSP/PCR-SSO), um Fehler serologischer Verfahren zu vermeiden1).
In der CTFS II wurde kein klarer Zusammenhang zwischen der Anzahl der HLA-DR-Mismatches und der Inzidenz von Abstoßungen festgestellt1). Wie in Nagetiermodellen gezeigt, sind mehrere unterschiedliche Immunwege an der Abstoßung von Hornhauttransplantaten beteiligt, und diese Redundanz der Immunantwort wird als eine Ursache für die uneinheitlichen Ergebnisse der HLA-Matching-Studien angesehen1).
Es wurden mehrere Fälle von Hornhauttransplantat-Abstoßung nach COVID-19-Impfung berichtet. Dies wurde sowohl bei mRNA-Impfstoffen (BNT162b2), Vektorimpfstoffen (ChAdOx1) als auch bei Totimpfstoffen (Sinopharm) beobachtet.
Zwei Fälle einer akuten PKP-Abstoßung 2 Wochen nach der ersten Dosis des BNT162b2-Impfstoffs wurden berichtet6). Beide hatten keine vorherige Abstoßungsanamnese und sprachen gut auf lokale und systemische Steroide an6).
Es gibt auch einen Fall einer endothelialen Abstoßung nach Femtosekundenlaser-Hornhauttransplantation 2 Wochen nach der ChAdOx1-Impfung8). Eine Khodadoust-Linie und eine Entzündung der Vorderkammer wurden festgestellt, und der Patient erholte sich nach 5 Wochen Steroidbehandlung8).
Zwei Fälle von Abstoßung nach dem Sinopharm-Totimpfstoff wurden ebenfalls berichtet9). Eine Literaturübersicht ergab mindestens 20 Fälle von impfstoffbedingter Abstoßung, von denen die meisten auf eine Steroidbehandlung ansprachen9).
Es gibt einen Fall einer Abstoßung 10 Tage nach der BNT162b2-Impfung bei einem PKP, das mehr als 20 Jahre zurücklag10).
Obwohl ein Kausalzusammenhang nicht bestätigt ist, wurde die Hypothese aufgestellt, dass die Impfung über die Induktion von MHC-Klasse-II-Antigen-präsentierenden Zellen eine Abstoßungsreaktion auslösen könnte9).
Hornhauttransplantat-Abstoßungen nach COVID-19-Impfung wurden sowohl bei mRNA-, Vektor- als auch Totimpfstoffen berichtet. Sie treten meist 1–3 Wochen nach der Impfung auf und sprechen in der Regel auf eine Steroidbehandlung an. Metaanalysen haben bei soliden Organtransplantationen keine erhöhte Abstoßungsrate durch Impfung gezeigt, aber für Hornhauttransplantationen sammeln sich Fallberichte. Da der Kausalzusammenhang nicht gesichert ist, wird Hornhauttransplantat-Patienten empfohlen, die Steroiddosis vor der Impfung zu erhöhen und nach der Impfung frühzeitig einen Arzt aufzusuchen.
Es werden transplantatbegrenzte KP, eine Khodadoust-Linie, Hornhautödem und Vorderkammerzellen festgestellt. Die epitheliale Abstoßungslinie beginnt in der Nähe der hyperämischen Limbusgefäße und wandert über die Transplantatgrenze.
Die wichtigsten Erkrankungen, die von einer endothelialen Abstoßung abgegrenzt werden müssen, sind:
Bei der Abstoßung ist das Hauptmerkmal, dass die KP auf das Transplantat beschränkt sind, und ein Augeninnendruckanstieg ist selten. Bei der HSV/VZV-Endothelitis haften die KP auch außerhalb des Transplantats und gehen mit einem akuten Augeninnendruckanstieg einher. Bei der CMV-Endothelitis sind münzenförmige KP und ein chronisch persistierender Augeninnendruckanstieg charakteristisch. Bei schwieriger definitiver Diagnose werden Kammerwasser-PCR, Serum-Antikörpertests und das Ansprechen auf die Steroidtherapie insgesamt beurteilt.
Die Behandlung der Abstoßungsreaktion basiert auf der entzündungshemmenden Wirkung von Steroiden.
Leicht (epithelialer/parenchymatöser Typ)
Schwer (endothelialer Typ, Khodadoust-Linie positiv)
Eine akute Abstoßung kann bei frühzeitiger Behandlung in über 50% der Fälle rückgängig gemacht werden, während eine verzögerte Behandlung zu irreversiblem Endothelzellverlust und Transplantatversagen führt. Zur Patientenschulung ist es wichtig, die postoperativen subjektiven Symptome (Rötung, verschwommenes Sehen, Augenschmerzen, Photophobie) zu vermitteln und bei Auffälligkeiten eine frühzeitige Konsultation sicherzustellen.
Die Prävention von Abstoßungsreaktionen nach Hornhauttransplantation erfolgt nach einem zweistufigen Protokoll basierend auf der Risikostratifizierung.
Postoperatives Management bei Augen mit normalem Risiko
Steroid-Augentropfen: Rinderon Augentropfen 0,01 % (Betamethason) 5-mal täglich → Umstellung auf Flumetholon Augentropfen 0,1 % (Fluorometholon) 2- bis 3-mal täglich (Ausschleichen über 6 Monate)
Systemische Gabe: Prednison 20 mg für einige Tage oder keine Gabe
CsA: Kombinierte Augentropfen, Fortsetzung über mehrere Monate
Postoperatives Management bei Hochrisiko-Augen
Steroid-Augentropfen: Betamethason 0,1 % × 4-mal/Tag → Fortsetzung über mehr als 1 Jahr
Systemische Steroide: Rinderon Injektion 0,4 % 2 mg einmal täglich intravenöse Infusion ab OP-Tag für 3 Tage, dann Rinderon Tabletten 0,5 mg 2 Tabletten in geteilter Dosis 1, ausschleichend über 2 Wochen
CsA: Neoral Kapseln 25 mg 3 mg/kg/Tag, Talspiegel 70–100 ng/mL
Cyclosporin A (CsA) wird bei Hochrisikofällen wie Hornhautstroma-Gefäßeinsprossung in ≥2 Quadranten, Wiederholungstransplantationen oder Abstoßungsanamnese eingesetzt. Bei systemischer Gabe den Talspiegel bei 70–100 ng/mL halten und systemische Nebenwirkungen einschließlich Nierenfunktion überwachen. Etwa sechs Monate postoperativ fortsetzen.
Bei einem 18-jährigen PKP-Patienten mit bilateraler simultaner Abstoßung wurde nach Remission durch IV-Methylprednisolon-Puls aufgrund einer Steroidreaktion erfolgreich auf CsA 1 % Augentropfen zur Erhaltung umgestellt5). CsA 1 % Augentropfen ermöglichen bei Steroid-Respondern eine frühe Reduktion potenter Steroide und sind für die langfristige Transplantaterhaltung nützlich5).
Tacrolimus wird als Umstellungsmedikament bei Patienten eingesetzt, die unter oralem Cyclosporin eine Abstoßung entwickeln. Der Talspiegel wird bis 2 Monate postoperativ bei 8–10 ng/mL, danach bei 5–6 ng/mL angestrebt (Prograf 0,05–0,1 mg/kg/Tag). Es gibt Berichte, dass Tacrolimus 0,03 % Augentropfen zur Abstoßungsprophylaxe bei Hochrisiko-Hornhauttransplantationen wirksam sind.
Lockerung oder Bruch von Fäden können sowohl Abstoßung als auch Spätinfektion auslösen. Daher Fäden sofort nach Entdeckung entfernen. Nach Fadenentfernung die Steroid- und Antibiotika-Augentropfenbehandlung vorübergehend verstärken. Auch nach Remission kann die langfristige Fortsetzung von Steroid-Augentropfen helfen, Rezidive zu verhindern3).
Bei Beginn mit Betamethason 0,1 % zunächst eine Erhaltungsphase mit 4-mal täglich über mehrere Monate bis ein Jahr fortsetzen, dann auf ein niedrig konzentriertes Steroid wie Fluorometholon 0,1 % 1- bis 2-mal täglich zur Langzeiterhaltung umstellen. Bei Augeninnendruckerhöhung Umstellung auf Loteprednol oder Hinzunahme von Glaukom-Augentropfen erwägen.
Bei einem Anstieg des Augeninnendrucks aufgrund einer Steroidresponse kann ein Wechsel von Prednisolonacetat zu Loteprednol, das weniger Einfluss auf den Augeninnendruck hat, oder eine Kombination mit CsA 1 % Augentropfen in Betracht gezogen werden. CsA 1 % Augentropfen ermöglichen eine frühzeitige Reduktion der Steroide, was sowohl für die Druckkontrolle als auch für die Unterdrückung der Abstoßung nützlich ist. Bei Bedarf können auch Glaukom-Augentropfen hinzugefügt werden.
Die Hornhaut bewahrt durch die Anterior Chamber-Associated Immune Deviation (ACAID) eine physiologische Immuntoleranz. In der ACAID werden Antigen-präsentierende Zellen in einer TGF-β-dominanten Umgebung tolerogen, wodurch die verzögerte Überempfindlichkeitsreaktion gegen Spenderantigene und die Produktion komplementbindender Antikörper unterdrückt werden. Bei Vorliegen von Risikofaktoren wie Neovaskularisation, Entzündung oder Fadenlockerung kann dieses Immunprivileg jedoch leicht zusammenbrechen.
Der zentrale Mechanismus der Abstoßung ist die verzögerte Überempfindlichkeitsreaktion, deren Haupteffektorzellen CD4+ Th1-Zellen sind. Aktivierte Th1-Zellen produzieren IFN-γ, das in der gesamten Dicke des transplantierten Hornhauttransplantats MHC-Klasse-II-Antigen-präsentierende Zellen induziert und so die zelluläre Immunantwort vorantreibt8). Auch die Beteiligung antikörpervermittelter Mechanismen wurde in letzter Zeit beachtet, wobei vorgeschlagen wird, dass Anti-HLA-Antikörper über Komplementaktivierung chronische Endothelzellschäden verursachen könnten1).
Die Unterschiede in den Abstoßungsraten zwischen den Operationsverfahren beruhen hauptsächlich auf der Menge des transplantierten Spendergewebes und der unterschiedlichen Antigenität3).
Periphere anteriore Synechien (PAS) werden als Risikofaktor für Abstoßung nach DMEK betrachtet. In einem Maus-Hornhauttransplantationsmodell zeigte die Gruppe mit PAS eine signifikant erhöhte Abstoßung7). Es wird angenommen, dass der direkte Kontakt zwischen Iris und Spenderendothel durch PAS die zytotoxische T-Lymphozytenaktivität induziert und die Abstoßung fördert7).
Die Abstoßung von Hornhauttransplantaten wird hauptsächlich durch die zelluläre Immunität vermittelt, aber Nagetierstudien haben mehrere unterschiedliche Immunwege identifiziert, die zur Abstoßung führen1). Es wird angenommen, dass diese Redundanz der Immunantwort ein Grund für inkonsistente Ergebnisse in HLA-Matching-Studien ist1). In den letzten Jahren wurde auch die Rolle von Anti-HLA-Antikörpern und der antikörpervermittelten Abstoßung beachtet, was zur Aufklärung des Mechanismus des späten Endothelversagens beitragen könnte1).
Die COVID-19-Impfung löst eine systemische Immunantwort aus, die neben SARS-CoV-2-neutralisierenden Antikörpern auch antigenspezifische CD8+- und Th1-CD4+-T-Zell-Antworten induziert6). Diese Immunaktivierung kann über Kreuzreaktion oder unspezifische Immunaktivierung gegen das transplantierte Hornhautgewebe eine Abstoßung auslösen6). Beim inaktivierten Impfstoff (Sinopharm) wurde vermutet, dass die Immunogenität des Adjuvans Aluminiumhydroxid die Hauptursache für die Abstoßung sein könnte9). Auf Metaanalyse-Ebene wurde jedoch kein Anstieg der Abstoßung nach COVID-19-Impfung bei soliden Organtransplantationen bestätigt, und auch bei Hornhauttransplantationen ist der kausale Zusammenhang derzeit nicht gesichert.
Weltweit häufen sich Fallberichte über COVID-19-Impfstoff-assoziierte Abstoßungsreaktionen von Hornhauttransplantaten 9). Eine Literaturübersicht hat über 20 Fälle zusammengestellt, wobei die Mehrzahl Retransplantationen betrifft, die 1–2 Wochen nach der Impfung auftreten und unter Steroidtherapie meist ausheilen 9). Eine prophylaktische Steroidgabe vor der Impfung wurde vorgeschlagen, jedoch gibt es keine randomisierten kontrollierten Studien, und die Entscheidung muss individuell pro Fall getroffen werden 8)9).
Zur Wirksamkeit des HLA-Matchings wurde die CTFS-II-Studie prospektiv durchgeführt, aber derzeit konnte kein eindeutiger klinischer Nutzen des HLA-DR-Matchings bei Hornhauttransplantationen nachgewiesen werden 1). Allerdings wird die Rolle von Anti-HLA-Antikörpern und der antikörpervermittelten Abstoßung zunehmend klarer, was zur Aufklärung des Mechanismus des späten Endothelversagens beitragen könnte 1).
Beim Vergleich von UT-DSAEK und DMEK zeigten sowohl die Metaanalyse von Sela 2023 2) als auch die multizentrische RCT von Dunker 2020 11) keinen signifikanten Unterschied in der 12-Monats-Abstoßungsrate, während die DMEK-Gruppe eine bessere korrigierte Sehschärfe erzielte. Allerdings war das Transplantatversagen in der DMEK-Gruppe tendenziell etwas häufiger 2), und die Wahl des Verfahrens sollte auf der Grundlage der individuellen Augenerkrankungen, der Vorgeschichte und der Erfahrung der Einrichtung getroffen werden.
Folgende zukünftige Richtungen sind von Interesse.