Queratoplastia Penetrante (PKP)
Tasa de rechazo: Aproximadamente 4.9–28.9% 7)
Causa principal de fracaso: Rechazo (temprano) + fallo endotelial (tardío) 3)
Características: Mayor antigenicidad debido a la inclusión de tejido donante de espesor total

El trasplante de córnea es uno de los trasplantes de órganos más exitosos. Para la queratoplastia penetrante (PKP) primaria en ojos de bajo riesgo, la tasa de supervivencia a 5 años alcanza el 95%. Esta alta tasa de éxito se sustenta en el privilegio inmunológico de la córnea.
Los factores que constituyen el privilegio inmunológico corneal son los siguientes:
Sin embargo, en ojos de alto riesgo con neovascularización corneal, la tasa de fracaso a los 3 años puede superar el 35%. Incluso bajo privilegio inmunológico, la causa más común de fracaso del injerto es el rechazo inmunológico irreversible 1).
El “rechazo del injerto” se refiere a la respuesta inmune específica del huésped contra la córnea donante. El fracaso primario del injerto (primary graft failure) es una condición en la que el injerto no se aclara dentro de las 8 semanas posteriores a la cirugía debido a defectos en el tejido donante, trauma quirúrgico o conservación inadecuada, y no es inmunomediado 3). Ocurre en aproximadamente el 0.1% de las PKP.
El diagnóstico de rechazo se realiza solo para injertos que han mantenido la transparencia durante al menos 2 semanas después de la cirugía. Más de la mitad de los casos se concentran dentro del primer año postoperatorio, con un pico entre los 6 meses y el año. Sin embargo, también puede ocurrir más de 20 años después de la cirugía. La tasa de progresión de rechazo a fracaso se reporta en aproximadamente el 49%.
El trasplante de córnea es el trasplante de tejido más frecuente a nivel mundial. Según una encuesta internacional de 2012, la PKP representaba aproximadamente el 70% de todos los trasplantes de córnea 1). En los últimos años, la DSAEK y la DMEK para enfermedades endoteliales se han extendido rápidamente, y la DALK para queratocono y cicatrices postqueratitis se ha convertido en una opción estándar, cambiando significativamente la composición de los procedimientos quirúrgicos. Sin embargo, la PKP sigue siendo esencial para opacidades corneales extensas y deformidades, y conlleva el mayor riesgo de rechazo 1).
Queratoplastia Penetrante (PKP)
Tasa de rechazo: Aproximadamente 4.9–28.9% 7)
Causa principal de fracaso: Rechazo (temprano) + fallo endotelial (tardío) 3)
Características: Mayor antigenicidad debido a la inclusión de tejido donante de espesor total
Queratoplastia Lamelar Anterior Profunda (DALK)
Tasa de rechazo: 1–24% 4)
Ventaja: Elimina el riesgo de rechazo endotelial
Desafío: Puede ocurrir rechazo estromal 4)
Queratoplastia Endotelial con Descemetorhexis Automatizada (DSAEK)
Tasa de rechazo: Promedio 10% (rango 0–45%)
Tasa de fallo primario: Promedio 5% (rango 0–29%)
Características: Algunos informes indican que no hay diferencia significativa en comparación con PKP3)
Queratoplastia endotelial de la membrana de Descemet (DMEK)
Tasa de rechazo: Promedio 1.9% (rango 0–5.9%)7)
Tasa de fallo primario: 1.7%
Características: Menor antigenicidad y baja tasa de rechazo3)
Estudios de cohortes grandes han demostrado que DMEK tiene un riesgo de rechazo significativamente menor en comparación con PKP y DSAEK3). Un metanálisis que comparó UT-DSAEK y DMEK no encontró diferencias significativas en el riesgo de rechazo a los 12 meses postoperatorios2). En un ensayo controlado aleatorizado multicéntrico holandés de 54 ojos, el grupo DMEK tuvo una tasa significativamente mayor de alcanzar 20/25 o mejor visión a los 12 meses en comparación con el grupo DSAEK (66% vs 33%, P=0.02), mientras que no hubo diferencias significativas en la densidad de células endoteliales o cambios refractivos11).
Más de la mitad de los casos ocurren dentro del primer año después de la cirugía, especialmente entre los 6 meses y el año. Sin embargo, el rechazo también puede ocurrir mucho después de la cirugía, por lo que si aparecen síntomas como enrojecimiento, visión borrosa o disminución de la visión incluso años después, se necesita atención médica inmediata. Se han reportado casos de rechazo desencadenado por vacunación más de 20 años después de la cirugía10).
La tasa de rechazo para PKP es aproximadamente del 4.9–28.9%, mientras que para DMEK es significativamente menor, con un promedio del 1.9% (rango 0–5.9%). Esta diferencia se debe principalmente a la cantidad de tejido donante trasplantado. PKP trasplanta epitelio y estroma que contienen células dendríticas, lo que resulta en una mayor antigenicidad. En contraste, DMEK trasplanta solo la membrana de Descemet y el endotelio, que tiene menor antigenicidad y no requiere suturas, reduciendo el riesgo. Sin embargo, informes indican que aproximadamente el 6% de los casos de DMEK experimentan rechazo después de la suspensión de los esteroides, lo que destaca la importancia del uso prolongado de esteroides.
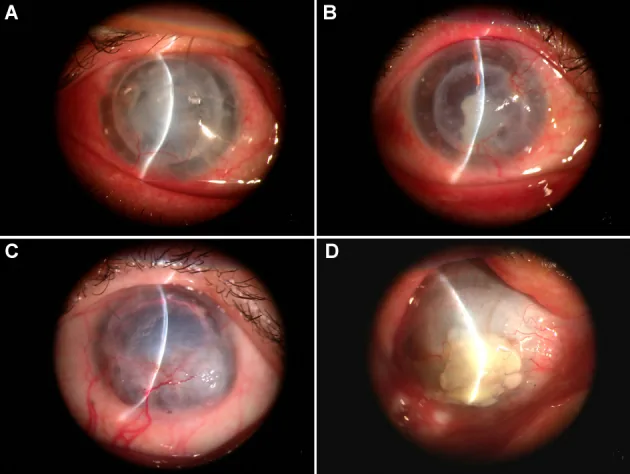
Los pacientes presentan visión borrosa, hiperemia conjuntival, dolor ocular, sensación de cuerpo extraño y disminución de la agudeza visual. Hay picos de inicio a los 3 meses y 1 año después de la cirugía. Si aparecen síntomas subjetivos, es necesaria atención médica inmediata.
Los criterios diagnósticos de rechazo incluyen cualquiera de los siguientes: hiperemia conjuntival, fotofobia, disminución de la agudeza visual, células en cámara anterior, precipitados queráticos (KP), líneas de rechazo endotelial o epitelial, infiltrados subepiteliales y edema localizado del injerto1).
Los KP localizados en el injerto son característicos, y no se observan KP en la córnea receptora. La línea de Khodadoust es un depósito lineal en el endotelio corneal y representa el frente de avance del rechazo endotelial.
El rechazo se clasifica en tres tipos según la capa afectada: epitelial, estromal y endotelial. El rechazo endotelial tiene el mayor impacto en el pronóstico del injerto, y el retraso en el tratamiento conduce a una falla endotelial irreversible y pérdida de visión.
| Tipo de rechazo | Frecuencia | Hallazgos principales |
|---|---|---|
| Epitelial | Aproximadamente 2% | Cresta lineal que migra desde el limbo (línea de rechazo epitelial) |
| Estromal | — | El edema estromal es el único hallazgo |
| Tipo endotelial | Aproximadamente 50% | KP, línea de Khodadoust, edema |
Rechazo epitelial (epithelial rejection) tiene una frecuencia baja de aproximadamente el 2% de todos los rechazos. Como lesión precursora, se observan infiltrados subepiteliales redondos de 0.2–0.5 mm justo debajo de la membrana de Bowman. Al progresar, forma una lesión lineal edematosa elevada (línea de rechazo epitelial). Apenas afecta la cicatrización transparente del injerto, pero puede desencadenar rechazo endotelial.
Rechazo estromal (stromal rejection) tiene como único hallazgo el edema estromal. En DALK, el rechazo inmune estromal puede presentarse como infiltración estromal y neovascularización de la interfaz 4). Es difícil de diferenciar del edema corneal por rechazo endotelial en ojos con PKP.
Rechazo endotelial (endothelial rejection) representa aproximadamente el 50% de todos los rechazos y es clínicamente el más importante. Los depósitos endoteliales corneales localizados dentro del injerto son un hallazgo clave, y cuando se forma una línea de Khodadoust, se acompaña de edema estromal en el mismo sitio. El tipo mixto (epitelial + endotelial, etc.) se observa en aproximadamente el 30%.
La línea de Khodadoust es un depósito endotelial corneal lineal característico del rechazo endotelial. Representa el frente de avance del rechazo que se mueve progresivamente a través del endotelio del injerto; en el área donde la línea ha pasado, las células endoteliales se dañan, causando edema estromal. Si se observa la línea de Khodadoust, es necesario iniciar un tratamiento intensivo con esteroides de inmediato.
| Hallazgo | Rechazo | Endotelitis por HSV/VZV | Endotelitis por CMV |
|---|---|---|---|
| Distribución de KP | Localizado dentro del injerto | También adherido fuera del injerto | También adherido fuera del injerto |
| Color de los KP | Blanco a blanco grisáceo | Marrón | Marrón a blanco |
| Hallazgos característicos | Línea de Khodadoust | Triángulo de Arlt | Lesión en moneda |
El rechazo se caracteriza por KP localizados en el injerto, mientras que la endotelitis viral se diferencia por la presencia de KP también fuera del injerto. Dado que los depósitos endoteliales corneales pueden ser de origen donante en el momento del trasplante de córnea, registrar la distribución de los KP durante los exámenes diarios es útil para el diagnóstico diferencial.
Los casos en los que la PKP es propensa al rechazo se denominan ojos de alto riesgo e incluyen los siguientes factores.
En DMEK, el rechazo puede desencadenarse durante la reducción de esteroides. En un caso, el rechazo ocurrió 15 meses después de DMEK al cambiar de betametasona a fluorometolona7). Las sinequias anteriores periféricas (PAS) también se han reportado como factor de riesgo para el rechazo en DMEK7).
Si bien el beneficio de la compatibilidad HLA es claro en el trasplante de órganos, los resultados son inconsistentes en el trasplante de córnea1). El Corneal Transplant Follow-up Study II (CTFS II) realizado en el Reino Unido fue un gran ensayo clínico prospectivo que examinó el impacto de la compatibilidad HLA clase II (HLA-DR) en PKP de alto riesgo1). Desde 1998 hasta 2011, se recolectaron 1133 trasplantes y se estratificaron en grupos de 0, 1 o 2 incompatibilidades HLA-DR bajo la condición de ≤2 incompatibilidades HLA clase I1). Se utilizaron métodos basados en ADN (PCR-SSP/PCR-SSO) para la tipificación tisular de donante y receptor para evitar errores de las técnicas serológicas1).
En CTFS II, no se encontró una relación clara entre el número de incompatibilidades HLA-DR y la incidencia de rechazo1). Como se ha demostrado en modelos de roedores, el rechazo del injerto corneal implica múltiples vías inmunitarias distintas, y esta redundancia de la respuesta inmunitaria se considera una de las razones que explican los resultados inconsistentes de los estudios de compatibilidad HLA1).
Se han reportado múltiples casos de rechazo de trasplante de córnea después de la vacunación contra la COVID-19. Puede ocurrir con vacunas de ARNm (BNT162b2), de vector viral (ChAdOx1) e inactivadas (Sinopharm).
Se reportaron dos casos de rechazo agudo de PKP 2 semanas después de la primera dosis de la vacuna BNT162b26). Ninguno tenía antecedentes de rechazo previo y ambos respondieron bien a los esteroides tópicos y sistémicos6).
También hay un caso de rechazo endotelial después de un trasplante de córnea con láser de femtosegundo que ocurrió 2 semanas después de la vacunación con ChAdOx18). Se observaron línea de Khodadoust e inflamación de la cámara anterior, y se recuperó después de 5 semanas de tratamiento con esteroides8).
También se reportaron dos casos de rechazo después de la vacuna inactivada Sinopharm9). Una revisión de la literatura ha acumulado al menos 20 casos de rechazo relacionado con la vacuna, y la mayoría se recuperó con tratamiento con esteroides9).
Hay un caso de rechazo que ocurrió 10 días después de la vacunación con BNT162b2 en un PKP que había estado estable durante más de 20 años después de la cirugía10).
Aunque la causalidad no está establecida, se ha propuesto la hipótesis de que la vacunación puede desencadenar el rechazo mediante la inducción de células presentadoras de antígenos MHC clase II9).
Se ha informado rechazo del trasplante de córnea después de la vacunación contra la COVID-19 con vacunas de ARNm, vector e inactivadas. A menudo ocurre de 1 a 3 semanas después de la vacunación, y la mayoría de los casos responden al tratamiento con esteroides. Los metanálisis han descartado el rechazo inducido por la vacuna en trasplantes de órganos sólidos, pero la acumulación de casos continúa para los trasplantes de córnea. Dado que la causalidad no está establecida, se recomienda que los pacientes con trasplante de córnea aumenten el uso de esteroides antes de la vacunación y busquen atención médica temprana después de la vacunación.
Verifique KP localizado en el injerto, línea de Khodadoust, edema corneal y células en la cámara anterior. Las líneas de rechazo epitelial comienzan cerca de los vasos limbares congestionados y se mueven a través del borde del injerto.
Las principales condiciones que requieren diferenciación del rechazo endotelial son las siguientes.
En el rechazo, los KP se limitan al injerto y la elevación de la presión intraocular es rara. En la endoteliitis por HSV/VZV, los KP también se adhieren fuera del injerto y se acompañan de elevación aguda de la presión intraocular. En la endoteliitis por CMV, son característicos los KP en forma de lesión de moneda y la elevación crónica persistente de la presión intraocular. Si la confirmación es difícil, se evalúan de manera integral la PCR de humor acuoso, las pruebas de anticuerpos séricos y la respuesta al tratamiento con esteroides.
El tratamiento básico del rechazo es la antiinflamación con esteroides.
Leve (tipo epitelial/estromal)
Grave (tipo endotelial, línea de Khodadoust positiva)
Con el tratamiento temprano, más del 50% de los episodios de rechazo agudo se recuperan; sin embargo, el tratamiento tardío puede provocar una pérdida irreversible de células endoteliales y fracaso del injerto. La educación del paciente es importante: los pacientes deben conocer los síntomas posoperatorios (enrojecimiento, visión borrosa, dolor ocular, fotofobia) y buscar atención médica temprana si ocurre algún cambio.
Para la prevención del rechazo después del trasplante de córnea, se utiliza un protocolo de dos pasos basado en la estratificación del riesgo.
Manejo posoperatorio para ojos de riesgo normal
Gotas de esteroides: Gotas oftálmicas de Rinderon 0.01% (betametasona) 5 veces al día → cambiar a gotas oftálmicas de Flumetholon 0.1% (fluorometolona) 2-3 veces al día (reducir gradualmente en 6 meses)
Administración sistémica: Prednisona 20 mg durante unos días, o ninguna administración
CsA: Gotas oftálmicas combinadas, continuar durante varios meses
Manejo postoperatorio de ojos de alto riesgo
Gotas de esteroides: Betametasona 0.1% × 4 veces/día → continuar durante 1 año o más
Esteroides sistémicos: Inyección de Rinderon 0.4% 2 mg una vez al día por vía intravenosa durante 3 días desde el día de la cirugía, luego comprimidos de Rinderon 0.5 mg 2 comprimidos divididos en 1, reducir gradualmente en 2 semanas
CsA: Cápsulas de Neoral 25 mg 3 mg/kg/día, nivel valle 70-100 ng/mL
Ciclosporina A (CsA) se utiliza en casos de alto riesgo como invasión vascular del estroma corneal en 2 o más cuadrantes, retrasplantes y antecedentes de rechazo. Durante la administración sistémica, mantener el nivel valle entre 70-100 ng/mL y monitorizar los efectos secundarios sistémicos, incluida la función renal. Continuar durante aproximadamente 6 meses después de la cirugía.
En un caso de PKP de 18 años con rechazo bilateral simultáneo, después de la remisión con pulsos de metilprednisolona IV, debido a la respuesta a esteroides, se cambió a gotas de CsA al 1% y se mantuvo con éxito5). Las gotas de CsA al 1% permiten la reducción temprana de esteroides potentes en respondedores a esteroides y son útiles para el mantenimiento del injerto a largo plazo5).
Tacrolimus se utiliza como fármaco de cambio en casos que desarrollan rechazo mientras toman ciclosporina oral. El nivel valle objetivo es de 8-10 ng/mL hasta 2 meses después de la cirugía, luego 5-6 ng/mL (Prograf 0.05-0.1 mg/kg/día). Existen informes de que las gotas de tacrolimus al 0.03% son efectivas para prevenir el rechazo en trasplantes de córnea de alto riesgo.
Las suturas flojas o rotas pueden desencadenar tanto rechazo como infección tardía, por lo que deben retirarse inmediatamente al descubrirlas. Después de la retirada de la sutura, intensificar temporalmente el tratamiento con gotas de esteroides y antibióticos. Incluso después de la remisión, se espera que la continuación a largo plazo de las gotas de esteroides suprima la recurrencia3).
Al comenzar con betametasona al 0.1%, primero continuar una fase de mantenimiento de 4 veces al día durante varios meses a 1 año, luego cambiar a un esteroide de baja concentración como fluorometolona al 0.1% y mantener a largo plazo 1-2 veces al día. Si la presión intraocular aumenta, considerar cambiar a loteprednol o agregar gotas para glaucoma.
Si hay aumento de la presión intraocular debido a la respuesta a esteroides, considere cambiar de acetato de prednisolona a loteprednol, que tiene menos efecto sobre la presión intraocular, o combinarlo con gotas oftálmicas de CsA al 1%. Las gotas de CsA al 1% permiten una reducción temprana de los esteroides y son útiles para equilibrar el manejo de la presión intraocular y la supresión del rechazo. También se utiliza la combinación con gotas para glaucoma según sea necesario.
La córnea mantiene la tolerancia inmunológica fisiológica a través de la desviación inmunitaria asociada a la cámara anterior (ACAID). En la ACAID, las células presentadoras de antígenos se vuelven tolerogénicas en un ambiente dominado por TGF-β, suprimiendo la hipersensibilidad de tipo retardado y la producción de anticuerpos fijadores del complemento contra antígenos del donante. Sin embargo, cuando existen factores de alto riesgo como neovascularización, inflamación o suturas flojas, este privilegio inmunitario se rompe fácilmente.
El mecanismo central del rechazo es la hipersensibilidad de tipo retardado, y las principales células efectoras son las células T CD4+ Th1. Las células Th1 activadas producen IFN-γ, induciendo células presentadoras de antígenos de clase II del MHC en todo el espesor de la córnea trasplantada, lo que impulsa la respuesta inmunitaria celular 8). La participación de mecanismos mediados por anticuerpos también ha llamado la atención en los últimos años, sugiriendo que los anticuerpos anti-HLA pueden causar daño endotelial crónico a través de la activación del complemento 1).
Las diferencias en las tasas de rechazo entre las técnicas quirúrgicas se deben principalmente a la cantidad y antigenicidad del tejido donante trasplantado 3).
Las sinequias anteriores periféricas (PAS) se han señalado como factor de riesgo de rechazo después de DMEK. En un modelo de trasplante de córnea en ratón, el grupo con PAS mostró un aumento significativo del rechazo 7). Se cree que el contacto directo entre el iris y el endotelio donante debido a las PAS induce la actividad de los linfocitos T citotóxicos y promueve el rechazo 7).
El rechazo del trasplante de córnea está mediado principalmente por la inmunidad celular, pero estudios en roedores han identificado múltiples vías inmunitarias distintas que conducen al rechazo 1). Esta redundancia en la respuesta inmune se considera una de las razones de los resultados inconsistentes en los estudios de emparejamiento HLA 1). Recientemente, también ha ganado atención el papel de los anticuerpos anti-HLA y el rechazo mediado por anticuerpos, lo que podría dilucidar los mecanismos del fallo endotelial tardío 1).
La vacunación contra la COVID-19 provoca una respuesta inmune sistémica, induciendo anticuerpos neutralizantes contra el SARS-CoV-2, así como respuestas de células T CD8+ y CD4+ de tipo Th1 específicas de antígeno 6). Esta activación inmune puede desencadenar el rechazo del injerto corneal a través de reactividad cruzada o activación inmune inespecífica 6). Para las vacunas inactivadas (Sinopharm), se ha sugerido que la inmunogenicidad del adyuvante hidróxido de aluminio podría ser la causa principal del rechazo 9). Sin embargo, a nivel de metanálisis, no se ha confirmado un aumento del rechazo después de la vacunación contra la COVID-19 en el trasplante de órganos sólidos, y la relación causal en el trasplante de córnea tampoco se ha establecido en este momento.
Se están acumulando informes de casos de rechazo de trasplante de córnea asociado con las vacunas contra la COVID-19 en todo el mundo 9). Una revisión de la literatura ha recopilado más de 20 casos, revelando que la mayoría son retrasplantes, el inicio ocurre de 1 a 2 semanas después de la vacunación y la mayoría se recupera con tratamiento con esteroides 9). Se ha propuesto la administración profiláctica de esteroides antes de la vacunación, pero no existen ensayos controlados aleatorizados y las decisiones deben tomarse caso por caso 8)9).
En cuanto a la efectividad del emparejamiento HLA, el ensayo CTFS II lo investigó prospectivamente, pero en la actualidad no se ha demostrado un beneficio clínico claro del emparejamiento HLA-DR en el trasplante de córnea 1). Sin embargo, el papel de los anticuerpos anti-HLA y el rechazo mediado por anticuerpos se está aclarando, lo que puede contribuir a dilucidar el mecanismo de la insuficiencia endotelial tardía 1).
En las comparaciones entre UT-DSAEK y DMEK, tanto el metanálisis de Sela 2023 2) como el ECA multicéntrico de Dunker 2020 11) mostraron que no hay diferencias significativas en las tasas de rechazo a los 12 meses, mientras que el grupo DMEK obtuvo una mejor agudeza visual corregida. Sin embargo, el fracaso del injerto tendió a ser ligeramente mayor en el grupo DMEK 2), y la elección de la técnica quirúrgica debe basarse en una evaluación integral de la patología ocular individual del paciente, los antecedentes y la experiencia institucional.
Las siguientes direcciones están atrayendo la atención para el futuro.