Ghép giác mạc xuyên thấu (PKP)
Tỷ lệ thải ghép: khoảng 4,9-28,9% 7)
Nguyên nhân chính gây thất bại: thải ghép (sớm) + suy nội mô (muộn) 3)
Đặc điểm: Chứa mô hiến toàn bộ độ dày, do đó có tính kháng nguyên cao nhất

Ghép giác mạc là một trong những ca ghép tạng có tỷ lệ thành công cao nhất. Trong ghép giác mạc xuyên thấu (PKP) lần đầu ở mắt nguy cơ thấp, tỷ lệ sống sau 5 năm đạt 95%. Thành công cao này được hỗ trợ bởi đặc quyền miễn dịch của giác mạc.
Các yếu tố tạo nên đặc quyền miễn dịch của giác mạc như sau:
Tuy nhiên, ở những mắt nguy cơ cao có tân mạch giác mạc, tỷ lệ thất bại sau 3 năm có thể vượt quá 35%. Ngay cả dưới đặc quyền miễn dịch, nguyên nhân phổ biến nhất của thất bại mảnh ghép là phản ứng thải ghép miễn dịch không hồi phục 1).
“Thải ghép” đề cập đến đáp ứng miễn dịch đặc hiệu của vật chủ chống lại giác mạc của người hiến. Thất bại mảnh ghép nguyên phát là tình trạng giác mạc không trở nên trong suốt trong vòng 8 tuần sau phẫu thuật do khiếm khuyết của chính mô hiến, chấn thương phẫu thuật hoặc bảo quản không phù hợp, và không qua trung gian miễn dịch 3). Xảy ra ở khoảng 0,1% các ca PKP.
Chẩn đoán thải ghép chỉ được thực hiện đối với mảnh ghép đã duy trì độ trong suốt ít nhất 2 tuần sau phẫu thuật. Hơn một nửa số trường hợp thải ghép xảy ra trong năm đầu tiên sau phẫu thuật, với đỉnh điểm từ 6 tháng đến 1 năm. Tuy nhiên, thải ghép cũng có thể xảy ra sau hơn 20 năm phẫu thuật. Tỷ lệ tiến triển từ thải ghép đến thất bại được báo cáo là khoảng 49%.
Ghép giác mạc là loại ghép mô thường được thực hiện nhất trên toàn cầu, và trong một khảo sát quốc tế năm 2012, PKP chiếm khoảng 70% tổng số ca ghép giác mạc 1). Trong những năm gần đây, DSAEK và DMEK cho bệnh nội mô đã phát triển nhanh chóng, và DALK cho bệnh giác mạc hình chóp và sẹo sau viêm nhu mô đã trở thành lựa chọn tiêu chuẩn, do đó tỷ lệ các kỹ thuật phẫu thuật đã thay đổi đáng kể. Tuy nhiên, PKP vẫn cần thiết cho các trường hợp đục giác mạc rộng và dị dạng, và mang nguy cơ thải ghép cao nhất 1).
Ghép giác mạc xuyên thấu (PKP)
Tỷ lệ thải ghép: khoảng 4,9-28,9% 7)
Nguyên nhân chính gây thất bại: thải ghép (sớm) + suy nội mô (muộn) 3)
Đặc điểm: Chứa mô hiến toàn bộ độ dày, do đó có tính kháng nguyên cao nhất
Ghép giác mạc lớp sâu (DALK)
Tỷ lệ thải ghép: 1-24% 4)
Lợi ích: Loại bỏ nguy cơ thải ghép nội mô
Thách thức: Thải ghép nhu mô vẫn có thể xảy ra 4)
Ghép nội mô giác mạc (DSAEK)
Tỷ lệ thải ghép: trung bình 10% (khoảng 0-45%)
Tỷ lệ thất bại nguyên phát: Trung bình 5% (khoảng 0-29%)
Đặc điểm: Không có sự khác biệt đáng kể so với PKP theo báo cáo3)
Ghép nội mô màng Descemet (DMEK)
Tỷ lệ thải ghép: Trung bình 1,9% (khoảng 0-5,9%)7)
Tỷ lệ thất bại nguyên phát: 1,7%
Đặc điểm: Tính kháng nguyên thấp nhất và tỷ lệ thải ghép thấp nhất3)
DMEK đã được chứng minh là có nguy cơ thải ghép thấp hơn đáng kể so với PKP và DSAEK trong một nghiên cứu thuần tập lớn3). Trong một phân tích tổng hợp so sánh UT-DSAEK và DMEK, không có sự khác biệt đáng kể về nguy cơ thải ghép sau 12 tháng phẫu thuật2). Trong một thử nghiệm ngẫu nhiên đa trung tâm tại Hà Lan trên 54 mắt, tỷ lệ đạt thị lực 20/25 trở lên sau 12 tháng cao hơn đáng kể ở nhóm DMEK so với nhóm DSAEK (66% so với 33%, P=0,02), trong khi không có sự khác biệt đáng kể về mật độ tế bào nội mô hoặc thay đổi khúc xạ11).
Hơn một nửa số trường hợp xảy ra trong năm đầu tiên sau phẫu thuật, đặc biệt là từ 6 tháng đến 1 năm. Tuy nhiên, thải ghép có thể xảy ra ngay cả sau một thời gian dài, vì vậy nếu các triệu chứng như đỏ mắt, mờ mắt hoặc giảm thị lực xuất hiện nhiều năm sau phẫu thuật, bệnh nhân cần đi khám ngay. Có báo cáo về trường hợp thải ghép do tiêm chủng sau hơn 20 năm phẫu thuật10).
Tỷ lệ thải ghép của PKP dao động từ 4,9% đến 28,9%, trong khi DMEK trung bình là 1,9% (khoảng 0-5,9%), thấp hơn đáng kể. Sự khác biệt này chủ yếu do lượng mô hiến tặng được ghép. PKP ghép cả biểu mô và nhu mô chứa tế bào tua, làm tăng tính kháng nguyên. Ngược lại, DMEK chỉ ghép màng Descemet và nội mô, có tính kháng nguyên thấp và không cần chỉ khâu, do đó giảm nguy cơ. Tuy nhiên, sau khi ngừng steroid, thải ghép có thể xảy ra ở khoảng 6% trường hợp DMEK, vì vậy việc duy trì steroid lâu dài là quan trọng.
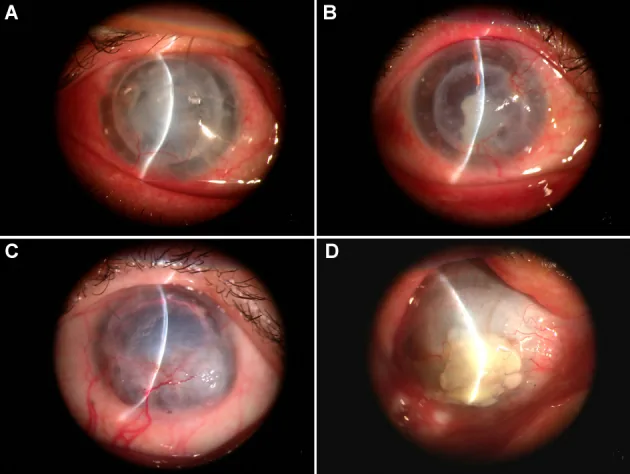
Biểu hiện: nhìn mờ, đỏ mắt, đau mắt, cảm giác dị vật, giảm thị lực. Có hai đỉnh phát bệnh vào 3 tháng và 1 năm sau phẫu thuật. Khi có triệu chứng, cần đi khám ngay.
Tiêu chuẩn chẩn đoán thải ghép bao gồm: đỏ mắt, sợ ánh sáng, giảm thị lực, tế bào tiền phòng, tủa trên nội mô giác mạc (KP), đường thải ghép nội mô hoặc biểu mô, thâm nhiễm dưới biểu mô, phù mảnh ghép khu trú1).
KP khu trú trên mảnh ghép là đặc trưng, không có KP trên giác mạc người nhận. Đường Khodadoust là tủa dạng đường trên bề mặt sau giác mạc, biểu thị mặt trước tiến triển của thải ghép nội mô.
Thải ghép được phân loại thành ba dạng theo lớp bị ảnh hưởng: biểu mô, nhu mô, nội mô. Dạng nội mô ảnh hưởng nhiều nhất đến tiên lượng mảnh ghép; chậm trễ điều trị dẫn đến suy nội mô không hồi phục và giảm thị lực.
| Dạng thải ghép | Tần suất | Dấu hiệu chính |
|---|---|---|
| Biểu mô | Khoảng 2% | Đường gờ di chuyển từ rìa giác mạc (đường thải ghép biểu mô) |
| Nhu mô | — | Phù nhu mô là dấu hiệu duy nhất |
| Loại nội mô | Khoảng 50% | KP • Đường Khodadoust • Phù |
Thải ghép biểu mô (epithelial rejection) hiếm gặp, chiếm khoảng 2% tổng số các trường hợp thải ghép. Là tổn thương tiền thân, quan sát thấy thâm nhiễm dưới biểu mô hình tròn đường kính 0,2–0,5 mm ngay dưới màng Bowman. Khi tiến triển, hình thành tổn thương dạng đường gờ phù nề (đường thải ghép biểu mô). Hầu như không ảnh hưởng đến quá trình lành trong suốt của mảnh ghép, nhưng có thể là yếu tố kích hoạt thải ghép nội mô.
Thải ghép nhu mô (stromal rejection) có biểu hiện duy nhất là phù nhu mô. Trong DALK, có thể thấy thâm nhiễm nhu mô và tân mạch mặt phân cách như thải ghép miễn dịch nhu mô 4). Khó phân biệt với phù giác mạc do thải ghép nội mô ở mắt đã phẫu thuật PKP.
Thải ghép nội mô (endothelial rejection) chiếm khoảng 50% tổng số các trường hợp thải ghép và quan trọng nhất về mặt lâm sàng. Lắng đọng mặt sau giác mạc khu trú trong mảnh ghép là dấu hiệu quan trọng, và khi hình thành đường Khodadoust, kèm theo phù nhu mô tại vị trí đó. Thể hỗn hợp (biểu mô + nội mô) gặp trong khoảng 30% trường hợp.
Đường Khodadoust là lắng đọng mặt sau giác mạc dạng đường đặc trưng của thải ghép nội mô. Nó đại diện cho mặt trước tiến triển của thải ghép di chuyển dần dần trên bề mặt nội mô mảnh ghép. Ở những vùng đường đi qua, tế bào nội mô bị tổn thương gây phù nhu mô. Khi phát hiện đường Khodadoust, cần bắt đầu ngay liệu pháp steroid mạnh.
| Dấu hiệu | Thải ghép | Viêm nội mô do HSV/VZV | Viêm nội mô do CMV |
|---|---|---|---|
| Phân bố KP | Khu trú trong mảnh ghép | Cũng bám ngoài mảnh ghép | Cũng bám ngoài mảnh ghép |
| Màu sắc của KP | Trắng đến trắng xám | Nâu | Nâu đến trắng |
| Dấu hiệu đặc trưng | Đường Khodadoust | Tam giác Arlt | Tổn thương dạng đồng xu |
Phản ứng thải ghép đặc trưng bởi KP khu trú trong mảnh ghép, trong khi viêm nội mô do virus có KP cả bên ngoài mảnh ghép, giúp phân biệt. Lưu ý rằng các lắng đọng ở mặt sau giác mạc có thể từ người hiến tặng khi ghép giác mạc, do đó ghi nhận sự phân bố KP khi khám hàng ngày rất hữu ích trong chẩn đoán phân biệt.
Các trường hợp dễ xảy ra phản ứng thải ghép sau PKP được gọi là mắt nguy cơ cao, bao gồm các yếu tố sau:
Trong DMEK, thải ghép có thể được kích hoạt khi giảm steroid. Trong một trường hợp, thải ghép xảy ra 15 tháng sau DMEK khi chuyển từ betamethasone sang fluorometholone7). Dính mống mắt trước ngoại vi (PAS) cũng được báo cáo là yếu tố nguy cơ thải ghép DMEK7).
Trong ghép tạng, lợi ích của hòa hợp HLA là rõ ràng, nhưng trong ghép giác mạc, kết quả không nhất quán1). Nghiên cứu Theo dõi Ghép Giác mạc II (CTFS II) được thực hiện tại Vương quốc Anh là một thử nghiệm lâm sàng tiến cứu lớn đã kiểm tra ảnh hưởng của hòa hợp HLA lớp II (HLA-DR) trong PKP nguy cơ cao1). Đã thu thập 1133 ca ghép từ năm 1998 đến 2011, và được phân tầng thành các nhóm 0, 1 và 2 bất hòa HLA-DR với điều kiện bất hòa HLA lớp I ≤ 2 kháng nguyên1). Các phương pháp dựa trên DNA (PCR-SSP/PCR-SSO) được sử dụng để định typ mô của người cho và người nhận nhằm tránh sai sót của phương pháp huyết thanh học1).
Trong CTFS II, không tìm thấy mối quan hệ rõ ràng giữa số lượng bất hòa HLA-DR và tỷ lệ mắc thải ghép1). Như đã được chứng minh trong mô hình động vật gặm nhấm, nhiều con đường miễn dịch khác nhau tham gia vào thải ghép giác mạc, và sự dư thừa của đáp ứng miễn dịch này được cho là một phần giải thích cho sự không nhất quán của kết quả nghiên cứu hòa hợp HLA1).
Một số trường hợp thải ghép giác mạc sau tiêm vắc-xin COVID-19 đã được báo cáo. Điều này được quan sát thấy ở cả vắc-xin mRNA (BNT162b2), vắc-xin vector virus (ChAdOx1) và vắc-xin bất hoạt (Sinopharm).
Hai trường hợp thải ghép cấp tính PKP được báo cáo hai tuần sau liều đầu tiên của vắc-xin BNT162b26). Cả hai đều không có tiền sử thải ghép trước đó và đáp ứng tốt với corticosteroid tại chỗ và toàn thân6).
Cũng có một trường hợp thải ghép nội mô ở ghép giác mạc bằng laser femtosecond hai tuần sau khi tiêm vắc-xin ChAdOx18). Quan sát thấy đường Khodadoust và viêm tiền phòng, và hồi phục sau 5 tuần điều trị bằng corticosteroid8).
Hai trường hợp thải ghép sau vắc-xin bất hoạt Sinopharm cũng được báo cáo9). Một tổng quan y văn cho thấy ít nhất 20 trường hợp thải ghép liên quan đến vắc-xin đã được ghi nhận, và phần lớn hồi phục với điều trị corticosteroid9).
Ngay cả ở PKP đã hơn 20 năm sau phẫu thuật, thải ghép xảy ra 10 ngày sau khi tiêm vắc-xin BNT162b210).
Mặc dù mối quan hệ nhân quả chưa được xác định, giả thuyết cho rằng tiêm chủng có thể kích hoạt thải ghép thông qua cảm ứng các tế bào trình diện kháng nguyên MHC lớp II9).
Thải ghép giác mạc sau tiêm vắc-xin COVID-19 đã được báo cáo với cả vắc-xin mRNA, vector và bất hoạt. Thường xảy ra trong vòng 1-3 tuần sau tiêm, và phần lớn đáp ứng với điều trị corticosteroid. Trong các phân tích tổng hợp, thải ghép tạng đặc do tiêm chủng đã bị bác bỏ, nhưng đối với ghép giác mạc, các trường hợp vẫn đang được tích lũy. Vì mối quan hệ nhân quả chưa chắc chắn, bệnh nhân ghép giác mạc được khuyến cáo tăng liều corticosteroid trước khi tiêm chủng và tái khám sớm sau tiêm.
Xác nhận sự hiện diện của kết tủa giác mạc khu trú trên mảnh ghép, đường Khodadoust, phù giác mạc và tế bào trong tiền phòng. Đường thải ghép biểu mô bắt đầu gần các mạch máu vùng rìa sung huyết và di chuyển qua ranh giới mảnh ghép.
Các tình trạng chính cần phân biệt với thải ghép nội mô như sau.
Trong thải ghép, tủa khu trú trong mảnh ghép, và tăng nhãn áp hiếm gặp. Trong viêm nội mô do HSV/VZV, tủa cũng bám ngoài mảnh ghép và kèm tăng nhãn áp cấp tính. Trong viêm nội mô do CMV, tủa dạng đồng xu và tăng nhãn áp mạn tính dai dẳng. Nếu khó xác định, hãy thực hiện xét nghiệm PCR dịch tiền phòng, xét nghiệm kháng thể huyết thanh và đánh giá đáp ứng với điều trị steroid một cách toàn diện.
Điều trị thải ghép dựa trên việc sử dụng steroid để giảm viêm.
Nhẹ (loại biểu mô hoặc nhu mô)
Nặng (loại nội mô hoặc dòng Khodadoust dương tính)
Với điều trị sớm, hơn 50% trường hợp thải ghép cấp hồi phục, trong khi điều trị chậm trễ dẫn đến mất tế bào nội mô không hồi phục và suy ghép. Giáo dục bệnh nhân về các triệu chứng chủ quan sau phẫu thuật (đỏ mắt, mờ mắt, đau mắt, sợ ánh sáng) và tầm quan trọng của việc tái khám sớm khi có thay đổi là rất quan trọng.
Quản lý dự phòng thải ghép sau ghép giác mạc sử dụng phác đồ hai bước dựa trên phân tầng nguy cơ.
Quản lý hậu phẫu cho mắt nguy cơ thông thường
Nhỏ mắt steroid: Lindelon 0,01% (betamethason) 5 lần/ngày → chuyển sang Flumetron 0,1% (fluorometholon) 2-3 lần/ngày (giảm dần trong 6 tháng)
Đường toàn thân: Prednison 20 mg trong vài ngày, hoặc không dùng
CsA: Nhỏ mắt phối hợp, tiếp tục trong vài tháng
Quản lý hậu phẫu cho mắt nguy cơ cao
Nhỏ mắt steroid: Betamethason 0,1% × 4 lần/ngày → tiếp tục trên 1 năm
Steroid toàn thân: Tiêm Lindelon 0,4% 2 mg 1 lần/ngày tĩnh mạch trong 3 ngày từ ngày phẫu thuật, sau đó viên Lindelon 0,5 mg 2 viên chia 2 lần, giảm dần trong 2 tuần
CsA: Viên nang Neoral 25 mg 3 mg/kg/ngày, nồng độ đáy 70-100 ng/mL
Cyclosporin A (CsA) được sử dụng trong các trường hợp nguy cơ cao như xâm lấn mạch máu nhu mô giác mạc từ 2 góc phần tư trở lên, ghép lại, tiền sử thải ghép. Khi dùng toàn thân, duy trì nồng độ đáy 70-100 ng/mL, theo dõi tác dụng phụ toàn thân bao gồm chức năng thận. Tiếp tục khoảng 6 tháng sau phẫu thuật.
Trong trường hợp PKP ở bệnh nhân 18 tuổi bị thải ghép hai bên đồng thời, sau khi lui bệnh bằng methylprednisolon tĩnh mạch, do đáp ứng với steroid, đã chuyển sang nhỏ mắt CsA 1% và duy trì thành công5). Nhỏ mắt CsA 1% cho phép giảm dần sớm steroid mạnh ở những người đáp ứng steroid, hữu ích cho duy trì mảnh ghép lâu dài5).
Tacrolimus được dùng làm thuốc thay thế cho các trường hợp thải ghép khi đang dùng cyclosporin đường uống. Nồng độ đáy mục tiêu 8-10 ng/mL đến 2 tháng sau phẫu thuật, sau đó 5-6 ng/mL (Prograf 0,05-0,1 mg/kg/ngày). Nhỏ mắt tacrolimus 0,03% được báo cáo có hiệu quả trong phòng ngừa thải ghép ở ghép giác mạc nguy cơ cao.
Chỉ khâu lỏng hoặc đứt có thể gây ra cả thải ghép và nhiễm trùng muộn, do đó cần cắt bỏ ngay khi phát hiện. Sau khi cắt chỉ, tăng cường tạm thời nhỏ mắt steroid và kháng sinh. Ngay cả sau khi lui bệnh, tiếp tục nhỏ mắt steroid dài hạn có thể ức chế tái phát3).
Khi bắt đầu với betamethason 0,1%, giai đoạn duy trì 4 lần/ngày tiếp tục trong vài tháng đến 1 năm, sau đó chuyển sang steroid nồng độ thấp như fluorometholon 0,1% 1-2 lần/ngày để duy trì lâu dài. Nếu tăng nhãn áp, cân nhắc chuyển sang loteprednol hoặc thêm thuốc nhỏ mắt glôcôm.
Nếu có tăng nhãn áp do đáp ứng steroid, cân nhắc chuyển từ prednisolon acetat sang loteprednol ít ảnh hưởng đến nhãn áp hơn, hoặc kết hợp với thuốc nhỏ mắt CsA 1%. Thuốc nhỏ mắt CsA 1% cho phép giảm steroid sớm, hữu ích trong việc kiểm soát nhãn áp và ức chế thải ghép. Cũng sử dụng thuốc nhỏ mắt điều trị glôcôm khi cần.
Giác mạc duy trì dung nạp miễn dịch sinh lý thông qua sự lệch hướng miễn dịch liên quan đến tiền phòng (ACAID). Trong ACAID, các tế bào trình diện kháng nguyên trở nên dung nạp nguyên trong môi trường ưu thế TGF-β, ức chế phản ứng quá mẫn muộn và sản xuất kháng thể gắn bổ thể chống lại kháng thể của người cho. Tuy nhiên, sự hiện diện của các yếu tố nguy cơ như tân mạch, viêm và lỏng chỉ khâu có thể dễ dàng phá vỡ đặc quyền miễn dịch này.
Cơ chế trung tâm của thải ghép là phản ứng quá mẫn muộn, và tế bào hiệu ứng chính là tế bào Th1 CD4+. Các tế bào Th1 được hoạt hóa sản xuất IFN-γ, cảm ứng các tế bào trình diện kháng nguyên MHC lớp II trên toàn bộ bề dày giác mạc ghép, thúc đẩy đáp ứng miễn dịch tế bào8). Vai trò của cơ chế qua trung gian kháng thể cũng được chú ý gần đây, với bằng chứng cho thấy kháng thể kháng HLA có thể gây tổn thương nội mô mạn tính thông qua hoạt hóa bổ thể1).
Sự khác biệt về tỷ lệ thải ghép giữa các kỹ thuật phẫu thuật chủ yếu do lượng mô ghép và tính kháng nguyên khác nhau3).
Dính mống mắt trước ngoại vi (PAS) được xác định là yếu tố nguy cơ thải ghép sau DMEK. Trên mô hình ghép giác mạc chuột, thải ghép tăng đáng kể ở nhóm có PAS 7). Sự tiếp xúc trực tiếp giữa mống mắt và nội mô người cho do PAS được cho là kích thích hoạt động của tế bào lympho T gây độc tế bào, thúc đẩy thải ghép 7).
Thải ghép giác mạc chủ yếu qua trung gian miễn dịch tế bào, nhưng các nghiên cứu trên loài gặm nhấm đã xác định nhiều con đường miễn dịch khác nhau dẫn đến thải ghép 1). Sự dư thừa của đáp ứng miễn dịch này được cho là một trong những nguyên nhân khiến kết quả các nghiên cứu về hòa hợp HLA không nhất quán 1). Gần đây, vai trò của kháng thể kháng HLA và thải ghép qua trung gian kháng thể cũng được chú ý, có thể giúp làm sáng tỏ cơ chế suy nội mô muộn 1).
Tiêm vắc-xin COVID-19 kích hoạt đáp ứng miễn dịch toàn thân, tạo ra kháng thể trung hòa SARS-CoV-2 cũng như đáp ứng tế bào T CD8+ và Th1 CD4+ đặc hiệu kháng nguyên 6). Sự tăng cường miễn dịch này có thể kích hoạt thải ghép giác mạc thông qua phản ứng chéo hoặc kích hoạt miễn dịch không đặc hiệu 6). Đối với vắc-xin bất hoạt (Sinopharm), tính sinh miễn dịch của nhôm hydroxit (chất bổ trợ) được cho là nguyên nhân chính gây thải ghép 9). Tuy nhiên, ở cấp độ phân tích tổng hợp, chưa xác nhận được sự gia tăng thải ghép sau tiêm vắc-xin COVID-19 trong ghép tạng đặc, và mối quan hệ nhân quả trong ghép giác mạc hiện cũng chưa được xác lập.
Các báo cáo ca bệnh về thải ghép giác mạc liên quan đến vắc xin COVID-19 đã được tích lũy trên toàn cầu 9). Một tổng quan tài liệu đã thu thập hơn 20 trường hợp, phần lớn là ghép lại, xảy ra trong vòng 1-2 tuần sau tiêm chủng, và hầu hết hồi phục với điều trị steroid 9). Lợi ích của việc dùng steroid dự phòng trước tiêm chủng đã được đề xuất, nhưng không có thử nghiệm ngẫu nhiên có đối chứng, và quyết định cần được đưa ra riêng cho từng trường hợp 8)9).
Về hiệu quả của việc hòa hợp HLA, thử nghiệm CTFS II đã xem xét một cách tiến cứu, nhưng hiện tại chưa có lợi ích lâm sàng rõ ràng của việc hòa hợp HLA-DR trong ghép giác mạc 1). Tuy nhiên, vai trò của kháng thể kháng HLA và thải ghép qua trung gian kháng thể đang trở nên rõ ràng, có thể góp phần làm sáng tỏ cơ chế suy nội mô muộn 1).
Trong so sánh UT-DSAEK và DMEK, cả phân tích tổng hợp của Sela 2023 2) và thử nghiệm ngẫu nhiên đa trung tâm của Dunker 2020 11) đều cho thấy không có sự khác biệt đáng kể về tỷ lệ thải ghép 12 tháng, trong khi nhóm DMEK cho thị lực điều chỉnh tốt hơn. Tuy nhiên, suy mảnh ghép có xu hướng nhiều hơn một chút ở nhóm DMEK 2), và việc lựa chọn kỹ thuật nên dựa trên tình trạng mắt cá nhân, tiền sử và kinh nghiệm của trung tâm.
Các hướng đi trong tương lai sau đây đang được chú ý: