Phụ thuộc liều
Liều hàng ngày: RR ở bệnh nhân dùng >100 mg/ngày là 2,71, trong khi ở liều ≤100 mg/ngày là 1,69
Liều tích lũy: Bệnh nhân có liều tích lũy suốt đời cao hơn có xu hướng mật độ tế bào nội mô thấp hơn

Amantadine là một chất đối kháng thụ thể glutamate loại NMDA, ban đầu được phát triển như một thuốc dự phòng cúm A. Hiện nay được sử dụng để điều trị run trong bệnh Parkinson (PD), rối loạn vận động do levodopa và mệt mỏi trong bệnh đa xơ cứng (MS).
Một tác dụng phụ hiếm gặp của thuốc này là phù giác mạc hai mắt. Trong một tổng quan y văn gồm 33 ca, 70% bệnh nhân là nữ, tuổi trung bình 52 1). Trong một nghiên cứu giám sát hai năm của Cơ quan Y tế Cựu chiến binh, phù giác mạc được tìm thấy ở 0,27% bệnh nhân dùng amantadine. Một nghiên cứu dọc ở Đài Loan báo cáo nguy cơ tương đối (RR) phù giác mạc khi sử dụng amantadine ở bệnh nhân PD là 1,98.
Phù giác mạc tương tự đã được báo cáo với các thuốc dopaminergic khác như methylphenidate, ropinirole và bupropion. Tất cả đều cải thiện sau khi ngừng thuốc, và sử dụng đồng thời nhiều thuốc dopaminergic có thể làm tăng nguy cơ do tác dụng cộng hợp.
Nhìn mờ hai mắt tiến triển chậm trong vài tuần đến vài tháng là triệu chứng chính. Thường khởi phát sau vài tuần đến vài tháng kể từ khi bắt đầu thuốc, nhưng cũng có báo cáo sau nhiều năm điều trị 1). Trong tổng quan y văn, thị lực trung bình khi khởi phát là 20/200 (mắt kém hơn) 1).
Các yếu tố nguy cơ sau đây đã được báo cáo đối với độc tính của amantadine.
Phụ thuộc liều
Liều hàng ngày: RR ở bệnh nhân dùng >100 mg/ngày là 2,71, trong khi ở liều ≤100 mg/ngày là 1,69
Liều tích lũy: Bệnh nhân có liều tích lũy suốt đời cao hơn có xu hướng mật độ tế bào nội mô thấp hơn
Ảnh hưởng mãn tính lên nội mô
Nghiên cứu tiến cứu: Bệnh nhân dùng amantadine có tốc độ giảm mật độ tế bào nội mô giác mạc là 1,51%/năm, cao hơn so với bệnh nhân PD không dùng thuốc (0,94%) và người khỏe mạnh (0,55%)
Liều càng cao, ảnh hưởng càng lớn: Sự giảm tỷ lệ tế bào hình lục giác và tăng hệ số biến thiên tăng lên phụ thuộc vào liều
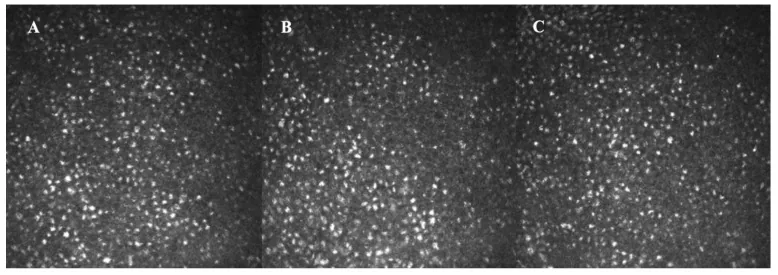
Chẩn đoán phù giác mạc do amantadine được thực hiện trên lâm sàng. Sau khi loại trừ các nguyên nhân khác gây phù giác mạc, xác nhận mối liên quan với tiền sử sử dụng amantadine.
Trong loạn dưỡng nội mô Fuchs, có thể quan sát thấy các giọt giác mạc (guttata) đặc trưng trên kính hiển vi nội mô hoặc đèn khe, trong khi phù giác mạc do amantadine không có guttata. Ngoài ra, Fuchs là bệnh mạn tính tiến triển, trong khi phù do amantadine thường hồi phục sau khi ngừng thuốc.
Cơ bản của điều trị là ngừng amantadine ngay lập tức. Trong tổng quan y văn, phần lớn các trường hợp hết phù giác mạc trong vòng 30 ngày sau khi ngừng thuốc (trung vị 30 ngày, khoảng tứ phân vị 14–35 ngày), và thị lực cải thiện đến trung vị 20/25 1). Phối hợp với bác sĩ thần kinh để xem xét chuyển sang thuốc thay thế.
Để điều trị triệu chứng phù giác mạc, đôi khi sử dụng thuốc nhỏ mắt nước muối ưu trương (natri clorua 5%). Tuy nhiên, do rối loạn chức năng nội mô là bản chất, hiệu quả còn hạn chế. Nếu tiến triển thành bệnh giác mạc bọng nước, sử dụng kính áp tròng băng để kiểm soát đau và thuốc nhỏ mắt kháng sinh dự phòng.
Trong tổng quan y văn, 5/33 trường hợp (10 mắt) cần ghép giác mạc 1). Các phương pháp được chọn là ghép nội mô màng Descemet (DMEK) hoặc ghép nội mô tự động bóc tách màng Descemet (DSAEK). Có báo cáo về thất bại mảnh ghép không do miễn dịch nếu ghép giác mạc trong khi tiếp tục dùng amantadine, do đó cần ngừng thuốc trước khi ghép.
Cơ chế chính xác chưa được biết, nhưng độc tính phụ thuộc liều lên tế bào nội mô giác mạc được cho là nguyên nhân chính. Tế bào nội mô giác mạc có chức năng bơm qua bơm Na⁺-K⁺ ATPase và các chất vận chuyển ion như SLC4A11 để bơm nước từ nhu mô giác mạc vào tiền phòng, cùng với chức năng hàng rào qua các liên kết chặt giữa các tế bào. Các chức năng này duy trì hàm lượng nước của giác mạc ổn định và giữ cho giác mạc trong suốt.
Trong kiểm tra mô bệnh học của các trường hợp phù giác mạc do amantadine cần ghép giác mạc, người ta thấy giác mạc dạng giọt và mất tế bào nội mô giác mạc từ mức độ trung bình đến hoàn toàn, không kèm viêm. Người ta ước tính rằng stress do thuốc tác động lên tế bào nội mô giác mạc, và khi vượt quá ngưỡng, sẽ dẫn đến rối loạn chức năng và mất tế bào nội mô, gây tích tụ dịch trong nhu mô giác mạc do chức năng bơm suy giảm, dẫn đến phù.
Độc tính mạn tính phụ thuộc liều được coi là cơ chế chính, thay vì phản ứng vô căn (khởi phát trong vòng 1 tháng sau khi bắt đầu thuốc). Trong tổng quan y văn, chỉ có 9,7% tổng số ca khởi phát trong vòng 1 tháng 1).
Tế bào nội mô giác mạc người hầu như không có khả năng tái tạo; các tế bào bị tổn thương được bù đắp bằng cách các tế bào xung quanh dẹt ra và mở rộng diện tích. Ngay cả sau khi phù giác mạc biến mất sau khi ngừng amantadine, mật độ tế bào nội mô thường vẫn thấp, tiềm ẩn nguy cơ suy giác mạc trong tương lai. Do đó, khuyến cáo theo dõi lâu dài.