剂量依赖性
每日剂量:每日剂量超过100 mg的患者相对风险(RR)为2.71,而每日剂量≤100 mg的患者为1.69
累积剂量:终生累积剂量越高的患者,内皮细胞密度往往越低

金刚烷胺是一种NMDA型谷氨酸受体拮抗剂,最初作为甲型流感的预防药物开发。目前用于治疗帕金森病(PD)相关的震颤、左旋多巴诱发的运动障碍以及多发性硬化(MS)的疲劳。
该药的一种罕见副作用是双眼角膜水肿。在33例文献综述中,70%的患者为女性,中位年龄52岁1)。退伍军人健康管理局的一项为期两年的监测研究发现,服用金刚烷胺的患者中有0.27%出现角膜水肿。台湾的一项纵向研究报告,PD患者使用金刚烷胺时角膜水肿的相对风险(RR)为1.98。
其他多巴胺激动剂如哌甲酯、罗匹尼罗和安非他酮也有类似的角膜水肿报告。所有病例在停药后均恢复,联合使用多种多巴胺激动剂可能因相加效应而增加风险。
主要症状为数周至数月内缓慢进展的双眼视力模糊。通常在用药后数周至数月发病,但也有治疗开始数年后报告的病例1)。文献综述中,发病时中位视力为20/200(较差眼)1)。
以下因素已被报道为金刚烷胺毒性的风险因素。
剂量依赖性
每日剂量:每日剂量超过100 mg的患者相对风险(RR)为2.71,而每日剂量≤100 mg的患者为1.69
累积剂量:终生累积剂量越高的患者,内皮细胞密度往往越低
对内皮的慢性影响
前瞻性研究:服用金刚烷胺的患者角膜内皮细胞密度年减少率为1.51%/年,高于未服药的帕金森病患者(0.94%)和健康人(0.55%)
剂量越高影响越大:六角形细胞比例下降和变异系数升高呈剂量依赖性增加
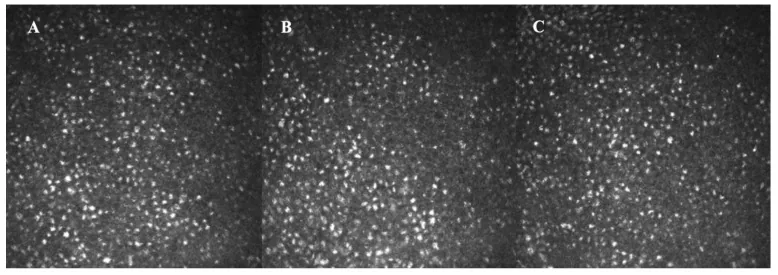
金刚烷胺诱导的角膜水肿的诊断基于临床。在排除其他角膜水肿原因后,确认与金刚烷胺使用史的相关性。
Fuchs角膜内皮营养不良在镜面显微镜或裂隙灯显微镜下特征性地可见角膜滴状赘疣(guttata),而金刚烷胺诱发的角膜水肿则无滴状赘疣。此外,Fuchs是慢性进行性的,而金刚烷胺诱发性水肿在停药后大多可恢复。
治疗的基础是迅速停用金刚烷胺。文献综述显示,大多数病例在停药后30天内(中位数30天,四分位距14-35天)角膜水肿消失,视力恢复至中位数20/251)。与神经内科主治医生协作,考虑更换为替代药物。
角膜水肿的对症治疗可使用高渗盐水(5%氯化钠)滴眼液。但由于本质是内皮功能障碍,效果有限。若进展为大疱性角膜病变,可使用绷带式隐形眼镜进行疼痛管理,并预防性使用抗菌滴眼液。
文献综述中,33例中有5例(10眼)需要角膜移植1)。可选择Descemet膜内皮角膜移植术(DMEK)或Descemet膜剥离自动角膜内皮移植术(DSAEK)。有报告称,若在继续使用金刚烷胺的情况下进行角膜移植,会导致非免疫性移植失败,因此移植前需停药。
确切机制尚不清楚,但主要认为是角膜内皮细胞的剂量依赖性毒性。角膜内皮细胞通过Na⁺-K⁺ ATP酶泵和SLC4A11等离子转运体将水从角膜基质泵入前房,具有泵功能,并通过细胞间紧密连接具有屏障功能。这些功能维持角膜含水量恒定和透明性。
对需要角膜移植的金刚烷胺诱导的角膜水肿病例的组织病理学检查显示,中度至完全的角膜内皮细胞丧失,无滴状角膜或炎症。推测药物诱导的应激作用于角膜内皮细胞,当超过阈值时,导致内皮细胞功能障碍和丧失进行性加重,泵功能下降使角膜基质内水分积聚,从而引起水肿。
剂量依赖性慢性毒性被认为是主要机制,而非特发性反应(用药后1个月内发病)。文献综述显示,1个月内发病的病例仅占9.7%1)。
人类角膜内皮细胞几乎没有再生能力,受损细胞由周围细胞扁平化并扩大面积来代偿。停用金刚烷胺后即使角膜水肿消退,内皮细胞密度仍常保持低值,存在未来角膜代偿不全的风险。因此建议长期随访。