眼压和视力
视力下降:从轻度下降到手动视力不等。病例报告中矫正视力可降至20/801)。
眼压升高:真实眼压升高,但中央角膜的Goldmann压平眼压计可能显示假性低值2)。这是因为界面的液体垫效应容易被压缩1)。
周边测量:应使用Tono-Pen或动态轮廓眼压计测量周边眼压2)。

界面液综合征(interface fluid syndrome, IFS)是LASIK术后一种罕见但威胁视力的并发症,液体在角膜瓣和角膜基质床之间(界面)积聚。自早期报告以来,它被描述为压力诱导的层间基质角膜炎(pressure-induced interlamellar stromal keratitis, PISK),与眼压升高相关1)。
IFS的主要原因是类固醇诱导的眼压升高1)3)。类固醇诱导的高眼压导致界面液体积聚,也可能导致眼压被低估3)。它通常发生在术后早期(数天至数周),但也有LASIK术后10年发生的迟发性病例报道1)。
除LASIK外,IFS也可能发生在SMILE(小切口角膜基质透镜取出术)或板层角膜移植术后。埃及报道LASIK术后IFS的发生率为2.9%,但由于该研究使用了强效类固醇(地塞米松),一般发生率推测要低得多。
患者在LASIK术后数天至数月(有时数年)以视物模糊为主诉就诊。可能伴有疼痛或畏光1)。典型情况下,发生在LASIK术后长期使用局部类固醇的患者1)。
眼压和视力
视力下降:从轻度下降到手动视力不等。病例报告中矫正视力可降至20/801)。
眼压升高:真实眼压升高,但中央角膜的Goldmann压平眼压计可能显示假性低值2)。这是因为界面的液体垫效应容易被压缩1)。
周边测量:应使用Tono-Pen或动态轮廓眼压计测量周边眼压2)。
角膜所见
界面混浊:在角膜瓣与基质床之间可见弥漫性混浊1)。
液体蓄积:裂隙灯显微镜检查有时可观察到明显的液体层,但并非总是清晰可见。
角膜水肿:可能出现上皮下水肿或微囊泡(微小水疱)1)。
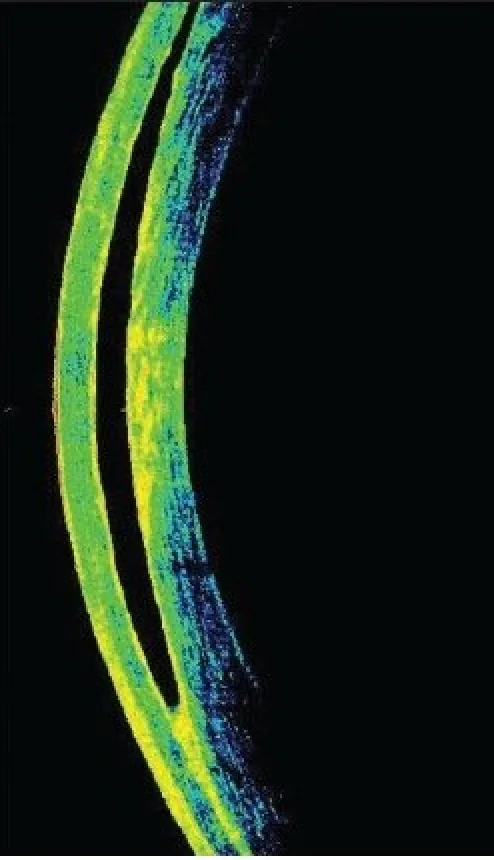
OCT表现:眼前段OCT可清晰显示界面的液体蓄积,有助于确诊1)2)。
IFS的原因大致分为两类。第一类是类固醇引起的眼压升高,这是最常见的原因1)3)。第二类是角膜内皮功能不全。
任何导致眼压升高的疾病都可能成为IFS的原因。已有报道包括葡萄膜炎、Posner-Schlossman综合征、巨细胞病毒性内皮炎、眼前节毒性综合征(TASS)、外伤、感染性角膜炎等。患有Fuchs角膜内皮营养不良等角膜内皮功能不全的患者发病风险也较高。
所有接受过在角膜基质与角膜瓣之间产生潜在间隙的手术的患者都有发生IFS的风险。最常见于LASIK患者,但SMILE或板层角膜移植术后也可发生。
IFS的分期根据角膜水肿程度和混浊模式分类如下。
| 分期 | 表现 |
|---|---|
| 0期 | LASIK术后正常角膜 |
| 1期 | 轻度至中度肿胀,混浊轻微 |
| 2期 | 中度至重度肿胀,弥漫性混浊和液体囊袋 |
| 3期 | 融合的大液体囊袋,散在混浊 |
诊断依据临床病程和裂隙灯显微镜检查,并通过眼前节OCT确认1)。OCT可确认角膜瓣与基质床界面间的液体蓄积1)。角膜密度测量(Scheimpflug成像角膜亮度测量)也有助于IFS的评估和分级1)。
眼压测量时,Goldmann压平眼压计的中央测量可能出现假性低值,需注意2)。推荐周边部Tonopen测量或动态轮廓眼压计1)2)。
| 疾病 | 鉴别要点 |
|---|---|
| DLK | 术后2-5天发病,有疼痛,眼压正常 |
| 微生物性角膜炎 | 眼压正常,可见浸润 |
| 上皮植入 | 眼压正常,无界面液 |
与DLK的鉴别尤为重要。DLK的治疗是使用类固醇,但对IFS使用类固醇会进一步升高眼压并加重症状1)。DLK可见炎性单核细胞和粒细胞,而IFS则无炎性细胞1)。
IFS的基本治疗是停用类固醇和开始使用降眼压药物1)。
β受体阻滞剂(如噻吗洛尔)是一线药物,效果不佳时可联合碳酸酐酶抑制剂和α受体激动剂1)。有病例报告显示,联合使用0.2%溴莫尼定、0.5%噻吗洛尔和2.0%多佐胺,36小时后视力改善1)。降眼压药物持续使用1-3个月后逐渐减量停药1)。
如果药物控制眼压不佳,可能需要手术干预。有报告对伴有Fuchs角膜内皮营养不良的IFS采用DMEK(角膜内皮移植术)进行管理。
如果合并上皮植入,需掀开角膜瓣进行机械性清除1)。联合使用50%酒精和0.02%丝裂霉素C涂抹以预防复发1)。
及时诊断IFS对于防止永久性视力丧失至关重要。如果误诊为DLK并使用类固醇,IFS会恶化,因此两者的鉴别决定了治疗策略。1)
IFS的病理生理学主要有两种机制被提出。
第一种机制是眼压升高导致的液体移动。眼压升高时,液体通过角膜内皮从高压区(前房侧)移动到低压区(界面间隙)。LASIK瓣制作产生的界面成为低压区,导致液体在此积聚。类固醇诱导的眼压升高是此机制最常见的诱因1)3)。
第二种机制是角膜内皮功能障碍。如Fuchs角膜内皮营养不良等导致角膜内皮泵功能受损时,角膜基质的水分排出不足,液体更容易在界面积聚。
DLK中可见炎性单核细胞和粒细胞聚集,而IFS中无炎症细胞,仅存在水肿1)。共聚焦显微镜下可观察到微腔隙(微小空隙),被认为是基质水肿的结果1)。
迟发性IFS的机制中,有假说认为上皮植入形成瘘管,为液体流入界面提供了“空间”1)。
类固醇诱导的眼压升高导致界面液体积聚,同时也导致眼压被低估。降低眼压可使炎症消退。3)
在IFS中,实际眼压是升高的。但使用Goldmann压平眼压计测量中央角膜时,界面积聚的液体的缓冲作用使角膜容易被压缩,导致眼压测量值假性偏低。因此,对于有LASIK病史的患者,建议进行周边眼压测量或使用动态轮廓眼压计。
IFS的临床谱正在扩大。传统上被认为是术后早期并发症,但已有LASIK术后10年发生迟发性PISK伴上皮植入的病例报道1)。该病例推测上皮植入形成瘘管,促进了液体流入界面1)。此外,还有一例因葡萄膜炎治疗加用类固醇后,LASIK术后9年发生PISK的报道1)。
随着SMILE的普及,SMILE术后IFS也成为鉴别诊断中应考虑的并发症。传统眼压测量方法的局限性已被认识,前段OCT筛查的重要性得到强调2)。当出现不明原因的视力下降或眼压升高时,建议进行OCT检查1)。
IFS通常发生在术后1至3天,但也可能在数年后发生。对于长期使用类固醇的LASIK术后患者,持续的眼压监测非常重要。1)