劑量依賴性
每日劑量:每日劑量超過100 mg的患者相對風險(RR)為2.71,而每日劑量≤100 mg的患者為1.69
累積劑量:終生累積劑量越高的患者,內皮細胞密度往往越低

金剛烷胺是一種NMDA型麩胺酸受體拮抗劑,最初開發為A型流感的預防藥物。目前用於治療帕金森病(PD)相關的震顫、左旋多巴誘發的運動障礙以及多發性硬化症(MS)的疲勞。
該藥的罕見副作用是雙眼角膜水腫。在33例文獻回顧中,70%的患者為女性,中位年齡52歲1)。退伍軍人健康管理局的一項兩年監測研究發現,服用金剛烷胺的患者中有0.27%出現角膜水腫。台灣的一項縱向研究報告,PD患者使用金剛烷胺時角膜水腫的相對風險(RR)為1.98。
其他多巴胺促效劑如哌甲酯、羅匹尼羅和安非他酮也有類似的角膜水腫報告。所有病例在停藥後均恢復,併用多種多巴胺促效劑可能因相加效應而增加風險。
主要症狀為數週至數月內緩慢進展的雙眼視力模糊。通常在服藥後數週至數月發病,但也有治療開始數年後報告的病例1)。文獻回顧中,發病時中位視力為20/200(較差眼)1)。
以下因素已被報導為金剛烷胺毒性的風險因素。
劑量依賴性
每日劑量:每日劑量超過100 mg的患者相對風險(RR)為2.71,而每日劑量≤100 mg的患者為1.69
累積劑量:終生累積劑量越高的患者,內皮細胞密度往往越低
對內皮的慢性影響
前瞻性研究:服用金剛烷胺的患者角膜內皮細胞密度年減少率為1.51%/年,高於未服藥的帕金森病患者(0.94%)和健康人(0.55%)
劑量越高影響越大:六角形細胞比例下降和變異係數升高呈劑量依賴性增加
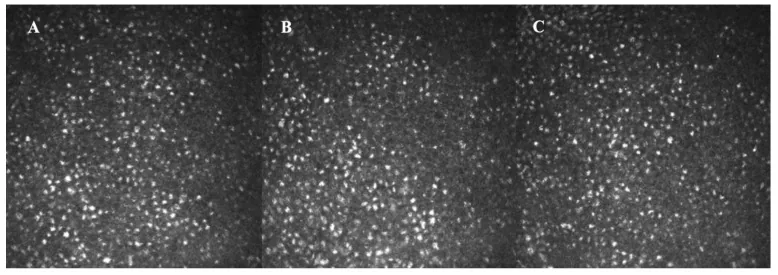
金剛烷胺誘發角膜水腫的診斷基於臨床。在排除其他角膜水腫原因後,確認與金剛烷胺使用史的關聯。
Fuchs角膜內皮營養不良在鏡面顯微鏡或裂隙燈顯微鏡下特徵性地可見角膜滴狀贅疣(guttata),而金剛烷胺誘發的角膜水腫則無滴狀贅疣。此外,Fuchs是慢性進行性的,而金剛烷胺誘發性水腫在停藥後大多可恢復。
治療的基礎是迅速停用金剛烷胺。文獻綜述顯示,大多數病例在停藥後30天內(中位數30天,四分位距14-35天)角膜水腫消失,視力恢復至中位數20/251)。與神經內科主治醫師協作,考慮更換為替代藥物。
角膜水腫的對症治療可使用高滲鹽水(5%氯化鈉)眼藥水。但由於本質是內皮功能障礙,效果有限。若進展為大皰性角膜病變,可使用繃帶式隱形眼鏡進行疼痛管理,並預防性使用抗菌眼藥水。
文獻綜述中,33例中有5例(10眼)需要角膜移植1)。可選擇Descemet膜內皮角膜移植術(DMEK)或Descemet膜剝離自動角膜內皮移植術(DSAEK)。有報告稱,若在繼續使用金剛烷胺的情況下進行角膜移植,會導致非免疫性移植失敗,因此移植前需停藥。
確切機制尚不清楚,但主要認為是角膜內皮細胞的劑量依賴性毒性。角膜內皮細胞通過Na⁺-K⁺ ATP酶泵和SLC4A11等離子轉運體將水從角膜基質泵入前房,具有泵功能,並通過細胞間緊密連接具有屏障功能。這些功能維持角膜含水量恆定和透明性。
對需要角膜移植的金剛烷胺誘發角膜水腫病例的組織病理學檢查顯示,中度至完全的角膜內皮細胞喪失,無滴狀角膜或發炎。推測藥物誘導的應力作用於角膜內皮細胞,當超過閾值時,導致內皮細胞功能障礙和喪失進行性加重,幫浦功能下降使角膜基質內水分積聚,從而引起水腫。
劑量依賴性慢性毒性被認為是主要機制,而非特發性反應(用藥後1個月內發病)。文獻回顧顯示,1個月內發病的病例僅佔9.7%1)。
人類角膜內皮細胞幾乎沒有再生能力,受損細胞由周圍細胞扁平化並擴大面積來代償。停用金剛烷胺後即使角膜水腫消退,內皮細胞密度仍常保持低值,存在未來角膜代償不全的風險。因此建議長期追蹤。