ภาวะตาแห้ง หลังการผ่าตัดแก้ไขสายตาเป็นภาวะแทรกซ้อนที่พบบ่อยหลัง LASIK , PRK และ SMILE กลไกหลักคือการหลั่งน้ำตาลดลงจากการสะท้อนเนื่องจากการตัดเส้นประสาทกระจกตา
อุบัติการณ์หลัง LASIK ในระยะสั้นหลังผ่าตัดคือ 50-90% ส่วนใหญ่ดีขึ้นภายใน 6-12 เดือน แต่บางรายอาจกลายเป็นดื้อต่อการรักษา
ความเสี่ยงตามประเภทการผ่าตัด: LASIK > PRK > SMILE SMILE ทำให้เกิดการตัดเส้นประสาทน้อยที่สุดเนื่องจากแผลผ่าตัดเล็ก
เกณฑ์การวินิจฉัย (ญี่ปุ่น): อาการทางคลินิก + BUT ≤5 วินาที เพื่อการวินิจฉัยที่แน่นอน
การรักษาแนวแรก: น้ำตาเทียม ไร้สารกันเสีย + ยาหยอดไดควาฟอซอลโซเดียม (3%) (คำแนะนำที่เข้มแข็งในแนวทางตาแห้ง )
กรณีดื้อต่อการรักษา: IPL, LipiFlow, ปลั๊กอุดจุดน้ำตา , ไซโคลสปอริน , ยาหยอด PRGF เป็นทางเลือก
ภาวะตาแห้ง หลังการผ่าตัดแก้ไขสายตา (post-refractive surgery dry eye) คือภาวะตาแห้ง ที่เกิดขึ้นหลังการผ่าตัดแก้ไขสายตาที่เปลี่ยนแปลงรูปร่างของกระจกตา เช่น LASIK (laser in situ keratomileusis), PRK (photorefractive keratectomy) และ SMILE (small incision lenticule extraction)
ภาวะตาแห้ง ถูกนิยามว่าเป็น “โรคที่ความคงตัวของชั้นน้ำตาลดลงจากปัจจัยต่างๆ ทำให้เกิดอาการไม่สบายตาและความผิดปกติทางการมองเห็น และอาจมีรอยโรคที่ผิวตาร่วมด้วย” ภาวะตาแห้ง หลังการผ่าตัดแก้ไขสายตาตามนิยามนี้มีสาเหตุหลักมาจากการตัดเส้นประสาทกระจกตา และการขัดขวางรีเฟล็กซ์ของต่อมน้ำตาจากการผ่าตัดกระจกตา
มีหลักฐานว่าการบาดเจ็บของเยื่อบุกระจกตา และการลดลงของเวลาแตกตัวของชั้นน้ำตา (BUT ) สามารถเกิดขึ้นได้หลังการผ่าตัดส่วนหน้าของลูกตาทั่วไป รวมถึง LASIK และ PRK ปริมาณการหลั่งน้ำตา (ค่า Schirmer) มีแนวโน้มลดลงในการผ่าตัดที่มีการกรีดหรือตัดกระจกตา 2)
ในแนวทางการผ่าตัดแก้ไขสายตา (ฉบับที่ 8) ระบุว่าภาวะตาแห้ง เป็นหนึ่งในภาวะแทรกซ้อนหลังการทำ LASIK 1) และจำเป็นต้องมีการประเมินและการจัดการเชิงรุกก่อนการผ่าตัด
อาการตาแห้ง ในระยะแรกหลังผ่าตัดโดยทั่วไปจะดีขึ้นภายใน 6–12 เดือน แต่ในบางกรณีอาจพัฒนาเป็นภาวะตาแห้ง ที่ดื้อต่อการรักษาแบบเดิม 3)
Q
ทำไม LASIK จึงทำให้เกิดภาวะตาแห้งได้ง่าย?
A
ในการทำ LASIK เมื่อสร้างแผ่นปิดกระจกตา ด้วยไมโครเคราโตมหรือเลเซอร์เฟมโตวินาที จะมีการตัดข่ายประสาทกระจกตา ชั้นหน้าอย่างกว้างขวาง ส่งผลให้สัญญาณรีเฟล็กซ์ไปยังต่อมน้ำตาผ่านเส้นประสาทไทรเจมินัล ถูกขัดขวางอย่างมาก ทำให้การหลั่งน้ำตาทั้งแบบพื้นฐานและแบบรีเฟล็กซ์ลดลง นอกจากนี้ การกระพริบตาลดลงและการเสื่อมสภาพของต่อมไมโบเมียน หลังผ่าตัดก็มีส่วนทำให้ผู้ป่วยจำนวนมากมีอาการตาแห้ง เป็นเวลา 1–3 เดือนหลังการผ่าตัด
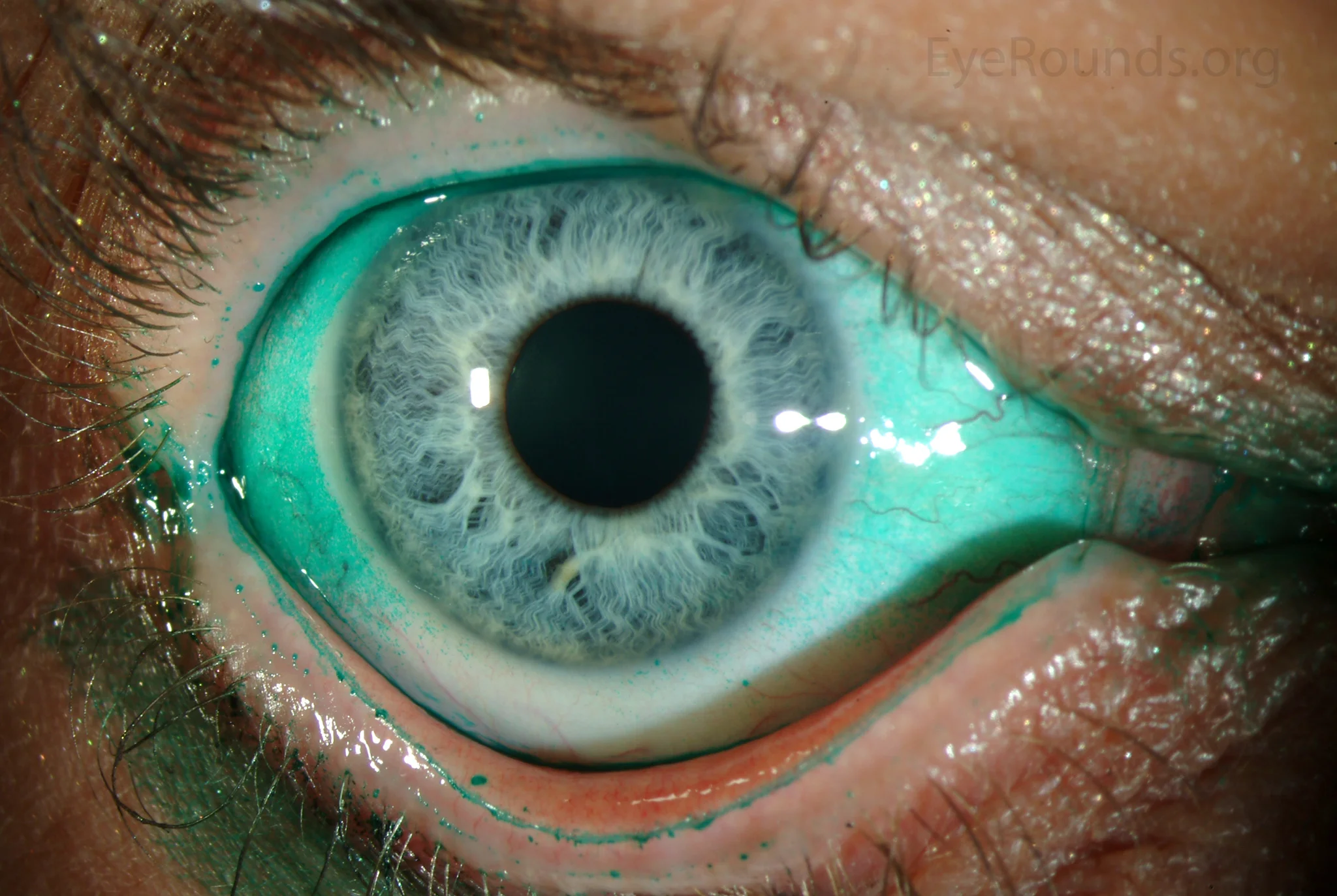
ภาพการย้อมสีลิสซามีนกรีนแสดงรอยโรคเยื่อบุตาขาวและกระจกตาในภาวะตาแห้งรุนแรง Vislisel J, Critser B. Diffuse lissamine green staining in severe keratoconjunctivitis sicca. EyeRounds.org Atlas, University of Iowa, 2016. Source ID: Wikimedia Commons / File:LG3-LRG.jpg. License: CC BY-SA 4.0.
ผิวลูกตาในภาวะตาแห้ง รุนแรงที่สังเกตด้วยการย้อมสีลิสซามีนกรีน แสดงการย้อมสีเยื่อบุตา ขาวแบบกระจายทั่วทั้งเยื่อบุตา และการย้อมสีแบบจุดบนเยื่อบุกระจกตา ซึ่งสอดคล้องกับรอยโรคเยื่อบุกระจกตา และเยื่อบุตา ขาวจากการย้อมสีลิสซามีนกรีนและฟลูออเรสซีน ที่กล่าวถึงในหัวข้อ “อาการหลักและอาการแสดงทางคลินิก”
อาการตาแห้ง หลังการผ่าตัดแก้ไขสายตาคล้ายกับอาการตาแห้ง ทั่วไป แต่อาการที่เกี่ยวข้องกับการมองเห็น มักเด่นชัดกว่า
ความรู้สึกแห้ง รู้สึกมีสิ่งแปลกปลอม แสบร้อน ปวดตา
ตามัวและความคมชัดในการมองเห็น ที่เปลี่ยนแปลงไป (ดีขึ้นชั่วคราวหลังกระพริบตา)
อาการกลัวแสง และไวต่อแสง ความรู้สึกไม่สบายเมื่อใส่คอนแทคเลนส์ (หากใส่ก่อนการผ่าตัด)
การเปลี่ยนแปลงของชั้นน้ำตา:
เวลาแตกตัวของน้ำตา (BUT ) สั้นลง (น้อยกว่า 5 วินาทีถือว่าผิดปกติ)
ค่า Schirmer ลดลง (น้อยกว่า 5 มม./5 นาที)
ความสูงของขอบน้ำตาลดลง (น้อยกว่า 0.25 มม.)
ชั้นไขมันไม่สม่ำเสมอเนื่องจากการระเหยเพิ่มขึ้น
การเปลี่ยนแปลงความรู้สึกของกระจกตา :
ความรู้สึกลดลงเมื่อวัดด้วยเครื่องวัดความรู้สึกกระจกตา Cochet-Bonnet (น้อยกว่า 45 มม.)
ลดลงมากที่สุดในช่วงต้นหลังผ่าตัด (1-3 เดือน) และฟื้นตัวภายใน 6-12 เดือน
การฟื้นตัวหลัง SMILE เร็วกว่าหลัง LASIK 4)
รูปแบบการแตกตัวของชั้นน้ำตา (TFOD):
Spot break (ชนิดขาดน้ำ): การแตกตัวเร็วแบบจุด สาเหตุหลักคือความผิดปกติของชั้นเมือกหลังการตัดเส้นประสาทกระจกตา
Line break (ชนิดน้ำตาน้อย): การแตกตัวเป็นเส้น ผลจากการหลั่งแบบรีเฟล็กซ์ลดลง
Area break: การแตกในช่วงต้นเป็นบริเวณกว้าง
กลไกหลักของตาแห้ง หลังการผ่าตัด LASIK มีดังนี้:
เมื่อสร้างแผ่นปิดกระจกตา (flap) ข่ายประสาทกระจกตา ในชั้นสโตรมาส่วนหน้า (แขนงตาจากเส้นประสาทไทรเจมินัล ) จะถูกตัดเป็นบริเวณกว้าง
สัญญาณรีเฟล็กซ์ไปยังต่อมน้ำตาผ่านเส้นประสาทไทรเจมินัล ถูกปิดกั้น → การหลั่งพื้นฐานและการหลั่งรีเฟล็กซ์ลดลง
การรับรู้ความรู้สึกของกระจกตา ลดลงทำให้รีเฟล็กซ์กระพริบตาอ่อนลง → การกระพริบตาไม่สมบูรณ์เพิ่มขึ้น → การระเหยเพิ่มขึ้น
ปริมาณน้ำตาและความคงตัวลดลง → วงจรอุบาทว์ของความเสียหายต่อเยื่อบุกระจกตา และเยื่อบุตา
การทำงานของต่อมไมโบเมียน แย่ลงชั่วคราวเนื่องจากการอักเสบหลังผ่าตัด → เพิ่มองค์ประกอบแบบระเหย
การเปรียบเทียบความเสี่ยงตามประเภทการผ่าตัด
LASIK (วิธีแผ่นปิด) : การตัดข่ายประสาทสโตรมาส่วนหน้าอย่างกว้างขวางโดยการสร้างแผ่นปิดกระจกตา อุบัติการณ์ตาแห้ง หลังผ่าตัดสูงที่สุด อุบัติการณ์ 50-90% (ระยะสั้นหลังผ่าตัด)
PRK (การกร่อนผิว) : การกร่อนใต้เยื่อบุผิว แต่เนื่องจากไม่สร้างแผ่นปิด อัตราการคงไว้ซึ่งเส้นประสาทกระจกตา จึงสูงกว่า LASIK ในระยะแรกหลังผ่าตัด มีการ缩短ของ BUT เนื่องจากการลอกของเยื่อบุผิว แต่ในระยะยาวจะรุนแรงน้อยกว่า LASIK
SMILE (การสกัดเลนส์ผ่านแผลเล็ก)กระจกตา จึงน้อยที่สุด มีรายงานว่าตาแห้ง หลังผ่าตัดรุนแรงน้อยกว่า LASIK การฟื้นตัวของเส้นประสาทหลัง SMILE รายงานว่าเร็วกว่า FS-LASIK 4)
ปัจจัยเสี่ยงก่อนผ่าตัด
ตาแห้ง ก่อนผ่าตัดตาแห้ง ก่อนผ่าตัดมีแนวโน้มว่ามีระดับความรุนแรงของตาแห้ง หลัง LASIK มากกว่าเมื่อเทียบกับผู้ป่วยที่ไม่มีตาแห้ง 2)
ผู้หญิงและผู้สูงอายุ : ปัจจัยเสี่ยงทั่วไปของตาแห้ง ยังส่งผลหลังการผ่าตัด
การแก้ไขสายตาสั้น ระดับสูง (ปริมาณการเลเซอร์มาก) : การเลเซอร์ที่ลึกขึ้นจะลดอัตราการคงไว้ของเส้นประสาทกระจกตา
ความผิดปกติของต่อมไมโบเมียน (MGD ) ก่อนผ่าตัด : มีความเสี่ยงสูงต่อตาแห้ง แบบระเหยหลังผ่าตัด
ประวัติการใส่คอนแทคเลนส์เป็นเวลานาน : ความหนาแน่นของเส้นประสาทกระจกตา ที่ลดลงและความผิดปกติของชั้นน้ำตาก่อนผ่าตัดมีแนวโน้มแย่ลงหลังผ่าตัด
ตาแห้ง หลังผ่าตัดมักเป็นรูปแบบผสม
ชนิดขาดน้ำตา (ATD) : Schirmer ต่ำ สาเหตุหลักคือการหลั่งแบบรีเฟล็กซ์ลดลงชนิดระเหยเพิ่มขึ้น (EDE) : ร่วมกับ MGD ชั้นน้ำมันไม่สม่ำเสมอ BUT สั้นลงชนิดการเปียกต่ำ (LWE ) : การหลั่งมิวซินและมิวซินเยื่อหุ้มลดลงหลังการตัดเส้นประสาทกระจกตา
การวินิจฉัยตาแห้ง จะได้รับการยืนยันหากเข้าเกณฑ์ ทั้งสองข้อ ต่อไปนี้ 2) .
มีอาการทางความรู้สึก (ไม่สบายตา, ความผิดปกติทางการมองเห็น )
ระยะเวลาแตกตัวของฟิล์มน้ำตา (BUT ) 5 วินาทีหรือน้อยกว่า
หลังการผ่าตัดแก้ไขสายตา สามารถประเมินการเปลี่ยนแปลงหลังผ่าตัดได้อย่างเป็นกลางโดยการประเมิน BUT และอาการทางความรู้สึกเป็นประจำตั้งแต่ก่อนผ่าตัด
สำหรับการวินิจฉัยภาวะตาแห้ง หลังผ่าตัด แนะนำให้ทำการตรวจดังต่อไปนี้ (เรียงตามลำดับที่มีผลกระทบต่อน้ำตาน้อยที่สุด):
รายการตรวจ สิ่งที่ประเมิน เกณฑ์ความผิดปกติ การประเมินอาการ主观 (OSDI/SPEED) ความถี่และความรุนแรงของอาการ OSDI ≥ 13 ถือว่าเล็กน้อย การสังเกตขอบน้ำตา ปริมาณน้ำตา (ด้วยกล้องจุลทรรศน์ชนิดกรีด) น้อยกว่า 0.25 มม. บ่งชี้ว่าลดลง NIBUT (ระยะเวลาการแตกตัวของฟิล์มน้ำตา แบบไม่รุกล้ำ) ความคงตัวของน้ำตา (ไม่รุกล้ำ) สั้นลง (ขึ้นอยู่กับเครื่องมือ) Fluorescein BUT (ระยะเวลาการแตกตัวของฟิล์มน้ำตา ด้วยฟลูออเรสซีน ) ความคงตัวของน้ำตา (วิธีมาตรฐาน) 5 วินาทีหรือน้อยกว่าถือว่าผิดปกติ การย้อมฟลูออเรสซีน ความผิดปกติของเยื่อบุกระจกตา และเยื่อบุตา ผลการตรวจ SPK การทดสอบ Schirmer Iปริมาณการหลั่งน้ำตา ผิดปกติหาก ≤5 มม./5 นาที การทดสอบความรู้สึกของกระจกตา (Cochet-Bonnet) การทำงานของเส้นประสาทกระจกตา ลดลงหาก ≤45 มม. การตรวจไมโบกราฟี โครงสร้างของต่อมไมโบเมียน ต่อมหายไปหรืออุดตัน
การทดสอบความรู้สึกของกระจกตา เป็นการทดสอบเฉพาะสำหรับตาแห้ง หลังการผ่าตัดแก้ไขสายตา ซึ่งมีประโยชน์ในการประเมินระดับการตัดเส้นประสาทกระจกตา หลังการผ่าตัด
สังเกตรูปแบบการแตกของชั้นน้ำตาทันทีหลังจากลืมตาเพื่อระบุชนิดย่อยของตาแห้ง ในตาแห้ง หลังการผ่าตัด มักพบการผสมของ Spot/Dimple break (ชนิดการลดความชุ่มชื้น) และ Line break (ชนิดการลดน้ำตา) ซึ่งทำให้สามารถวินิจฉัยที่เชื่อมโยงโดยตรงกับ TFOT ได้
ก่อนการผ่าตัดแก้ไขสายตา ควรประเมินสิ่งต่อไปนี้และเริ่มการรักษาภาวะตาแห้ง ก่อนผ่าตัด 3)
การให้คะแนนอาการตามอัตวิสัย เช่น OSDI (OSDI ≥ 13 เป็นเกณฑ์บ่งชี้ระดับเล็กน้อย)
ค่า BUT และ Schirmer (BUT ≤ 5 วินาที, Schirmer ≤ 5 มม./5 นาที เป็นข้อบ่งชี้ในการรักษาก่อนผ่าตัด)
Meibography และการประเมินขอบเปลือกตา (ยืนยันการมีและความรุนแรงของ MGD )
การย้อมสีกระจกตา และเยื่อบุตา (lissamine green, fluorescein)
การทดสอบความรู้สึกของกระจกตา (Cochet-Bonnet)
ระยะเวลาแตกตัวของฟิล์มน้ำตาแบบไม่รุกราน (NIBUT )
การตรวจพบและรักษาภาวะตาแห้ง อย่างจริงจังก่อนผ่าตัดช่วยปรับปรุงผลลัพธ์ทางการมองเห็น และความพึงพอใจของผู้ป่วยหลังผ่าตัด 3) โดยเฉพาะในกรณีที่มี MGD ร่วมด้วย มีรายงานว่าการรักษาก่อนผ่าตัดด้วย IPL, LipiFlow หรือการประคบอุ่นช่วยปรับปรุง OSDI และ BUT อย่างมีนัยสำคัญที่ 3 เดือนหลังผ่าตัด 3) และการปรับสภาพพื้นผิวตาก่อนผ่าตัดให้เหมาะสมเป็นหนึ่งในกลยุทธ์ที่มีประสิทธิภาพที่สุดในการป้องกันภาวะตาแห้ง หลังผ่าตัด ในแนวทางการผ่าตัดแก้ไขสายตา (ฉบับที่ 8) 1) ภาวะตาแห้ง ถือเป็นปัจจัยที่ต้องใช้ความระมัดระวัง และกลุ่มอาการตาแห้ง เป็นข้อห้ามเด็ดขาดสำหรับ SMILE
Q
หากฉันต้องการเข้ารับการผ่าตัดแก้ไขสายตา หากมีภาวะตาแห้งก่อนผ่าตัด จะไม่สามารถผ่าตัดได้หรือไม่?
A
แม้ว่าจะมีภาวะตาแห้ง ก่อนผ่าตัด ประโยชน์และความปลอดภัยของ LASIK ถือว่าเทียบเท่ากับผู้ป่วยที่ไม่มีภาวะตาแห้ง 2) อย่างไรก็ตาม ผู้ป่วยที่มีภาวะตาแห้ง ก่อนผ่าตัดมักจะมีระดับตาแห้ง ที่รุนแรงกว่าหลัง LASIK ดังนั้นจึงเป็นสิ่งสำคัญที่จะเริ่มการรักษาภาวะตาแห้ง อย่างจริงจังก่อนผ่าตัดและปรับสภาพพื้นผิวตาให้เหมาะสม ในกรณีที่มี MGD มีรายงานว่าการรักษาก่อนผ่าตัดด้วย LipiFlow หรือการประคบอุ่นช่วยปรับปรุง OSDI และ BUT อย่างมีนัยสำคัญที่ 3 เดือนหลังผ่าตัด 3)
จากสาเหตุของความไม่เสถียรของชั้นฟิล์มน้ำตาที่ระบุโดย TFOD ให้เลือกการรักษาตามชั้นที่เป็นสาเหตุ (TFOT)
ตารางการรักษาแบบแบ่งชั้น TFOT :
ชั้นเป้าหมายการรักษา วิธีการรักษา ชั้นน้ำ (ชนิดขาดน้ำตา) ยาหยอดตาไดควาโฟซอลโซเดียม, ยาหยอดตากรดไฮยาลูโรนิก, อุดจุดน้ำตา ชั้นน้ำมัน (ชนิดระเหยมากเกินไป / MGD ) ประคบอุ่น, ทำความสะอาดเปลือกตา, ไดควาโฟซอลโซเดียม (ส่งเสริมการกระจายชั้นน้ำมัน), IPL, LipiFlow มิวซินชนิดหลั่งและชนิดเยื่อหุ้ม ไดควาโฟซอลโซเดียม, รีบามิไพด์ เยื่อบุผิวและเซลล์กุณโฑ รีบามิไพด์, ยาหยอดตาซีรัมออโตโลกัส การอักเสบ (ดื้อต่อการรักษา) การใช้สเตียรอยด์ ระยะสั้น, ยาหยอดตาไซโคลสปอรีน
ลักษณะเฉพาะของตาแห้ง หลังผ่าตัดคือ ต้องระวังการเกิด “ตาแห้ง ชนิดรับความรู้สึก” (องค์ประกอบทางโภชนาการประสาท) เนื่องจากการลดลงของความรู้สึกที่กระจกตา (การตัดเส้นประสาท) หากมีความรู้สึกลดลง นอกเหนือจากการรักษามาตรฐาน TFOT แล้ว การเพิ่มการรักษาเสริมเพื่อส่งเสริมการฟื้นตัวของเส้นประสาท (เช่น กรดไขมันโอเมก้า-3, PRGF, ยาหยอดตาซีรัมออโตโลกัส) ก็มีประสิทธิภาพ 3) .
การรักษาทางเลือกแรกสำหรับตาแห้ง หลังผ่าตัดคือ น้ำตาเทียม ที่ปราศจากสารกันเสีย และยาที่กระตุ้นการผลิตมิวซิน.
ยาหยอดตาไดควาโฟซอลโซเดียม 3% (Diquas®) :
เป็นตัวกระตุ้นตัวรับ P2Y2 มีฤทธิ์สองอย่างคือ กระตุ้นการหลั่งน้ำและมิวซิน และส่งเสริมการกระจายตัวของชั้นไขมัน มีประสิทธิภาพในภาวะตาแห้ง หลังผ่าตัด และแนวทางการรักษาภาวะตาแห้ง แนะนำให้ “ปฏิบัติ” (คำแนะนำที่แข็งแกร่ง)2) ในการทดลองแบบสุ่มมีกลุ่มควบคุมในตา 61 ข้างที่เข้ารับการทำ LASIK ด้วยเลเซอร์เฟมโตวินาที มีรายงานว่าไดควาโฟซอล 3% + HA 0.15% ช่วยปรับปรุง OSDI, TBUT และชั้นไขมันได้อย่างมีนัยสำคัญเมื่อเทียบกับ HA 0.15% เพียงอย่างเดียว3)
ยาหยอดตาเรบามิไพด์ 2% (Mucosta® ยาหยอดตา UD) :
มีฤทธิ์กระตุ้นการผลิตมิวซินและต้านการอักเสบ ในการทดลองแบบสุ่มมีกลุ่มควบคุมในตา 60 ข้างที่มีภาวะตาแห้ง หลังการผ่าตัดแก้ไขสายตา มีรายงานว่าเรบามิไพด์ 4 ครั้ง/วัน ช่วยปรับปรุงค่า Schirmer, TBUT , การย้อมสีกระจกตา และดัชนีการกระเจิงแสงได้อย่างมีนัยสำคัญเมื่อเทียบกับน้ำตาเทียม 3)
ยาหยอดตาโซเดียมไฮยาลูโรเนต 0.1% / 0.3% (Hyalein®) :
ปกป้องเยื่อบุกระจกตา และรักษาความชุ่มชื้น ควรใช้รูปแบบที่ไม่มีสารกันเสีย (Hyalein Mini®) ใน TFOS DEWS III มีการยืนยันว่าสารทดแทนน้ำตาหลายชนิดที่มี HA ช่วยปรับปรุงอาการและอาการแสดงของภาวะตาแห้ง หลังผ่าตัด5)
ยาหยอดตา Diquas (3%) 6 ครั้ง/วัน
ยาหยอดตา Hyalein Mini (0.1%) เมื่อตาแห้ง / ตามต้องการ
ยาหยอดตา Mucosta UD (2%) 4 ครั้ง/วัน + Hyalein Mini (0.1%) เมื่อตาแห้ง
ในกรณีที่มีการหลั่งแบบรีเฟล็กซ์ลดลงอย่างชัดเจน ให้เลือกยาหยอดตาที่ไม่มีสารกันเสีย หากสงสัยว่ามีการอักเสบ ให้เพิ่มสเตียรอยด์ ระยะสั้น
ยาหยอดตา Hyalein Mini (0.3%) 6 ครั้ง/วัน
ยาหยอดตา Flumetholon (0.1%) 4 ครั้ง/วัน (ระยะเวลาการใช้สเตียรอยด์ ควรสั้นที่สุดเท่าที่จำเป็น)
ยาหยอดตา Diquas (3%) 6 ครั้ง/วัน
มีข้อบ่งใช้ในภาวะตาแห้ง ชนิดขาดน้ำตาที่ตอบสนองต่อการรักษาด้วยยาหยอดตาไม่เพียงพอ แนวทางการรักษาภาวะตาแห้ง แนะนำให้ “ปฏิบัติ” สำหรับ punctal plug และมีรายงานการปรับปรุงอาการก่อนและหลังการรักษาด้วย punctal plug สำหรับภาวะตาแห้ง หลัง LASIK 2)
Punctal plug ชนิดซิลิโคน : Super Eagle™ plug, Punctal Plug® F เป็นต้น ให้การอุดแบบถาวร
ปลั๊กคอลลาเจนเหลว (KeepTear®) : ปลั๊กเหลวที่ทำจากแอทีโลคอลลาเจน จะกลายเป็นเจลที่อุณหภูมิร่างกาย (36°C) และอุดท่อน้ำตา เหมาะสำหรับระยะที่ตาแห้ง กำเริบชั่วคราว เก็บในตู้เย็นที่อุณหภูมิ 2–10°C
ในตาแห้ง ชนิด BUT สั้นลง (ชนิดขาดน้ำ) การอุดจุดน้ำตาอาจเพิ่มปริมาณน้ำตาแต่ไม่ช่วยให้การมองเห็น ดีขึ้น และอาจทำให้น้ำตาไหลและตามัว สิ่งสำคัญคือต้องประเมินชนิดย่อยของตาแห้ง หลังผ่าตัดอย่างแม่นยำ และใช้เฉพาะในชนิดที่ขาดน้ำตาเท่านั้น
หากตาแห้ง หลังผ่าตัดมี MGD ร่วมด้วย ควรรักษาอย่างจริงจัง 3)
การประคบอุ่นและทำความสะอาดเปลือกตา : นวดเปลือกตาหลังประคบร้อน (40–42°C, 5–10 นาที) การดูแลพื้นฐานสำหรับ MGD
IPL (แสงพัลส์ความเข้มสูง) : การศึกษาไปข้างหน้าสองชิ้นตรวจสอบประสิทธิภาพในตาแห้ง ดื้อรักษาที่เกิดจาก LASIK (กรณีปานกลางถึงรุนแรงที่ไม่ตอบสนองต่อการรักษาทั่วไป >1 ปี) ชิ้นหนึ่ง (42 ตา) พบว่าหลัง IPL 2 ครั้ง NIBUT , OSDI, ชั้นไขมันน้ำตา และการทำงานของต่อมไมโบมดีขึ้นอย่างมีนัยสำคัญ อีกชิ้น (RCT 50 ราย) พบว่า IPL ร่วมกับหน้ากากความร้อนตาดีกว่า IPL เพียงอย่างเดียวในการปรับปรุงพารามิเตอร์ทั้ง主观และ客观 3)
ผลของการรักษา MGD ก่อนผ่าตัด : ในผู้ป่วย 32 รายที่มี MGD อยู่ก่อนแล้วก่อน LASIK การให้การรักษาด้วยคลื่นความร้อนแบบเวกเตอร์ 1 สัปดาห์ก่อน LASIK ช่วยให้ OSDI และ BUT ดีขึ้นอย่างมีนัยสำคัญที่ 3 เดือนหลังผ่าตัด 3)
ใน RCT (แบบปกปิด) ในผู้ป่วย 61 รายที่ได้รับ IPL ก่อนผ่าตัด 3 ครั้ง (ก่อนผ่าตัด, 1 สัปดาห์ และ 3 สัปดาห์หลังผ่าตัด) กลุ่ม IPL มีการปรับปรุง OSDI, NIBUT , TMH และ meibography อย่างมีนัยสำคัญที่ 3 เดือน ในขณะที่กลุ่มควบคุมมี TMH ลดลงหลังผ่าตัด ที่ 6 เดือน ความแตกต่างของ OSDI ลดลง แต่ความแตกต่างของพารามิเตอร์น้ำตาตามวัตถุประสงค์ยังคงอยู่ 3)
IPL เป็นแสงพัลส์ 532–1200 nm ฉายรอบดวงตา ทำให้เส้นเลือดฝอยอุดตันเพื่อลดการอักเสบเรื้อรังรอบต่อมไมโบมและเพิ่มการหลั่งของต่อม โดยทั่วไป 4–5 ครั้ง (ห่างกัน 3–4 สัปดาห์) เป็นหนึ่งคอร์สการรักษา แพทย์จะบีบต่อมไมโบมหลังการรักษาเพื่อเพิ่มประสิทธิภาพ ห้ามใช้หรือใช้ด้วยความระมัดระวังในโรคผิวหนังที่มีเม็ดสี, ผิวหนัง Fitzpatrick type VI, และตาที่เพิ่งผ่าตัดแก้ไขสายตา (ภายใน 4 สัปดาห์)
Q
การรักษาที่มีประสิทธิภาพสำหรับตาแห้งดื้อรักษาหลัง LASIK คืออะไร?
A
สำหรับตาแห้ง ดื้อรักษาหลัง LASIK ที่ไม่ตอบสนองต่อยาหยอดตาทั่วไป IPL, การประคบอุ่น และการรักษาด้วยคลื่นความร้อนแบบเวกเตอร์ (LipiFlow) มีประสิทธิภาพ 3) IPL ช่วยปรับปรุงการทำงานของต่อมไมโบม, NIBUT , OSDI และชั้นไขมัน การใช้ IPL ร่วมกับหน้ากากความร้อนตาดีกว่า IPL เพียงอย่างเดียว ในกรณีดื้อรักษา ยาหยอดตาซีรั่มตนเอง (PRGF) ก็เป็นทางเลือกหนึ่ง
เส้นประสาทรับความรู้สึกของกระจกตา ส่วนใหญ่ประกอบด้วยข่ายประสาทกระจกตา ที่มาจากเส้นประสาทนาโซซิเลียรี (nasociliary nerve) ซึ่งเป็นแขนงของเส้นประสาทตา (V1) ของเส้นประสาทไทรเจมินัล เส้นประสาทเหล่านี้ก่อตัวเป็นข่ายประสาทหนาแน่นในสโตรมาชั้นหน้าและทำหน้าที่นำเข้าข้อมูลรับความรู้สึกหลักของกระจกตา
ในระหว่างการสร้างแผ่นปิดในการผ่าตัดเลสิก (โดยใช้ไมโครเคราโตมหรือเลเซอร์เฟมโตวินาที ) ข่ายประสาทชั้นหน้าจะถูกตัดขาดอย่างกว้างขวางในแนวรอบวง การตัดเส้นประสาทนี้ก่อให้เกิดเหตุการณ์ต่อเนื่องดังนี้:
การขัดขวางรีเฟล็กซ์อาร์ค :
การกระตุ้นผิวกระจกตา (ทางนำเข้า) → นิวเคลียสเส้นประสาทไทรเจมินัล → เส้นประสาทพาราซิมพาเทติกไปยังต่อมน้ำตา (ทางนำออก) ถูกตัดขาด
การหลั่งน้ำตาแบบรีเฟล็กซ์ (ทั้งการหลั่งพื้นฐานและการหลั่งแบบรีเฟล็กซ์) ลดลงอย่างชัดเจน
ปริมาณน้ำตาลดลง → เยื่อบุกระจกตา และเยื่อบุตา ขาวแห้ง → เวลาการแตกตัวของฟิล์มน้ำตา (BUT ) สั้นลง
ผลต่อมิวซินชนิดเยื่อหุ้ม :
เส้นประสาทกระจกตา ยังเป็นแหล่งของปัจจัยเลี้ยงเส้นประสาทสำหรับเยื่อบุกระจกตา หลังการตัดเส้นประสาท การส่งปัจจัยเลี้ยงเส้นประสาท (เช่น EGF และ NGF) ลดลง และการแสดงออกของมิวซินชนิดเยื่อหุ้ม (MUC16) ลดลง การแสดงออกของมิวซินลดลง → ความสามารถในการเปียกน้ำลดลง → เกิด Spot/Dimple break (ตาแห้ง ชนิดความสามารถในการเปียกน้ำลดลง)
กระบวนการฟื้นฟูเส้นประสาท :
เส้นประสาทกระจกตา จะค่อยๆ ฟื้นฟูในช่วง 6 ถึง 12 เดือนหลังการผ่าตัด
หลังเลสิก การฟื้นฟูใช้เวลานานขึ้นเนื่องจากการตัดเส้นประสาท 360 องศา ในกรณีส่วนใหญ่ ประมาณ 80% จะฟื้นตัวภายในหนึ่งปี แต่บางกรณีอาจใช้เวลาหลายปี
หลัง SMILE การฟื้นฟูความหนาแน่นของเส้นประสาทจะเร็วกว่าเนื่องจากมีแผลผ่าเล็กเพียง 2-3 มม.4)
สามารถติดตามการฟื้นฟูเส้นประสาทได้อย่างเป็นกลางโดยการประเมินความหนาแน่นของเส้นประสาทกระจกตา เมื่อเวลาผ่านไปโดยใช้กล้องจุลทรรศน์คอนโฟคอล ในร่างกาย (IVCM)
หากความรู้สึกของกระจกตา ลดลงนานกว่า 6 เดือน มีความเสี่ยงที่จะเปลี่ยนเป็นโรคกระจกตา เสื่อมจากเส้นประสาท (neurotrophic keratopathy) และควรพิจารณาใช้ยาหยอดตาปัจจัยการเจริญเติบโตของเส้นประสาท (NGF)
เนื่องจาก SMILE นำเลนส์ชั้นในออกผ่านแผลขนาดเล็กเพียง 2-3 มม. การตัดเส้นประสาทในแนววงกลมจึงน้อยมาก การศึกษาเปรียบเทียบระหว่าง FS-LASIK และ SMILE รายงานว่า SMILE ส่งผลให้ความหนาแน่นของเส้นประสาทกระจกตา ฟื้นตัวเร็วขึ้นและส่งผลต่อพารามิเตอร์น้ำตาน้อยกว่าเมื่อเทียบกับ FS-LASIK 4)
การอักเสบที่เกี่ยวข้องกับการผ่าตัดทำให้การทำงานของ MGD แย่ลงชั่วคราว ส่งเสริมภาวะตาแห้ง แบบระเหย การแทรกซึมของไซโตไคน์ที่ก่อให้เกิดการอักเสบ (MMP-9, IL-1β ฯลฯ) เข้าไปในเยื่อบุตา และสโตรมาของกระจกตา หลัง LASIK มีส่วนทำให้ชั้นน้ำตาไม่เสถียร มีรายงานว่ายาหยอด cyclosporine ช่วยปรับปรุง OSDI, เวลาการแตกตัวของน้ำตา และความไวของกระจกตา หลังการผ่าตัดแก้ไขสายตาผิดปกติหลายประเภท รวมถึง LASIK อย่างมีนัยสำคัญ 3)
โดยทั่วไปการอักเสบหลังผ่าตัดจะทุเลาลงเองภายใน 1-3 เดือน แต่ในผู้ป่วยที่มีโรคเยื่อบุตาอักเสบจากภูมิแพ้ ก่อนผ่าตัด, MGD ร่วมด้วย หรือผู้ที่ตอบสนองต่อสเตียรอยด์ การอักเสบมักจะคงอยู่หรือแย่ลง หากจำเป็นต้องใช้ยาหยอดสเตียรอยด์ เป็นเวลานานหลังผ่าตัด ควรตรวจวัดความดันลูกตา อย่างสม่ำเสมอ และควรให้ความสนใจกับความสัมพันธ์กับกลุ่มอาการของเหลวที่รอยต่อ (IFS )
การเปลี่ยนแปลงรูปร่างของกระจกตา อันเนื่องมาจากการผ่าตัดแก้ไขสายตาผิดปกติอาจส่งผลต่อรูปแบบการสัมผัสระหว่างเปลือกตาบนกับกระจกตา (lid-globe apposition) ทำให้เกิดการเปลี่ยนแปลงในการกระจายและการแพร่กระจายของน้ำตา โดยเฉพาะอย่างยิ่ง การแบนของกระจกตา หลังการแก้ไขสายตาสั้น ระดับสูงอาจขัดขวางการแพร่กระจายของน้ำตา
นอกจากนี้ ความไวของกระจกตา ที่ลดลงหลังผ่าตัดทำให้รีเฟล็กซ์การกระพริบตาอ่อนลงและลดจำนวนการกระพริบตาเต็มที่ ซึ่งขัดขวางการแพร่กระจายเชิงกลของน้ำตาและการกระจายตัวของชั้นไขมัน ส่งเสริมภาวะตาแห้ง แบบระเหย การฝึกกระพริบตาเต็มที่ (การฝึกกระพริบตาเต็มที่อย่างมีสติ) เป็นหนึ่งในการดูแลตนเองที่แนะนำในการจัดการภาวะตาแห้ง หลังผ่าตัด 3)
TFOS DEWS III (2025) แนะนำให้ปรับสภาพผิวตาให้เหมาะสมก่อนและหลังการผ่าตัดแก้ไขสายตาผิดปกติที่กระจกตา เป็นการรักษามาตรฐาน 5) โดยเฉพาะอย่างยิ่ง การศึกษาระยะยาวหลายชิ้นแสดงให้เห็นว่าการแทรกแซงก่อนผ่าตัดในผู้ป่วยที่มีภาวะตาแห้ง แบบระเหย (MGD ) ช่วยปรับปรุงสภาพผิวตาและพารามิเตอร์การมองเห็น หลังผ่าตัด 3)
TFOS DEWS III ยังได้รวบรวมหลักฐานล่าสุดเกี่ยวกับสารทดแทนน้ำตารุ่นต่อไป (เช่น perfluorohexyloctane, โปรตีนจากไหม, rhPRG4 ฯลฯ) ซึ่งคาดว่าจะเป็นทางเลือกในการรักษาเพิ่มเติมนอกเหนือจากยาหยอด HA มาตรฐาน 5)
มีรายงานว่าการฉีดโบทูลินัมทอกซิน (โบท็อกซ์) เข้าที่เปลือกตาล่างด้านในช่วยปรับปรุงอาการและอาการแสดงของโรคตาแห้ง นอกจากนี้ การศึกษาหนึ่งพบว่าโบทูลินัมทอกซินช่วยปรับปรุงอาการตาแห้ง หลังการทำ LASIK ได้อย่างมีนัยสำคัญ โดยมีภาวะแทรกซ้อนน้อยกว่าการใช้ปลั๊กอุดท่อน้ำตาและยาหยอดตา ทำให้เป็นทางเลือกที่มีแนวโน้มดีในอนาคต 3) กลไกที่เสนอคือโบทูลินัมทอกซินยับยั้งการหดตัวของท่อน้ำตา ทำให้การระบายน้ำตาช้าลง และเพิ่มปริมาณน้ำตาที่คงอยู่บนผิวตา อย่างไรก็ตาม มีความเสี่ยงของผลข้างเคียง เช่น หนังตาตก และภาพซ้อน จึงจำเป็นต้องทำในสถานพยาบาลเฉพาะทาง
ในการศึกษาเปรียบเทียบย้อนหลัง (77 ตา) ในผู้ป่วยตาแห้ง หลังการทำ LASIK ยาหยอดตา PRGF ช่วยปรับปรุงการมองเห็น TBUT , OSDI, คะแนนอาการ และค่า Schirmer ได้อย่างมีนัยสำคัญเมื่อเทียบกับน้ำตาเทียม ทั่วไป 3) PRGF ประกอบด้วยปัจจัยการเจริญเติบโต (เช่น EGF และ NGF) ซึ่งอาจส่งเสริมการฟื้นตัวของเส้นประสาทกระจกตา ยาหยอดตาซีรัมออโตโลกัสเป็นยาหยอดตาทางชีวภาพที่คล้ายกันซึ่งเตรียมจากซีรัมของผู้ป่วยเอง และแสดงประสิทธิภาพสำหรับตาแห้ง ที่ดื้อต่อการรักษาซึ่งเกี่ยวข้องกับโรคเส้นประสาทกระจกตา อย่างไรก็ตาม การเตรียมและการใช้ยาหยอดตาซีรัมออโตโลกัสและ PRGF จำเป็นต้องมีการจัดการตามระเบียบปฏิบัติในสถานพยาบาลเฉพาะทาง 3)
มีข้อบ่งชี้ถึงความสัมพันธ์ระหว่างการรับประทานกรดไขมันโอเมก้า-3 และการปรับปรุงพารามิเตอร์ของเส้นประสาทกระจกตา จึงเป็นที่สนใจในฐานะตัวช่วยฟื้นฟูเส้นประสาทกระจกตา หลังการผ่าตัดแก้ไขสายตา 5) นอกจากนี้ยังมีการวิจัยเกี่ยวกับยาหยอดตาปัจจัยเลี้ยงเซลล์ประสาท (NGF) สำหรับโรคกระจกตาอักเสบจากเส้นประสาทเสื่อม และโรคเส้นประสาทกระจกตา หลังการผ่าตัด
ใน TFOS DEWS III มีการระบุว่าการบำบัดด้วยแสงระดับต่ำ (LLLT) อาจมีผลคล้ายกับ IPL สำหรับตาแห้ง ที่เกี่ยวข้องกับ MGD และกำลังถูกวิจัยในฐานะทางเลือกการรักษาใหม่ที่ไม่ต้องสัมผัสและไม่เจ็บปวด 5) LLLT ใช้แสงอินฟราเรดใกล้ (633–850 นาโนเมตร) ฉายรอบดวงตาเพื่อปรับปรุงการทำงานของต่อมไมโบเมียน และมีฤทธิ์ต้านการอักเสบและส่งเสริมการสร้างเนื้อเยื่อใหม่ การประยุกต์ใช้กับตาแห้ง หลังการผ่าตัดยังมีหลักฐานทางคลินิกจำกัด แต่คาดหวังว่าเป็นทางเลือกสำหรับผู้ป่วยที่ไม่เหมาะกับ IPL (เช่น ผู้ที่มีรอยโรคที่มีเม็ดสี) หรือผู้ที่ต้องการการรักษาที่รุกรานน้อยกว่า 5)
ในแนวทางปฏิบัติสากลของ KLEx (การสกัดเลนติคิวล์กระจกตา ผ่านแผลเล็ก) โดย Wang et al. 6) ได้ให้คำแนะนำตามหลักฐานสำหรับการจัดการผิวตาหลังการทำ SMILE โดยเน้นการประเมินตาแห้ง ก่อนการผ่าตัดและการรักษาด้วยยาหยอดตาอย่างจริงจังหลังการผ่าตัด แม้ว่า SMILE จะมีความเสี่ยงต่อตาแห้ง หลังการผ่าตัดต่ำกว่า LASIK แต่ทางที่ดีที่สุดคือควรปรับปรุงสภาพตาแห้ง ก่อนการผ่าตัดก่อนทำการผ่าตัด 6)
ใน PPP โรคกระจกตา โป่งพองของ AAO 7) มีการรับรู้ว่าภาวะตาแห้ง ที่เกิดร่วมกับโรคเส้นประสาทกระจกตา เป็นภาวะแทรกซ้อนในการจัดการภาวะกระจกตาโป่งพอง หลังผ่าตัด และจำเป็นต้องจัดการควบคู่กันระหว่างการแก้ไขสายตาเอียง ที่ไม่สม่ำเสมอ (RGP , เลนส์สเคลอรัล ฯลฯ) และการรักษาภาวะตาแห้ง เลนส์สเคลอรัลถูกจัดให้เป็นทางเลือกที่มีประสิทธิภาพทั้งในการแก้ไขสายตาเอียง ที่ไม่สม่ำเสมอและการปรับปรุงอาการตาแห้ง 7)
แบบจำลองทางคณิตศาสตร์ของ Reinstein et al. 8) แสดงให้เห็นว่า SMILE สามารถรักษาสโตรมาส่วนหน้าของกระจกตา ได้ค่อนข้างดี ความสัมพันธ์กับภาวะตาแห้ง หลังผ่าตัดจำเป็นต้องตีความไม่เพียงแค่จากแบบจำลองเชิงกลนี้เท่านั้น แต่ยังต้องรวมกับการศึกษาทางคลินิกที่เกี่ยวข้องกับเส้นประสาทกระจกตา และตัวชี้วัดน้ำตา 4, 8)
การทบทวนวรรณกรรมอย่างเป็นระบบโดย Moshirfar et al. 9) ได้รวบรวมการประเมินความเสี่ยงของภาวะกระจกตาโป่งพอง หลังผ่าตัด ในการเลือกเทคนิคการผ่าตัด การประเมินความเสี่ยงของภาวะกระจกตาโป่งพอง และการประเมินภาวะตาแห้ง ก่อนผ่าตัดจะดำเนินการแยกจากกัน และการตัดสินใจจะขึ้นอยู่กับรูปร่างกระจกตา ปริมาณการกรอ และสภาพน้ำตาอย่างครอบคลุม
ในฉันทามติระหว่างประเทศโดย Gomes et al. 10) แสดงให้เห็นว่าผู้ป่วยกระจกตา โป่งพองมีภาวะตาแห้ง ร่วมด้วยในอัตราสูง และแนะนำให้ทำการเสริมน้ำตาและการรักษาต้านการอักเสบอย่างจริงจังในการจัดการผิวตาก่อนและหลัง CXL (การเชื่อมขวางกระจกตา ) 10)
Igarashi et al. 11) รายงานในการทดลองแบบสุ่มและมีกลุ่มควบคุมในภาวะตาแห้งหลังการผ่าตัดแก้ไขสายตาผิดปกติ ที่กระจกตา ว่า ยาหยอดตารีบามิไพด์ 2% ช่วยปรับปรุงค่า Schirmer, BUT , คะแนนการย้อมสีกระจกตา และดัชนีการสะท้อนแบบกระจายได้อย่างมีนัยสำคัญเมื่อเทียบกับน้ำตาเทียม รีบามิไพด์มีฤทธิ์สองประการคือส่งเสริมการผลิตมิวซินและต้านการอักเสบ และแสดงให้เห็นว่ามีประสิทธิภาพทั้งในชนิดขาดน้ำและชนิดขาดมิวซินในภาวะตาแห้ง หลังผ่าตัด 11)
การทดลอง KERALINK โดย Larkin et al. 12) แสดงให้เห็นประสิทธิภาพของ CXL ในผู้ป่วยเด็กที่เป็นโรคกระจกตา รูปกรวย แต่ในการจัดการยาหยอดตาระหว่างการทดลอง แนะนำให้ใช้ผลิตภัณฑ์เสริมน้ำตาอย่างต่อเนื่อง ซึ่งย้ำอีกครั้งถึงความสำคัญของการจัดการร่วมกันของกระจกตา โป่งพองและภาวะตาแห้ง 12)
Santhiago et al. 13) แสดงให้เห็นว่า PTA ≥ 40% เป็นปัจจัยเสี่ยงต่อภาวะกระจกตาโป่งพอง หลังผ่าตัด เนื่องจากการกรอลึกอาจส่งผลต่อเส้นประสาทกระจกตา ได้เช่นกัน ดังนั้นในการออกแบบเทคนิคการผ่าตัด การประเมินความเสี่ยงของภาวะกระจกตาโป่งพอง และความเสี่ยงของภาวะตาแห้ง ควบคู่กันจึงเป็นเรื่องที่สมเหตุสมผล 4, 13)
ระบบคะแนนความเสี่ยงของภาวะกระจกตาโป่งพอง (ectasia) โดย Randleman และคณะ14) เป็นกรอบการประเมินรูปร่างกระจกตา ความหนาของสโตรมาที่เหลือ และระดับสายตาสั้น ก่อนการผ่าตัด นอกเหนือจากนี้ จะประเมินภาวะตาแห้ง ด้วย BUT , Schirmer และ OSDI เพื่อประมาณความเสี่ยงของภาวะแทรกซ้อนหลังผ่าตัดอย่างครอบคลุม
รายงานของ Seiler และคณะ15) เกี่ยวกับภาวะกระจกตาโป่งพอง หลังการทำ LASIK ในผู้ป่วยโรคกระจกตา รูปกรวยแบบไม่ชัดเจน (forme fruste keratoconus) เป็นรายงานแรกๆ ที่แสดงให้เห็นถึงความสำคัญของการประเมินก่อนผ่าตัดสำหรับภาวะกระจกตาโป่งพอง ที่แฝงอยู่ ความเสี่ยงของตาแห้ง ที่รุนแรงขึ้นจะถูกประเมินแยกจากความเสี่ยงของรูปร่างกระจกตา ก่อนการผ่าตัด
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第8版). 日眼会誌. 2024;128(2):135-138.
ドライアイ研究会診療ガイドライン作成委員会(島﨑潤ほか). ドライアイ診療ガイドライン. 日本眼科学会雑誌. 2019;123(5):489-592.
Jones L, Downie LE, Korb D, et al. TFOS DEWS III: Management and Therapy. Am J Ophthalmol. 2025;279:289-386.
Recchioni A, Sisó-Fuertes I, Hartwig A, et al. Short-term impact of FS-LASIK and SMILE on dry eye metrics and corneal nerve morphology. Cornea. 2020;39(7):851-857.
Jones L, Craig JP, Markoulli M, et al. TFOS DEWS III: Management and Therapy report. Am J Ophthalmol. 2025;279:289-386.
Wang Y, Xie L, Yao K, et al. Evidence-Based Guidelines for Keratorefractive Lenticule Extraction Surgery. Ophthalmology. 2025;132:397-419.
American Academy of Ophthalmology Corneal/External Disease Preferred Practice Pattern Panel. Corneal Ectasia Preferred Practice Pattern. San Francisco, CA: AAO ; 2024.
Reinstein DZ, Archer TJ, Randleman JB. Mathematical model to compare the relative tensile strength of the cornea after PRK, LASIK , and SMILE . J Refract Surg. 2013;29:454-460.
Moshirfar M, Tukan AN, Bundogji N, et al. Ectasia after corneal refractive surgery: a systematic review. Ophthalmol Ther. 2021;10:753-776.
Gomes JA, Tan D, Rapuano CJ, et al. Global consensus on keratoconus and ectatic diseases. Cornea. 2015;34:359-369.
Igarashi T, Ogawa K, Utsugi C, et al. Rebamipide ophthalmic suspension for dry eye after refractive surgery: a randomized controlled trial. Jpn J Ophthalmol. 2015;59(5):349-355.
Larkin DFP, Chowdhury K, Burr JM, et al. Effect of corneal cross-linking versus standard care on keratoconus progression in young patients: The Keralink randomized controlled trial. Ophthalmology. 2021;128:1516-1526.
Santhiago MR, Smadja D, Gomes BF, et al. Association between the percent tissue altered and post-LASIK ectasia in eyes with normal preoperative topography. Am J Ophthalmol. 2014;158:87-95.e1.
Randleman JB, Woodward M, Lynn MJ, Stulting RD. Risk assessment for ectasia after corneal refractive surgery. Ophthalmology. 2008;115:37-50.
Seiler T, Quurke AW. Iatrogenic keratectasia after LASIK in a case of forme fruste keratoconus. J Cataract Refract Surg. 1998;24:1007-1009.