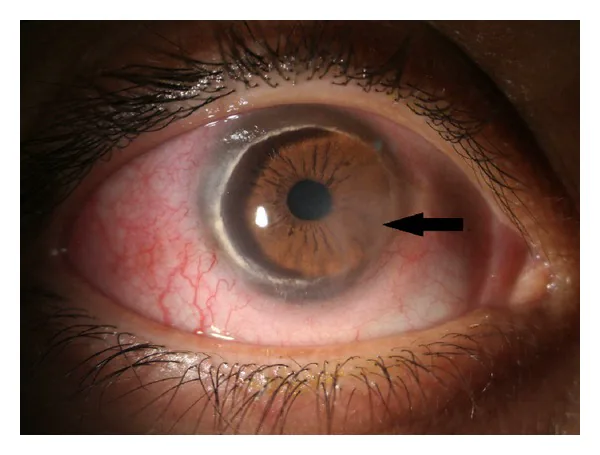
โรคกระจกตา เสื่อมขอบเทอร์เรียน (TMD) เป็นโรคเสื่อมที่พบได้ยาก ไม่มีการอักเสบ มีลักษณะกระจกตา ส่วนปลายบางลง ร่วมกับการสะสมของไขมันและเส้นเลือดฝอยที่ผิว
มักเป็นทั้งสองข้างและไม่สมมาตร พบในผู้ชายอายุมากกว่า 40 ปีบ่อยกว่าเล็กน้อย
การบางลงเริ่มจากด้านบนและค่อยๆ ลุกลามไปตามแนวเส้นรอบวง เยื่อบุกระจกตา ยังคงปกติ
ทำให้เกิดสายตาเอียง แบบ against-the-rule อย่างรุนแรง ซึ่งเป็นสาเหตุหลักของการมองเห็น ลดลง
การวิเคราะห์รูปทรงกระจกตา แสดงรูปแบบก้ามปูกลับหัว (reverse crab claw pattern) ที่มีลักษณะเฉพาะ 1) 2) แบ่งเป็นชนิดในวัยรุ่นที่มีอาการอักเสบ และชนิดทั่วไปในวัยกลางคน/สูงอายุที่ไม่มีอาการและดำเนินโรคช้า
ในกรณีที่ใกล้ทะลุ จะเลือกผ่าตัดปลูกถ่ายกระจกตา ชั้นผิวส่วนปลาย การปลูกถ่ายแผ่นแปะรูปพระจันทร์เสี้ยว หรือการปลูกถ่ายกระจกตา แบบชั้นวงแหวน 4) 11)
โรคกระจกตา เสื่อมขอบเทอร์เรียน (TMD) เป็นโรคเสื่อมที่พบได้ยาก มีลักษณะกระจกตา ส่วนปลายบางลง ร่วมกับการสะสมของไขมันและเส้นเลือดฝอยที่ผิว ดำเนินโรคช้า โดยทั่วไปไม่มีการอักเสบ เป็นทั้งสองข้างและไม่สมมาตร ในระยะแรก จะมีความขุ่นของสโตรมาแบบละเอียดเป็นรูปโค้งที่บริเวณขอบกระจกตา โดยมีบริเวณใสระหว่างความขุ่นกับลิมบัส เมื่อดำเนินโรค ขอบของบริเวณที่บางลงจะกลายเป็นรูปพัดคล้ายเปลือกหอย ร่วมกับการสะสมของไขมันและเนื้อเยื่อเกี่ยวพันเทียม เมื่อการบางลงรุนแรง สโตรมาจะอ่อนแอและโป่งออกมาด้านหน้า ทำให้เกิดสายตาเอียง แบบ against-the-rule อย่างรุนแรงหรือสายตาเอียง ไม่สม่ำเสมอ ส่งผลให้การมองเห็น ลดลง
โรคนี้ได้รับการบรรยายครั้งแรกในปี ค.ศ. 1900 โดยจักษุแพทย์ชาวฝรั่งเศส Louis-Auguste Terrien และเป็นเวลากว่าหนึ่งศตวรรษที่โรคนี้ถูกจัดให้เป็นตัวอย่างสำคัญของกระจกตา เสื่อมส่วนปลายที่มีลักษณะเด่นคือสโตรมาบางลง ยังไม่ทราบค่าความชุกที่แน่นอน แต่เป็นโรคที่พบได้ยากทั่วโลก แม้แต่จักษุแพทย์ผู้เชี่ยวชาญด้านกระจกตา ก็พบผู้ป่วยไม่มากตลอดอาชีพ การดำเนินโรคโดยทั่วไปช้า ใช้เวลาหลายปีถึงหลายสิบปีกว่าอาการจะปรากฏชัด อย่างไรก็ตาม ในระยะลุกลาม สายตาเอียง แบบ against-the-rule ทำให้เกิดปัญหาในการอ่านหนังสือและขับขี่ และไม่ค่อยทำให้กระจกตา ทะลุ ดังนั้นการติดตามระยะยาวและการแทรกแซงในเวลาที่เหมาะสมจึงมีความสำคัญ
อายุที่เริ่มป่วยมักมากกว่า 40 ปี พบในผู้ชายบ่อยกว่าเล็กน้อย อัตราส่วนชายต่อหญิงประมาณ 3:1 ในช่วงอายุ 20-40 ปี โดยมีการกระจายแบบสองยอดระหว่างผู้ป่วยทั่วไปในวัยกลางคนและผู้ป่วยที่เริ่มป่วยในวัยหนุ่มสาว 4) ในการศึกษาแบบหลายศูนย์จำนวน 25 รายโดย Chan และคณะ พบว่า 28% (7 ราย) เป็นข้างเดียว ซึ่งแก้ไขความเชื่อดั้งเดิมที่ว่าโรคนี้เป็นทั้งสองข้างเสมอ 3) รายงานผู้ป่วยอายุน้อยที่สุดคือเด็กหญิงอายุ 6 ปี 5) และ Mandal และคณะได้รายงานรายละเอียดของเด็กชายอายุ 10 ปีที่เป็น TMD ข้างเดียว 2)
ทราบชนิดทางคลินิกสองชนิด
ชนิดทางคลินิก ลักษณะเฉพาะ ชนิดทั่วไปในวัยกลางคน ไม่มีอาการ, ดำเนินช้า, ไม่มีการอักเสบ, เป็นทั้งสองข้างและไม่สมมาตร ชนิดเริ่มต้นในวัยหนุ่มสาว พบบ่อยในผู้ชายอายุ 20-30 ปี ร่วมกับเยื่อบุตาอักเสบ ชั้นนอกที่เกิดซ้ำและการอักเสบของส่วนหน้าของตา 13)
การบางลงมักเริ่มจากด้านบน แสดงความขุ่นใต้เยื่อบุผิวเล็กน้อยและความขุ่นของสโตรมาชั้นหน้า บริเวณใสยังคงอยู่ระหว่างบริเวณขุ่นและลิมบัส หลังจากความขุ่น เกิดพานนัสหลอดเลือดละเอียดที่ผิวส่วนปลาย ขยายเป็นวงกลมเป็นเวลาหลายปีถึงหลายสิบปี เส้นสีเหลืองขาวจากการสะสมไขมันปรากฏที่ขอบของการดำเนินโรค และหลอดเลือดข้ามร่องไปจนถึงปลาย การบางลงพบบ่อยที่ด้านบน แต่สามารถเกิดในทิศทางใดก็ได้ ไม่ค่อยขยายไปถึงลิมบัส ด้านล่าง ระหว่างดำเนินโรค เยื่อบุผิวยังคงสมบูรณ์ ซึ่งเป็นลักษณะเฉพาะ
ประมาณ 20% ของกรณีพบต้อเนื้อ เทียม การทะลุเองนั้นพบได้น้อย แต่ควรสังเกตว่าการทะลุสามารถเกิดขึ้นได้ง่ายจากการบาดเจ็บเล็กน้อย ในชุดของ Chan พบการทะลุของกระจกตา ใน 5 จาก 25 ตา โดย 4 ตาเป็นการทะลุเอง 3)
Q
TMD เกิดในเด็กหรือไม่?
A
TMD มักเกิดในช่วงอายุ 20-40 ปี แต่มีรายงานหลายกรณีในวัยเด็ก กรณีที่อายุน้อยที่สุดคือเด็กหญิงอายุ 6 ปีที่มีการบางของกระจกตา ตั้งแต่ตำแหน่ง 4 ถึง 8 นาฬิกา 5) Mandal และคณะรายงาน TMD ข้างเดียวในเด็กชายอายุ 10 ปีที่มีการบางของสโตรมาเป็นรูปโค้งตั้งแต่ 9 ถึง 3 นาฬิกา ร่วมกับการสะสมไขมันและเส้นเลือดใหม่ 2) ในกรณีเด็ก ความเสี่ยงต่อภาวะตาขี้เกียจ จากสายตาเอียง ไม่สม่ำเสมอสูง ดังนั้นการแก้ไขค่าสายตาตั้งแต่เนิ่นๆ และการติดตามอย่างสม่ำเสมอจึงสำคัญ 2) การทะลุเองก็สามารถเกิดขึ้นได้ในกรณีเด็ก ดังนั้นควรอธิบายความเสี่ยงต่อการทะลุและติดตามอย่างระมัดระวัง 14)
ภาพถ่ายด้วยหลอดกรีดของภาวะเสื่อมขอบกระจกตาเทอร์เรียน Vejdani AH, et al. Partial and Total Descemet’s Detachments in a Patient with Severe Terrien’s Marginal Degeneration and Juvenile Idiopathic Arthritis. Case Reports in Ophthalmological Medicine. 2014;2014:279491. Figure 1. PM
CI D: PMC4131067. License: CC BY.
ภาพถ่ายด้วยหลอดกรีดของตาขวา แสดงร่องบางเป็นวงกลม ความขุ่น การสะสมไขมัน และเส้นเลือดใหม่ในกระจกตา ส่วนปลาย รอยโรคบางที่เด่นชัดบริเวณส่วนปลายร่วมกับการสะสมไขมันและเส้นเลือดใหม่ที่ซ้อนทับ
ตามัว : อาการที่พบบ่อยที่สุด และจะแย่ลงเรื่อยๆ เมื่อสายตาเอียง ไม่สม่ำเสมอเป็นมากขึ้น โดยทั่วไปจะไม่มีอาการปวดไม่มีอาการ : ในรายที่เป็นน้อย มักไม่มีอาการอื่นนอกจากสายตาเอียง มักพบโดยบังเอิญจากการตรวจสุขภาพหรือการรักษาโรคอื่นรู้สึกมีสิ่งแปลกปลอมและปวด : ในชนิดที่เริ่มเป็นตั้งแต่อายุน้อย อาจมีอาการอักเสบเป็นซ้ำร่วมกับปวดและตาแดง 13) การมองเห็น ลดลงเฉียบพลันการมองเห็น ลดลงอย่างกะทันหันและปวดเนื่องจากการทะลุหลังได้รับบาดเจ็บเล็กน้อย3) 15)
กระจกตา ส่วนปลายบางมีบริเวณใส : ในระยะแรก จะมีบริเวณใสกว้าง 1-2 มม. อยู่ระหว่างบริเวณขุ่นและลิมบัส การสะสมของไขมัน : พบการสะสมของไขมันสีขาวเหลืองเป็นเส้นตรงที่ขอบด้านกลางของร่อง (ปลายพานนัส) หลอดเลือดพาดผ่านร่องไปจนเลยการสะสมเส้นเลือดงอกใหม่ที่ผิว (พานนัส) : เส้นเลือดเล็กๆ ยื่นจากลิมบัส ไปยังบริเวณที่บาง โดยทั่วไปจะดำเนินไปอย่างเงียบๆ โดยไม่มีการอักเสบของลิมบัส ต้อเนื้อ เทียมความสมบูรณ์ของเยื่อบุผิว : เยื่อบุกระจกตา ยังคงสมบูรณ์ไม่มีข้อบกพร่อง และไม่ติดสีฟลูออเรสซีน นี่คือความแตกต่างที่สำคัญจากแผลที่กระจกตา แบบมัวร์นและกระจกตา อักเสบแบบเป็นแผลส่วนปลายสายตาเอียง ไม่สม่ำเสมออย่างรุนแรงสายตาเอียง ไม่สม่ำเสมออย่างรุนแรง ในกรณีของ Mandal ในเด็กชายอายุ 10 ปี วัดสายตาเอียง ไม่สม่ำเสมอได้ 6.3 D และการมองเห็น ดีขึ้นจาก 20/200 เป็น 20/60 ด้วยแว่นสายตา (-6 DC ที่ 90°)2) อาการแสดงที่ไม่ปกติ : ในชนิดที่เริ่มเป็นตั้งแต่อายุน้อยร่วมกับตาแดง และเยื่อบุตาอักเสบ เหนือตาขาว การบางจะดำเนินไปพร้อมกับอาการอักเสบของส่วนหน้าของตาที่เป็นซ้ำ13) ผล AS-OCT : อาจพบแถบสะท้อนแสงสูงใต้เยื่อบุผิวรอบบริเวณที่บาง ซึ่งบ่งชี้ถึงระยะอักเสบแฝงแม้ว่าทางคลินิกจะดูไม่อักเสบ2) 6) ในกรณีของ Mandal ความหนากระจกตา บริเวณที่บางวัดได้ 305 ไมครอนทางด้านขมับและ 355 ไมครอนทางด้านจมูก2) การวัดความหนากระจกตา ซ้ำเป็นตัวบ่งชี้สำคัญในการประเมินการดำเนินโรค และมีรายงานกรณีที่ลดลง 15 ไมครอนในหนึ่งปี2)
สาเหตุหลักของการมองเห็น ลดลงคือสายตาเอียง เฉียงสูง หากสามารถแก้ไขได้ด้วยแว่นตา ผลกระทบต่อชีวิตประจำวันจะเล็กน้อย แต่เมื่อสายตาเอียง ไม่สม่ำเสมอเด่นชัดขึ้น ความคลาดเคลื่อนลำดับสูงจะเพิ่มขึ้น และผู้ป่วยเริ่มสังเกตเห็นภาพบิดเบี้ยว หรือภาพซ้อน แม้จะแก้ไขด้วยแว่นตาแล้ว การมองเห็น ตอนกลางคืนลดลง กลัวแสง และความไวต่อคอนทราสต์ลดลงเป็นอาการทั่วไปในระยะลุกลาม ในกรณีที่ตา両ข้างไม่สมมาตร ความแตกต่างของค่าสายตาระหว่างสองตาจะกว้างขึ้น ซึ่งอาจทำให้เกิดภาพไม่เท่ากัน ในเด็ก หากเกิดสายตาเอียง ไม่สม่ำเสมออย่างรุนแรงในช่วงวิกฤตของการพัฒนาการมองเห็น อาจนำไปสู่ภาวะตาขี้เกียจ ที่ไม่สามารถฟื้นคืนได้ ดังนั้นการแก้ไขค่าสายตาตั้งแต่เนิ่นๆ และการฝึกตาขี้เกียจ จึงเป็นตัวกำหนดพยากรณ์โรค 2)
ยังไม่ทราบสาเหตุที่แน่ชัด ปัจจุบันมีสองสมมติฐานที่แข่งขันกัน: ทฤษฎีต้นกำเนิดจากความเสื่อมและทฤษฎีต้นกำเนิดจากการอักเสบ 4) ทางจุลกายวิภาค พบความบกพร่องของเยื่อโบว์แมน การแตกของเยื่อเดสเซเมท และการเกิดถุงน้ำในชั้นสโตรมา ภายใต้กล้องจุลทรรศน์แบบใช้แสง พบการเสื่อมของคอลลาเจนเส้นใยใต้เยื่อบุผิว และภายใต้กล้องจุลทรรศน์อิเล็กตรอน พบสารตั้งต้นคอลลาเจน เมทริกซ์สโตรมา และการกินไขมันโดยเซลล์ฮิสทิโอไซต์ที่มีกิจกรรมไลโซโซมสูง 4) เชื่อว่ากิจกรรมไลโซโซมของเซลล์ฮิสทิโอไซต์มีส่วนในการทำลายเส้นใยคอลลาเจน ในกรณีที่เริ่มมีอาการเร็ว มีรายงานการแทรกซึมของเซลล์อักเสบรอบๆ การบุกรุกของหลอดเลือด ซึ่งบ่งชี้ถึงการมีส่วนร่วมของกลไกภูมิคุ้มกัน 13) ยังไม่มีการพิสูจน์การถ่ายทอดทางพันธุกรรมที่ชัดเจน และรายงานผู้ป่วยในครอบครัวพบน้อยมาก ไม่มีความสัมพันธ์ที่แน่นแฟ้นกับโรคทางระบบใดๆ แต่รายงานการเกิดร่วมกับโรคกระจกตา รูปกรวยและ PPCD ชี้ให้เห็นถึงพื้นฐานร่วมกันของความเปราะบางทางโครงสร้างของกระจกตา
การเกิดร่วมกับโรคกระจกตา รูปกรวย : Pouliquen และคณะรายงานกรณี TMD และโรคกระจกตา รูปกรวยเกิดขึ้นในตาเดียวกันหรือทั้งสองตาของผู้ป่วยรายเดียวกัน 7) โรคกระจกตา เสื่อมแบบหลายรูปร่างส่วนหลัง (PPCD ) : Wagoner และคณะรายงานกรณีการเกิดร่วมของ TMD และ PPCD 8) ความผิดปกติของรูปทรงกระจกตา ที่อาจเกิดขึ้นในตาตรงข้าม : Nahata และคณะรายงานหญิงอายุ 20 ปีที่มี TMD ข้างเดียว ในขณะที่ตาตรงข้ามปกติทางคลินิก (การมองเห็น 20/20) แต่การวิเคราะห์ภูมิประเทศของกระจกตา แสดงให้เห็นความชันด้านล่างและส่วนนูนด้านหลัง ซึ่งบ่งชี้ถึงการเปลี่ยนแปลงภูมิประเทศคล้ายโรคกระจกตา รูปกรวย 1) มีการเสนอความสัมพันธ์ระหว่าง TMD และสเปกตรัมของโรคกระจกตา โป่งพองมีการรายงานการเกิดร่วมกับโรคกระจกตา เสื่อมเยื่อฐานด้านหน้าและ erythema elevatum diutinum เป็นครั้งคราว
เกี่ยวข้องกับหลอดเลือดอักเสบ : Keenan และคณะรายงานกรณีโรคกระจกตา อักเสบผิวเผินส่วนปลายของ Fuchs ที่เกี่ยวข้องกับหลอดเลือดอักเสบและการพัฒนา TMD แบบไม่สมมาตร 16)
ในตา TMD ระยะลุกลาม เนื้อเยื่อจะบางลงอย่างมาก ดังนั้นแม้การบาดเจ็บเล็กน้อยก็อาจทำให้เกิดการทะลุของกระจกตา ได้ ในชุดกรณีของ Chan พบการทะลุใน 5 จาก 25 ตา 3) Chung และคณะรายงานการทะลุเองในเด็ก 14) ส่วน Srinivasan และคณะรายงานในผู้ใหญ่ 15)
ใน TMD การบาดเจ็บเล็กน้อยอาจทำให้กระจกตา ทะลุได้ ดังนั้นควรหลีกเลี่ยงกีฬาที่มีการปะทะสูง (รักบี้ มวย ศิลปะการต่อสู้ กีฬาที่ใช้ลูกบอล ฯลฯ) 2) 14) สิ่งสำคัญคือต้องตรวจตาเป็นประจำเพื่อติดตามความก้าวหน้าของการบางของกระจกตา และแก้ไขสายตาเอียง ที่แย่ลงตั้งแต่เนิ่นๆ ด้วยแว่นตาหรือคอนแทคเลนส์ ในเด็ก ควรเริ่มแก้ไขค่าสายตาโดยเร็วที่สุดเพื่อป้องกันภาวะตาขี้เกียจ จากสายตาเอียง ไม่สม่ำเสมอ 2)
การวินิจฉัย TMD เป็นการวินิจฉัยทางคลินิก และการตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด (slit-lamp) มีประโยชน์มากที่สุด การวิเคราะห์รูปทรงกระจกตา และการถ่ายภาพด้วยแสงคลื่นความถี่ร่วมของส่วนหน้าดวงตา (AS-OCT ) ช่วยเพิ่มความแม่นยำในการวินิจฉัย และช่วยในการประเมินระยะอักเสบและการวินิจฉัยแยกโรค ในปี 2021 การศึกษา Nordic Terrien degeneration ได้เสนอเกณฑ์การวินิจฉัยที่เน้นการบางส่วนปลายร่วมกับการสะสมไขมัน เส้นเลือดใหม่ที่ผิว และความสมบูรณ์ของเยื่อบุผิว 9)
การตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด
ลักษณะพื้นฐาน : ยืนยันขอบที่กำลังขยายตัวของการสะสมไขมัน ขอบด้านกลางตาชันและขอบด้านปลายตาค่อยๆ ลาด เยื่อบุผิวสมบูรณ์ และเส้นเลือดที่ผิวซึ่งยื่นจากลิมบัส ไปยังบริเวณที่บาง
ลักษณะระยะลุกลาม : การมีต้อเนื้อ เทียม (ประมาณ 20%) ขอบรูปพัดคล้ายเปลือกหอย และการคงความลึกของช่องหน้าตา ซึ่งเป็นจุดที่แตกต่างจากแผล Mooren และแผลส่วนปลายจากรูมาตอยด์
การย้อมฟลูออเรสซีน
การวิเคราะห์รูปทรงกระจกตาและ AS-OCT
รูปแบบก้ามปูกลับด้าน : แสดงการแบนของกระจกตา ส่วนปลายที่บาง และความโค้งสัมพัทธ์ของกระจกตา ที่ห่างจากจุดกึ่งกลางประมาณ 90 องศา 1) 2) ในขณะที่รูปแบบก้ามปูในภาวะกระจกตา เสื่อมขอบโปร่งแสง (PMD ) อยู่ด้านล่าง ใน TMD จะอยู่ด้านบน จึงเรียกว่า “กลับด้าน” 2)
การประเมินปริมาณสายตาเอียง เฉียง : ในกรณีของ Mandal ตรวจพบสายตาเอียง เฉียง 6.3 D 2) มีประโยชน์ในการติดตามการเปลี่ยนแปลงเมื่อเวลาผ่านไป
การประเมินระยะอักเสบด้วย AS-OCT : ในระยะสงบ จะเห็นเพียงการบางของเนื้อเยื่อเฉพาะที่ ในขณะที่ระยะอักเสบ จะปรากฏแถบสะท้อนแสงสูงใต้เยื่อบุผิวที่ติดกับบริเวณที่บาง 6) สามารถตรวจพบระยะอักเสบแฝงได้แม้ไม่มีสัญญาณการอักเสบทางคลินิก 2)
การประเมินตาข้างตรงข้าม : Nahata และคณะรายงานว่าพบรูปแบบที่ไม่สม่ำเสมอ (การเปลี่ยนแปลงคล้ายโรคกระจกตา รูปกรวย) ในการวิเคราะห์รูปร่างกระจกตา ในตาข้างตรงข้ามที่ปกติทางคลินิก และเน้นย้ำถึงความจำเป็นในการประเมินตาข้างตรงข้ามอย่างเป็นระบบแม้ในกรณีที่ดูเหมือนเป็นข้างเดียว 1)
โรคหลักที่ต้องแยกจาก TMD แสดงไว้ด้านล่าง 2) 4) การมีหรือไม่มีไขมันสะสม การมีหรือไม่มีข้อบกพร่องของเยื่อบุผิว การมีหรือไม่มีอาการปวด/อักเสบ และตำแหน่งที่พบบ่อยของกระจกตา บางเป็นจุดที่ใช้ในการแยกโรค
โรค จุดที่แตกต่างจาก TMD แผลที่กระจกตา แบบ Moorenปวด/อักเสบรุนแรง มีข้อบกพร่องของเยื่อบุผิว ขอบยื่น (overhanging edge) ไม่มีไขมันสะสม โรคกระจกตา เสื่อมชนิด Pellucid (PMD ) พบบ่อยบริเวณด้านล่างระหว่าง 4 ถึง 8 นาฬิกา ไม่มีไขมันสะสม ไม่มีเส้นเลือดใหม่ ร่องเสื่อมบริเวณขอบกระจกตา (furrow degeneration) ผู้สูงอายุ เป็นสองตา ไม่มีเส้นเลือดใหม่ ไม่ลุกลาม โรคกระจกตา อักเสบผิวเผินส่วนปลายของ Fuchs เป็นสองตา มีแถบสีเทา ไม่มีไขมันสะสม ร่วมกับเยื่อเนื้อเยื่อเกี่ยวพันเทียมและกระจกตา บาง 10) โรคกระจกตา อักเสบเป็นแผลส่วนปลายจากรูมาตอยด์ (PUK ) ร่วมกับโรคคอลลาเจน ปวด/ตาแดง /ข้อบกพร่องของเยื่อบุผิว ร่วมกับเยื่อบุตาอักเสบ เยื่อบุตาอักเสบ ที่ขอบตาจากเชื้อสแตฟิโลค็อกคัสทุติยภูมิจากเปลือกตาอักเสบ เรื้อรัง, ช่องว่างใสระหว่างสิ่งแทรกซึมกับลิมบัส เยื่อบุตาอักเสบ ส่วนปลายติดเชื้อดำเนินไปอย่างรวดเร็ว, สิ่งแทรกซึมเป็นหนอง, เกี่ยวข้องกับคอนแทคเลนส์ เดลเลน (ร่องบุ๋มกระจกตา ) การขาดน้ำเฉพาะที่บริเวณที่ฟิล์มน้ำตาขาด, เกิดขึ้นข้างต้อเนื้อ หรือตุ่มกรอง
เนื่องจาก TMD ที่เริ่มในวัยหนุ่มสาวมักมีเยื่อบุตาอักเสบ และส่วนหน้าอักเสบร่วมด้วย การแยกจากแผลที่กระจกตา แบบมัวร์นหรือ PUK ที่เกี่ยวข้องกับโรคคอลลาเจนจึงสำคัญเป็นพิเศษในกรณีที่ไม่ปกติ 13) อาจจำเป็นต้องตรวจเลือดเพื่อคัดกรองโรคคอลลาเจนและหลอดเลือดอักเสบ (แอนติบอดีต่อนิวเคลียส, รูมาตอยด์แฟกเตอร์, ANCA, HLA-B27, ซีโรโลจีซิฟิลิส ฯลฯ) ในกรณีของ Mandal และคณะ การวินิจฉัย TMD ได้รับการยืนยันหลังจากตรวจทั้งหมดต่อไปนี้และได้ผลลบ: HLA-B27, c-ANCA, p-ANCA, แอนติบอดีต่อนิวเคลียส, รูมาตอยด์แฟกเตอร์, แอนติบอดีต่อ CCP, แอนติเจน HBs, HCV, HIV 2) .
ประเด็นทางคลินิกสำหรับการวินิจฉัยแยกโรคสรุปได้ดังนี้ ประการแรก การมีอาการปวดและความบกพร่องของเยื่อบุผิว: หากไม่มีทั้งสองอย่าง มีโอกาสสูงที่จะเป็น TMD หรือภาวะเสื่อมของร่องตามวัย ประการที่สอง การมีคราบไขมันสะสม: หากมีคราบเส้นสีขาวเหลืองที่ขอบที่กำลังลุกลาม บ่งชี้ถึง TMD อย่างมาก ประการที่สาม ตำแหน่งที่พบบ่อยของกระจกตา บาง: หากเด่นด้านบน ให้คิดถึง TMD; หากเด่นด้านล่าง ให้คิดถึง PMD ; หากรอบวง ให้คิดถึง PUK ประการที่สี่ พฤติกรรมของเส้นเลือดใหม่: การแผ่ขยายอย่างเงียบๆ ของเยื่อพนัสผิวบางจากลิมบัส ไปยังบริเวณที่บางเป็นลักษณะเฉพาะของ TMD แตกต่างจากปฏิกิริยาหลอดเลือดที่มาพร้อมกับการอักเสบของแผลที่กระจกตา แบบมัวร์นที่ยังดำเนินอยู่
Q
ควรประเมินตาข้างตรงข้ามใน TMD หรือไม่?
A
ควรประเมินอย่างแน่นอน Nahata และคณะรายงานหญิงอายุ 20 ปีที่มี TMD ที่ตาขวา โดยตาข้างตรงข้ามที่ปกติทางคลินิก (สายตา 20/20) ก็พบความโค้งด้านล่างเพิ่มขึ้นและการนูนด้านหลังในการวิเคราะห์ภูมิประเทศกระจกตา บ่งชี้ถึงการเปลี่ยนแปลงภูมิประเทศคล้ายโรคกระจกตา รูปกรวย 1) แม้ในกรณีที่ถือว่าเป็น TMD ข้างเดียว ก็อาจมีความผิดปกติของรูปทรงกระจกตา ที่แฝงอยู่หรือการเปลี่ยนแปลงที่อยู่ในสเปกตรัมของโรคกระจกตา โป่งพองในตาข้างตรงข้าม แนะนำให้ติดตามผลด้วยภูมิประเทศกระจกตา ในการตรวจครั้งแรกและอย่างน้อยปีละครั้ง 1) .
เนื่องจาก TMD ดำเนินไปอย่างช้าๆ และกรณีทั่วไปไม่มีอาการ พื้นฐานของการรักษาคือ การสังเกตและการแก้ไขสายตาผิดปกติ การแทรกแซงเชิงรุกจำเป็นในกรณีที่มีการอักเสบเฉียบพลันหรือเสี่ยงต่อการทะลุ
การสังเกต : ในกรณีทั่วไปที่ไม่มีอาการ ไม่จำเป็นต้องรักษา; ติดตามการดำเนินโรคด้วยการตรวจด้วยหลอดกรีดและการวิเคราะห์ภูมิประเทศกระจกตา ทุก 6 เดือนถึง 1 ปี ความเร็วในการดำเนินโรคแตกต่างกันมากในแต่ละบุคคล; บางกรณีเกือบคงที่เป็นเวลาหลายสิบปี ในขณะที่บางกรณีถึงระดับสายตาเอียง สูงภายในไม่กี่ปีการแก้ไขด้วยแว่นตา : เป็นทางเลือกแรกสำหรับสายตาเอียง สายตาเอียง เล็กน้อยถึงปานกลางสามารถแก้ไขได้ด้วยแว่นตา ปรับปรุงค่าสายตาผ่านการตรวจวัดค่าสายตาเป็นระยะคอนแทคเลนส์ชนิดแข็งที่ซึมผ่านออกซิเจนได้ (RGP -CL) และคอนแทคเลนส์ชนิดสเคลอรัล (scleral lens) : สำหรับสายตาเอียง ไม่สม่ำเสมอระดับรุนแรงที่ไม่สามารถแก้ไขด้วยแว่นตา ให้ลองแก้ไขด้วย RGP -CL หรือคอนแทคเลนส์ชนิดสเคลอรัล 4) คอนแทคเลนส์ชนิดสเคลอรัลครอบคลุมกระจกตา ทั้งหมดและปรับการหักเหของแสง ผ่านชั้นน้ำตา จึงลดความคลาดเคลื่อนที่เกิดจากการเปลี่ยนแปลงรูปร่างที่ไม่สม่ำเสมอในส่วนรอบนอก และง่ายต่อการประยุกต์ใช้ในระยะลุกลามของ TMD อย่างไรก็ตาม ในผู้สูงอายุ ความทนทานต่อคอนแทคเลนส์มักต่ำ และในเด็กก็อาจสวมใส่ยาก 2) ยาหยอดตาหล่อลื่น : สำหรับความไม่สม่ำเสมอของผิว ใช้น้ำตาเทียม เช่น คาร์บอกซีเมทิลเซลลูโลส 0.5% ในกรณีเด็กที่รายงานโดย Mandal และคณะ การใช้ยาหยอดตาหล่อลื่นเพียงอย่างเดียวก็ช่วยบรรเทาอาการได้ 2) ยาหยอดตาสเตียรอยด์ ความเข้มข้นต่ำ : สำหรับการอักเสบที่มีเยื่อบุตา ดำแดงหรือเยื่อบุตาอักเสบ ชั้นนอก ให้ใช้ยาหยอดตาสเตียรอยด์ ความเข้มข้นต่ำ เช่น ฟลูออโรเมโธโลน 0.1% วันละสามครั้ง ในกรณีที่เริ่มมีอาการตั้งแต่อายุน้อย อาจต้องใช้ต่อเนื่องเป็นเวลานาน ดังนั้นควรระวังผลข้างเคียง เช่น ความดันลูกตา และต้อกระจก ชนิดใต้แคปซูลหลัง โดยใช้ความเข้มข้นต่ำที่สุดที่ได้ผลและระยะเวลาสั้นที่สุด
การผ่าตัดมีข้อบ่งชี้เมื่อมีการทะลุที่ใกล้จะเกิดขึ้นเนื่องจากการบางลงแบบคืบหน้า หรือเมื่อสายตาเอียง ทำให้การมองเห็น ลดลงอย่างมาก ในแนวทางปฏิบัติที่พึงประสงค์ของ AAO สำหรับกรณีที่มีการสูญเสียเนื้อเยื่อสโตรมาส่วนรอบนอกอย่างชัดเจนและสายตาเอียง เพิ่มขึ้นรวมถึง TMD แนะนำให้ปลูกถ่ายแผ่นแปะรูปพระจันทร์เสี้ยวหรือรูปวงแหวนในส่วนรอบนอก 11)
การปลูกถ่ายแผ่นแปะรูปพระจันทร์เสี้ยว (crescentic patch graft) : ปลูกถ่ายแผ่นกระจกตา หรือตาขาว (แบบชั้นหรือเต็มความหนา) ในบริเวณที่บางลง ช่วยเสริมสร้างการสูญเสียสโตรมาบางส่วนและสามารถยับยั้งการลุกลามของสายตาเอียง ในระยะยาว มีรายงานระยะยาวว่าสามารถยับยั้งการลุกลามของสายตาเอียง แบบกลับด้านรุนแรงได้นานถึง 20 ปี 4) Fernandes และคณะรายงานกรณี TMD ทั้งสองข้างที่ทะลุหลังได้รับบาดเจ็บเล็กน้อย ได้รับการปลูกถ่ายแผ่นแปะและได้การมองเห็น ที่ดี 12) การปลูกถ่ายกระจกตา แบบชั้นรูปวงแหวน (annular lamellar keratoplasty)4) เย็บกราฟต์รูปโดนัทตลอดแนวขอบตาทั้งหมดการปลูกถ่ายกระจกตา เพื่อการรักษาแบบชั้นอัตโนมัติ (ALTK)11) คอนแทคเลนส์ชนิดนิ่มเพื่อการรักษา : หากตำแหน่งที่ทะลุมีขนาดเล็ก สามารถปิดชั่วคราวด้วยกาวเนื้อเยื่อ (ไซยาโนอะคริเลต) ร่วมกับคอนแทคเลนส์ชนิดนิ่ม และวางแผนผ่าตัดแบบสองระยะการปลูกถ่ายกระจกตา แบบทะลุทะลวง (PK)กระจกตา ส่วนกลางหรือกรณีสายตาเอียง ไม่สม่ำเสมอเป็นบริเวณกว้าง อาจเลือกใช้ PK แบบเยื้องศูนย์หรือการปลูกถ่ายอัตโนมัติแบบหมุน 11) PK แบบเยื้องศูนย์เป็นเทคนิคการเย็บกราฟต์รูปวงกลมที่เลื่อนจากศูนย์กลางไปยังขอบ ทำให้สามารถตัดรอยโรคออกได้ในขณะที่หลีกเลี่ยงบริเวณรูม่านตา แต่การจัดการสายตาเอียง หลังผ่าตัดทำได้ยาก และการเลือกผู้ป่วยมีความสำคัญอย่างยิ่งการดูแลหลังผ่าตัด : ทุกขั้นตอนต้องใช้ยาหยอดตาสเตียรอยด์ เฉพาะที่เป็นระยะเวลานาน การติดตามการติดเชื้อที่เกี่ยวข้องกับไหมเย็บ และการประเมินรูปร่างของกระจกตา ที่เหลืออยู่ ไหมเย็บจะถูกตัดออกทีละน้อยในช่วงต้นหลังผ่าตัดเพื่อปรับสายตาเอียง ให้เหมาะสม และใส่คอนแทคเลนส์ชนิดแข็งซึมผ่านก๊าซ (RGP -CL) กลับเข้าไปใหม่หากจำเป็น
บริเวณรอยโรคของ TMD เยื่อบุผิวอาจมีลักษณะปกติ หนาขึ้น หรือบางลง เยื่อ Bowman มักจะหายไปหรือเสื่อมสภาพ และเยื่อ Descemet อาจพบการบางลงหรือฉีกขาด ภายในสโตรมาของรอยโรคจะเกิดถุงน้ำในสโตรมา (intra-stromal cyst) และภายใต้กล้องจุลทรรศน์แบบใช้แสงจะพบการเสื่อมของคอลลาเจนแบบเส้นใยใต้เยื่อบุผิว ผลการตรวจด้วยกล้องจุลทรรศน์อิเล็กตรอนพบสารตั้งต้นของคอลลาเจน เมทริกซ์สโตรมา และการกินไขมันโดยฮิสทิโอไซต์ที่มีกิจกรรมไลโซโซมสูง และเชื่อว่ากิจกรรมไลโซโซมของฮิสทิโอไซต์มีส่วนร่วมในการทำลายเส้นใยคอลลาเจนอย่างช้าๆ 4)
TMD ถูกมองว่าเป็นโรคเสื่อมที่ไม่มีการอักเสบมานาน แต่ Austin และคณะในปี 1981 รายงาน TMD ชนิดอักเสบที่เริ่มมีอาการในวัยหนุ่มสาว ทำให้เกิดแนวคิดเรื่องการอยู่ร่วมกันของทฤษฎีการเสื่อมและการอักเสบ 13) ในชุดผู้ป่วยหลายศูนย์โดย Chan และคณะ ได้วิเคราะห์สัดส่วนของผู้ป่วยที่มีอาการอักเสบและลักษณะการพยากรณ์โรคอย่างละเอียด แสดงให้เห็นว่าชนิดอักเสบดำเนินโรคเร็วกว่าและต้องการการผ่าตัดมากกว่าชนิดไม่อักเสบ 3)
Rodriguez และคณะแสดงให้เห็นว่า AS-OCT ความละเอียดสูงสามารถแยกแยะชนิดอักเสบและไม่อักเสบของกระจกตา ส่วนปลายบางได้ ในระยะสงบจะพบเพียงสโตรมาบางเฉพาะที่ แต่ในระยะอักเสบจะปรากฏแถบสะท้อนแสงสูงใต้เยื่อบุผิวที่ติดกับบริเวณที่บาง 6) ในผู้ป่วยเด็กของ Mandal และคณะ แม้ไม่มีอาการอักเสบทางคลินิก แต่พบแถบสะท้อนแสงสูงใต้เยื่อบุผิวใน AS-OCT ซึ่งบ่งชี้ถึงระยะอักเสบแฝงที่อาจเกิดขึ้นได้ 2) ผลการตรวจนี้ใช้ในการกำหนดกลยุทธ์การรักษา (การบ่งชี้การใช้ยาหยอดตาสเตียรอยด์ ) และการพยากรณ์โรค
ใน TMD ส่วนที่บางของกระจกตา จะแบนลง และเกิดความโค้งสัมพัทธ์ในทิศทางตั้งฉาก 90 องศา ทำให้เกิดสายตาเอียง แบบเฉียงอย่างรุนแรง การเปลี่ยนแปลงนี้ปรากฏในการวิเคราะห์รูปร่างกระจกตา เป็นรูปแบบก้ามปูกลับหัว 1) 2) ในขณะที่รูปแบบก้ามปูใน PMD อยู่บริเวณส่วนล่าง ใน TMD รอยโรคมักอยู่บริเวณส่วนบน จึงเรียกว่า “กลับหัว” 2) ในระยะลุกลาม ส่วนที่บางจะโป่งออกมาด้านหน้าอย่างชัดเจน และสายตาเอียง ไม่สม่ำเสมอก็แก้ไขได้ยาก
เดิมทีเชื่อว่า TMD ทำให้เกิดการทะลุเองได้น้อย แต่ในกรณีลุกลามที่มีการบางของสโตรมาอย่างมาก การทะลุอาจเกิดขึ้นได้ง่ายจากการบาดเจ็บเล็กน้อย (เช่น การขยี้ตา การกระแทกทื่อ หรือการใส่/ถอดคอนแทคเลนส์) ในชุดรายงานของ Chan และคณะ พบการทะลุใน 5 จาก 25 ตา และในจำนวนนี้ 4 ตาเป็นการทะลุเองโดยไม่มีสาเหตุจากการบาดเจ็บที่ชัดเจน 3) Chung และคณะรายงานกรณีเด็กที่มี TMD ซึ่งเกิดการทะลุเอง 14) และ Srinivasan และคณะรายงานกรณีผู้ใหญ่ที่มีอาการเริ่มต้นคือการทะลุเอง 15) ในกรณีที่ความหนาของส่วนที่บางลดลงเหลือประมาณ 100 ไมครอน ความเสี่ยงต่อการทะลุจะเพิ่มขึ้นอย่างรวดเร็ว ดังนั้นการติดตามเชิงปริมาณด้วย AS-OCT และการตัดสินใจผ่าตัดตั้งแต่เนิ่นๆ จึงเป็นสิ่งสำคัญ
Q
จะแยก TMD ออกจากแผลที่กระจกตาแบบ Mooren ได้อย่างไร?
A
TMD ไม่เจ็บปวด เยื่อบุผิวสมบูรณ์ และมีไขมันสะสมและเส้นเลือด新生ที่ผิวบริเวณขอบที่ลุกลาม ในทางตรงกันข้าม แผลที่กระจกตา แบบ Mooren จะมีอาการปวดและตาแดง มีข้อบกพร่องของเยื่อบุผิว และมีลักษณะเด่นคือขอบที่ยื่นออกมา (overhanging edge) ใน TMD มักไม่มีการอักเสบของส่วนหน้าของตา และการบางจะดำเนินไปอย่างช้าๆ ในระยะเวลาหลายปี อย่างไรก็ตาม มีชนิดย่อยในผู้ป่วยอายุน้อยที่อาจมี episodes การอักเสบร่วมด้วย 13) และในกรณีที่ไม่ปกติ การตรวจเลือดเพื่อคัดกรองโรคคอลลาเจนและหลอดเลือดอักเสบ รวมถึงการประเมินการอักเสบด้วย AS-OCT มีประโยชน์ในการวินิจฉัยแยกโรค 2) 6)
การศึกษา Nordic Terrien degeneration study ปี 2021 ได้เสนอเกณฑ์การวินิจฉัยสำหรับ TMD ซึ่งก่อนหน้านี้ยังไม่เป็นมาตรฐานเดียวกัน และได้กำหนดเกณฑ์ทางคลินิกที่เน้นการสะสมไขมัน เส้นเลือด新生ที่ผิว และความสมบูรณ์ของเยื่อบุผิว 9) การทำให้เกณฑ์การวินิจฉัยเป็นมาตรฐานคาดว่าจะช่วยอำนวยความสะดวกในการลงทะเบียนผู้ป่วยจากหลายสถาบันและการออกแบบการศึกษาแบบติดตามไปข้างหน้า การใช้ AS-OCT ความละเอียดสูงเพื่อแยกแยะระยะอักเสบและระยะสงบกำลังถูกนำมาใช้ในการตัดสินใจรักษามากขึ้น และกลายเป็นเครื่องมือที่มั่นคงในการตรวจหาการอักเสบที่ซ่อนอยู่ซึ่งอาจตรวจไม่พบด้วยการตรวจด้วย slit-lamp ทั่วไป 6)
เลนส์สเคลอรัลเป็นทางเลือกที่ไม่ต้องผ่าตัดที่มีแนวโน้มดีสำหรับสายตาเอียง ไม่ปกติระดับรุนแรง เนื่องจากเลนส์จะข้ามกระจกตา ส่วนกลางและดูดซับผลกระทบทางการหักเหจากส่วนรอบนอกที่บาง 4) เลนส์ RGP ขนาดใหญ่และเลนส์ไฮบริดก็เป็นทางเลือกเช่นกัน และกำลังถูกพิจารณาอย่างจริงจังเพื่อหลีกเลี่ยงการผ่าตัด การเชื่อมขวางกระจกตา (CXL ) บริเวณรอบนอกกำลังถูกอภิปรายเพื่อประยุกต์ใช้กับ TMD แต่หลายกรณีมีความหนากระจกตา ต่ำกว่าที่กำหนด (400 ไมครอนขึ้นไป) จึงจำกัดการใช้งาน การปลูกถ่ายกระจกตา ที่สร้างขึ้นทางวิศวกรรมชีวภาพเพื่อเสริมสร้างโครงสร้าง การประยุกต์ใช้ทางคลินิกของเนื้อเยื่อผู้บริจาคที่กำจัดเซลล์ออก และโครงร่างรูปพระจันทร์เสี้ยวที่พิมพ์ด้วยเครื่องพิมพ์ 3 มิติ อาจเป็นหัวข้อวิจัยในอนาคต แต่ปัจจุบันยังไม่มีการทดลองแบบสุ่มที่มีกลุ่มควบคุมขนาดใหญ่สำหรับ TMD และหลักฐานในปัจจุบันขึ้นอยู่กับชุดผู้ป่วยและการศึกษาแบบย้อนหลัง การวินิจฉัยตั้งแต่เนิ่นๆ การให้ความรู้ผู้ป่วย การติดตามความคืบหน้า และการผ่าตัดอย่างทันท่วงทียังคงเป็นเสาหลักของการจัดการทางคลินิก
เนื้อหาในบทความนี้มีวัตถุประสงค์เพื่อให้ข้อมูลแก่ผู้เชี่ยวชาญทางการแพทย์เท่านั้น และไม่ใช่พื้นฐานสำหรับการวินิจฉัยหรือการรักษาเฉพาะบุคคล การตัดสินใจทางคลินิกควรทำโดยแพทย์ผู้รักษาตามสภาพของผู้ป่วย
Nahata H, Nagaraja H, Shetty R. Topographic changes in contralateral eye of a case of Terrien’s marginal degeneration. BMJ Case Rep. 2022;15:e249493. doi:10.1136/bcr-2022-249493
Mandal S, Sachdeva G, Nagpal R, Maharana PK. Early onset unilateral Terrien’s marginal degeneration. BMJ Case Rep. 2022;15:e248889. doi:10.1136/bcr-2022-248889
Chan AT, Ulate R, Goldich Y, et al. Terrien marginal degeneration: clinical characteristics and outcomes. Am J Ophthalmol. 2015;160:867-872.
Ding Y, Murri MS , Birdsong OC, et al. Terrien marginal degeneration. Surv Ophthalmol. 2019;64:162-174.
Vest A, Jean-Charles A, Bechet L, et al. Terrien’s marginal corneal degeneration in a six-year-old girl: A case report. J Fr Ophtalmol. 2018;41:e433-e435.
Rodriguez M, Yesilirmak N, Chhadva P, et al. High-Resolution optical coherence tomography in the differentiation of inflammatory versus noninflammatory peripheral corneal thinning. Cornea. 2017;36:48-52.
Pouliquen Y, Renard G, Savoldelli M. Keratoconus associated with Terrien’s marginal degeneration. A clinical and ultrastructural study. Acta Ophthalmol Suppl. 1989;192:174-181.
Wagoner MD, Teichmann KD. Terrien’s marginal degeneration associated with posterior polymorphous dystrophy. Cornea. 1999;18:612-615.
Ruutila M, Fagerholm P, Lagali N, et al. Diagnostic criteria for Terrien marginal degeneration: Nordic Terrien degeneration study. Cornea. 2021;40:133-141.
Harada S, Mohamed YH, Kusano M, Inoue D, Uematsu M. Bilateral Fuchs’ Superficial Marginal Keratitis Diagnosis and Treatment. Life (Basel). 2024;14(12):1644. doi:10.3390/life14121644.
American Academy of Ophthalmology. Preferred Practice Pattern: Corneal Edema and Opacification. San Francisco, CA: American Academy of Ophthalmology; 2018.
Fernandes M, Vira D. Patch graft for corneal perforation following trivial trauma in bilateral Terrien’s marginal degeneration. Middle East Afr J Ophthalmol. 2015;22:255-257.
Austin P, Brown SI. Inflammatory Terrien’s marginal corneal disease. Am J Ophthalmol. 1981;92:189-192.
Chung J, Jin KH, Kang J, et al. Spontaneous corneal perforation in Terrien’s marginal degeneration in childhood: a case report. Medicine (Baltimore). 2017;96:e9095.
Srinivasan S, Murphy CC, Fisher AC, et al. Terrien marginal degeneration presenting with spontaneous corneal perforation. Cornea. 2006;25:977-980.
Keenan JD, Mandel MR, Margolis TP. Peripheral ulcerative keratitis associated with vasculitis manifesting asymmetrically as Fuchs superficial marginal keratitis and Terrien marginal degeneration. Cornea. 2011;30:825-827.