Grado I
Diametro < 5 mm: lesione superficiale limitata al limbo.
Profondità di infiltrazione: limitata a circa metà dello stroma corneale.

Il dermoide corneale (corneal dermoid) è un tumore benigno congenito della cornea, del limbo e della congiuntiva. Si tratta di un coristoma, cioè una proliferazione ectopica di tessuto cutaneo normale nella cornea o nella congiuntiva, chiamato anche dermoide limbare. Un coristoma è un tumore costituito da tessuto normale in sede anomala.
L’incidenza nei neonati è di 1-3:10.000, rappresentando il 25% delle lesioni orbitarie congenite 2). Il dermoide limbare è il più frequente, specialmente al limbo inferotemporale. Di solito è unilaterale, non ereditario e si verifica sporadicamente. Dopo la nascita, le dimensioni rimangono generalmente stabili. Il diametro varia da 3 mm a 10 mm per quelli più grandi.
Il dermoide corneale e la cisti dermoide orbitaria sono entità completamente diverse e non vanno confuse.
Il dermoide corneale è un tumore benigno congenito (coristoma) e non sono stati riportati casi di trasformazione maligna. Dopo la nascita è una lesione non proliferativa le cui dimensioni generalmente non cambiano. Tuttavia, può causare ambliopia o problemi estetici, quindi è importante un follow-up regolare.
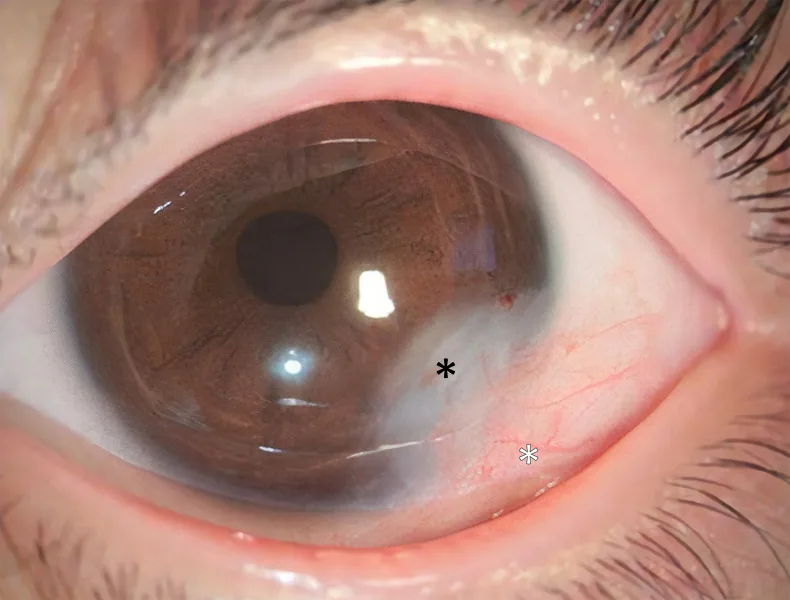
Il dermoide corneale è un tumore solido, bianco, emisferico, a margini netti, che predilige il limbo corneale inferotemporale. Il colore varia dal bianco latte al marrone chiaro e sulla superficie possono essere presenti peli. La superficie del dermoide è cheratinizzata come la pelle, quindi le lacrime rimbalzano in quel punto.
Astigmatismo obliquo e ambliopia da anisometropia ipermetropica sono associati in circa 2/3 dei casi. La bilateralità si osserva nel 10-25% di tutti i dermoidi della superficie oculare5).
Una classificazione in tre gradi si basa sui reperti clinici e dell’OCT del segmento anteriore (AS-OCT)5).
Grado I
Diametro < 5 mm: lesione superficiale limitata al limbo.
Profondità di infiltrazione: limitata a circa metà dello stroma corneale.
Grado II
Lesione di grandi dimensioni: copre la maggior parte della cornea e raggiunge lo stroma profondo fino alla membrana di Descemet.
Caratteristica: la membrana di Descemet stessa non è infiltrata.
Grado III
Gravissimo : Ricopre l’intera cornea, estendendosi dalla superficie anteriore del bulbo oculare fino all’epitelio pigmentato dell’iride.
Frequenza : È il tipo più raro.
Il dermoide corneale è causato da un’anomalia di sviluppo del primo e secondo arco branchiale durante il periodo embrionale. Una displasia dell’ectoderma che forma la cornea e la congiuntiva porta a una migrazione aberrante del tessuto cutaneo nella cornea e nella congiuntiva, formando un dermoide. La maggior parte dei casi è sporadica, ma può verificarsi in associazione con le seguenti sindromi.
Sindrome che associa un dermoide limbico a orecchie accessorie, fistole auricolari, ipoplasia mandibolare e anomalie vertebrali. Si verifica con una frequenza di 1 su 3.000-5.000 nati, con un rapporto maschi-femmine di 3:21). La maggior parte dei casi è sporadica. Diabete materno, ipertensione, infezioni virali (influenza, rosolia), esposizione a cocaina, tamoxifene e acido retinoico sono stati riportati come fattori predisponenti1).
Se viene identificato un dermoide limbico, è necessario eseguire un esame sistemico per verificare la presenza della sindrome di Goldenhar.
Il dermoide corneale (dermoide limbico) può essere una manifestazione oculare della sindrome di Goldenhar. La sindrome di Goldenhar è una malattia congenita che comprende orecchie accessorie, fistole auricolari, ipoplasia mandibolare e anomalie vertebrali, con un’incidenza di 1 su 3.000-5.000 nati1). In presenza di un dermoide limbico, è importante eseguire un esame sistemico per verificare queste associazioni.
La diagnosi di dermoide corneale si basa principalmente sui reperti clinici e generalmente non è necessaria una biopsia. Se è disponibile un campione di resezione, l’esame istopatologico può confermare la diagnosi.
In caso di sospetta sindrome di Goldenhar, si raccomanda una valutazione multidisciplinare che includa ORL e pediatria. Sono raccomandati esami audiometrici, TC cranica, radiografia della colonna vertebrale, ecografia cardiaca e renale 1).
La cosa più importante nel dermoide corneale è la prevenzione e il trattamento dell’ambliopia. La chirurgia non corregge l’astigmatismo, quindi non è un trattamento per l’ambliopia. Prima dell’intervento è necessario iniziare la correzione refrattiva (occhiali) e l’occlusione dell’occhio sano per il trattamento dell’ambliopia.
Per i dermoidi di grado I con astigmatismo inferiore a 1 D e minima irregolarità superficiale, è appropriato un follow-up conservativo. Gli esami regolari vengono eseguiti ogni 6-12 mesi, valutando l’acuità visiva, le dimensioni della lesione e la rifrazione in cicloplegia.
La chirurgia è puramente estetica e in linea di principio non vi è indicazione per un intervento precoce. La chirurgia viene presa in considerazione nei seguenti casi:
La tecnica chirurgica viene scelta in base al grado.
| Grado | Tecnica raccomandata |
|---|---|
| Grado I (superficiale) | Escissione + cheratoplastica superficiale |
| Grado II | Cheratoplastica lamellare profonda (DALK) ± innesto di membrana amniotica |
| Grado III | Ricostruzione completa del segmento anteriore |
Dopo l’escissione del tumore, si esegue una cheratoplastica superficiale. La semplice escissione da sola porta frequentemente a recidive o pseudo-pterigio. L’innesto non deve essere di cornea fresca; è sufficiente una cornea conservata con congelamento. Il diametro del trepano è solitamente di circa 7,0 mm. La sutura viene eseguita con punti staccati in nylon 10-0, circa 12 punti. Se rimane tessuto tumorale residuo, può verificarsi una forte reazione infiammatoria postoperatoria o pseudo-pterigio, quindi è necessario cercare di ottenere un’escissione completa.
Abdulmannan et al. (2022) hanno riportato i risultati della gestione di 5 casi di dermoide limbico in neonati e bambini. 4 casi presentavano astigmatismo ≥1D, ma l’astigmatismo non è migliorato dopo l’intervento; il miglioramento visivo è stato principalmente dovuto all’uso di occhiali e all’occlusione dell’occhio sano 6).
La rimozione del dermoide con l’intervento chirurgico non migliora l’astigmatismo. L’intervento ha uno scopo estetico e non è un trattamento per l’ambliopia. Per l’ambliopia dovuta ad astigmatismo, sono necessari la correzione refrattiva con occhiali e la terapia di occlusione dell’occhio sano. È stato riportato che l’astigmatismo non cambia o tende ad aumentare leggermente dopo l’intervento 6).
L’intervento per il dermoide corneale ha uno scopo estetico e, in linea di principio, non vi è indicazione per un intervento precoce. I dermoidi che coprono l’area pupillare richiedono un intervento precoce, ma se sono limitati al limbo e non aumentano, viene eseguito dopo la prima infanzia. L’intervento nei bambini piccoli richiede l’anestesia generale.
Esistono diverse ipotesi sul meccanismo di formazione del dermoide corneale. Una suggerisce che derivi da una trasformazione metaplastica delle cellule mesodermiche tra il bordo della coppa ottica e l’ectoderma superficiale nelle fasi iniziali dello sviluppo. Un’altra ipotesi propone la sequestrazione di cellule pluripotenti durante l’embriogenesi delle strutture oculari circostanti.
Il dermoide, come tumore da inclusione, è composto da tessuti di derivazione ectodermica (capelli, pelle, raramente denti) e tessuti di derivazione mesodermica (tessuto adiposo, cartilagine). Istologicamente, mostra una struttura simile all’epidermide e al derma, comprendente tessuto connettivo collageno, follicoli piliferi e ghiandole sebacee.
Il tessuto dermoide stesso non ha attività proliferativa.
Mitamura et al. (2021) hanno riportato una crescita simil-pterigio contenente tessuto dermoide residuo in una donna giapponese di 79 anni che aveva subito l’escissione di un dermoide limbare all’età di 12 anni. All’immunoistochimica, Ki67 (marcatore di proliferazione cellulare) era positivo nelle cellule epiteliali dello pterigio e nelle cellule endoteliali dei neovasi, ma negativo nei componenti dermoidi (tessuto adiposo, tessuto connettivo, nervi periferici) 3). Il tessuto dermoide residuo dopo escissione incompleta non ha capacità proliferativa, ma potrebbe agire come fattore modificante nello sviluppo dello pterigio.
Questo rapporto sottolinea l’importanza dell’escissione completa e conferma che il tessuto dermoide stesso è una lesione congenita non proliferativa.
Poddi et al. (2025) hanno riportato una tecnica chirurgica per il dermoide limbare di grado I, consistente in escissione seguita da applicazione di mitomicina C (0,02%) e trapianto di membrana amniotica a tre strati fissato con colla di fibrina. In una donna di 18 anni, non si è verificata recidiva durante un follow-up di due anni, con normalizzazione della topografia corneale, riduzione delle aberrazioni di ordine superiore e miglioramento della migliore acuità visiva corretta 2).
Per un dermoide gigante della superficie corneale e oculare (17×14 mm), Choudhary et al. (2021) hanno riportato una tecnica che combina DALK pre-descemetica (cheratoplastica lamellare anteriore profonda) e SLET (trasferimento epiteliale limbare semplice) dall’occhio controlaterale. Ciò ha prevenuto la formazione di pseudo-pterigio ottenendo un risultato estetico soddisfacente 4).
È stata riportata anche la cheratoplastica lamellare utilizzando lenticoli estratti con chirurgia SMILE, che sta attirando attenzione come tecnica che non richiede cornea da donatore.
Fu et al. (2024) hanno eseguito il sequenziamento completo dell’esoma (WES) su un bambino di 4 anni con sindrome di Goldenhar e hanno identificato cinque mutazioni geniche (PRDM16, FAT4, POLR1C, PLEC, MED12) potenzialmente associate a microtia 1). La chiarificazione delle basi genetiche della sindrome di Goldenhar potrebbe contribuire alla futura diagnosi e prevenzione.
- Fu Y, Yu H, Zhang J, Zhou N. Goldenhar syndrome with limbal neoformation, microtia and skeletal deformities: a case report and literature review. BMC Ophthalmol. 2024;24:81.
- Poddi M, Romano V, Borgia A, et al. Combined Multilayered Amniotic Membrane Graft and Fibrin Glue as a Surgical Management of Limbal Dermoid Cyst. J Clin Med. 2025;14:607.
- Mitamura M, Kase S, Ohguchi T, Ishida S. A case of pterygium-like proliferation containing postoperative limbal dermoid remnants: a clinicopathological study. BMC Ophthalmol. 2021;21:12.
- Juneja A, Puthalath AS, Gupta N, Verma PK. Isolated bilateral limbal dermoid, preauricular skin tags and ametropic amblyopia. BMJ Case Rep. 2021;14:e245078.
- Abdulmannan DM. Successful Management of Limbal Dermoid in Infancy and Childhood: A Case Series. Cureus. 2022;14(3):e22835.