Grade I
Diamètre < 5 mm : lésion superficielle limitée au limbe.
Profondeur d’infiltration : limitée à environ la moitié du stroma cornéen.

Le dermoïde cornéen (corneal dermoid) est une tumeur bénigne congénitale de la cornée, du limbe ou de la conjonctive. Il s’agit d’un choristome, c’est-à-dire une prolifération ectopique de tissu cutané normal dans la cornée ou la conjonctive, également appelé dermoïde limbique. Un choristome est une tumeur constituée de tissu normal présent dans un site anormal.
L’incidence chez les nouveau-nés est de 1 à 3 pour 10 000, représentant 25 % des lésions orbitaires congénitales 2). Le dermoïde limbique est le plus fréquent, surtout au niveau du limbe inférotemporal. Il est généralement unilatéral, non héréditaire et survient de façon sporadique. Après la naissance, sa taille reste généralement stable. Le diamètre varie de 3 mm à 10 mm pour les plus grands.
Il est important de ne pas confondre le dermoïde cornéen avec le kyste dermoïde orbitaire, qui sont des entités totalement différentes.
Le dermoïde cornéen est une tumeur bénigne congénitale (choristome) et aucun cas de transformation maligne n’a été rapporté. Après la naissance, il s’agit d’une lésion non proliférative dont la taille ne change généralement pas. Cependant, il peut entraîner une amblyopie ou des problèmes esthétiques, d’où l’importance d’un suivi régulier.
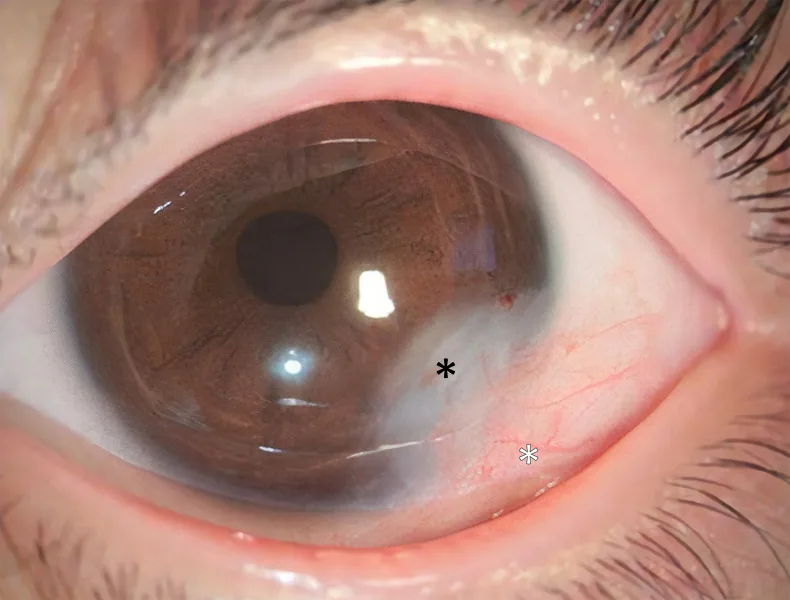
Le dermoïde cornéen est une tumeur solide, blanche, hémisphérique, bien délimitée, siégeant de préférence au niveau du limbe cornéen inférotemporal. Sa couleur va du blanc laiteux au brun clair et des poils peuvent être présents à sa surface. La surface du dermoïde est kératinisée comme la peau, de sorte que les larmes perlent à cet endroit.
Un astigmatisme oblique et une amblyopie par anisométropie hypermétrope sont associés dans environ 2/3 des cas. La bilatéralité est observée dans 10 à 25 % de l’ensemble des dermoïdes de la surface oculaire5).
Une classification en trois stades est basée sur les données cliniques et de l’OCT du segment antérieur (AS-OCT)5).
Grade I
Diamètre < 5 mm : lésion superficielle limitée au limbe.
Profondeur d’infiltration : limitée à environ la moitié du stroma cornéen.
Grade II
Lésion de grande taille : recouvre la majeure partie de la cornée et atteint la couche stromale profonde jusqu’à la membrane de Descemet.
Caractéristique : la membrane de Descemet elle-même n’est pas envahie.
Grade III
Très sévère : Recouvre toute la cornée, s’étendant de la surface antérieure du globe jusqu’à l’épithélium pigmenté de l’iris.
Fréquence : C’est le type le plus rare.
Le dermoïde cornéen résulte d’une anomalie de développement des premier et deuxième arcs branchiaux pendant la période embryonnaire. Une dysplasie de l’ectoderme formant la cornée et la conjonctive entraîne une migration aberrante du tissu cutané vers la cornée et la conjonctive, formant un dermoïde. La plupart des cas sont sporadiques, mais ils peuvent survenir en association avec les syndromes suivants.
Syndrome associant un dermoïde limbique à des oreilles accessoires, des fistules auriculaires, une hypoplasie mandibulaire et des anomalies vertébrales. Il survient chez 1 naissance sur 3 000 à 5 000, avec un ratio homme-femme de 3:21). La plupart des cas sont sporadiques. Le diabète maternel, l’hypertension, les infections virales (grippe, rubéole), l’exposition à la cocaïne, au tamoxifène ou à l’acide rétinoïque ont été rapportés comme facteurs prédisposants1).
Lorsqu’un dermoïde limbique est identifié, un examen systémique doit être réalisé pour vérifier la présence d’un syndrome de Goldenhar.
Le dermoïde cornéen (dermoïde limbique) peut être une manifestation oculaire du syndrome de Goldenhar. Le syndrome de Goldenhar est une maladie congénitale associant des oreilles accessoires, des fistules auriculaires, une hypoplasie mandibulaire et des anomalies vertébrales, avec une incidence de 1 naissance sur 3 000 à 5 0001). En présence d’un dermoïde limbique, il est important de réaliser un examen systémique pour vérifier ces associations.
Le diagnostic du dermoïde cornéen repose principalement sur les signes cliniques et une biopsie n’est généralement pas nécessaire. Si un spécimen de résection est disponible, un examen histopathologique peut confirmer le diagnostic.
En cas de suspicion de syndrome de Goldenhar, une évaluation multidisciplinaire incluant ORL et pédiatrie est recommandée. Des examens tels que l’audiométrie, la TDM cérébrale, la radiographie du rachis, l’échographie cardiaque et rénale sont recommandés 1).
Le plus important dans le dermoïde cornéen est la prévention et le traitement de l’amblyopie. La chirurgie ne corrige pas l’astigmatisme et ne traite donc pas l’amblyopie. Il est nécessaire de commencer la correction réfractive (lunettes) et l’occlusion de l’œil sain avant la chirurgie.
Pour les dermoïdes de grade I avec un astigmatisme inférieur à 1 D et une irrégularité de surface minimale, une observation conservatrice est appropriée. Des examens réguliers sont effectués tous les 6 à 12 mois pour évaluer l’acuité visuelle, la taille de la lésion et la réfraction sous cycloplégie.
La chirurgie est purement esthétique et n’est généralement pas indiquée en urgence. La chirurgie est envisagée dans les cas suivants :
La technique chirurgicale est choisie en fonction du grade.
| Grade | Technique recommandée |
|---|---|
| Grade I (superficiel) | Excision + greffe de cornée superficielle |
| Grade II | Kératoplastie lamellaire profonde (DALK) ± greffe de membrane amniotique |
| Grade III | Reconstruction complète du segment antérieur |
Après l’excision de la tumeur, une greffe de cornée superficielle est réalisée. Une simple excision seule entraîne fréquemment des récidives ou un pseudo-ptérygion. Le greffon n’a pas besoin d’être de la cornée fraîche ; une cornée conservée par congélation convient. Le diamètre du trépan est généralement d’environ 7,0 mm. La suture est réalisée avec du nylon 10-0 en points séparés, environ 12 points. Comme une tumeur résiduelle peut provoquer une forte réaction inflammatoire postopératoire ou un pseudo-ptérygion, il faut s’efforcer de réaliser une excision complète.
Abdulmannan et al. (2022) ont rapporté les résultats de la prise en charge de 5 cas de dermoïde limbique chez les nourrissons et les enfants. 4 cas présentaient un astigmatisme ≥ 1D, mais l’astigmatisme ne s’est pas amélioré après la chirurgie ; l’amélioration de l’acuité visuelle était principalement due au port de lunettes et à l’occlusion de l’œil sain 6).
L’ablation du dermoïde par chirurgie n’améliore pas l’astigmatisme. La chirurgie a un but esthétique et ne traite pas l’amblyopie. Pour l’amblyopie due à l’astigmatisme, une correction réfractive par lunettes et une occlusion de l’œil sain sont nécessaires. Il a été rapporté que l’astigmatisme ne change pas ou a tendance à augmenter légèrement après la chirurgie 6).
La chirurgie du dermoïde cornéen a un but esthétique et, en principe, il n’y a pas d’indication pour une chirurgie précoce. Les dermoïdes recouvrant la zone pupillaire nécessitent une chirurgie précoce, mais s’ils sont limités au limbe et n’augmentent pas, elle est réalisée après la petite enfance. La chirurgie chez les jeunes enfants nécessite une anesthésie générale.
Plusieurs hypothèses existent concernant le mécanisme de formation du dermoïde cornéen. L’une d’elles suggère qu’il provient d’une transformation métaplasique des cellules mésodermiques entre le bord de la cupule optique et l’ectoderme superficiel au début du développement. Une autre hypothèse évoque la séquestration de cellules pluripotentes au cours de l’embryogenèse des structures oculaires environnantes.
Le dermoïde, en tant que tumeur d’inclusion, est composé de tissus dérivés de l’ectoderme (poils, peau, rarement dents) et de tissus dérivés du mésoderme (tissu adipeux, cartilage). Histologiquement, il présente une structure similaire à l’épiderme et au derme, comprenant du tissu conjonctif collagène, des follicules pileux et des glandes sébacées.
Le tissu dermoïde lui-même n’a pas d’activité proliférative.
Mitamura et al. (2021) ont rapporté un cas de croissance pseudo-ptérygienne contenant du tissu dermoïde résiduel chez une femme japonaise de 79 ans ayant subi une excision d’un dermoïde limbique à l’âge de 12 ans. L’immunohistochimie a montré que le Ki67 (marqueur de prolifération cellulaire) était positif dans les cellules épithéliales du ptérygion et les cellules endothéliales des néovaisseaux, mais négatif dans les composants dermoïdes (tissu adipeux, tissu conjonctif, nerfs périphériques) 3). Bien que le tissu dermoïde résiduel après excision incomplète n’ait pas de capacité proliférative, il pourrait agir comme un facteur modificateur dans le développement du ptérygion.
Ce rapport souligne l’importance d’une excision complète lors de la résection et confirme que le tissu dermoïde lui-même est une lésion congénitale non proliférative.
Poddi et al. (2025) ont rapporté une technique chirurgicale pour le dermoïde limbique de grade I, consistant en une excision suivie de l’application de mitomycine C (0,02 %) et d’une greffe de membrane amniotique en trois couches fixée avec de la colle de fibrine. Chez une femme de 18 ans, aucun signe de récidive n’a été observé pendant un suivi de deux ans, avec une normalisation de la topographie cornéenne, une réduction des aberrations d’ordre élevé et une amélioration de la meilleure acuité visuelle corrigée 2).
Pour un dermoïde géant de la surface oculaire (17 × 14 mm), Choudhary et al. (2021) ont rapporté une technique combinant une kératoplastie lamellaire antérieure profonde pré-descemétique (DALK) et un transfert épithélial limbique simple (SLET) de l’œil controlatéral. Cette approche a permis d’obtenir un résultat esthétique satisfaisant tout en prévenant la formation de pseudo-ptérygion 4).
La kératoplastie lamellaire utilisant des lenticules extraits par chirurgie SMILE a également été rapportée, attirant l’attention en tant que technique ne nécessitant pas de cornée de donneur.
Fu et al. (2024) ont réalisé un séquençage complet de l’exome (WES) chez un garçon de 4 ans atteint du syndrome de Goldenhar et ont identifié cinq mutations génétiques (PRDM16, FAT4, POLR1C, PLEC, MED12) potentiellement associées à la microtie 1). L’élucidation des bases génétiques du syndrome de Goldenhar pourrait contribuer au diagnostic et à la prévention futurs.
- Fu Y, Yu H, Zhang J, Zhou N. Goldenhar syndrome with limbal neoformation, microtia and skeletal deformities: a case report and literature review. BMC Ophthalmol. 2024;24:81.
- Poddi M, Romano V, Borgia A, et al. Combined Multilayered Amniotic Membrane Graft and Fibrin Glue as a Surgical Management of Limbal Dermoid Cyst. J Clin Med. 2025;14:607.
- Mitamura M, Kase S, Ohguchi T, Ishida S. A case of pterygium-like proliferation containing postoperative limbal dermoid remnants: a clinicopathological study. BMC Ophthalmol. 2021;21:12.
- Juneja A, Puthalath AS, Gupta N, Verma PK. Isolated bilateral limbal dermoid, preauricular skin tags and ametropic amblyopia. BMJ Case Rep. 2021;14:e245078.
- Abdulmannan DM. Successful Management of Limbal Dermoid in Infancy and Childhood: A Case Series. Cureus. 2022;14(3):e22835.