傳入性障礙

成人發病緩慢進展型自體免疫糖尿病(LADA)之神經眼科學探討
一目了然的要點
Section titled “一目了然的要點”1. LADA中的神經眼科考量
Section titled “1. LADA中的神經眼科考量”LADA(成人隱匿性自身免疫性糖尿病)是一種疾病概念,最初被報導為具有GAD65自身抗體但表現出T2DM表型的成人患者的亞類。它也被稱為「1.5型糖尿病」。)
**診斷標準(日本糖尿病學會IDS)**包括以下三項。
- 發病年齡30歲以上
- 至少一種胰島自體抗體陽性
- 診斷後6個月內不依賴胰島素
盛行率佔所有糖尿病的2-12%,被誤診為T2D的比例估計為5-10%5)。胰島細胞抗體(ICA)的發現可追溯到1974年,極大地改變了糖尿病的分類。
從神經眼科學角度來看,慢性高血糖引起的微血管損傷可導致糖尿病視網膜病變、NAION(非動脈炎性前部缺血性視神經病變)、皮質中風引起的同向偏盲、動眼神經麻痺、眼球震顫等。LADA患者的糖尿病視網膜病變盛行率顯著低於T2D患者(20.3% vs 26.4%,P < 0.001)。診斷時約12%的病例存在視網膜病變。
LADA自體抗體陽性,緩慢進展為胰島素依賴,而T2D自體抗體陰性,長期維持非胰島素依賴。它兼具LADA和T2D的遺傳與臨床特徵,被定位為「1.5型」。
2. 主要症狀與臨床發現
Section titled “2. 主要症狀與臨床發現”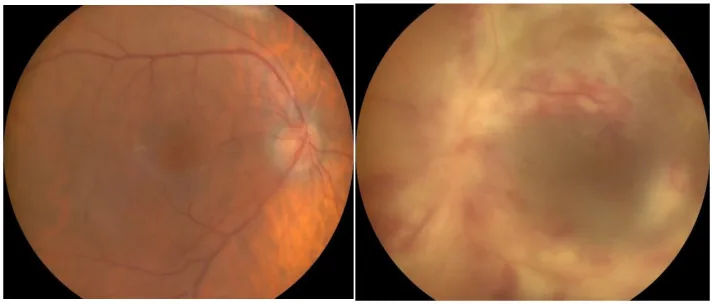
- 多尿、多食、多飲、脫水:高血糖相關的全身症狀。
- 視覺症狀:糖尿病視網膜病變、非動脈炎性前部缺血性視神經病變或皮質腦中風導致的視力障礙或視野缺損。
- DKA症狀:酮酸中毒相關的抽搐和昏迷(類似T1D的急性發作)。
- 小纖維神經病變:從足部開始的疼痛、灼熱感和刺痛。由Aδ纖維和C纖維萎縮引起。
臨床所見(神經眼科所見)
Section titled “臨床所見(神經眼科所見)”傳出性障礙
其他眼部表現如下。
- 角膜異常:內皮細胞大小不均、Descemet膜皺褶。60歲以下出現Descemet膜皺褶時應懷疑糖尿病。
- 虹膜睫狀體炎:多為僅前房有細胞的輕微發炎,使用類固醇眼藥水可迅速緩解。
- 眼眶毛黴菌症:發生於血糖控制不良的患者。死亡率高,使用抗真菌藥物治療。
3. 原因與風險因子
Section titled “3. 原因與風險因子”自體免疫機轉
Section titled “自體免疫機轉”產生針對胰島β細胞的自體抗體(GAD65、ICA、IA-2A、IAA),導致β細胞破壞。胰島素缺乏的過程涉及T1DM和T2DM兩種機制的複合作用。
- T1DM常見風險:自體免疫疾病個人史或家族史、遺傳易感性(HLA-DR4-DQ8、HLA-DR3-DQ2)3)
- T2DM常見風險:肥胖、缺乏運動、吸菸、低出生體重、含糖飲料攝取、過量飲酒
- 合併自體免疫疾病:橋本病(甲狀腺疾病盛行率17.7%)5)、修格蘭氏症候群4)、白斑3)、惡性貧血3)
- COVID-19相關:SARS-CoV-2可能透過ACE2受體誘發針對胰臟β細胞的自體免疫反應。據報導,20%的住院COVID-19患者在住院後獲得新的自體抗體1)
- 肥胖促進因子:即使GAD65抗體陽性,若BMI穩定,3年內可能不發展為LADA,顯示體重增加可能促進LADA發病4)
有病例報告顯示COVID-19後出現IA2等自體抗體1)。已提出透過ACE2受體介導的β細胞損傷機制,但目前尚未確立因果關係。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”自體抗體與代謝檢查
Section titled “自體抗體與代謝檢查”- GAD65抗體:靈敏度最高。LADA診斷的主要標誌物5)
- 其他自體抗體:ICA、IA-2A、ZnT8A、四跨膜蛋白7
- C肽檢查:β細胞功能指標。C肽 < 0.3 nmol/L 表示與T1D相當的胰島素依賴狀態
- HbA1c:透過重複測量評估血糖控制情況
- CGM(連續血糖監測):了解血糖波動2)
- 血脂譜、eGFR、血清肌酸酐、胱抑素C:併發症評估
例如,在COVID-19後LADA病例中,報告了以下檢查值模式:GAD65 < 5 nmol/L(正常)、C肽2.38 ng/mL(正常)、IA2 20.6 DK單位/mL(高,正常<5.4)1)。
- 裂隙燈顯微鏡檢查:檢查角膜異常和虹膜睫狀體炎
- 散瞳眼底檢查:檢查黃斑周圍微動脈瘤、出血、滲出物、水腫、視網膜新生血管、玻璃體細胞和視網膜剝離
- 糖尿病乳頭症的鑑別:RAPD陰性。若出現水平半盲或弓狀暗點,需懷疑缺血性視神經病變。透過螢光眼底血管攝影檢查周邊無血管區及新生血管。
各糖尿病型的比較如下所示。
| 項目 | LADA | T1D | T2D |
|---|---|---|---|
| 發病年齡 | 30歲以上 | 多為35歲以下 | 35歲以後 |
| 自體抗體 | 陽性 | 多為陽性 | 陰性 |
| C肽 | 正常至低值 | 低值 | 正常至高值 |
| 胰島素依賴 | 緩慢進展 | 發病後立即 | 長期非依賴 |
其他鑑別診斷包括MODY(強烈家族史、自體抗體陰性)和LADY(年輕發病緩慢進展型自體免疫性糖尿病)。
GAD65抗體(靈敏度最高)和C肽檢查的組合對診斷最為重要。C肽低值且自體抗體陽性可確診LADA。IDS分類標準(發病年齡≥30歲、自體抗體陽性、診斷後6個月內胰島素非依賴)也用於診斷。
5. 標準治療方法
Section titled “5. 標準治療方法”全身治療(血糖控制)
Section titled “全身治療(血糖控制)”治療目標是保護β細胞功能和嚴格血糖控制。
- C-peptide < 0.3 nmol/L:選擇與T1D類似的胰島素基礎治療
- C-peptide高值:除胰島素治療外,建議合併其他降血糖藥物(國際專家小組推薦)
- GLP-1受體促效劑(如semaglutide)、DPP-4抑制劑(如sitagliptin)、metformin
- SU藥物禁忌:增加β細胞負荷,導致功能惡化和血糖控制不佳5)
- SGLT2抑制劑:在LADA中的益處尚未確定
作為DPP-4抑制劑的保護作用,有報告指出sitagliptin 100 mg/日使一名90歲女性的HbA1c維持在5.9%達一年3)。此外,在一例合併橋本病的LADA病例中,HbA1c從7.9%惡化至11.7%,metformin、sitagliptin、gliclazide 120 mg/日、dapagliflozin和dulaglutide均無效,但胰島素基礎-餐時方案使HbA1c達到5.7%5)。
視網膜病變治療
其他眼部併發症
SU藥物直接作用於β細胞,強制促進胰島素分泌,增加β細胞負擔,進一步損害因自體免疫而逐漸耗竭的殘餘β細胞功能。據報導,LADA中使用SU藥物會導致血糖控制不佳5),因此禁忌使用。
6. 病理生理學與詳細發病機制
Section titled “6. 病理生理學與詳細發病機制”自體抗體的類型與作用
Section titled “自體抗體的類型與作用”LADA中自體抗體的特徵如下所示。
| 抗體 | 特徵 |
|---|---|
| GAD65 | 在T1DM和LADA中最常見 |
| ICA | 在T1DM和LADA中陽性率均高 |
| IA-2A和IAA | 單獨T1DM陽性率高 |
GAD65不僅存在於胰臟胰島,也存在於甲狀腺、腦、垂體、腎臟、肝臟、腎上腺、卵巢和睪丸中4)。因此,高滴度的GAD65抗體與甲狀腺自體免疫風險增加相關,LADA患者的甲狀腺疾病盛行率達17.7%5)。
T1DM側的機轉基於以下路徑:遺傳易感性→免疫學因子→自體抗體導致的β細胞凋亡→胰島素缺乏。T2DM側的機轉包括:肥胖→內臟脂肪堆積→輕度發炎→自體免疫→β細胞功能障礙。
COVID-19與β細胞損傷的機轉
Section titled “COVID-19與β細胞損傷的機轉”Lee等人(2023)報告了一例46歲男性T2DM患者,在COVID-19感染後IA2抗體陽性(20.6 DK單位/mL,正常<5.4),診斷為LADA1)。ACE2受體在胰腺外分泌腺和胰島細胞中表現,SARS-CoV-2棘蛋白與ACE2結合,經TMPRSS2啟動後進入細胞。提出了一個機制鏈:ACE2抑制→血管收縮素II升高→NHE2持續活化→活性氧增加→氧化壓力→胰島素抵抗和β細胞損傷。
微血管損傷和神經病變的機制
Section titled “微血管損傷和神經病變的機制”慢性高血糖最早且最頻繁地損害視網膜血管,導致糖尿病視網膜病變。在神經病變中,代謝相關損傷導致Aδ纖維和C纖維萎縮(小纖維神經病變),引起從足部開始的疼痛和灼熱感。
自體免疫鏈(與乾燥症候群和橋本氏病的關聯)
Section titled “自體免疫鏈(與乾燥症候群和橋本氏病的關聯)”Wen等人(2021)報告了兩名患有乾燥症候群(SS)和橋本氏病(HT)的中年女性,儘管GAD65抗體或IAA抗體陽性,但在3年的OGTT中維持了正常血糖4)。自體抗體陽性並不立即意味著進展為LADA;只有在肥胖等促進因素加入後才發病。
7. 最新研究與未來展望(研究階段報告)
Section titled “7. 最新研究與未來展望(研究階段報告)”Teplizumab(延緩第1型糖尿病發病的免疫療法)
Section titled “Teplizumab(延緩第1型糖尿病發病的免疫療法)”Teplizumab是2022年11月FDA核准的抗CD3單株抗體。它與T細胞表面的CD3結合,使自體反應性T細胞失活,從而延緩第1型糖尿病的發病。對於LADA尚未核准或研究,但由於自體免疫機制的共通性,有望延緩發病。
Semaglutide與非動脈炎性前部缺血性視神經病變風險
Section titled “Semaglutide與非動脈炎性前部缺血性視神經病變風險”Hathaway 等人(2024)報告,在T2DM患者中,使用semaglutide組的非動脈炎性前部缺血性視神經病變風險顯著較高,HR為4.28(95%CI 1.62-11.29,P < 0.001)6)。在LADA中使用GLP-1RA時,需注意非動脈炎性前部缺血性視神經病變的發生。
semaglutide與糖尿病視網膜病變惡化
Section titled “semaglutide與糖尿病視網膜病變惡化”HbA1c快速下降時,糖尿病視網膜病變惡化的風險增加,包括增殖性視網膜病變進展和黃斑水腫新發風險升高。開始使用包括semaglutide在內的GLP-1RA時,眼科監測很重要。
DPP-4抑制劑的β細胞保護作用
Section titled “DPP-4抑制劑的β細胞保護作用”Marcon 等人(2022)報告了一例GAD65 > 250 U/ml陽性的90歲女性患者,使用西格列汀100 mg/天治療,一年內HbA1c維持在5.9%3)。DPP-4抑制劑可能延緩LADA的β細胞破壞,但需要進一步的隨機對照試驗。
CGM對心理健康的影響
Section titled “CGM對心理健康的影響”Gupta等人(2023)報告了一例因DKA確診的LADA患者(44歲男性),在引入CGM後,血糖波動範圍為80-408 mg/dL,導致既往OCD惡化並自殺2)。DM患者的憂鬱風險約為正常人的兩倍,這凸顯了CGM使用前進行精神科評估的重要性。
COVID-19後自體免疫研究的挑戰
Section titled “COVID-19後自體免疫研究的挑戰”需要對COVID-19患者中胰島自體抗體(IA2、GAD65、ICA)的發生率進行大規模研究1)。此外,還需要長期追蹤研究,以確定患有SS/HT的GAD65-Ab陽性非糖尿病患者未來是否會進展為LADA4)。
目前僅FDA核准用於T1DM。由於LADA具有類似的自體免疫機制,理論上可能有效,但尚未進行研究和核准。期待未來的臨床試驗。
8. 參考文獻
Section titled “8. 參考文獻”- Lee N, Prabhu P, Swaminath S, et al. Development of Islet Antigen 2 (IA2) Antibodies Post-COVID-19 Infection: A Sign of Autoimmunity or Latent Autoimmune Diabetes Mellitus in Adults (LADA)? Cureus. 2023;15(6):e40971.
- Gupta R, Edupuganti S, Zamir I, et al. Latent Autoimmune Diabetes in Adults and a Continuous Glucose Monitoring Device: An Unfortunate Outcome. Cureus. 2023;15(11):e49141.
- Marcon LMR, Fanelli CG, Calafiore R. Type 1 Diabetes (T1D) and Latent Autoimmune Diabetes in Adults (LADA): The Difference Between a Honeymoon and a Holiday. Case Reports in Endocrinology. 2022;2022:9363543.
- Wen S, Jiang W, Zhou L. Islet Autoantibodies in the Patients with Sjogren’s Syndrome and Thyroid Disease and Risk of Progression to Latent Autoimmune Diabetes in Adults: A Case Series. Diabetes Metab Syndr Obes. 2021;14:1025-1033.
- Ibrahim A, Ahmed Mohmed MH, Darwish H, et al. A Case of Persistent Hyperglycemia: Autoimmune Link Between Hashimoto’s Thyroiditis and Latent Autoimmune Diabetes in Adults. Cureus. 2025;17(8):e91219.
- Hathaway JT, Shah MP, Hathaway DB, et al. Risk of Nonarteritic Anterior Ischemic Optic Neuropathy in Patients Prescribed Semaglutide. JAMA Ophthalmol. 2024.
