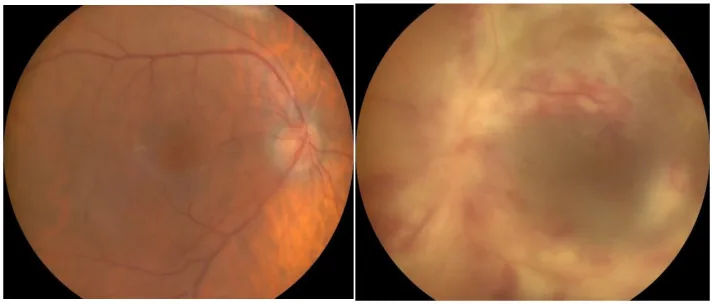
LADA คือเบาหวานชนิด 1.5 ซึ่งมีแอนติบอดีต่อตนเองเป็นบวก แต่ไม่ต้องพึ่งอินซูลินเป็นเวลา 6 เดือนหลังการวินิจฉัย
คิดเป็น 2–12% ของเบาหวานทั้งหมด และมักถูกวินิจฉัยผิดเป็น T2D
ความชุกของจอประสาทตาเสื่อมจากเบาหวาน ต่ำกว่าอย่างมีนัยสำคัญ (20.3%) เมื่อเทียบกับ T2D (26.4%) และพบได้ประมาณ 12% ในขณะที่วินิจฉัย
โรคกล้ามเนื้อตาอัมพาตจากเบาหวาน (อัมพาตของเส้นประสาทสมองคู่ที่ III, IV, VI) มักหายได้เองภายในไม่กี่เดือน
การวินิจฉัยต้องอาศัยการตรวจร่วมกันระหว่างแอนติบอดี GAD65 (มีความไวสูงที่สุด) และ C-peptide
ยาซัลโฟนิลยูเรีย (SU) มีข้อห้ามใช้เพราะทำให้การทำงานของเซลล์เบตาแย่ลง
การรักษาด้วยอินซูลินหรือยับยั้ง DPP4 เพื่อรักษาการทำงานของเซลล์เบตาเป็นหลักสำคัญของการรักษา
LADA (โรคเบาหวานชนิดภูมิต้านตนเองแฝงในผู้ใหญ่) เป็นแนวคิดโรคที่รายงานครั้งแรกในฐานะกลุ่มย่อยของผู้ใหญ่ที่มีแอนติบอดีต่อตนเองต่อ GAD65 แต่มีฟีโนไทป์ของ T2DM เรียกอีกอย่างว่า “เบาหวานชนิด 1.5”
เกณฑ์การวินิจฉัย (สมาคมโรคเบาหวานทางภูมิคุ้มกัน IDS) ประกอบด้วย 3 ข้อต่อไปนี้
อายุเริ่มต้น ≥ 30 ปี
ผลบวกต่อแอนติบอดีต่อตนเองของเกาะตับอ่อนอย่างน้อย 1 ชนิด
ไม่ต้องพึ่งอินซูลินเป็นเวลา 6 เดือนหลังการวินิจฉัย
ความชุกอยู่ที่ 2–12% ของผู้ป่วยเบาหวานทั้งหมด และประมาณว่า 5–10% ได้รับการวินิจฉัยผิดว่าเป็น T2D 5) การค้นพบแอนติบอดีต่อเซลล์เกาะตับอ่อน (ICA) ย้อนกลับไปในปี 1974 ซึ่งปฏิวัติการจำแนกประเภทของโรคเบาหวาน
จากมุมมองทางประสาทจักษุวิทยา ภาวะจุลภาคเสียหายจากน้ำตาลในเลือดสูงเรื้อรังทำให้เกิดจอประสาทตาเสื่อมจากเบาหวาน NAION (เส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่ใช่อักเสบจากหลอดเลือดแดง) ตาบอดครึ่งซีกชนิดเดียวกันจากโรคหลอดเลือดสมองในสมองส่วนคอร์เทกซ์ อัมพาตของเส้นประสาทควบคุมการเคลื่อนไหวลูกตา และอาตา ความชุกของจอประสาทตาเสื่อมจากเบาหวาน ในผู้ป่วย LADA ต่ำกว่าผู้ป่วย T2D อย่างมีนัยสำคัญ (20.3% เทียบกับ 26.4%, P < 0.001) ประมาณ 12% ของผู้ป่วยมีจอประสาทตา เสื่อมเมื่อได้รับการวินิจฉัย
Q
LADA แตกต่างจากเบาหวานชนิดที่ 2 อย่างไร?
A
LADA มีผลบวกต่อแอนติบอดีตนเองและค่อยๆ พัฒนาไปสู่การพึ่งอินซูลิน ในขณะที่ T2D มีผลลบต่อแอนติบอดีตนเองและไม่พึ่งอินซูลินเป็นเวลานาน LADA ถูกจัดเป็น “ชนิด 1.5” เนื่องจากมีลักษณะทางพันธุกรรมและทางคลินิกร่วมกันของทั้ง LADA และ T2D
ภาพประกอบ LADA Emil Robert Stoicescu, Laura Andreea Ghenciu, Roxana Iacob et al. CMV Retinitis in the Context of SARS-CoV-2 Infection: A Case Study and Comprehensive Review of Viral Interactions. Pathogens. 2024 Oct 29; 13(11):938. Figure 1. PM
CI D: PMC11597558. License: CC BY.
คำอธิบายภาพ LADA
ปัสสาวะมาก กินมาก ดื่มมาก ภาวะขาดน้ำ : อาการทั่วร่างกายที่เกี่ยวข้องกับระดับน้ำตาลในเลือดสูงอาการทางตา : ความผิดปกติทางการมองเห็น และข้อบกพร่องของลานสายตาจากเบาหวานขึ้นจอตา โรคเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่เกิดจากหลอดเลือดแดงอักเสบ และโรคหลอดเลือดสมองในชั้นคอร์เทกซ์อาการ DKA : ชักและหมดสติที่เกี่ยวข้องกับภาวะกรดคีโตน (กรณีเฉียบพลันคล้าย T1D)โรคเส้นประสาทขนาดเล็ก : ปวด แสบร้อน เสียวซ่าที่เริ่มจากเท้า เนื่องจากการฝ่อของเส้นใย Aδ และ C
ความผิดปกติของกระแสประสาทนำเข้า
จอประสาทตาเสื่อมจากเบาหวาน หลอดเลือดโป่งพองขนาดเล็ก , เลือดออก, สารคัดหลั่ง, จุดภาพชัด บวม, หลอดเลือดใหม่ในจอตา, เซลล์ในวุ้นตา , จอตาลอก
หัวประสาทตาบวมจากเบาหวาน : หัวประสาทตาบวมร่วมกับหลอดเลือดฝอยขยาย อาจมีเลือดออกและจุดขาวรอบข้าง RAPD เป็นลบ การตรวจลานสายตา แสดงเพียงจุดบอดขยาย หายเองได้ใน 3–6 เดือน
ประสาทตาขาดเลือด : เกิดจากการไหลเวียนผิดปกติในหลอดเลือดแดงซิลิอารีส่วนหลังและแขนงของหลอดเลือดแดงจอตาส่วนกลาง
โรคหลอดเลือดสมองส่วนคอร์เทกซ์ (ตาบอดครึ่งซีกชนิดเดียวกัน) : เกิดจากโรคหลอดเลือดสมองจากน้ำตาลในเลือดสูงเรื้อรัง
ความผิดปกติแบบส่งออก
อัมพาตเส้นประสาทควบคุมการเคลื่อนไหวลูกตา : อัมพาตของเส้นประสาทสมองคู่ที่ 3, 4 และ 6 อัมพาตกล้ามเนื้อตาจากเบาหวานพบบ่อยที่สุดที่เส้นประสาทสมองคู่ที่ 3 รองลงมาคือคู่ที่ 6 และพบน้อยที่คู่ที่ 4 ส่วนใหญ่หายเองได้ในไม่กี่เดือน
ลักษณะของอัมพาตเส้นประสาทกล้ามเนื้อตา : แตกต่างจากหลอดเลือดโป่งพองในสมอง คือไม่เกิดม่านตา ไม่เท่ากัน
ความผิดปกติของม่านตา : ในโรคเบาหวาน ม่านตา มักจะหดตัวและขยายได้ยากด้วยยาหยอดขยายม่านตา (ความผิดปกติของเส้นประสาทซิมพาเทติก/กล้ามเนื้อขยายม่านตา )
อาตา
อาการทางตาอื่นๆ ที่ทราบมีดังนี้
ความผิดปกติของกระจกตา : เซลล์เยื่อบุผนังกระจกตา มีขนาดไม่เท่ากัน เกิดรอยย่นของเยื่อเดสเซเมท หากพบรอยย่นของเยื่อเดสเซเมท ในผู้ที่มีอายุต่ำกว่า 60 ปี ให้สงสัยโรคเบาหวานม่านตาอักเสบ ร่วมกับซิลิอารีบอดี ้ช่องหน้าลูกตา และดีขึ้นอย่างรวดเร็วด้วยยาหยอดสเตียรอยด์ โรคมิวคอร์ไมโคซิสในเบ้าตา : เกิดในผู้ป่วยที่ควบคุมระดับน้ำตาลในเลือดได้ไม่ดี อัตราการเสียชีวิตสูงและรักษาด้วยยาต้านเชื้อรา
มีการสร้างแอนติบอดีต่อตนเอง (GAD65, ICA, IA-2A, IAA) ต่อเซลล์เบต้าของตับอ่อน ทำให้เซลล์เบต้าถูกทำลาย กระบวนการที่นำไปสู่การขาดอินซูลินเป็นการรวมกลไกของ T1DM และ T2DM
ปัจจัยเสี่ยงร่วมของ T1DM : ประวัติส่วนตัวหรือครอบครัวเป็นโรคภูมิต้านตนเอง ความบกพร่องทางพันธุกรรม (HLA-DR4-DQ8, HLA-DR3-DQ2)3) ความเสี่ยงร่วมของ T2DM : โรคอ้วน ขาดการออกกำลังกาย การสูบบุหรี่ น้ำหนักแรกเกิดต่ำ การดื่มเครื่องดื่มที่มีน้ำตาล การดื่มแอลกอฮอล์มากเกินไปโรคภูมิต้านตนเองร่วม : โรคไทรอยด์อักเสบฮาชิโมโตะ (ความชุกของโรคไทรอยด์ 17.7%)5) , กลุ่มอาการโจเกรน4) , โรคด่างขาว3) , โลหิตจางชนิดเพอร์นิเชียส3) เกี่ยวข้องกับ COVID-19 : SARS-CoV-2 อาจกระตุ้นปฏิกิริยาภูมิต้านตนเองต่อเซลล์เบต้าของตับอ่อนผ่านตัวรับ ACE2 มีรายงานว่าผู้ป่วย COVID-19 ที่เข้ารับการรักษาในโรงพยาบาล 20% ได้รับแอนติบอดีตนเองใหม่หลังเข้ารับการรักษา1) ปัจจัยส่งเสริมโรคอ้วน : แม้ว่า GAD65-Ab จะเป็นบวก หาก BMI คงที่ LADA อาจไม่เกิดขึ้นเป็นเวลา 3 ปี และการเพิ่มของน้ำหนักอาจเร่งการเกิด LADA4)
Q
การติดเชื้อ COVID-19 เพิ่มความเสี่ยงในการเกิด LADA หรือไม่?
A
มีรายงานผู้ป่วยที่พบแอนติบอดีตนเอง เช่น IA2 หลังติดเชื้อ COVID-191) มีการเสนอกลไกการทำลายเซลล์เบต้าผ่านตัวรับ ACE2 แต่ยังไม่มีการพิสูจน์ความสัมพันธ์เชิงสาเหตุในปัจจุบัน
แอนติบอดี GAD65 : ความไวสูงที่สุด ตัวบ่งชี้หลักในการวินิจฉัย LADA 5) แอนติบอดีตนเองอื่นๆ : ICA, IA-2A, ZnT8A, Tetraspanin 7การตรวจ C-peptide : ตัวบ่งชี้การทำงานของเซลล์เบตา C-peptide < 0.3 nmol/L บ่งชี้ภาวะพึ่งอินซูลินเทียบเท่ากับ T1DHbA1c : การประเมินการควบคุมระดับน้ำตาลในเลือดโดยการวัดซ้ำCGM (การตรวจวัดระดับน้ำตาลในเลือดอย่างต่อเนื่อง) : การทำความเข้าใจความผันผวนของระดับน้ำตาล2) โปรไฟล์ไขมัน, eGFR, ครีเอตินินในซีรัม, ซิสทาทิน ซี : การประเมินภาวะแทรกซ้อน
ตัวอย่างเช่น ในกรณี LADA หลังโควิด-19 มีรายงานรูปแบบค่าตรวจทางห้องปฏิบัติการ: GAD65 < 5 nmol/L (ปกติ), C-peptide 2.38 ng/mL (ปกติ), IA2 20.6 หน่วย DK/mL (สูง, ปกติ < 5.4)1) .
การตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด (Slit-lamp)กระจกตา และม่านตาอักเสบ ร่วมกับซิลิอารีบอดี การตรวจอวัยวะภายในลูกตาหลังขยายม่านตา : ยืนยันไมโครแอนนิวริซึมรอบจอประสาทตา , เลือดออก, สารคัดหลั่ง, บวมน้ำ, หลอดเลือดใหม่ในจอตา, เซลล์ในวุ้นตา , จอตาลอกการแยกโรคเบาหวานขึ้นจอประสาทตา : RAPD เป็นลบ หากพบภาวะตาบอดครึ่งซีกแนวนอนหรือจุดบอดรูปโค้ง ให้สงสัยโรคเส้นประสาทตา ขาดเลือด ยืนยันบริเวณที่ไม่มีหลอดเลือดส่วนปลายหรือเส้นเลือดใหม่ด้วยการตรวจฟลูออเรสซีน แองจิโอกราฟี
การเปรียบเทียบโรคเบาหวานชนิดต่างๆ แสดงไว้ด้านล่าง
รายการ LADA T1D T2D อายุที่เริ่มเป็น 30 ปีขึ้นไป ส่วนใหญ่อายุน้อยกว่า 35 ปี 35 ปีขึ้นไป แอนติบอดีต่อตนเอง บวก มักเป็นบวก ลบ ซี-เปปไทด์ ปกติถึงต่ำ ต่ำ ปกติถึงสูง การพึ่งอินซูลิน ดำเนินไปอย่างช้าๆ ตั้งแต่เริ่มมีอาการ ไม่พึ่งพาเป็นเวลานาน
โรคที่ต้องวินิจฉัยแยกโรคอื่นๆ ได้แก่ MODY (ประวัติครอบครัวชัดเจน, ภูมิต้านตนเองเป็นลบ) และ LADY (เบาหวานชนิดภูมิต้านตนเองที่ดำเนินช้าในวัยหนุ่มสาว)
Q
การตรวจใดสำคัญที่สุดในการวินิจฉัย LADA?
A
การรวมกันของการตรวจแอนติบอดี GAD65 (ความไวสูงที่สุด) และการตรวจ C-peptide มีความสำคัญที่สุดในการวินิจฉัย LADA ได้รับการยืนยันเมื่อ C-peptide ต่ำและภูมิต้านตนเองเป็นบวก เกณฑ์การจำแนก IDS (อายุเริ่มต้น ≥30 ปี, ภูมิต้านตนเองเป็นบวก, ไม่พึ่งอินซูลินเป็นเวลา 6 เดือนหลังการวินิจฉัย) ก็ใช้ในการวินิจฉัยเช่นกัน
เป้าหมายการรักษาคือการรักษาการทำงานของเซลล์เบต้าและการควบคุมระดับน้ำตาลในเลือดอย่างเข้มงวด
C-peptide < 0.3 nmol/L : เลือกการรักษาด้วยอินซูลินเช่นเดียวกับ T1DC-peptide สูง : นอกจากการรักษาด้วยอินซูลินแล้ว แนะนำให้ใช้ยาลดน้ำตาลชนิดอื่นร่วมด้วย (คำแนะนำจากคณะผู้เชี่ยวชาญนานาชาติ)
GLP-1RA (เช่น semaglutide), ยายับยั้ง DPP4 (เช่น sitagliptin), metformin
ยาซัลโฟนิลยูเรียห้ามใช้ : เพิ่มภาระต่อเซลล์เบตา ทำให้การทำงานแย่ลงและการควบคุมน้ำตาลไม่ดี5) ยายับยั้ง SGLT2 : ประโยชน์ใน LADA ยังไม่ชัดเจน
ในฐานะผลการป้องกันของยายับยั้ง DPP4 มีรายงานหญิงอายุ 90 ปีรักษาระดับ HbA1c 5.9% ได้นาน 1 ปีด้วย sitagliptin 100 มก./วัน3) นอกจากนี้ยังมีรายงานผู้ป่วย LADA ร่วมกับโรคฮาชิโมโตะที่ HbA1c แย่ลงจาก 7.9% เป็น 11.7% และยาทั้งหมด (metformin, sitagliptin, gliclazide 120 มก./วัน, dapagliflozin, dulaglutide) ไม่ได้ผล แต่สามารถบรรลุ HbA1c 5.7% ด้วยอินซูลิน basal-bolus5) .
การรักษาจอประสาทตา
เลเซอร์เฉพาะจุด : การจี้ด้วยเลเซอร์เฉพาะจุดสำหรับจอประสาทตา บวมจากเบาหวาน
การจี้จอประสาทตา ทั่วทั้งจอ (PRP ) : การรักษาหลักสำหรับจอประสาทตาเสื่อมจากเบาหวาน ชนิดงอกเส้นเลือดใหม่ (PDR)
การรักษาด้วยยาต้าน VEGF วุ้นตา เป็นทางเลือกหรือการรักษาเสริมสำหรับ PDR
ภาวะแทรกซ้อนทางตาอื่นๆ
จอประสาทตาเสื่อมจากเบาหวาน
กล้ามเนื้อตาอัมพาต : ส่วนใหญ่หายได้เองภายในไม่กี่เดือน
แผลที่กระจกตา
ม่านตาอักเสบ และซิลิอารีบอดี ้อักเสบสเตียรอยด์
ไม่ควรใช้ยา SU (เช่น glimepiride) ในผู้ป่วย LADA อาจทำให้การทำงานของเบตาเซลล์แย่ลงอย่างถาวร 5) .
ในผู้ป่วยที่ใช้ semaglutide มีรายงานความเสี่ยงที่เพิ่มขึ้นของโรคเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่เกิดจากหลอดเลือดแดงอักเสบ (NAION ) ดังนั้นควรระวังอาการทางสายตา (ดูหัวข้อ “งานวิจัยล่าสุดและแนวโน้มในอนาคต”)
การลดลงของ HbA1c อย่างรวดเร็วอาจทำให้จอประสาทตาเสื่อมจากเบาหวาน แย่ลงชั่วคราว
Q
เหตุใดจึงไม่สามารถใช้ยาซัลโฟนิลยูเรีย (SU) ในการรักษา LADA ได้?
A
ยา SU ออกฤทธิ์โดยตรงต่อเซลล์เบต้าเพื่อกระตุ้นการหลั่งอินซูลินแบบบังคับ ทำให้เพิ่มภาระต่อเซลล์เบต้าและทำให้การทำงานของเซลล์เบต้าที่เหลืออยู่ซึ่งถูกทำลายโดยภูมิคุ้มกันตนเองแย่ลง มีรายงานว่าการใช้ SU ใน LADA ส่งผลให้การควบคุมระดับน้ำตาลในเลือดไม่ดี 5) และห้ามใช้
ลักษณะของแอนติบอดีต่อตนเองใน LADA แสดงไว้ด้านล่าง
แอนติบอดี ลักษณะ GAD65 พบได้บ่อยที่สุดทั้งใน T1DM และ LADA ICA อัตราการเป็นบวกสูงทั้งใน T1DM และ LADA IA-2A และ IAA อัตราการตรวจพบผลบวกสูงใน T1DM เพียงอย่างเดียว
GAD65 มีอยู่ไม่เพียงแต่ในตับอ่อนเท่านั้น แต่ยังมีในต่อมไทรอยด์ สมอง ต่อมใต้สมอง ไต ตับ ต่อมหมวกไต รังไข่ และอัณฑะ4) ดังนั้น แอนติบอดีต่อ GAD65 ที่มีไทเทอร์สูงจึงสัมพันธ์กับความเสี่ยงที่เพิ่มขึ้นของภาวะภูมิต้านตนเองของต่อมไทรอยด์ และความชุกของโรคต่อมไทรอยด์ในผู้ป่วย LADA สูงถึง 17.7%5)
กลไกทางฝั่ง T1DM ประกอบด้วย: ความโน้มเอียงทางพันธุกรรม → ปัจจัยทางภูมิคุ้มกัน → การตายของเซลล์เบตาที่เกิดจากแอนติบอดีตนเอง → การขาดอินซูลิน ส่วนกลไกทางฝั่ง T2DM ได้แก่: โรคอ้วน → การสะสมไขมันในอวัยวะภายใน → การอักเสบระดับต่ำ → ภูมิต้านตนเอง → ความผิดปกติของเซลล์เบตา
Lee และคณะ (2023) รายงานกรณีชายอายุ 46 ปีที่มีประวัติเป็น T2DM ซึ่งตรวจพบแอนติบอดี IA2 เป็นบวก (20.6 DK หน่วย/มล., ปกติ <5.4) หลังติดเชื้อ COVID-19 และได้รับการวินิจฉัยว่าเป็น LADA1) ตัวรับ ACE2 แสดงออกบนต่อมไร้ท่อภายนอกของตับอ่อนและเซลล์เกาะตับอ่อน และโปรตีนหนามของ SARS-CoV-2 จับกับ ACE2 และถูกกระตุ้นโดย TMPRSS2 เพื่อเข้าสู่เซลล์ มีการเสนอกลไกต่อเนื่อง: การยับยั้ง ACE2 → การเพิ่มขึ้นของ angiotensin II → การกระตุ้น NHE2 อย่างต่อเนื่อง → การเพิ่มขึ้นของอนุมูลอิสระ → ความเครียดออกซิเดชัน → การดื้อต่ออินซูลินและการทำลายเซลล์เบตา
ภาวะน้ำตาลในเลือดสูงเรื้อรังทำลายหลอดเลือดจอประสาทตา ตั้งแต่เนิ่นๆ และบ่อยที่สุด ทำให้เกิดจอประสาทตาเสื่อมจากเบาหวาน ในโรคเส้นประสาท ความเสียหายจากการเผาผลาญทำให้เส้นใย Aδ และ C ฝ่อ (โรคเส้นประสาทเส้นใยเล็ก) ทำให้เกิดอาการปวดและแสบร้อนที่เริ่มจากเท้า
Wen และคณะ (2021) รายงานหญิงวัยกลางคนสองรายที่เป็นกลุ่มอาการโจเกรน (SS) และโรคฮาชิโมโตะ (HT) ซึ่งยังคงมีระดับน้ำตาลในเลือดปกติในการทดสอบ OGTT เป็นเวลา 3 ปี แม้จะมี GAD65-Ab หรือ IAA-Ab เป็นบวก4) การมีแอนติบอดีตนเองเป็นบวกไม่ได้หมายถึงการดำเนินไปสู่ LADA ทันที โรคนี้จะเกิดขึ้นเมื่อมีปัจจัยส่งเสริมเช่นโรคอ้วนร่วมด้วยเท่านั้น
Teplizumab เป็นแอนติบอดีโมโนโคลนอลต่อต้าน CD3 ที่ได้รับการอนุมัติจาก FDA ในเดือนพฤศจิกายน 2022 มันจับกับ CD3 บนพื้นผิวของเซลล์ T และทำให้เซลล์ T ที่ตอบสนองต่อตนเองไม่ทำงาน ซึ่งช่วยชะลอการเกิด T1DM สำหรับ LADA ยังไม่ได้รับการอนุมัติหรือศึกษา แต่เนื่องจากกลไกภูมิต้านตนเองที่คล้ายคลึงกัน จึงคาดหวังถึงความเป็นไปได้ในการชะลอการเกิด
Hathaway และคณะ (2024) รายงานว่าความเสี่ยงของภาวะเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่เกิดจากหลอดเลือดแดงอักเสบในกลุ่มผู้ใช้ semaglutide ในผู้ป่วยเบาหวานชนิดที่ 2 สูงขึ้นอย่างมีนัยสำคัญ โดยมี HR 4.28 (95% CI 1.62-11.29, P < 0.001)6) เมื่อใช้ GLP-1 receptor agonists ในผู้ป่วยเบาหวานชนิด LADA ควรระวังการเกิดภาวะเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่เกิดจากหลอดเลือดแดงอักเสบ
เมื่อระดับ HbA1c ลดลงอย่างรวดเร็ว ความเสี่ยงของการเสื่อมสภาพของจอประสาทตา จากเบาหวานจะเพิ่มขึ้น รวมถึงการดำเนินไปของจอประสาทตา ชนิดงอกใหม่และความเสี่ยงใหม่ของการเกิดจอประสาทตา บวมน้ำ การตรวจติดตามทางจักษุวิทยามีความสำคัญเมื่อเริ่มใช้ GLP-1RA รวมถึงเซมากลูไทด์
Marcon และคณะ (2022) รายงานกรณีผู้หญิงอายุ 90 ปีที่มี GAD65 > 250 U/ml เป็นบวก ได้รับ sitagliptin 100 มก./วัน และคงระดับ HbA1c ที่ 5.9% เป็นเวลาหนึ่งปี 3) ยับยั้ง DPP4 อาจชะลอการทำลายเซลล์เบตาใน LADA แต่จำเป็นต้องมีการศึกษา RCT เพิ่มเติม
Gupta และคณะ (2023) รายงานกรณีผู้ป่วย LADA (ชายอายุ 44 ปี) ที่ได้รับการวินิจฉัยว่าเป็น DKA หลังจากติดตั้ง CGM พบความผันผวนของระดับน้ำตาลในเลือด 80-408 มก./ดล. ซึ่งทำให้ประวัติ OCD แย่ลงและนำไปสู่การฆ่าตัวตาย 2) ผู้ป่วย DM มีความเสี่ยงต่อภาวะซึมเศร้าประมาณสองเท่า ซึ่งชี้ให้เห็นถึงความสำคัญของการประเมินทางจิตเวชก่อนใช้ CGM
จำเป็นต้องมีการศึกษาขนาดใหญ่เกี่ยวกับอุบัติการณ์ของแอนติบอดีต่อตนเองของเกาะเล็กตับอ่อน (IA2, GAD65, ICA) ในผู้ป่วยโควิด-19 1) นอกจากนี้ ยังจำเป็นต้องมีการศึกษาติดตามระยะยาวเพื่อดูว่าผู้ป่วยที่ไม่เป็นเบาหวานซึ่งมี GAD65-Ab บวกและมี SS และ HT จะพัฒนาเป็น LADA ในอนาคตหรือไม่ 4)
Q
สามารถใช้ teplizumab สำหรับ LADA ได้หรือไม่?
A
ปัจจุบัน teplizumab ได้รับการอนุมัติจาก FDA สำหรับ T1DM เท่านั้น เนื่องจาก LADA มีกลไกภูมิต้านตนเองคล้ายกัน ในทางทฤษฎีอาจมีประสิทธิภาพ แต่ยังไม่มีการวิจัยหรือการอนุมัติ คาดว่าจะมีการทดลองทางคลินิกในอนาคต
Lee N, Prabhu P, Swaminath S, et al. Development of Islet Antigen 2 (IA2) Antibodies Post-COVID-19 Infection: A Sign of Autoimmunity or Latent Autoimmune Diabetes Mellitus in Adults (LADA)? Cureus. 2023;15(6):e40971.
Gupta R, Edupuganti S, Zamir I, et al. Latent Autoimmune Diabetes in Adults and a Continuous Glucose Monitoring Device: An Unfortunate Outcome. Cureus. 2023;15(11):e49141.
Marcon LMR, Fanelli CG, Calafiore R. Type 1 Diabetes (T1D) and Latent Autoimmune Diabetes in Adults (LADA): The Difference Between a Honeymoon and a Holiday. Case Reports in Endocrinology. 2022;2022:9363543.
Wen S, Jiang W, Zhou L. Islet Autoantibodies in the Patients with Sjogren’s Syndrome and Thyroid Disease and Risk of Progression to Latent Autoimmune Diabetes in Adults: A Case Series. Diabetes Metab Syndr Obes. 2021;14:1025-1033.
Ibrahim A, Ahmed Mohmed MH, Darwish H, et al. A Case of Persistent Hyperglycemia: Autoimmune Link Between Hashimoto’s Thyroiditis and Latent Autoimmune Diabetes in Adults. Cureus. 2025;17(8):e91219.
Hathaway JT, Shah MP, Hathaway DB, et al. Risk of Nonarteritic Anterior Ischemic Optic Neuropathy in Patients Prescribed Semaglutide. JAMA Ophthalmol. 2024.
ถาม AI เกี่ยวกับบทความนี้
คัดลอกข้อความบทความแล้ววางในผู้ช่วย AI ที่คุณต้องการใช้
เปิดผู้ช่วย AI ด้านล่าง แล้ววางข้อความที่คัดลอกลงในช่องแชต