อาการของเปลือกตา
เปลือกตาบนบวม เปลือกตาบนหดรั้ง และ เปลือกตาบนเคลื่อนช้า เป็นลักษณะเฉพาะ
เครื่องหมาย Dalrymple: รอยแยกเปลือกตากว้างขึ้นเนื่องจากการหดรั้งของเปลือกตาบน
สัญญาณฟอน เกรเฟ (von Graefe sign): การหย่อนของหนังตาบนล่าช้าเมื่อมองลง (lid lag).

โรคตาจากต่อมไทรอยด์ (thyroid eye disease: TED) เป็นโรคภูมิคุ้มกันทำลายตนเองที่ความผิดปกติของภูมิคุ้มกันที่เกี่ยวข้องกับความผิดปกติของต่อมไทรอยด์กระตุ้นให้เกิดการอักเสบของเนื้อเยื่อภายในเบ้าตา ทำให้ปริมาตรของไขมันในเบ้าตาและกล้ามเนื้อนอกลูกตาเพิ่มขึ้น ความดันหลังลูกตาที่เพิ่มขึ้นทำให้เกิดตาโปน พบได้บ่อยร่วมกับภาวะต่อมไทรอยด์ทำงานเกิน (โรคเกรฟส์/เบสโดว์) แต่ก็สามารถเกิดขึ้นได้เมื่อการทำงานของต่อมไทรอยด์ปกติ (euthyroid ophthalmopathy) โรคตาจากต่อมไทรอยด์ดำเนินไปโดยไม่ขึ้นกับฮอร์โมนไทรอยด์ และเป็นหนึ่งในโรคภูมิคุ้มกันทำลายตนเองที่เกี่ยวข้องกับแอนติบอดีต่อต่อมไทรอยด์
ผู้ป่วยโรคเกรฟส์ (เบสโดว์) ประมาณ 40-50% มีอาการทางตา รอยโรคในเบ้าตาชนิดรุนแรงพบได้ค่อนข้างน้อย โดยเกิดขึ้นในผู้ป่วยโรคเกรฟส์ทั้งหมด 5-10%
ความชุกของโรคคือ 16/100,000 คน-ปีในผู้หญิง และ 2.9/100,000 คน-ปีในผู้ชาย1) อายุที่เริ่มมีอาการมีสองช่วงสูงสุดคือช่วง 40-50 ปี และ 60-70 ปี1) การสูบบุหรี่เป็นปัจจัยเสี่ยงที่สำคัญที่สุดของโรคตาจากต่อมไทรอยด์ ซึ่งเพิ่มความเสี่ยงในการเกิดโรคอย่างมีนัยสำคัญ2) พบรูปแบบตามอายุ โดยที่ตาโปนเป็นอาการหลักในผู้ป่วยอายุน้อย ส่วนภาพซ้อนเป็นอาการหลักในผู้ป่วยสูงอายุ
การดำเนินโรคตามธรรมชาติของโรคตาจากต่อมไทรอยด์เป็นไปตามเส้นโค้งรันเดิล โดยเปลี่ยนจากระยะ active (ระยะอักเสบ ปกติ 1-3 ปี) ไปสู่ระยะ stable (ระยะไม่อักเสบ)3) ช่วงเวลาของการรักษาจะพิจารณาจากเส้นโค้งนี้
อาการของเปลือกตา
เปลือกตาบนบวม เปลือกตาบนหดรั้ง และ เปลือกตาบนเคลื่อนช้า เป็นลักษณะเฉพาะ
เครื่องหมาย Dalrymple: รอยแยกเปลือกตากว้างขึ้นเนื่องจากการหดรั้งของเปลือกตาบน
สัญญาณฟอน เกรเฟ (von Graefe sign): การหย่อนของหนังตาบนล่าช้าเมื่อมองลง (lid lag).
ตาโปน
พบบ่อยในผู้ป่วยอายุน้อย (ความเปราะบางของเนื้อเยื่อรองรับเบ้าตา).
ประเมินด้วย Hertel exophthalmometer ค่าปกติในคนญี่ปุ่นคือ 10–15 มม. (เฉลี่ย 13 มม.) ความแตกต่างระหว่างตาทั้งสองข้างภายใน 2 มม. ถือว่าปกติ
ภาพซ้อน
พบบ่อยในผู้สูงอายุ. เกิดจากตาเหล่แบบจำกัดการเคลื่อนที่เนื่องจากการอักเสบและพังผืดของกล้ามเนื้อนอกลูกตา.
กล้ามเนื้อเรกตัสล่างได้รับผลกระทบมากที่สุด → การจำกัดการมองขึ้นบนพบบ่อยที่สุด รองลงมาคือการจำกัดการมองออกด้านข้างจากการเกี่ยวข้องของกล้ามเนื้อเรกตัสกลาง
ความบกพร่องทางการมองเห็น
เนื่องจากโรคกระจกตา (โรคกระจกตาจากหนังตาปิดไม่สนิท) หรือ โรคเส้นประสาทตาถูกกดทับ (DON)
DON เกิดขึ้นประมาณ 5% ของผู้ป่วยทั้งหมด1) และต้องได้รับการรักษาฉุกเฉิน สัญญาณต่างๆ ได้แก่ RAPD บวก, CFF ลดลง, และความบกพร่องของลานสายตา
สามารถเกิดขึ้นได้แม้การทำงานของต่อมไทรอยด์ปกติ เรียกว่า euthyroid ophthalmopathy โรคตาจากต่อมไทรอยด์เป็นโรคภูมิคุ้มกันทำลายตนเองที่ดำเนินไปโดยอิสระจากระดับฮอร์โมนไทรอยด์ และสามารถเกิดขึ้นได้หากแอนติบอดีต่อตนเองที่เกี่ยวข้องกับต่อมไทรอยด์ (TRAb, TSAb) เป็นบวก หากมีอาการหนังตาหดหรือตาโปน จำเป็นต้องตรวจแอนติบอดีต่อตนเองที่เกี่ยวข้องกับต่อมไทรอยด์แม้การทำงานของต่อมไทรอยด์ปกติ
ในระยะแรก อาการหลักคือ ความแห้ง ระคายเคือง น้ำตาไหล และกลัวแสง เมื่อโรคดำเนินไป จะมีอาการบวมรอบเบ้าตา ตาโปน เห็นภาพซ้อน และหนังตาหดรัดตัว ในรายที่รุนแรง อาจเกิดแผลที่กระจกตาและโรคเส้นประสาทตาจากการกดทับ
ต่อไปนี้คืออาการแสดงที่เปลือกตาซึ่งจำเพาะต่อโรคตาจากต่อมไทรอยด์
| ชื่ออาการแสดง | ชื่อภาษาอังกฤษ | ลักษณะที่พบ |
|---|---|---|
| Dalrymple sign | Dalrymple sign | การเปิดของรอยแยกเปลือกตากว้างขึ้นเนื่องจากเปลือกตาบนหดรั้ง ทำให้เห็นตาขาวเหนือขอบกระจกตาส่วนบน |
| von Graefe sign | lid lag | ปรากฏการณ์ที่เปลือกตาบนตามการมองลงช้ากว่าปกติ |
| Stellwag sign | Stellwag sign | การกระพริบตาลดลงและการปิดตาไม่สนิท |
| Gifford sign | Gifford sign | การพลิกหนังตาบนได้ยาก |
วัดภาวะตาโปนด้วย Hertel exophthalmometer ค่าปกติในคนญี่ปุ่นคือ 10–15 มม. (เฉลี่ย 13 มม.) และความแตกต่างระหว่างสองตาที่ ≤2 มม. ถือว่าปกติ ค่า Hertel >18 มม. บ่งชี้ถึงภาวะตาโปน1).
เกิดจากกล้ามเนื้อนอกลูกตาที่หนาตัวกดทับเส้นประสาทตา (optic nerve) บริเวณปลายเบ้าตา (orbital apex) พบได้ประมาณ 5% ของผู้ป่วยทั้งหมด1) และเป็นภาวะฉุกเฉิน RAPD (relative afferent pupillary defect) ผลบวก CFF (critical fusion frequency) ลดลง และความบกพร่องของลานสายตาเป็นสัญญาณเริ่มต้น ความผิดปกติของการมองเห็นสีก็เป็นสิ่งสำคัญเช่นกัน
อาการปวด ตาเห็นภาพซ้อน และการเปลี่ยนแปลงรูปลักษณ์เป็นปัจจัยหลักที่ทำให้คุณภาพชีวิตลดลง ความชุกของภาวะวิตกกังวลและซึมเศร้าในผู้ป่วยโรคตาจากต่อมไทรอยด์อยู่ที่ 36% ซึ่งสูงกว่าประชากรทั่วไป (18.9%) ประมาณสองเท่า 5) ผู้ป่วยระดับปานกลาง 62% และผู้ป่วยระดับรุนแรง 89% มีความบกพร่องของคุณภาพชีวิตสูง (คะแนน ≥4/7) 5) มีรายงานว่าคุณภาพชีวิตลดลงเทียบเท่าหรือต่ำกว่าโรคเบาหวาน โรคถุงลมโป่งพอง และภาวะหัวใจล้มเหลว
เกิดจากตาเหล่แบบจำกัดการเคลื่อนไหว (restrictive strabismus) อันเนื่องมาจากกล้ามเนื้อนอกลูกตา (โดยเฉพาะกล้ามเนื้อเรกตัสล่าง) โตและหดตัวจากการอักเสบและพังผืด ทำให้การเคลื่อนไหวของตาปกติถูกจำกัด กล้ามเนื้อเรกตัสล่างถูกกระทบบ่อยที่สุด ดังนั้นภาวะการมองขึ้นผิดปกติจึงพบบ่อยที่สุด ลำดับความถี่ของการเกี่ยวข้องของกล้ามเนื้อนอกลูกตาคือ: เรกตัสล่าง > เรกตัสกลาง > เรกตัสบน > เรกตัสข้าง และพบบ่อยในผู้สูงอายุ
ความผิดปกติทางภูมิคุ้มกันที่เกี่ยวข้องกับความผิดปกติของต่อมไทรอยด์กระตุ้นให้เกิดการอักเสบของเนื้อเยื่อภายในเบ้าตา แอนติบอดีต่อตนเองต่อตัวรับ TSH (TRAb) กระตุ้น TSHR บนไฟโบรบลาสต์ในเบ้าตา กระตุ้นการผลิตไซโตไคน์ที่ก่อให้เกิดการอักเสบ (TNF-α, IL-6, IL-1β เป็นต้น) เซลล์ที CD4+/CD8+ แทรกซึมเข้าไปในเนื้อเยื่อเบ้าตาและขยายการตอบสนองต่อการอักเสบ
ไฟโบรบลาสต์ที่ถูกกระตุ้นจะเพิ่มการสังเคราะห์ไกลโคซามิโนไกลแคนและกรดไฮยาลูโรนิก ทำให้เกิดอาการบวมน้ำของเนื้อเยื่อและการกักเก็บน้ำ การเปลี่ยนแปลงของไฟโบรบลาสต์เป็นเซลล์ไขมันและไมโอไฟโบรบลาสต์ทำให้เกิดการขยายตัวของไขมันในเบ้าตาและพังผืดของกล้ามเนื้อนอกลูกตา3)
ตัวรับ IGF-1 (IGF-1R) สร้างสารเชิงซ้อนกับ TSHR และมีส่วนร่วมแบบเสริมฤทธิ์กันในการกระตุ้นไฟโบรบลาสต์ในเบ้าตา 4) กลไกนี้เป็นเป้าหมายการรักษาของเทโพรทูมูแมบ (ยาที่ยับยั้ง IGF-1R)
การสูบบุหรี่ เป็นปัจจัยเสี่ยงที่สำคัญที่สุด ซึ่งสัมพันธ์กับความเสี่ยงในการเกิดโรค ความรุนแรง และการดื้อต่อการรักษา 2) นอกจากนี้ ความไม่เสถียรของการทำงานของต่อมไทรอยด์ ระยะเฉียบพลันหลังการรักษาด้วยไอโอดีนกัมมันตรังสี อายุที่มากขึ้น และเพศชาย ก็มีส่วนทำให้เกิดความเสี่ยงต่อความรุนแรงของโรค
หากมีสามอาการ ได้แก่ หนังตาหดร่น ตาโปน และเห็นภาพซ้อน แสดงว่ามีความน่าจะเป็นสูงทางคลินิกว่าเป็นโรคตาจากต่อมไทรอยด์ (TED) แม้ว่าการทำงานของต่อมไทรอยด์จะปกติ ก็สามารถวินิจฉัย TED ได้หากตรวจพบแอนติบอดีต่อต่อมไทรอยด์เป็นบวก
วัดฮอร์โมนไทรอยด์ (FT₄, FT₃), TSH และแอนติบอดีต่อต่อมไทรอยด์ วัตถุที่วัด ได้แก่ TRAb (แอนติบอดีต่อตัวรับ TSH), TSAb (แอนติบอดีกระตุ้นต่อมไทรอยด์), แอนติบอดีต่อ TG (แอนติบอดีต่อไทโรโกลบูลิน) และแอนติบอดีต่อ TPO (แอนติบอดีต่อเปอร์ออกซิเดสของต่อมไทรอยด์) แอนติบอดีใดๆ เหล่านี้จะเป็นบวก
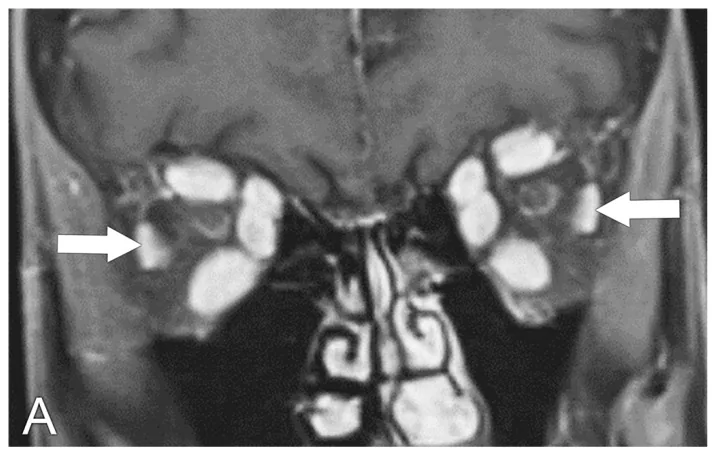
MRI (ทางเลือกแรก): ประเมินรูปร่างของกล้ามเนื้อนอกลูกตาด้วยภาพถ่วงน้ำหนัก T1 วิธี STIR (short-TI inversion recovery) แสดงบริเวณที่มีการอักเสบเป็นบริเวณสัญญาณสูง ซึ่งมีประโยชน์ในการประเมินกิจกรรมการอักเสบ ภาพตัดแนว冠状เป็นสิ่งจำเป็นเนื่องจากสามารถประเมินกล้ามเนื้อนอกลูกตาทั้งหมดยกเว้นกล้ามเนื้อเฉียงล่างพร้อมกัน ภาพตัดแนวแกนประเมินกล้ามเนื้อเรกตัสด้านในและด้านนอก
CT: แสดงให้เห็นกล้ามเนื้อนอกลูกตาหนาตัว (รูปแบบการหนาตัวของท้องกล้ามเนื้อโดยที่เอ็นกล้ามเนื้อยังคงปกติเป็นลักษณะเฉพาะของ TED) และใช้หน้าต่างกระดูกเพื่อประเมินผนังเบ้าตา
อัลตราซาวนด์แบบ B-scan: ใช้เป็นเครื่องมือเสริมในการประเมินการหนาตัวของกล้ามเนื้อนอกลูกตา
ระบบการให้คะแนน 7 รายการ (0-7 คะแนน) สำหรับประเมินกิจกรรมการอักเสบที่เสนอโดย Mourits และคณะในปี 1989 6)
7 รายการประเมิน: ① ปวดหลังลูกตาขณะพัก ② ปวดเมื่อขยับตา ③ หนังตาสีแดง ④ หนังตาบวม ⑤ เยื่อบุตาสีแดง ⑥ เยื่อบุตาบวมน้ำ ⑦ ต่อมน้ำตา/รอยพับรูปพระจันทร์เสี้ยวบวม
CAS ≥ 3/7 ถือเป็นระยะ active และเป็นข้อบ่งชี้สำหรับการรักษาด้วยสเตียรอยด์แบบพัลส์ CAS ≥ 4/7 เป็นเกณฑ์การคัดเข้าในการทดลองแบบสุ่มของ teprotumumab
| ความรุนแรง | เกณฑ์ | แนวทางการรักษา |
|---|---|---|
| เล็กน้อย | ผลกระทบต่อชีวิตประจำวันเล็กน้อย | เสริมซีลีเนียม + ติดตามผล |
| ปานกลางถึงรุนแรง | หนังตาหด ≥2 มม. ตาโปน ≥3 มม. เหนือค่าปกติ เห็นภาพซ้อน | สเตียรอยด์พัลส์ เทโปรทูมูแมบ |
| คุกคามการมองเห็น | โรคเส้นประสาทตาถูกกดทับ แผลที่กระจกตา | ผ่าตัดลดความดันเบ้าตาฉุกเฉินหรือสเตียรอยด์ขนาดสูง |
การจำแนกตาม EUGOGO (European Group on Graves’ Orbitopathy) ตามแนวทางปฏิบัติทางคลินิกปี 2021 1) การจำแนก NOSPECS (ชั้น 0–6) และ VISA (การมองเห็น การอักเสบ ตาเหล่ ลักษณะภายนอก) ยังใช้ในการประเมินความรุนแรงด้วย
| โรคที่ต้องแยก | จุดที่ใช้แยก | ผลการตรวจภาพ |
|---|---|---|
| โรคตาที่เกี่ยวข้องกับ IgG4 | ต่อมน้ำตาโต + กล้ามเนื้อนอกลูกตาโต, IgG4 ในซีรัมสูง | ต่อมน้ำตาและกล้ามเนื้อนอกลูกตาโตแบบกระจาย |
| กล้ามเนื้อนอกลูกตาอักเสบ (กล้ามเนื้อเบ้าตาอักเสบ) | เริ่มเฉียบพลัน ปวดรุนแรง | หนาตัวบริเวณเอ็นยึด (ในโรคตาจากต่อมไทรอยด์ หนาตัวที่ท้องกล้ามเนื้อ ส่วนเอ็นยึดปกติ) |
| เนื้องอกเบ้าตา เนื้องอกแพร่กระจาย | ข้างเดียว ลุกลาม | เกิดก้อน |
เป็นระบบการให้คะแนน 7 รายการ (0-7 คะแนน) เพื่อประเมินการอักเสบของโรคตาต่อมไทรอยด์ โดยประเมิน 7 รายการ ได้แก่ ① ปวดหลังลูกตาขณะพัก ② ปวดเมื่อขยับตา ③ หนังตาสีแดง ④ หนังตาบวม ⑤ เยื่อบุตาสีแดง ⑥ เยื่อบุตาบวมน้ำ ⑦ ต่อมน้ำตาหรือรอยพับครึ่งดวงตาบวม คะแนน ≥3 ถือเป็นระยะที่มีกิจกรรมของโรค เป็นตัวบ่งชี้สำคัญในการเลือกการรักษา ใช้ในการพิจารณาความเหมาะสมของการรักษาด้วยสเตียรอยด์แบบพัลส์หรือเทโพรทูมูแมบ
การทำให้การทำงานของต่อมไทรอยด์กลับสู่ปกติเป็นเงื่อนไขที่จำเป็น และการทำงานร่วมกับแผนกต่อมไร้ท่อเป็นสิ่งที่ขาดไม่ได้ การให้คำแนะนำเลิกบุหรี่ ดำเนินการในทุกกรณีเพื่อกำจัดการสูบบุหรี่ ซึ่งเป็นปัจจัยเสี่ยงที่ใหญ่ที่สุดต่อการกำเริบของโรคและการดื้อต่อการรักษา
การเสริมซีลีเนียม: การเสริมซีลีเนียม 200 ไมโครกรัม/วัน เป็นเวลา 6 เดือน มีประโยชน์และแนะนำให้ใช้เพื่อปรับปรุงกิจกรรมของโรคใน TED ระดับเล็กน้อย10)
การปกป้องกระจกตาและผิวตา: การใช้น้ำตาเทียมและยาหยอดปกป้องกระจกตาบ่อยๆ รวมถึงการป้ายยาขี้ผึ้งตาก่อนนอนเป็นพื้นฐาน ในกรณีตาแห้งรุนแรง ให้พิจารณาการเย็บหนังตาด้านข้าง (lateral tarsorrhaphy)
การให้สเตียรอยด์แบบ pulse (ทางเลือกแรก): ให้ methylprednisolone 500–1000 มก./สัปดาห์ นาน 6–12 สัปดาห์1) การให้สเตียรอยด์ทางหลอดเลือดดำมีประสิทธิภาพมากกว่าทางปาก9) แนะนำให้ขนาดสะสมไม่เกิน 8 กรัม (เพื่อลดความเสี่ยงต่อตับถูกทำลาย)
แนวทางมาตรฐาน: หนึ่งคอร์สคือ methylprednisolone 1 กรัม × 3 วัน
Prednisolone ชนิดรับประทาน: ในกรณีปานกลางถึงรุนแรงที่ไม่สามารถให้ทางหลอดเลือดดำได้ ให้เริ่มที่ 1 มก./กก./วัน
การฉีดสเตียรอยด์เฉพาะที่: สำหรับอาการบวมหนังตาบนและหนังตาหดตัวจากการอักเสบ การฉีด triamcinolone acetonide (Kenacort-A® 1 หลอด) เฉพาะที่มีประสิทธิภาพ
Teprotumumab (ยับยั้ง IGF-1R): เป็นยาที่คาดว่าจะช่วยปรับปรุงภาวะตาโปนและภาพซ้อนในผู้ป่วย TED ระดับปานกลางถึงรุนแรงที่มีการดำเนินโรค การวิเคราะห์อภิมานจาก RCT 5 ฉบับ (รวม 411 ราย) พบว่าลดภาวะตาโปนอย่างมีนัยสำคัญ เพิ่มอัตราการบรรลุ CAS 0–1 ที่สัปดาห์ที่ 24 อย่างมีนัยสำคัญ และเพิ่มอัตราการดีขึ้นของภาพซ้อนอย่างมีนัยสำคัญ 4) โดยไม่เพิ่มเหตุการณ์ไม่พึงประสงค์ร้ายแรงอย่างมีนัยสำคัญ หลักฐานสร้างขึ้นจาก RCT หลักสองฉบับ: Smith et al. (2017, 42 รายเทียบกับ 45 ราย) 7) และ Douglas et al. (2020, 41 รายเทียบกับ 42 ราย) 8).
ริตูซิแมบ (โมโนโคลนอลแอนติบอดีต้าน CD20): การทดลองแบบสุ่มในหลายสถาบันแสดงให้เห็นว่าอาจลดกิจกรรมของโรคใน TED ระดับปานกลางถึงรุนแรงที่ดื้อต่อการรักษา12).
โทซิลิซูแมบ (ยาที่ยับยั้งตัวรับ IL-6): มีการพิจารณาใช้ในผู้ป่วยที่ดื้อต่อสเตียรอยด์และริตูซิแมบ
ใน TED ระดับปานกลางถึงรุนแรง จะทำการฉายรังสีบริเวณเบ้าตาร่วมกับการรักษาด้วยยากดภูมิคุ้มกัน โดยปกติจะฉายรังสี 20 Gy/10 ครั้ง ในระยะเวลา 2 สัปดาห์ การใช้ร่วมกับสเตียรอยด์ถือว่ามีประสิทธิภาพมากกว่าการใช้ยาเดี่ยว
โดยหลักการแล้ว การผ่าตัดจะวางแผนหลังจากเข้าสู่ระยะคงที่ของเส้นโค้ง Rundle และการอักเสบสงบลงแล้ว ต้องปฏิบัติตามลำดับการผ่าตัดอย่างเคร่งครัด เนื่องจากผลของการผ่าตัดก่อนหน้าส่งผลโดยตรงต่อแผนการผ่าตัดครั้งต่อไป
ขั้นตอนที่ 1: การลดความดันในเบ้าตา
ข้อบ่งชี้: ตาโปนรุนแรง, โรคเส้นประสาทตาถูกกดทับ (ข้อบ่งชี้ฉุกเฉิน)
เทคนิคและผลลัพธ์: มี 5 เทคนิคที่ใช้การผสมผสานระหว่างผนังด้านใน พื้น ผนังด้านนอก และไขมัน การลดความดันหนึ่งผนังช่วยให้ตาโปนดีขึ้น -1.4 ถึง -2.3 มม. การลดความดันสามผนังร่วมกับไขมันช่วยให้ดีขึ้น -4.6 ถึง -5.0 มม.
การศึกษาแบบหลายศูนย์ใน 633 ตา ยืนยันความคงที่และความสามารถในการทำซ้ำโดยไม่มีความแตกต่างอย่างมีนัยสำคัญระหว่างศัลยแพทย์สำหรับเทคนิคเดียวกัน11).
ขั้นตอนที่ 2: การผ่าตัดตาเหล่
ข้อบ่งชี้: ภาพซ้อนและความผิดปกติของการเคลื่อนไหวลูกตาหลังจากระยะไม่อักเสบคงที่
เทคนิคพื้นฐาน: การเลื่อนกล้ามเนื้อเรคตัสล่างไปด้านหลังเป็นวิธีที่พบบ่อยที่สุด ปริมาณการผ่าตัดขึ้นอยู่กับระดับของตาเหล่แบบจำกัดการเคลื่อนไหว
ยังทำเพื่อจัดการกับภาพซ้อนที่เกิดขึ้นใหม่ (ประมาณ 30%) หลังการผ่าตัดลดความดันในเบ้าตา
ขั้นตอนที่ 3: การผ่าตัดเปลือกตา
ข้อบ่งชี้: หนังตาหดรั้งในระยะไม่อักเสบคงที่ ปัญหาทางหน้าที่หรือความสวยงาม
เทคนิคการผ่าตัด: สำหรับหนังตาบนหดรั้ง ให้เลือกตัดกล้ามเนื้อมึลเลอร์หรือเลื่อนกล้ามเนื้อลิเวเตอร์พาลพีบรีสุพีเรียริส การผ่าตัดร่วมกันระหว่างตัดกล้ามเนื้อมึลเลอร์และเลื่อนกล้ามเนื้อลิเวเตอร์มีรายงานผลลัพธ์ที่ดี
วางแผนหลังจากการเปลี่ยนแปลงหลังผ่าตัดลดเบ้าตาและผ่าตัดตาเหล่คงที่แล้ว
การผ่าตัดทำตามลำดับ: การลดความดันในเบ้าตา → การผ่าตัดตาเหล่ → การผ่าตัดเปลือกตา สิ่งสำคัญคือต้องทำตามลำดับนี้เพราะผลของการผ่าตัดก่อนหน้าส่งผลต่อแผนการผ่าตัดครั้งต่อไป โดยหลักการแล้ว การผ่าตัดใดๆ จะวางแผนหลังจากเข้าสู่ระยะไม่มีการอักเสบ (ระยะคงที่ของเส้นโค้ง Rundle) การผ่าตัดในระยะอักเสบจะเพิ่มความเสี่ยงต่อความผันผวนหลังผ่าตัดและการกลับเป็นซ้ำ
เป็นโมโนโคลนอลแอนติบอดีที่ยับยั้งตัวรับ IGF-1 (IGF-1R) มันปิดกั้นสัญญาณเชิงซ้อนของ IGF-1R และ TSHR บนไฟโบรบลาสต์ในเบ้าตา ยับยั้งการอักเสบและการบวมของเนื้อเยื่อ การวิเคราะห์อภิมานจาก RCT 5 รายการ (รวม 411 ราย) ยืนยันการปรับปรุงอย่างมีนัยสำคัญในภาวะตายื่น การเห็นภาพซ้อน และ CAS ไม่มีการเพิ่มขึ้นอย่างมีนัยสำคัญของเหตุการณ์ไม่พึงประสงค์ร้ายแรง แต่ความปลอดภัยระยะยาว (ความผิดปกติทางการได้ยิน ระดับน้ำตาลในเลือดสูง ฯลฯ) ยังอยู่ระหว่างการประเมิน
ความผิดปกติของภูมิคุ้มกันที่เกี่ยวข้องกับความผิดปกติของต่อมไทรอยด์กระตุ้นให้เกิดการอักเสบของเนื้อเยื่อภายในเบ้าตา ทำให้ปริมาตรของเนื้อเยื่อไขมันในเบ้าตาและกล้ามเนื้อนอกลูกตาเพิ่มขึ้น ความดันหลังลูกตาที่สูงขึ้นทำให้เกิดตาโปน
พยาธิสภาพของเนื้อเยื่อไขมันในเบ้าตา: เซลล์ไขมันขยายใหญ่ขึ้นและมีการแทรกซึมของลิมโฟไซต์ในเนื้อเยื่อคั่นกลาง ร่วมกับอาการบวมน้ำและการเกิดแผลเป็นจากการอักเสบเรื้อรัง การสังเคราะห์ไกลโคซามิโนไกลแคน (GAG) และกรดไฮยาลูโรนิกที่เพิ่มขึ้นทำให้เกิดการคั่งของของเหลวและเนื้อเยื่อบวม
พยาธิสภาพของกล้ามเนื้อนอกลูกตา: มีการแทรกซึมของเซลล์อักเสบที่นำโดยลิมโฟไซต์ระหว่างเส้นใยกล้ามเนื้อลาย ทำให้เส้นใยกล้ามเนื้อเสื่อมและตาย เกิดอาการบวมน้ำและหนาตัวของเนื้อเยื่อคั่นกลางจากการอักเสบ และมีเนื้อเยื่อเกี่ยวพันเพิ่มขึ้นระหว่างเส้นใยกล้ามเนื้อ ทำให้กล้ามเนื้อนอกลูกตาขยายใหญ่ขึ้น กล้ามเนื้อเรกตัสล่างถูกกระทบบ่อยที่สุด รองลงมาคือเรกตัสกลาง เรกตัสบน และเรกตัสนอก ดังนั้นความผิดปกติในการเงยตาจึงพบบ่อยที่สุด รองลงมาคือความผิดปกติในการกางตา
เกิดจากสองกลไกร่วมกัน
① พยาธิสภาพของกล้ามเนื้อลิเวเตอร์พาลพีบราซูพีเรียริส: เซลล์กล้ามเนื้อบวมน้ำจากการอักเสบทำให้หนังตาบวม เนื้อเยื่อไขมันแทรกซึมระหว่างเส้นใยกล้ามเนื้อ และเซลล์กล้ามเนื้อตายและกลายเป็นแผลเป็น ทำให้การทำงานของกล้ามเนื้อลิเวเตอร์เปลี่ยนแปลงไป
②พยาธิสภาพของกล้ามเนื้อมึลเลอร์: กล้ามเนื้อมึลเลอร์ซึ่งเป็นกล้ามเนื้อเรียบที่ควบคุมโดยระบบประสาทซิมพาเทติก จะหดตัวอย่างต่อเนื่องเนื่องจากภาวะซิมพาเทติกเกินที่เกิดร่วมกับภาวะต่อมไทรอยด์ทำงานเกิน ทำให้ยกแผ่นกระดูกอ่อนเปลือกตาและขยายรอยแยกเปลือกตาให้กว้างขึ้น
แอนติบอดีต่อตนเองต่อตัวรับ TSH (TRAb) กระตุ้น TSHR บนไฟโบรบลาสต์ในเบ้าตา ซึ่งผ่านสัญญาณขั้นปลายทำให้เกิดการผลิตไซโตไคน์ที่ก่อการอักเสบ (TNF-α, IL-6, IL-1β) เซลล์ที CD4+/CD8+ แทรกซึมเข้าไปในเนื้อเยื่อเบ้าตาและขยายการตอบสนองการอักเสบ ไฟโบรบลาสต์ที่ถูกกระตุ้นจะแยกตัวเป็นเซลล์ไขมันและไมโอไฟโบรบลาสต์ ซึ่งทำให้เกิดการขยายตัวของไขมันในเบ้าตาและพังผืดของกล้ามเนื้อนอกลูกตาตามลำดับ3)
IGF-1R (ตัวรับ IGF-1) สร้างสารเชิงซ้อนกับ TSHR และมีส่วนร่วมแบบเสริมฤทธิ์กันในการกระตุ้นไฟโบรบลาสต์ในเบ้าตา4) การปิดกั้นสัญญาณของสารเชิงซ้อนนี้เป็นกลไกการออกฤทธิ์ของเทโปรทูมูแมบ
การเปลี่ยนผ่านตามธรรมชาติจากระยะอักเสบที่ยังดำเนินอยู่ (ปกติ 1-3 ปี) ไปสู่ระยะคงที่ (ไม่มีการอักเสบ) ได้ถูกทำให้เป็นแนวคิดในรูปของเส้นโค้งรันเดิล13) การแทรกแซงทางการรักษาที่แท้จริงจะถูกเลือกหลังจากประเมินการดำเนินโรคและความรุนแรง1) ในระยะดำเนินอยู่ การรักษาระงับการอักเสบจะได้รับความสำคัญก่อน และการผ่าตัดจะถูกวางแผนในระยะคงที่ที่ไม่มีการอักเสบ
หลังจากได้รับการอนุมัติจาก FDA ข้อมูลยังคงสะสมอย่างต่อเนื่อง การวิเคราะห์อภิมานจากการทดลองแบบสุ่มที่มีกลุ่มควบคุม 5 การทดลอง (รวม 411 ราย) 4) ยืนยันประสิทธิภาพและความปลอดภัย แต่ผลการทดลองระยะที่ 4 เกี่ยวกับความปลอดภัยระยะยาว (เช่น การสูญเสียการได้ยิน ระดับน้ำตาลในเลือดสูง) เป็นที่จับตามอง นอกจากนี้ยังมีการพิจารณาความเป็นไปได้ในการขยายข้อบ่งชี้ไปยัง TED ในระยะไม่เคลื่อนไหว
การศึกษาแบบหลายศูนย์ใน 7 สถาบัน ศัลยแพทย์ 7 คน และตา 633 ข้าง 11) ยืนยันว่าไม่มีความแตกต่างอย่างมีนัยสำคัญระหว่างศัลยแพทย์เมื่อทำหัตถการเดียวกัน นี่เป็นข้อค้นพบที่สำคัญที่สนับสนุนความถูกต้องทางสถิติของ RCT แบบหลายศูนย์ การผ่าตัดลดแรงกดผนังด้านในด้วยกล้องส่องรายงานว่าช่วยให้ระดับลูกตายื่นดีขึ้นอย่างมีนัยสำคัญเมื่อเทียบกับการผ่าตัดแบบเปิดในการลดแรงกดผนังด้านในร่วมกับพื้นเบ้าตา (-3.67 มม. เทียบกับ -2.97 มม., p=0.008) นอกจากนี้ยังแสดงให้เห็นว่าระดับลูกตายื่นก่อนผ่าตัดมีความสัมพันธ์อย่างมีนัยสำคัญทางสถิติกับการเปลี่ยนแปลงของระดับลูกตายื่นหลังผ่าตัด (p<0.001) ซึ่งย้ำถึงความสำคัญของการประเมินก่อนผ่าตัด
เชื่อว่าความผันผวนของ TRAb และ TSAb ในระยะ active มีความสัมพันธ์กับ CAS และกำลังมีการวิจัยเกี่ยวกับการเลือกการรักษาโดยใช้ตัวบ่งชี้ทางชีวภาพ นอกจากนี้ยังรอคอย RCT ขนาดใหญ่ของ tocilizumab (ยาที่ยับยั้ง IL-6) สำหรับผู้ป่วยที่ดื้อต่อการรักษา
Bartalena L, Kahaly GJ, Baldeschi L, et al. The 2021 European Group on Graves’ Orbitopathy (EUGOGO) clinical practice guidelines for the medical management of Graves’ orbitopathy. Eur J Endocrinol. 2021;184(4):G43-G67.
Prummel MF, Wiersinga WM. Smoking and risk of Graves’ disease. JAMA. 1993;269(4):479-482.
Bahn RS. Graves’ ophthalmopathy. N Engl J Med. 2010;362(8):726-738.
Cong X, Pei L, Hu H. Teprotumumab for treating active thyroid eye disease: a meta-analysis. Medicine. 2024;103(18):e38059.
Wang Y, Sharma A, Padnick-Silver L, et al. Physician-perceived impact of thyroid eye disease on patient quality of life in the United States. Ophthalmol Ther. 2021;10(1):75-87.
Mourits MP, Koornneef L, Wiersinga WM, et al. Clinical criteria for the assessment of disease activity in Graves’ ophthalmopathy: a novel approach. Br J Ophthalmol. 1989;73(8):639-644.
Smith TJ, Kahaly GJ, Ezra DG, et al. Teprotumumab for thyroid-associated ophthalmopathy. N Engl J Med. 2017;376(18):1748-1761.
Douglas RS, Kahaly GJ, Patel A, et al. Teprotumumab for the treatment of active thyroid eye disease. N Engl J Med. 2020;382(4):341-352.
Kahaly GJ, Pitz S, Hommel G, et al. Randomized, single blind trial of intravenous versus oral steroid monotherapy in Graves’ orbitopathy. J Clin Endocrinol Metab. 2005;90(9):5234-5240.
Marcocci C, Kahaly GJ, Krassas GE, Bartalena L, Prummel M, Stahl M, et al.; European Group on Graves’ Orbitopathy. Selenium and the course of mild Graves’ orbitopathy. N Engl J Med. 2011;364(20):1920-1931. PMID: 21591944. doi:10.1056/NEJMoa1012985.
Hong A, Shoji MK, Villatoro GA, et al. Intersurgeon variability in proptosis reduction after orbital decompression for thyroid eye disease: a multicenter analysis. Ophthalmic Plast Reconstr Surg. 2024;40(3).
Salvi M, Vannucchi G, Campi I, et al. Rituximab treatment in active moderate-to-severe Graves’ orbitopathy: an international, multicenter, single-blind, randomized placebo-controlled study. J Clin Endocrinol Metab. 2015;100(11):422-431.
Rundle FF, Wilson CW. Development and course of exophthalmos and ophthalmoplegia in Graves’ disease with special reference to the effect of thyroidectomy. Clin Sci. 1945;5(3-4):177-194. PMID: 21011937.