علائم پلکی
تورم پلک فوقانی، پسرفت پلک فوقانی و تأخیر پلک فوقانی مشخصه هستند.
علامت دالریمپل: گشاد شدن شکاف پلکی به دلیل پسرفت پلک فوقانی.
نشانه فون گریف: افتادگی پلک فوقانی هنگام نگاه به پایین (lid lag).

بیماری چشم تیروئیدی (TED) یک بیماری خودایمنی است که در آن ناهنجاری عملکرد تیروئید باعث التهاب بافتهای داخل حدقه شده و حجم بافت چربی حدقه و عضلات خارج چشمی را افزایش میدهد. افزایش فشار بافت پشت کره چشم منجر به بیرونزدگی کره چشم میشود. شایعترین شکل آن همراه با پرکاری تیروئید (بیماری گریوز/بازدو) است، اما ممکن است با عملکرد طبیعی تیروئید نیز رخ دهد (افتالموپاتی یوتیروئید). بیماری چشم تیروئیدی مستقل از هورمون تیروئید پیشرفت میکند و یکی از بیماریهای خودایمنی مرتبط با آنتیبادیهای ضد تیروئید است.
حدود 40 تا 50 درصد از بیماران مبتلا به بیماری گریوز (بازدو) علائم چشمی دارند. درگیری شدید حدقه نسبتاً نادر است و در 5 تا 10 درصد از کل بیماران گریوز رخ میدهد.
شیوع در زنان 16/100,000 نفر-سال و در مردان 2.9/100,000 نفر-سال گزارش شده است1). سن شروع دو اوج دارد: دهه 40-50 و دهه 60-701). سیگار کشیدن بزرگترین عامل خطر برای بیماری چشم تیروئیدی است و خطر ابتلا را به طور قابل توجهی افزایش میدهد2). در جوانان، برجستگی چشم علامت اصلی است، در حالی که در سالمندان، دوبینی علامت اصلی است.
سیر طبیعی بیماری چشم تیروئیدی از منحنی راندل پیروی میکند: یک فاز فعال (التهابی، معمولاً 1-3 سال) و سپس یک فاز پایدار (غیرالتهابی)3). زمان مداخله درمانی بر اساس این منحنی تعیین میشود.
علائم پلکی
تورم پلک فوقانی، پسرفت پلک فوقانی و تأخیر پلک فوقانی مشخصه هستند.
علامت دالریمپل: گشاد شدن شکاف پلکی به دلیل پسرفت پلک فوقانی.
نشانه فون گریف: افتادگی پلک فوقانی هنگام نگاه به پایین (lid lag).
برآمدگی چشم
در جوانان شایعتر است (به دلیل ضعف بافتهای حمایتکننده کاسه چشم).
با دستگاه اگزوفتالمومتر هرتل اندازهگیری میشود. محدوده طبیعی در ژاپنیها ۱۰ تا ۱۵ میلیمتر (میانگین ۱۳ میلیمتر) است. تفاوت بین دو چشم کمتر از ۲ میلیمتر طبیعی است.
دوبینی
در سالمندان شایعتر است. علت آن استرابیسموس محدودکننده ناشی از التهاب و فیبروز عضلات خارج چشمی است.
عضله راست تحتانی بیشترین درگیری را دارد → محدودیت نگاه به بالا شایعترین است. بعد از آن، درگیری عضله راست داخلی باعث محدودیت نگاه به خارج میشود.
اختلال بینایی
ناشی از آسیب قرنیه (کراتوپاتی ناشی از اگزوپتالموس) یا نوروپاتی فشاری بینایی (DON) است.
DON در حدود ۵٪ از کل موارد رخ میدهد1) و نیاز به مداخله فوری دارد. علائم آن شامل RAPD مثبت، کاهش CFF و نقص میدان بینایی است.
حتی در شرایطی که عملکرد تیروئید طبیعی است، میتواند به عنوان افتالموپاتی یوتیروئید بروز کند. بیماری چشمی تیروئید یک بیماری خودایمنی است که مستقل از سطح هورمون تیروئید پیشرفت میکند و در صورت مثبت بودن آنتیبادیهای مرتبط با تیروئید (TRAb، TSAb) میتواند رخ دهد. در صورت وجود عقبرفتگی پلک یا بیرونزدگی چشم، حتی با عملکرد طبیعی تیروئید، آزمایش آنتیبادیهای مرتبط با تیروئید ضروری است.
در مراحل اولیه، خشکی، سوزش، اشکریزی و حساسیت به نور غالب است. با پیشرفت بیماری، تورم اطراف چشم، بیرونزدگی کره چشم، دوبینی و عقبرفتگی پلک آشکار میشود و در موارد شدید به زخم قرنیه و نوروپاتی فشاری عصب بینایی منجر میشود.
یافتههای پلکی مشخصه بیماری چشم تیروئید در زیر آورده شده است.
| نام علامت | نام انگلیسی | یافته |
|---|---|---|
| نشانه دالریمپل | Dalrymple sign | بزرگ شدن شکاف پلک به دلیل عقبرفتگی پلک فوقانی. سفیدی چشم در بالای لیمبوس قرنیه فوقانی نمایان میشود. |
| نشانه فون گریف | lid lag | پدیدهای که در آن پلک فوقانی هنگام نگاه به پایین با تأخیر دنبال میکند. |
| نشانه اشتلواگ | Stellwag sign | کاهش پلک زدن و بسته شدن ناقص پلک |
| نشانه گیفورد | Gifford sign | دشواری در برگرداندن پلک فوقانی |
برجستگی چشم با استفاده از اگزوفتالمومتر هرتل اندازهگیری میشود. مقدار طبیعی در ژاپنیها ۱۰ تا ۱۵ میلیمتر (میانگین ۱۳ میلیمتر) است و تفاوت بین دو چشم کمتر از ۲ میلیمتر طبیعی محسوب میشود. مقدار هرتل بیش از ۱۸ میلیمتر نشاندهنده برجستگی چشم است1).
این عارضه در اثر فشار عضلات خارج چشمی ضخیمشده بر عصب بینایی در ناحیه راس مدار (orbital apex) ایجاد میشود. در حدود ۵٪ از کل موارد رخ میدهد1) و اورژانسی است. RAPD مثبت، کاهش CFF و نقص میدان بینایی از نشانههای اولیه هستند. اختلال دید رنگی نیز یافته مهمی است.
درد، دوبینی و تغییر ظاهر از عوامل اصلی کاهش کیفیت زندگی هستند. شیوع همزمان اضطراب و افسردگی در بیماران تیروئیدی چشمی ۳۶٪ است که حدود دو برابر جمعیت عمومی (۱۸.۹٪) میباشد5). ۶۲٪ از بیماران متوسط و ۸۹٪ از بیماران شدید دارای اختلال بالای کیفیت زندگی (نمره ≥۴ از ۷) هستند5). کاهش کیفیت زندگی مشابه یا کمتر از دیابت، آمفیزم و نارسایی قلبی گزارش شده است.
علت آن استرابیسموس (انحراف چشم) محدودکننده ناشی از بزرگشدن و انقباض عضلات خارج چشمی (به ویژه عضله راست تحتانی) به دلیل التهاب و فیبروز است که حرکت طبیعی چشم را محدود میکند. عضله راست تحتانی بیشترین فراوانی درگیری را دارد، بنابراین اختلال در نگاه به بالا شایعترین است. ترتیب فراوانی درگیری عضلات خارج چشمی به صورت عضله راست تحتانی > عضله راست داخلی > عضله راست فوقانی > عضله راست خارجی است و در افراد مسن شایعتر است.
اختلال عملکرد تیروئید باعث ایجاد پاسخ ایمنی غیرطبیعی میشود که التهاب بافتهای داخل حدقه را تحریک میکند. آنتیبادیهای خودایمن علیه گیرنده TSH (TRAb) گیرنده TSH را روی فیبروبلاستهای حدقه فعال کرده و تولید سایتوکاینهای التهابی (مانند TNF-α، IL-6، IL-1β) را القا میکنند. سلولهای T CD4+/CD8+ به بافت حدقه نفوذ کرده و پاسخ التهابی را تشدید میکنند.
فیبروبلاستهای فعال شده سنتز گلیکوزآمینوگلیکان (GAG) و هیالورونیک اسید را افزایش میدهند که منجر به ادم بافتی و احتباس آب میشود. تمایز فیبروبلاستها به سلولهای چربی و میوفیبروبلاستها باعث افزایش حجم چربی حدقه و پیشرفت فیبروز عضلات خارج چشمی میشود3).
IGF-1受容体(IGF-1R)はTSHRと複合体を形成し、眼窩線維芽細胞の活性化に相乗的に関与する4)。この機序がテプロツムマブ(IGF-1R阻害薬)の治療標的となっている。
喫煙が最大のリスク因子であり、発症リスク・重症化・治療抵抗性のいずれとも関連する2)。そのほか甲状腺機能の不安定化、放射性ヨード治療後の急性期、高齢・男性も重症化リスクに関与する。
سه علامت عقبرفتگی پلک، بیرونزدگی چشم و دوبینی در صورت وجود همزمان، به شدت نشاندهنده TED از نظر بالینی است. حتی اگر عملکرد تیروئید طبیعی باشد، در صورت مثبت بودن آنتیبادیهای خودایمن مرتبط با تیروئید، میتوان TED را تشخیص داد.
هورمونهای تیروئید (FT₄، FT₃)، TSH و آنتیبادیهای خودایمن تیروئید اندازهگیری میشوند. موارد اندازهگیری عبارتند از: TRAb (آنتیبادی گیرنده TSH)، TSAb (آنتیبادی محرک تیروئید)، آنتیبادی ضد TG (آنتیبادی ضد تیروگلوبولین) و آنتیبادی ضد TPO (آنتیبادی ضد پراکسیداز تیروئید). حداقل یکی از این موارد مثبت خواهد بود.
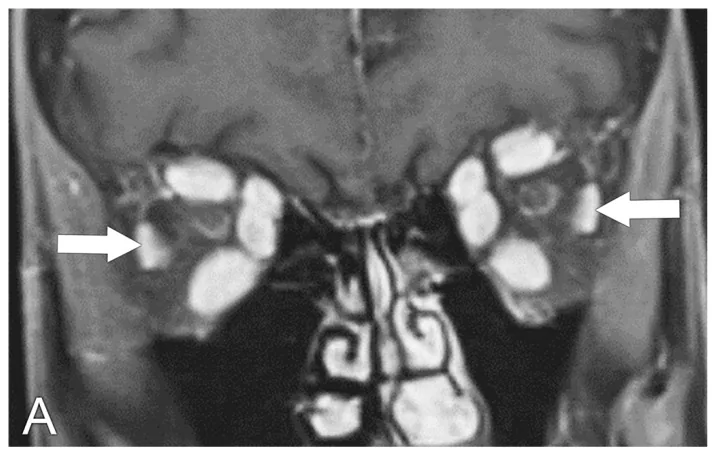
MRI (انتخاب اول): در تصاویر T1-weighted مورفولوژی عضلات خارج چشمی ارزیابی میشود. در روش STIR (short-TI inversion recovery)، محل التهاب به عنوان ناحیه با سیگنال بالا ظاهر میشود که برای ارزیابی فعالیت التهابی مفید است. برش کرونال ضروری است زیرا امکان ارزیابی همزمان تمام عضلات خارج چشمی به جز عضله مایل تحتانی را فراهم میکند. در برش محوری، عضلات راست داخلی و خارجی ارزیابی میشوند.
CT: ضخیم شدن عضلات خارج چشمی (الگوی بزرگ شدن شکم عضله با حفظ تاندون که مختص TED است) را تأیید کرده و برای ارزیابی دیواره استخوانی مدار از پنجره استخوانی استفاده میشود.
سونوگرافی B-scan: به صورت کمکی برای ارزیابی هیپرتروفی عضلات خارج چشمی استفاده میشود.
یک سیستم نمرهدهی ۷ موردی (۰-۷ امتیاز) برای ارزیابی فعالیت التهابی است که توسط Mourits و همکاران در سال ۱۹۸۹ پیشنهاد شده است6).
۷ مورد ارزیابی: ① درد خودبهخودی پشت کره چشم، ② درد هنگام حرکت چشم، ③ قرمزی پلک، ④ تورم پلک، ⑤ قرمزی ملتحمه، ⑥ ادم ملتحمه، ⑦ تورم کارونکل/چین هلالی.
CAS≥3/7 به عنوان فاز فعال در نظر گرفته شده و نشاندهنده اندیکاسیون پالستراپی استروئیدی است. CAS≥4/7 معیار ورود به کارآزمایی بالینی تصادفیشده تپروتوموماب است.
| شدت | معیار | رویکرد درمانی |
|---|---|---|
| خفیف | تأثیر ناچیز بر زندگی روزمره | مکمل سلنیوم + پیگیری |
| متوسط تا شدید | عقبرفتگی پلک ≥2 میلیمتر، بیرونزدگی ≥3 میلیمتر بیش از حد طبیعی، دوبینی | پالس استروئید، تپروتوموماب |
| تهدیدکننده بینایی | نوروپاتی فشاری بینایی، زخم قرنیه | جراحی فوری رفع فشار کاسه چشم یا استروئید با دوز بالا |
این طبقهبندی بر اساس راهنمای بالینی 2021 EUGOGO (گروه چشمهای گریوز اروپا) است 1). طبقهبندی NOSPECS (کلاسهای 0 تا 6) و طبقهبندی VISA (بینایی، التهاب، استرابیسم، ظاهر) نیز برای ارزیابی شدت استفاده میشوند.
| بیماری افتراقی | نکات افتراقی | یافتههای تصویربرداری |
|---|---|---|
| بیماری چشمی مرتبط با IgG4 | بزرگ شدن غده اشکی + بزرگ شدن عضلات خارج چشمی، IgG4 سرم بالا | بزرگ شدن منتشر غده اشکی و عضلات خارج چشمی |
| میوزیت خارج چشمی (میوزیت اربیت) | شروع حاد، درد شدید | ضخیم شدن از ناحیه تاندون (در بیماری تیروئیدی چشم، ضخیم شدن شکم عضله است و تاندون حفظ میشود) |
| تومور اربیت و تومور متاستاتیک | یک طرفه و پیشرونده | تشکیل توده |
یک سیستم امتیازدهی ۷ موردی (۰-۷ امتیاز) برای ارزیابی فعالیت التهابی بیماری چشم تیروئید است. هفت مورد شامل: ① درد خودبهخودی پشت کره چشم، ② درد هنگام حرکت چشم، ③ قرمزی پلک، ④ تورم پلک، ⑤ قرمزی ملتحمه، ⑥ ادم ملتحمه، ⑦ تورم کارونکل/چین هلالی ارزیابی میشود و امتیاز ۳ یا بیشتر نشاندهنده فاز فعال است. این یک شاخص مهم برای انتخاب درمان است و برای تصمیمگیری در مورد پالسدرمانی استروئیدی و تپروتوموماب استفاده میشود.
عادیسازی عملکرد تیروئید یک شرط ضروری است و همکاری با بخش غدد درونریز حیاتی میباشد. مشاوره ترک سیگار برای حذف سیگار که بزرگترین عامل خطر برای تشدید بیماری و مقاومت به درمان است، در تمام موارد انجام میشود.
مکمل سلنیوم: برای TED خفیف، مصرف سلنیوم ۲۰۰ میکروگرم در روز به مدت ۶ ماه برای بهبود فعالیت بیماری مفید و توصیه میشود10).
محافظت از قرنیه و سطح چشم: استفاده مکرر از اشک مصنوعی و قطرههای محافظ قرنیه و استفاده از پماد چشم قبل از خواب اساس درمان است. در موارد لاگوفتالموس شدید، تارسورافی جانبی (lateral tarsorrhaphy) در نظر گرفته میشود.
پالس درمانی با استروئید (خط اول): متیلپردنیزولون ۵۰۰ تا ۱۰۰۰ میلیگرم در هفته به مدت ۶ تا ۱۲ هفته تجویز میشود1). استروئید وریدی نسبت به استروئید خوراکی مؤثرتر است9). دوز تجمعی توصیه شده کمتر از ۸ گرم (برای کاهش خطر آسیب کبدی).
پروتکل استاندارد: متیلپردنیزولون ۱ گرم به مدت ۳ روز به عنوان یک دوره تجویز میشود.
پردنیزولون خوراکی: در موارد متوسط تا شدید که تزریق وریدی امکانپذیر نیست، با دوز ۱ میلیگرم/کیلوگرم/روز شروع میشود.
تزریق موضعی استروئید: برای ادم پلک فوقانی و عقبرفتگی التهابی پلک، تزریق موضعی تریامسینولون استونید (کناکورت-A® ۱ آمپول) مؤثر است.
تپروتوموماب (مهارکننده IGF-1R): این دارو برای TED فعال با شدت متوسط تا شدید استفاده میشود و میتواند باعث بهبود برجستگی چشم و دوبینی شود. در یک متاآنالیز از 5 کارآزمایی تصادفیشده (مجموعاً 411 نفر)، کاهش قابل توجه برجستگی چشم، دستیابی به CAS 0-1 در هفته 24، و بهبود دوبینی تأیید شده است4)، بدون افزایش قابل توجه عوارض جانبی جدی. شواهد اصلی از دو کارآزمایی تصادفیشده توسط Smith و همکاران (2017، 42 نفر در مقابل 45 نفر)7) و Douglas و همکاران (2020، 41 نفر در مقابل 42 نفر)8) به دست آمده است.
ریتوکسیماب (آنتیبادی مونوکلونال ضد CD20): یک کارآزمایی چندمرکزی تصادفیشده نشان داده است که این دارو ممکن است فعالیت بیماری را در TED مقاوم با شدت متوسط تا شدید کاهش دهد12).
توسیلیزوماب (مهارکننده گیرنده IL-6): استفاده از این دارو در موارد مقاوم به استروئید و ریتوکسیماب در حال بررسی است.
در TED با شدت متوسط تا شدید، پرتودرمانی مداری به همراه درمان سرکوبکننده ایمنی انجام میشود. معمولاً 20 گری در 10 جلسه طی 2 هفته تابش داده میشود. ترکیب با استروئید مؤثرتر از درمان به تنهایی است.
جراحی اصولاً پس از ورود به فاز پایدار منحنی راندل و فروکش التهاب برنامهریزی میشود. ترتیب انجام باید به دقت رعایت شود، زیرا نتیجه جراحی قبلی مستقیماً بر برنامه جراحی بعدی تأثیر میگذارد.
مرحله 1: جراحی کاهش فشار کاسه چشم
اندیکاسیون: بیرونزدگی شدید چشم، نوروپاتی فشاری عصب بینایی (اندیکاسیون اورژانسی)
روش جراحی و اثربخشی: پنج نوع روش جراحی شامل ترکیبی از دیواره داخلی، کف، دیواره خارجی و چربی وجود دارد. کاهش فشار یک دیواره منجر به بهبود 1.4- تا 2.3- میلیمتر و کاهش فشار سه دیواره همراه با چربی منجر به بهبود 4.6- تا 5.0- میلیمتر در بیرونزدگی چشم میشود.
در یک مطالعه چندمرکزی روی 633 چشم، تکرارپذیری پایدار و بدون تفاوت معنیدار بین جراحان برای یک روش جراحی یکسان تأیید شده است11).
مرحله ۲: جراحی استرابیسم
مرحله ۳: جراحی پلک
اندیکاسیون: عقبرفتگی پلک، مشکلات عملکردی و زیبایی در مرحله تثبیت غیرالتهابی
روش جراحی: برای عقبرفتگی پلک فوقانی، میتوان میوتومی عضله مولر یا عقبگذاری عضله بالابرنده پلک فوقانی را انتخاب کرد. ترکیب میوتومی عضله مولر و عقبگذاری عضله بالابرنده نتایج خوبی گزارش شده است.
برنامهریزی جراحی پس از پایدار شدن تغییرات پس از جراحی کاهش فشار کاسه چشم و جراحی استرابیسم انجام میشود.
جراحی به ترتیب رفع فشار مدار چشم → جراحی استرابیسم → جراحی پلک انجام میشود. رعایت این ترتیب مهم است زیرا نتیجه جراحی قبلی بر برنامه جراحی بعدی تأثیر میگذارد. هر یک از جراحیها اصولاً پس از ورود به مرحله غیرالتهابی (مرحله پایدار منحنی راندل) برنامهریزی میشود. انجام جراحی در مرحله التهابی خطر نوسانات پس از عمل و عود را افزایش میدهد.
یک آنتیبادی مونوکلونال است که گیرنده IGF-1 (IGF-1R) را مهار میکند. با مسدود کردن سیگنال کمپلکس IGF-1R و TSHR روی فیبروبلاستهای مداری، التهاب و تورم بافت را کاهش میدهد. متاآنالیز 5 کارآزمایی بالینی تصادفیشده (مجموعاً 411 مورد) بهبود قابل توجهی در پروپتوز، دوبینی و نمره CAS را تأیید کرده است. افزایش قابل توجهی در عوارض جانبی جدی مشاهده نشده است، اما ایمنی طولانیمدت (کم شنوایی، هیپرگلیسمی و غیره) همچنان در حال ارزیابی است.
اختلال عملکرد ایمنی ناشی از اختلال تیروئید باعث التهاب بافتهای داخل حدقه میشود و حجم بافت چربی حدقه و عضلات خارج چشمی را افزایش میدهد. افزایش فشار پشت کره چشم منجر به بیرونزدگی چشم میشود.
پاتولوژی بافت چربی حدقه: بزرگ شدن سلولهای چربی و نفوذ لنفوسیتها در بافت بینابینی رخ میدهد و ادم و تشکیل اسکار ناشی از التهاب مزمن مشاهده میشود. افزایش سنتز گلیکوزآمینوگلیکانها (GAG) و هیالورونیک اسید باعث احتباس مایع و تورم بافت میشود.
پاتولوژی عضلات خارج چشمی: نفوذ سلولهای التهابی عمدتاً لنفوسیتها بین فیبرهای عضلانی مخطط مشاهده میشود و فیبرهای عضلانی دچار دژنراسیون و نکروز میشوند. در بافت بینابینی، ادم و ضخیمشدگی ناشی از التهاب رخ میدهد و بافت همبند بین فیبرهای عضلانی افزایش یافته و هیپرتروفی عضلات خارج چشمی ایجاد میشود. شایعترین عضله درگیر، عضله راست تحتانی است و به ترتیب عضلات راست داخلی، راست فوقانی و راست خارجی کمتر درگیر میشوند. بنابراین اختلال در نگاه به بالا شایعترین و سپس اختلال در نگاه به خارج شایع است.
این پدیده در اثر ترکیب دو مکانیسم ایجاد میشود.
① پاتولوژی عضله بالابرنده پلک فوقانی: به دلیل التهاب، سلولهای عضلانی دچار ادم شده و پلک متورم میشود. بافت چربی بین فیبرهای عضلانی نفوذ کرده و سلولهای عضلانی دچار نکروز و اسکار شده و عملکرد عضله بالابرنده تغییر میکند.
②پاتولوژی عضله مولر: عضله مولر که یک عضله صاف با عصبدهی سمپاتیک است، به دلیل افزایش فعالیت سمپاتیک ناشی از پرکاری تیروئید، دچار انقباض مداوم شده و صفحه تارسال را بالا میکشد و شکاف پلکی را باز میکند.
آنتیبادیهای خودایمن علیه گیرنده TSH (TRAb) گیرنده TSH را روی فیبروبلاستهای مداری فعال کرده و از طریق سیگنالهای پاییندستی، سیتوکینهای التهابی (TNF-α، IL-6، IL-1β) تولید میکنند. سلولهای T CD4+/CD8+ به بافت مداری نفوذ کرده و پاسخ التهابی را تشدید میکنند. فیبروبلاستهای فعال شده به سلولهای چربی و میوفیبروبلاست تمایز مییابند که به ترتیب باعث انبساط چربی مداری و فیبروز عضلات خارج چشمی میشوند3).
گیرنده IGF-1 (IGF-1R) با گیرنده TSH کمپلکس تشکیل داده و به طور همافزایی در فعالسازی فیبروبلاستهای مداری شرکت میکند4). مسدود کردن این سیگنال کمپلکس، مکانیسم اثر تپروتوموماب است.
سیر طبیعی از فاز التهابی فعال (معمولاً ۱ تا ۳ سال) به فاز پایدار (غیرالتهابی) به عنوان منحنی راندل مفهومسازی شده است13). مداخلات درمانی واقعی بر اساس ارزیابی فعالیت و شدت بیماری انتخاب میشوند1). در فاز فعال، درمان سرکوبکننده التهاب اولویت دارد و در فاز پایدار غیرالتهابی، برنامه جراحی تنظیم میشود.
دادهها پس از تأیید FDA به طور مداوم جمعآوری میشوند. متاآنالیز پنج کارآزمایی تصادفیشده (مجموعاً ۴۱۱ مورد)4) اثربخشی و ایمنی را تأیید کرده است، اما نتایج آزمایش فاز IV برای ایمنی طولانیمدت (پیامدهای بلندمدت مانند کاهش شنوایی و هیپرگلیسمی) مورد توجه است. امکان گسترش اندیکاسیون به مرحله غیرفعال TED نیز در حال بررسی است.
یک مطالعه چندمرکزی بر روی ۷ مرکز، ۷ جراح و ۶۳۳ چشم 11) نشان داد که در صورت انجام یک روش جراحی یکسان، تفاوت معنیداری بین جراحان وجود ندارد. این یافته مهمی است که اعتبار آماری کارآزماییهای تصادفی کنترلشده چندمرکزی را تأیید میکند. کاهش فشار دیواره داخلی از طریق آندوسکوپی در مقایسه با جراحی باز برای کاهش فشار دیواره داخلی به همراه کف، بهبود قابلتوجهی در برجستگی چشم (۶۷/۳- میلیمتر در مقابل ۹۷/۲- میلیمتر، ۰۰۸/۰=p) گزارش شده است. همچنین نشان داده شده است که میزان برجستگی چشم قبل از عمل با تغییر برجستگی بعد از عمل ارتباط آماری معنیداری دارد (۰۰۱/۰>p) که اهمیت ارزیابی قبل از عمل را تأیید میکند.
تغییرات TRAb و TSAb در فاز فعال با CAS همبستگی دارد و تحقیقات در مورد انتخاب درمان بر اساس بیومارکرها در حال انجام است. همچنین برای توسیلیزوماب (مهارکننده IL-6) در موارد مقاوم به درمان، کارآزماییهای تصادفی کنترلشده در مقیاس بزرگ مورد انتظار است.
Bartalena L, Kahaly GJ, Baldeschi L, et al. The 2021 European Group on Graves’ Orbitopathy (EUGOGO) clinical practice guidelines for the medical management of Graves’ orbitopathy. Eur J Endocrinol. 2021;184(4):G43-G67.
Prummel MF, Wiersinga WM. Smoking and risk of Graves’ disease. JAMA. 1993;269(4):479-482.
Bahn RS. Graves’ ophthalmopathy. N Engl J Med. 2010;362(8):726-738.
Cong X, Pei L, Hu H. Teprotumumab for treating active thyroid eye disease: a meta-analysis. Medicine. 2024;103(18):e38059.
Wang Y, Sharma A, Padnick-Silver L, et al. Physician-perceived impact of thyroid eye disease on patient quality of life in the United States. Ophthalmol Ther. 2021;10(1):75-87.
Mourits MP, Koornneef L, Wiersinga WM, et al. Clinical criteria for the assessment of disease activity in Graves’ ophthalmopathy: a novel approach. Br J Ophthalmol. 1989;73(8):639-644.
Smith TJ, Kahaly GJ, Ezra DG, et al. Teprotumumab for thyroid-associated ophthalmopathy. N Engl J Med. 2017;376(18):1748-1761.
Douglas RS, Kahaly GJ, Patel A, et al. Teprotumumab for the treatment of active thyroid eye disease. N Engl J Med. 2020;382(4):341-352.
Kahaly GJ, Pitz S, Hommel G, et al. Randomized, single blind trial of intravenous versus oral steroid monotherapy in Graves’ orbitopathy. J Clin Endocrinol Metab. 2005;90(9):5234-5240.
Marcocci C, Kahaly GJ, Krassas GE, Bartalena L, Prummel M, Stahl M, et al.; European Group on Graves’ Orbitopathy. Selenium and the course of mild Graves’ orbitopathy. N Engl J Med. 2011;364(20):1920-1931. PMID: 21591944. doi:10.1056/NEJMoa1012985.
Hong A, Shoji MK, Villatoro GA, et al. Intersurgeon variability in proptosis reduction after orbital decompression for thyroid eye disease: a multicenter analysis. Ophthalmic Plast Reconstr Surg. 2024;40(3).
Salvi M, Vannucchi G, Campi I, et al. Rituximab treatment in active moderate-to-severe Graves’ orbitopathy: an international, multicenter, single-blind, randomized placebo-controlled study. J Clin Endocrinol Metab. 2015;100(11):422-431.
Rundle FF, Wilson CW. Development and course of exophthalmos and ophthalmoplegia in Graves’ disease with special reference to the effect of thyroidectomy. Clin Sci. 1945;5(3-4):177-194. PMID: 21011937.