أعراض الجفن
تورم الجفن العلوي وتراجع الجفن العلوي وتأخر الجفن العلوي هي سمات مميزة.
علامة دالريمبل: اتساع شق الجفن بسبب تراجع الجفن العلوي.
علامة فون غريف: تأخر الجفن العلوي عند النظر إلى الأسفل (lid lag).

مرض العين الدرقي (TED) هو مرض مناعي ذاتي يحدث فيه خلل وظيفي مناعي مرتبط بخلل وظيفة الغدة الدرقية، مما يؤدي إلى التهاب الأنسجة داخل الحجاج وزيادة حجم الدهون الحجاجية والعضلات خارج العين. يؤدي ارتفاع الضغط خلف المقلة إلى جحوظ العين. يحدث غالبًا مع فرط نشاط الغدة الدرقية (مرض غريفز/باسيدو)، ولكنه قد يحدث أيضًا مع وظيفة درقية طبيعية (اعتلال العين الدرقي مع وظيفة درقية طبيعية). يتطور مرض العين الدرقي بشكل مستقل عن هرمونات الغدة الدرقية، وهو أحد أمراض المناعة الذاتية التي تشارك فيها الأجسام المضادة الذاتية المرتبطة بالغدة الدرقية.
يعاني حوالي 40-50% من مرضى غريفز (باسيدو) من أعراض عينية. الآفات الحجاجية الشديدة نادرة نسبيًا، وتحدث في 5-10% من جميع مرضى غريفز.
يبلغ معدل الانتشار 16/100,000 شخص-سنة لدى النساء و2.9/100,000 شخص-سنة لدى الرجال1). يظهر المرض ذروتين عمريتين: في الأربعينيات والخمسينيات والستينيات والسبعينيات1). التدخين هو أكبر عامل خطر لاعتلال العين الدرقي، حيث يزيد بشكل كبير من خطر الإصابة2). يُلاحظ نمط عمري حيث يكون جحوظ العين هو العرض الرئيسي لدى الشباب، بينما يكون الشفع هو العرض الرئيسي لدى كبار السن.
يتبع المسار الطبيعي لاعتلال العين الدرقي منحنى روندل، حيث ينتقل من المرحلة النشطة (الالتهابية، عادةً 1-3 سنوات) إلى المرحلة المستقرة (غير الالتهابية)3). يتم تحديد توقيت التدخل العلاجي بناءً على هذا المنحنى.
أعراض الجفن
تورم الجفن العلوي وتراجع الجفن العلوي وتأخر الجفن العلوي هي سمات مميزة.
علامة دالريمبل: اتساع شق الجفن بسبب تراجع الجفن العلوي.
علامة فون غريف: تأخر الجفن العلوي عند النظر إلى الأسفل (lid lag).
جحوظ العين
شائع لدى الشباب (ضعف الأنسجة الداعمة للمحجر).
يتم التقييم باستخدام مقياس جحوظ العين لهيرتل. القيم الطبيعية لدى اليابانيين هي 10-15 ملم (المتوسط 13 ملم). الفرق بين العينين ضمن 2 ملم يعتبر طبيعيًا.
ازدواج الرؤية
شائع لدى كبار السن. يحدث بسبب الحول التقييدي الناتج عن التهاب وتليف العضلات خارج المقلة.
العضلة المستقيمة السفلية هي الأكثر إصابة → ضعف الارتفاع هو الأكثر شيوعًا. يليه ضعف الإبعاد بسبب إصابة العضلة المستقيمة الإنسية.
ضعف البصر
بسبب اعتلال القرنية (اعتلال القرنية الجفافي) أو الاعتلال العصبي البصري الانضغاطي (DON).
يحدث DON في حوالي 5% من جميع الحالات1) ويتطلب تدخلًا عاجلاً. تشمل العلامات: إيجابية RAPD، انخفاض CFF، وعيوب المجال البصري.
يمكن أن يحدث حتى مع وظيفة الغدة الدرقية الطبيعية، ويسمى اعتلال العين الدرقي في حالة الدرقية السوية. مرض العين الدرقي هو مرض مناعي ذاتي يتقدم بشكل مستقل عن مستويات هرمون الغدة الدرقية، ويمكن أن يحدث إذا كانت الأجسام المضادة الذاتية المرتبطة بالغدة الدرقية (TRAb، TSAb) إيجابية. إذا كانت هناك علامات تراجع الجفن أو جحوظ العين، فيجب إجراء اختبار للأجسام المضادة الذاتية المرتبطة بالغدة الدرقية حتى لو كانت وظيفة الغدة الدرقية طبيعية.
في المراحل المبكرة، تسود أعراض الجفاف والتهيج والدموع ورهاب الضوء. مع تقدم الحالة، يظهر تورم حول الحجاج، جحوظ العين، ازدواج الرؤية، وتراجع الجفن. في الحالات الشديدة، قد يحدث تقرح القرنية واعتلال العصب البصري الانضغاطي.
فيما يلي علامات الجفن المميزة لمرض العين الدرقي.
| اسم العلامة | الاسم الإنجليزي | العلامة |
|---|---|---|
| علامة دالريمبل | علامة دالريمبل | اتساع الشق الجفني بسبب تراجع الجفن العلوي، مع ظهور بياض العين فوق الحوف القرني العلوي |
| علامة فون غريف | تأخر الجفن | ظاهرة تأخر تتبع الجفن العلوي عند النظر إلى الأسفل |
| علامة شتيلواغ | علامة شتيلواغ | انخفاض الرمش وإغلاق غير كامل للجفن |
| علامة جيفورد | علامة جيفورد | صعوبة انقلاب الجفن العلوي |
يُقاس جحوظ العين باستخدام مقياس هيرتل للجحوظ. القيم الطبيعية لدى اليابانيين هي 10-15 ملم (المتوسط 13 ملم)، ويعتبر الفرق بين العينين بمقدار 2 ملم أو أقل طبيعيًا. تشير قيمة هيرتل التي تزيد عن 18 ملم إلى وجود جحوظ في العين1).
يحدث بسبب ضغط العضلات الخارجية للعين السميكة على العصب البصري في قمة الحجاج (orbital apex). يحدث في حوالي 5% من جميع الحالات1)، وهو حالة طارئة. يعتبر اختبار RAPD (خلل الحدقة الوارد النسبي) الإيجابي، وانخفاض CFF (تردد الاندماج الحرج)، وعيوب المجال البصري من العلامات المبكرة. كما أن تشوهات رؤية الألوان تعتبر علامة مهمة.
الألم والرؤية المزدوجة وتغير المظهر هي العوامل الرئيسية لانخفاض جودة الحياة. معدل انتشار القلق والاكتئاب بين مرضى اعتلال العين الدرقي هو 36%، أي حوالي ضعف معدل عامة السكان (18.9%) 5). 62% من المرضى المتوسطين و89% من المرضى الشديدين يعانون من ضعف كبير في جودة الحياة (درجة ≥4/7) 5). تم الإبلاغ عن انخفاض في جودة الحياة مماثل أو أقل من مرض السكري وانتفاخ الرئة وفشل القلب.
يحدث بسبب الحول المقيد الناتج عن تضخم وتقلص العضلات خارج العين (خاصة العضلة المستقيمة السفلية) بسبب الالتهاب والتليف، مما يحد من حركة العين الطبيعية. العضلة المستقيمة السفلية هي الأكثر تأثرًا، لذا فإن اضطراب النظر للأعلى هو الأكثر شيوعًا. ترتيب تواتر إصابة العضلات خارج العين هو: المستقيمة السفلية > المستقيمة الإنسية > المستقيمة العلوية > المستقيمة الوحشية، وهو أكثر شيوعًا لدى كبار السن.
تؤدي التشوهات المناعية المرتبطة بخلل وظيفة الغدة الدرقية إلى تحفيز الالتهاب في الأنسجة داخل الحجاج. تعمل الأجسام المضادة الذاتية لمستقبل TSH (TRAb) على تنشيط مستقبل TSH على الخلايا الليفية الحجاجية، مما يحفز إنتاج السيتوكينات الالتهابية (TNF-α، IL-6، IL-1β وغيرها). تتسلل الخلايا التائية CD4+/CD8+ إلى الأنسجة الحجاجية وتضخم الاستجابة الالتهابية.
تعزز الخلايا الليفية المنشطة تخليق الجليكوزامينوجليكان وحمض الهيالورونيك، مما يسبب وذمة الأنسجة واحتباس الماء. يؤدي تمايز الخلايا الليفية إلى خلايا دهنية وخلايا عضلية ليفية إلى توسع الدهون الحجاجية وتليف العضلات خارج العين3).
يشكل مستقبل IGF-1 (IGF-1R) مركبًا مع TSHR، ويساهم بشكل تآزري في تنشيط الخلايا الليفية الحجاجية 4). هذه الآلية هي الهدف العلاجي للتبروتوموماب (مثبط IGF-1R).
التدخين هو أكبر عامل خطر، ويرتبط بزيادة خطر الإصابة وشدة المرض ومقاومة العلاج 2). كما تساهم عدم استقرار وظيفة الغدة الدرقية، والفترة الحادة بعد العلاج باليود المشع، والتقدم في العمر، والجنس الذكري في زيادة خطر شدة المرض.
إذا تواجدت العلامات الثلاث: تراجع الجفن، جحوظ العين، والرؤية المزدوجة، فإن ذلك يشير سريريًا بقوة إلى مرض العين الدرقي. حتى لو كانت وظيفة الغدة الدرقية طبيعية، يمكن تشخيص مرض العين الدرقي إذا كانت الأجسام المضادة الذاتية المرتبطة بالغدة الدرقية إيجابية.
يتم قياس هرمونات الغدة الدرقية (FT₄، FT₃) وTSH والأجسام المضادة الذاتية للغدة الدرقية. تشمل الأجسام المضادة المقاسة: TRAb (الأجسام المضادة لمستقبلات TSH)، TSAb (الأجسام المضادة المحفزة للغدة الدرقية)، الأجسام المضادة لـ TG (الأجسام المضادة لثايروغلوبولين)، والأجسام المضادة لـ TPO (الأجسام المضادة لبيروكسيداز الغدة الدرقية). أي من هذه الأجسام المضادة يكون إيجابيًا.
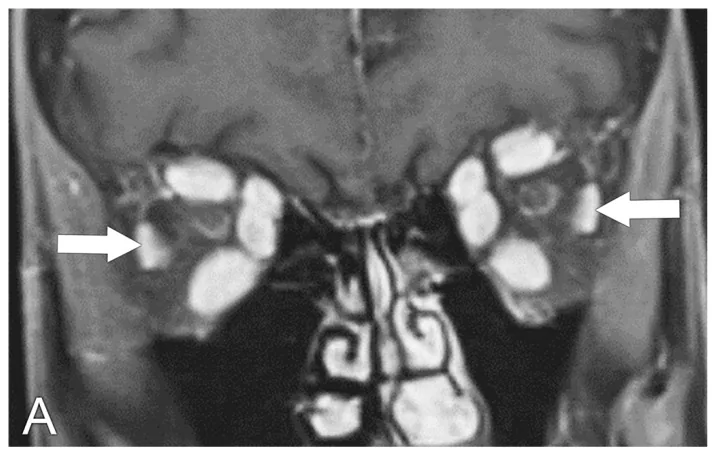
التصوير بالرنين المغناطيسي (الخيار الأول): تقييم شكل العضلات خارج العين باستخدام تسلسل T1. يُظهر تسلسل STIR (استرداد الانعكاس القصير TI) مناطق الالتهاب كإشارة عالية، مما يساعد في تقييم نشاط الالتهاب. المقطع الإكليلي ضروري لأنه يسمح بتقييم جميع العضلات خارج العين باستثناء العضلة المائلة السفلية في وقت واحد. المقطع المحوري يقيم العضلتين المستقيمتين الإنسية والوحشية.
التصوير المقطعي المحوسب (CT): يُظهر تضخم العضلات خارج العين (نمط تضخم بطن العضلة مع الحفاظ على الوتر هو سمة مميزة لمرض العين الدرقي)، ويُستخدم النافذة العظمية لتقييم جدار الحجاج.
الموجات فوق الصوتية من النوع B: تُستخدم بشكل مساعد لتقييم تضخم العضلات خارج العين.
هو نظام تسجيل من 7 بنود (0-7 نقاط) لتقييم النشاط الالتهابي اقترحه موريتس وآخرون في عام 1989 6).
البنود السبعة للتقييم: ① ألم خلف المقلة تلقائي، ② ألم عند حركة العين، ③ احمرار الجفن، ④ تورم الجفن، ⑤ احمرار الملتحمة، ⑥ وذمة الملتحمة، ⑦ تورم الغدة الدمعية/الطية الهلالية.
تُعتبر المرحلة النشطة إذا كانت درجة CAS ≥ 3/7، وتكون مؤشرًا للعلاج بالستيرويد النبضي. درجة CAS ≥ 4/7 هي معيار الإدراج في التجارب العشوائية للتبروتوموماب.
| الشدة | المعيار | خطة العلاج |
|---|---|---|
| خفيفة | تأثير طفيف على الحياة اليومية | مكملات السيلينيوم + المتابعة |
| متوسطة إلى شديدة | تراجع الجفن ≥2 مم، جحوظ ≥3 مم فوق الطبيعي، ازدواج الرؤية | النبض الستيرويدي، تيبروتوموماب |
| مهددة للرؤية | اعتلال عصبي بصري انضغاطي، قرحة القرنية | تخفيف ضغط الحجاج الطارئ أو الستيرويدات عالية الجرعة |
تصنيف EUGOGO (مجموعة عيون جريفز الأوروبية) وفقًا لإرشادات الممارسة السريرية لعام 2021 1). يُستخدم أيضًا تصنيف NOSPECS (الفئات 0-6) وتصنيف VISA (الرؤية والالتهاب والحول والمظهر) لتقييم الشدة.
| الأمراض التفريقية | نقاط التفريق | النتائج التصويرية |
|---|---|---|
| مرض العين المرتبط بـ IgG4 | تضخم الغدة الدمعية + تضخم عضلات العين الخارجية، ارتفاع IgG4 في الدم | تضخم منتشر في الغدة الدمعية وعضلات العين الخارجية |
| التهاب العضلات خارج العين (التهاب الحجاج العضلي) | بداية حادة، ألم شديد | سماكة في منطقة الوتر (في اعتلال العين الدرقي، تكون السماكة في بطن العضلة مع الحفاظ على الوتر) |
| ورم حجاجي، ورم نقيلي | أحادي الجانب، تقدمي | تكوين كتلة |
هو نظام تسجيل من 7 بنود (0-7 نقاط) لتقييم النشاط الالتهابي لمرض العين الدرقي. يتم تقييم 7 بنود: ① ألم خلف المقلة تلقائيًا، ② ألم أثناء حركة العين، ③ احمرار الجفن، ④ تورم الجفن، ⑤ احمرار الملتحمة، ⑥ وذمة الملتحمة، ⑦ تورم الغدة الدمعية/الطية الهلالية. تعتبر النتيجة ≥3 نقاط مرحلة نشطة. وهو مؤشر مهم لاختيار العلاج، ويستخدم لتحديد مدى ملاءمة العلاج بالستيرويد النبضي أو التبروتوموماب.
يعد تطبيع وظيفة الغدة الدرقية شرطًا أساسيًا، والتعاون مع قسم الغدد الصماء ضروري. الإقلاع عن التدخين يتم في جميع الحالات للقضاء على التدخين، وهو أكبر عامل خطر لتفاقم المرض ومقاومة العلاج.
مكملات السيلينيوم: يُوصى بتناول 200 ميكروغرام/يوم من السيلينيوم لمدة 6 أشهر لتحسين نشاط المرض في حالات TED الخفيفة، وهو مفيد وموصى به10).
حماية القرنية وسطح العين: الاستخدام المتكرر للدموع الاصطناعية وقطرات حماية القرنية، ووضع مرهم العين قبل النوم كأساس. في حالات جحوظ العين الشديد، يُنظر في خياطة الجفن الجانبية (lateral tarsorrhaphy).
العلاج النبضي بالستيرويدات (الخيار الأول): إعطاء ميثيل بريدنيزولون 500-1000 ملغ/أسبوع لمدة 6-12 أسبوعًا1). الستيرويدات الوريدية أكثر فعالية من الستيرويدات الفموية9). يُوصى بألا تتجاوز الجرعة التراكمية 8 غرام (لتقليل خطر تلف الكبد).
البروتوكول القياسي: دورة واحدة من ميثيل بريدنيزولون 1 غرام × 3 أيام.
بريدنيزولون فموي: في الحالات المتوسطة إلى الشديدة التي يصعب فيها الإعطاء الوريدي، يُبدأ بجرعة 1 ملغ/كغ/يوم.
حقن الستيرويد الموضعي: لتورم الجفن العلوي وتراجع الجفن الالتهابي، يكون الحقن الموضعي لتريامسينولون أسيتونيد (كيناكورت-A® 1 أمبولة) فعالاً.
تيبروتوموماب (مثبط مستقبل عامل النمو الشبيه بالأنسولين-1): هو دواء علاجي يُتوقع أن يحسن بروز العين والرؤية المزدوجة في حالات مرض العين الدرقي (TED) المتوسطة إلى الشديدة النشطة. أظهر تحليل تلوي لخمس تجارب عشوائية محكومة (411 حالة) انخفاضًا ملحوظًا في بروز العين، وتحسنًا ملحوظًا في تحقيق درجة نشاط المرض السريري (CAS) 0-1 عند الأسبوع 24، وتحسنًا ملحوظًا في معدل تحسن الرؤية المزدوجة 4)، دون زيادة ملحوظة في الأحداث الضائرة الخطيرة. تم بناء الأدلة من تجربتين عشوائيتين محكومتين رئيسيتين: Smith et al. (2017، 42 حالة مقابل 45 حالة) 7) وDouglas et al. (2020، 41 حالة مقابل 42 حالة) 8).
ريتوكسيماب (جسم مضاد وحيد النسيلة مضاد لـ CD20): أظهرت تجربة عشوائية متعددة المراكز أنه قد يقلل من نشاط المرض في حالات اعتلال العين المرتبط بالغدة الدرقية (TED) المتوسطة إلى الشديدة المقاومة للعلاج12).
توسيليزوماب (مثبط مستقبل IL-6): يُنظر في استخدامه في الحالات المقاومة للستيرويدات والريتوكسيماب.
في حالات TED المتوسطة إلى الشديدة، يتم إجراء العلاج الإشعاعي المداري مع العلاج المثبط للمناعة. عادةً ما يتم تشعيع 20 غراي/10 جلسات على مدى أسبوعين. يُعتقد أن الجمع مع الستيرويدات أكثر فعالية من العلاج الأحادي.
يتم التخطيط للجراحة من حيث المبدأ بعد دخول منحنى راندل في مرحلة الاستقرار وهدوء الالتهاب. يجب الالتزام الصارم بترتيب الإجراءات، حيث تؤثر نتيجة الجراحة السابقة مباشرة على خطة الجراحة اللاحقة.
الخطوة 1: تخفيف ضغط الحجاج
المؤشرات: جحوظ شديد، اعتلال عصبي بصري انضغاطي (مؤشر طارئ)
التقنية والنتائج: هناك 5 تقنيات تعتمد على مزيج من الجدار الإنسي والأرضية والجدار الوحشي والدهون. يؤدي تخفيف الضغط بجدار واحد إلى تحسن بمقدار -1.4 إلى -2.3 مم، وتخفيف الضغط بثلاثة جدران مع الدهون إلى تحسن بمقدار -4.6 إلى -5.0 مم في جحوظ العين.
في دراسة متعددة المراكز شملت 633 عينًا، تم تأكيد استقرار وتكرار النتائج دون اختلافات كبيرة بين الجراحين لنفس التقنية11).
الخطوة 2: جراحة الحول
المؤشرات: ازدواج الرؤية واضطرابات حركة العين بعد استقرار المرحلة غير الالتهابية
التقنية الأساسية: تراجع العضلة المستقيمة السفلية هو الأكثر شيوعًا. يتم تحديد مقدار الجراحة حسب درجة الحول التقييدي.
يتم إجراؤها أيضًا لعلاج ازدواج الرؤية الجديد (حوالي 30%) بعد جراحة تخفيف ضغط المدار.
الخطوة 3: جراحة الجفن
المؤشرات: تراجع الجفن في المرحلة غير الالتهابية المستقرة، مشاكل وظيفية أو تجميلية
التقنية الجراحية: يتم اختيار استئصال عضلة مولر أو إرجاع العضلة الرافعة للجفن العلوي لعلاج تراجع الجفن العلوي. تم الإبلاغ عن نتائج جيدة من خلال الجمع بين استئصال عضلة مولر وإرجاع العضلة الرافعة.
يتم التخطيط بعد استقرار التغيرات التالية لجراحة تخفيف ضغط الحجاج وجراحة الحول.
يتم إجراء العمليات بالترتيب التالي: تخفيف ضغط الحجاج → جراحة الحول → جراحة الجفن. من المهم الالتزام بهذا الترتيب لأن نتائج الجراحة السابقة تؤثر على خطة الجراحة اللاحقة. يتم التخطيط لأي عملية جراحية من حيث المبدأ بعد دخول المرحلة غير الالتهابية (مرحلة الاستقرار في منحنى راندل). إجراء الجراحة في المرحلة الالتهابية يزيد من خطر التقلبات بعد الجراحة والانتكاس.
هو جسم مضاد وحيد النسيلة يثبط مستقبل IGF-1 (IGF-1R). يمنع الإشارات المعقدة بين IGF-1R وTSHR على الخلايا الليفية الحجاجية، مما يثبط الالتهاب والتورم النسيجي. أظهر تحليل تلوي لـ 5 تجارب عشوائية محكومة (411 حالة) تحسنًا ملحوظًا في جحوظ العين والشفع ودرجة النشاط السريري (CAS). لا توجد زيادة ملحوظة في الأحداث الضائرة الخطيرة، لكن السلامة طويلة المدى (اضطرابات السمع، ارتفاع السكر في الدم، إلخ) لا تزال قيد التقييم.
يؤدي الخلل الوظيفي المناعي المرتبط بخلل الغدة الدرقية إلى التهاب الأنسجة داخل الحجاج، مما يزيد من حجم النسيج الدهني الحجاجي والعضلات خارج العين. يؤدي ارتفاع الضغط خلف المقلة إلى جحوظ العين.
أمراض النسيج الدهني الحجاجي: يحدث تضخم الخلايا الدهنية وارتشاح لمفاوي في النسيج الخلالي، مع وذمة وتندب ناتجين عن الالتهاب المزمن. يؤدي زيادة تخليق الجليكوزامينوجليكان وحمض الهيالورونيك إلى احتباس السوائل وتورم الأنسجة.
أمراض العضلات خارج العين: يظهر ارتشاح التهابي بقيادة الخلايا الليمفاوية بين ألياف العضلات المخططة، مما يؤدي إلى تنكس ونخر الألياف العضلية. يحدث وذمة وسماكة خلالية بسبب الالتهاب، ويتكون نسيج ضام بين الألياف العضلية مما يؤدي إلى تضخم العضلات خارج العين. العضلة المستقيمة السفلية هي الأكثر تأثرًا، تليها المستقيمة الإنسية، ثم العلوية، ثم الوحشية. لذلك، يكون اضطراب الارتفاع هو الأكثر شيوعًا، يليه اضطراب الإبعاد.
ينشأ عن آليتين متراكبتين.
① أمراض العضلة الرافعة للجفن العلوي: يحدث وذمة في الخلايا العضلية بسبب الالتهاب مما يؤدي إلى وذمة الجفن. يتسلل النسيج الدهني بين الألياف العضلية، وتتعرض الخلايا العضلية للنخر والتندب مما يغير وظيفة العضلة الرافعة.
②حالة العضلة المولرية: العضلة المولرية، وهي عضلة ملساء معصبة بالجهاز الودي، تنقبض باستمرار بسبب فرط النشاط الودي المصاحب لفرط نشاط الغدة الدرقية، مما يرفع الصفيحة الجفنية ويوسع شق الجفن.
تعمل الأجسام المضادة الذاتية لمستقبل TSH (TRAb) على تنشيط مستقبل TSH على الخلايا الليفية الحجاجية، مما يؤدي إلى إنتاج السيتوكينات الالتهابية (TNF-α، IL-6، IL-1β) عبر الإشارات النهائية. تتسلل الخلايا التائية CD4+/CD8+ إلى النسيج الحجاجي لتضخيم الاستجابة الالتهابية. تتمايز الخلايا الليفية المنشطة إلى خلايا دهنية وخلايا ليفية عضلية، مما يسبب تضخم الدهون الحجاجية وتليف العضلات خارج العين على التوالي3).
يشكل مستقبل IGF-1 (IGF-1R) مركبًا مع مستقبل TSH، ويساهم بشكل تآزري في تنشيط الخلايا الليفية الحجاجية4). حجب إشارات هذا المركب هو آلية عمل التبروتوموماب.
تم تصور الانتقال الطبيعي من مرحلة الالتهاب النشط (عادة 1-3 سنوات) إلى مرحلة الاستقرار (غير الالتهابية) على أنه منحنى راندل13). يتم اختيار العلاج الفعلي بعد تقييم النشاط والشدة1). في المرحلة النشطة، تعطى الأولوية للعلاج المثبط للالتهاب، ويتم التخطيط للجراحة في مرحلة الاستقرار غير الالتهابية.
بعد موافقة إدارة الغذاء والدواء الأمريكية، تستمر البيانات في التراكم. تم تأكيد الفعالية والسلامة من خلال تحليل تلوي لخمس تجارب عشوائية محكومة (إجمالي 411 حالة) 4)، لكن نتائج المرحلة الرابعة من التجارب السريرية تهم السلامة طويلة المدى (مثل ضعف السمع وارتفاع السكر في الدم). كما يتم النظر في إمكانية توسيع الاستطباب لمرض اعتلال العين الدرقي غير النشط.
أظهرت دراسة متعددة المراكز شملت 7 مراكز و7 جراحين و633 عينًا 11) أنه لا توجد فروق ذات دلالة إحصائية بين الجراحين عند إجراء نفس التقنية الجراحية. هذه نتيجة مهمة تدعم الصلاحية الإحصائية للتجارب العشوائية متعددة المراكز. تم الإبلاغ عن أن تخفيف الضغط بالمنظار للجدار الإنسي يحسن بروز العين بشكل أكبر مقارنة بالجراحة المفتوحة عند تخفيف ضغط الجدار الإنسي مع أرضية الحجاج (-3.67 مم مقابل -2.97 مم، p=0.008). كما تبين أن درجة بروز العين قبل الجراحة ترتبط إحصائيًا بالتغير بعد الجراحة (p<0.001)، مما يؤكد أهمية التقييم قبل الجراحة.
يُعتقد أن التغيرات في TRAb وTSAb خلال المرحلة النشطة ترتبط بـ CAS، وتجري أبحاث حول اختيار العلاج بناءً على المؤشرات الحيوية. كما يُنتظر إجراء تجارب عشوائية كبيرة على توسيليزوماب (مثبط IL-6) للحالات المقاومة للعلاج.
Bartalena L, Kahaly GJ, Baldeschi L, et al. The 2021 European Group on Graves’ Orbitopathy (EUGOGO) clinical practice guidelines for the medical management of Graves’ orbitopathy. Eur J Endocrinol. 2021;184(4):G43-G67.
Prummel MF, Wiersinga WM. Smoking and risk of Graves’ disease. JAMA. 1993;269(4):479-482.
Bahn RS. Graves’ ophthalmopathy. N Engl J Med. 2010;362(8):726-738.
Cong X, Pei L, Hu H. Teprotumumab for treating active thyroid eye disease: a meta-analysis. Medicine. 2024;103(18):e38059.
Wang Y, Sharma A, Padnick-Silver L, et al. Physician-perceived impact of thyroid eye disease on patient quality of life in the United States. Ophthalmol Ther. 2021;10(1):75-87.
Mourits MP, Koornneef L, Wiersinga WM, et al. Clinical criteria for the assessment of disease activity in Graves’ ophthalmopathy: a novel approach. Br J Ophthalmol. 1989;73(8):639-644.
Smith TJ, Kahaly GJ, Ezra DG, et al. Teprotumumab for thyroid-associated ophthalmopathy. N Engl J Med. 2017;376(18):1748-1761.
Douglas RS, Kahaly GJ, Patel A, et al. Teprotumumab for the treatment of active thyroid eye disease. N Engl J Med. 2020;382(4):341-352.
Kahaly GJ, Pitz S, Hommel G, et al. Randomized, single blind trial of intravenous versus oral steroid monotherapy in Graves’ orbitopathy. J Clin Endocrinol Metab. 2005;90(9):5234-5240.
Marcocci C, Kahaly GJ, Krassas GE, Bartalena L, Prummel M, Stahl M, et al.; European Group on Graves’ Orbitopathy. Selenium and the course of mild Graves’ orbitopathy. N Engl J Med. 2011;364(20):1920-1931. PMID: 21591944. doi:10.1056/NEJMoa1012985.
Hong A, Shoji MK, Villatoro GA, et al. Intersurgeon variability in proptosis reduction after orbital decompression for thyroid eye disease: a multicenter analysis. Ophthalmic Plast Reconstr Surg. 2024;40(3).
Salvi M, Vannucchi G, Campi I, et al. Rituximab treatment in active moderate-to-severe Graves’ orbitopathy: an international, multicenter, single-blind, randomized placebo-controlled study. J Clin Endocrinol Metab. 2015;100(11):422-431.
Rundle FF, Wilson CW. Development and course of exophthalmos and ophthalmoplegia in Graves’ disease with special reference to the effect of thyroidectomy. Clin Sci. 1945;5(3-4):177-194. PMID: 21011937.