눈꺼풀 증상
위눈꺼풀 부종, 위눈꺼풀 후퇴, 위눈꺼풀 지연이 특징적입니다.
Dalrymple 징후: 위눈꺼풀 후퇴로 인한 눈구멍 틈새 확대.
von Graefe 징후: 아래를 볼 때 윗눈꺼풀이 늦게 내려오는 현상(lid lag).

갑상샘눈병증(TED)은 갑상선 기능 이상과 관련된 면역 기능 이상이 안와 내부 조직의 염증을 유발하여 안와 지방 조직과 외안근의 부피를 증가시키는 자가면역 질환입니다. 구후 조직 압력 상승으로 안구 돌출이 발생합니다. 갑상선 기능 항진증(그레이브스병/바세도우병)과 동반된 발병이 가장 흔하지만, 갑상선 기능이 정상인 euthyroid ophthalmopathy로도 발병할 수 있습니다. 갑상샘눈병증은 갑상선 호르몬과 무관하게 진행되며, 갑상선 관련 자가항체가 관여하는 자가면역 질환 중 하나입니다.
그레이브스병 환자의 약 4050%에서 안구 증상이 나타납니다. 중증 안와 병변은 전체 그레이브스병 환자의 510%로 비교적 드뭅니다.
유병률은 여성에서 16/100,000인년, 남성에서 2.9/100,000인년으로 보고됩니다1). 발병 연령은 40-50대와 60-70대에 두 개의 피크를 보입니다1). 흡연은 갑상샘눈병증의 가장 큰 위험 인자이며 발병 위험을 유의하게 증가시킵니다2). 젊은 환자는 안구돌출이 주된 증상이고, 고령 환자는 복시가 주된 증상으로 연령별 패턴이 나타납니다.
갑상샘눈병증의 자연 경과는 Rundle 곡선을 따르며, 활동기(염증기, 보통 1-3년)를 거쳐 안정기(비염증기)로 이행합니다3). 치료 개입 시기는 이 곡선에 기반하여 결정됩니다.
눈꺼풀 증상
위눈꺼풀 부종, 위눈꺼풀 후퇴, 위눈꺼풀 지연이 특징적입니다.
Dalrymple 징후: 위눈꺼풀 후퇴로 인한 눈구멍 틈새 확대.
von Graefe 징후: 아래를 볼 때 윗눈꺼풀이 늦게 내려오는 현상(lid lag).
안구돌출
젊은 층에서 흔함(안와 지지 조직의 취약성).
Hertel 안구돌출계로 평가. 일본인 정상치는 10~15mm(평균 13mm). 좌우 차이가 2mm 이내면 정상.
복시
노인에서 흔함. 외안근의 염증 및 섬유화로 인한 구속사시가 원인.
하직근이 가장 흔히 침범 → 상전 장애가 가장 흔함. 다음으로 내직근 침범으로 인한 외전 장애.
시력 장애
갑상선 기능이 정상인 상태에서도 euthyroid ophthalmopathy로 발생할 수 있습니다. 갑상선 안병증은 갑상선 호르몬 수치와 독립적으로 진행되는 자가면역 질환으로, 갑상선 관련 자가항체(TRAb, TSAb)가 양성이면 발생할 수 있습니다. 안검 후퇴나 안구 돌출 소견이 있으면 갑상선 기능이 정상이더라도 갑상선 관련 자가항체 검사가 필요합니다.
초기에는 건조감, 자극감, 눈물, 눈부심이 주를 이룹니다. 병태가 진행됨에 따라 안와 주위 부종, 안구 돌출, 복시, 눈꺼풀 후퇴가 나타나며, 중증 사례에서는 각막 궤양, 압박성 시신경병증에 이를 수 있습니다.
다음은 갑상샘눈병증에 특징적인 눈꺼풀 소견입니다.
| 징후명 | 영어명 | 소견 |
|---|---|---|
| Dalrymple 징후 | Dalrymple sign | 위눈꺼풀 후퇴로 인한 눈꺼풀 틈 확대, 위쪽 각막 윤부 위로 흰자위가 노출됨. |
| von Graefe 징후 | 눈꺼풀 지연 | 아래를 볼 때 위눈꺼풀이 따라 내려오지 못하는 현상. |
| Stellwag 징후 | Stellwag 징후 | 눈 깜빡임 감소 및 불완전한 눈꺼풀 폐쇄 |
| Gifford 징후 | Gifford 징후 | 위눈꺼풀 뒤집기 어려움 |
안구돌출은 Hertel 안구돌출계로 측정합니다. 일본인의 정상 범위는 10~15mm(평균 13mm)이며, 좌우 차이가 2mm 이내이면 정상입니다. Hertel 값이 18mm를 초과하면 안구돌출을 시사합니다1).
비후된 외안근이 안와 첨부에서 시신경을 압박하여 발생합니다. 전체 증례의 약 5%에서 발생하며1), 응급성이 높습니다. RAPD(상대구심동공결손) 양성, CFF(임계융합빈도) 감소, 시야 장애가 초기 징후입니다. 색각 이상도 중요한 소견입니다.
통증, 복시, 외모 변화가 삶의 질 저하의 주요 요인입니다. 갑상선안병증 환자의 불안·우울증 동반율은 36%로, 일반 인구(18.9%)의 약 2배에 달합니다5). 중등증 환자의 62%, 중증 환자의 89%가 높은 삶의 질 장애(점수 ≥4/7점)를 보입니다5). 당뇨병, 폐기종, 심부전과 동등하거나 그 이하의 삶의 질 저하가 보고되었습니다.
갑상선 기능 이상에 동반된 면역 기능 이상이 안와 내 조직의 염증을 유발합니다. TSH 수용체(TSHR)에 대한 자가항체(TRAb)가 안와 섬유아세포의 TSHR을 활성화하여 염증성 사이토카인(TNF-α, IL-6, IL-1β 등) 생성을 유발합니다. CD4+/CD8+ T 세포가 안와 조직에 침윤하여 염증 반응을 증폭시킵니다.
활성화된 섬유아세포는 글리코사미노글리칸(GAG)과 히알루론산 합성을 증가시켜 조직 부종과 수분 보유를 유발합니다. 섬유아세포의 지방세포 및 근섬유아세포로의 분화로 안와 지방 팽창과 외안근 섬유화가 진행됩니다3).
IGF-1 수용체(IGF-1R)는 TSHR과 복합체를 형성하여 안와 섬유아세포의 활성화에 상승적으로 관여합니다4). 이 기전은 테프로투무맙(IGF-1R 억제제)의 치료 표적이 됩니다.
흡연이 가장 큰 위험 인자이며, 발병 위험, 중증도, 치료 저항성 모두와 관련됩니다2). 그 외에 갑상선 기능 불안정, 방사성 요오드 치료 후 급성기, 고령 및 남성도 중증화 위험에 기여합니다.
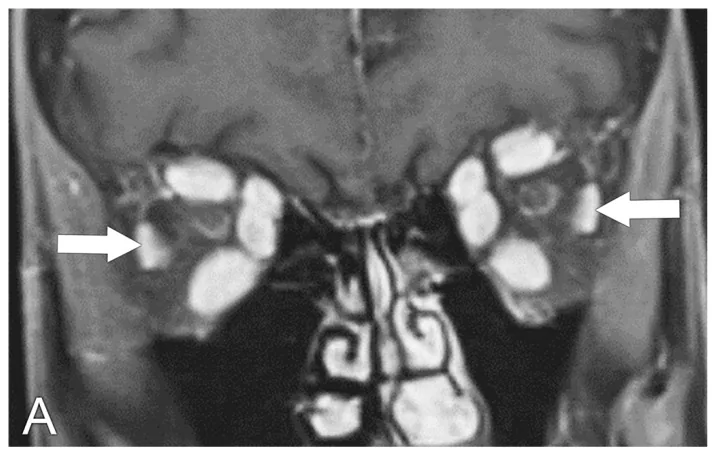
눈꺼풀 후퇴, 안구 돌출, 복시의 3대 증상이 나타나면 임상적으로 TED를 강력히 시사합니다. 갑상선 기능이 정상이더라도 갑상선 관련 자가항체가 양성이면 TED로 진단할 수 있습니다.
갑상선 호르몬(FT₄, FT₃), TSH, 갑상선 자가항체를 측정합니다. 측정 대상은 TRAb(TSH 수용체 항체), TSAb(갑상선 자극 항체), 항TG 항체(항갑상선글로불린 항체), 항TPO 항체(항갑상선과산화효소 항체)입니다. 이 중 하나 이상이 양성입니다.
MRI(1차 선택): T1 강조 영상에서 외안근의 형태를 평가합니다. STIR(short-TI inversion recovery) 기법은 염증 부위를 고신호 영역으로 나타내어 염증 활동성 평가에 유용합니다. 관상면은 하사근을 제외한 모든 외안근을 동시에 평가할 수 있어 필수적입니다. 축상면에서는 내직근과 외직근을 평가합니다.
CT: 외안근 비대(힘줄은 보존되고 근육배가 비대해지는 패턴이 TED의 특징)를 확인하고, 안와골벽 평가에 골창을 사용합니다.
B-scan 초음파: 외안근 비대 평가에 보조적으로 사용됩니다.
CAS는 1989년 Mourits 등이 제안한 염증 활동성 평가를 위한 7항목 점수 체계(0-7점)입니다6).
평가 7항목: ① 자발성 안구후부 통증, ② 안구 운동 시 통증, ③ 눈꺼풀 발적, ④ 눈꺼풀 부종, ⑤ 결막 발적, ⑥ 결막 부종, ⑦ 눈물언덕/반월주름 부종.
CAS ≥ 3/7이면 활동기로 판정하여 스테로이드 펄스 요법의 적응증이 됩니다. CAS ≥ 4/7은 테프로투무맙 RCT의 포함 기준입니다.
| 중증도 | 기준 | 치료 방침 |
|---|---|---|
| 경증 | 일상생활에 미치는 영향이 경미함 | 셀레늄 보충 + 경과 관찰 |
| 중등도~중증 | 눈꺼풀 후퇴 ≥2mm, 안구돌출 정상보다 ≥3mm, 복시 있음 | 스테로이드 펄스 요법, 테프로투무맙 |
| 시력 위협형 | 압박성 시신경병증, 각막궤양 | 응급 안와감압술 또는 고용량 스테로이드 |
EUGOGO(유럽 그레이브스 안병증 그룹)의 2021년판 임상 진료 가이드라인에 따른 분류입니다1). NOSPECS 분류(0~6등급)와 VISA 분류(시력, 염증, 사시, 외모)도 중증도 평가에 사용됩니다.
| 감별 질환 | 감별 포인트 | 영상 소견 |
|---|---|---|
| IgG4 관련 안질환 | 눈물샘 비대 + 외안근 비대, 혈청 IgG4 상승 | 눈물샘 및 외안근 미만성 비대 |
| 외안근염(안와근염) | 급성 발병, 심한 통증 | 힘줄 부위 비후 (갑상샘안병증은 근육배 비후이며 힘줄은 보존됨) |
| 안와종양/전이성 종양 | 단안성, 진행성 | 종괴 형성 |
갑상샘 기능 정상화가 필수 조건이며, 내분비내과와의 협력이 불가결합니다. 금연 지도는 병태 악화 및 치료 저항성의 최대 위험 인자인 흡연을 배제하기 위해 모든 증례에서 시행합니다.
셀레늄 보충: 경증 TED에 대해 셀레늄 200μg/일을 6개월간 보충하는 것이 질환 활동성 개선에 유익하며 권장됩니다10).
각막 및 안구 표면 보호: 인공눈물과 각막 보호 점안액을 자주 사용하고 취침 전 안연고를 도포하는 것이 기본입니다. 심한 토끼눈증(兎眼)의 경우 외측 가쪽눈꺼풀봉합술(lateral tarsorrhaphy)을 고려합니다.
스테로이드 펄스 요법(1차 선택): 메틸프레드니솔론 5001,000mg/주를 612주간 투여합니다1). 경구 스테로이드보다 정맥 스테로이드의 효과가 더 높습니다9). 누적 투여량은 8g 이내를 권장합니다(간 손상 위험 감소).
표준 프로토콜: 메틸프레드니솔론 1g×3일을 1코스로 시행합니다.
경구 프레드니솔론: 정맥 주사가 어려운 중등증~중증 예에서는 1mg/kg/일부터 시작합니다.
국소 스테로이드 주사: 위눈꺼풀 부종 및 염증성 눈꺼풀 뒤당김에 대해 트리암시놀론 아세토나이드(케나코트-A® 1앰플)의 국소 주사가 효과적입니다.
테프로투무맙(IGF-1R 억제제): 활동성 중등증중증 TED에서 안구 돌출 및 복시 개선이 기대되는 치료제입니다. 5건의 RCT(총 411명) 메타분석에서 안구 돌출의 유의한 감소, 24주째 CAS 01 달성률의 유의한 개선, 복시 개선율의 유의한 향상이 확인되었으며4), 중대한 이상 반응의 유의한 증가는 없었습니다. Smith 등(2017년, 42명 대 45명)7) 및 Douglas 등(2020년, 41명 대 42명)8)의 두 주요 RCT에서 근거가 구축되었습니다.
리툭시맙(항CD20 단클론항체): 다기관 무작위 시험에서 불응성 중등증~중증 TED의 질병 활성도를 낮출 가능성이 제시되었습니다12).
토실리주맙(IL-6 수용체 억제제): 스테로이드 및 리툭시맙 불응성 사례에 대한 사용이 검토되고 있습니다.
중등증~중증 TED에서는 면역억제 요법과 병용하여 시행합니다. 일반적으로 20Gy/10회를 2주에 걸쳐 조사합니다. 스테로이드와의 병용이 단독 투여보다 효과적인 것으로 알려져 있습니다.
수술은 원칙적으로 Rundle 곡선의 안정기에 접어들고 염증이 가라앉은 후에 계획합니다. 시행 순서는 엄격히 지켜야 하며, 선행 수술의 결과가 후속 수술 계획에 직접 영향을 미칩니다.
1단계: 안와감압술
적응증: 중증 안구돌출, 압박시신경병증(응급 적응증)
수술법 및 효과: 내측벽, 바닥, 외측벽 및 지방을 조합한 5가지 수술법이 있습니다. 1벽 감압으로 -1.4~-2.3mm, 3벽+지방 감압으로 -4.6~-5.0mm의 안구돌출 개선이 얻어집니다.
633안의 다기관 연구에서 동일 수술법 간 술자 간 유의한 차이 없이 안정적인 재현성이 확인되었습니다11).
2단계: 사시 수술
3단계: 눈꺼풀 수술
안와감압술 → 사시수술 → 눈꺼풀수술 순서로 진행합니다. 선행 수술의 결과가 후속 수술 계획에 영향을 미치므로 이 순서를 지키는 것이 중요합니다. 모든 수술은 원칙적으로 비활동기(런들 곡선의 안정기)에 들어간 후 계획합니다. 활동기에 수술을 하면 수술 후 변동이나 재발 위험이 높아집니다.
IGF-1 수용체(IGF-1R)를 억제하는 단일클론항체입니다. 안와 섬유아세포의 IGF-1R과 TSHR 복합체 신호를 차단하여 염증과 조직 팽창을 억제합니다. 5건의 무작위대조시험(총 411명)의 메타분석에서 안구돌출, 복시, CAS의 유의한 개선이 확인되었습니다. 중대한 이상반응의 유의한 증가는 없지만, 장기 안전성(청각장애, 고혈당 등)은 계속 평가 중입니다.
갑상선 기능 이상과 관련된 면역 기능 이상이 안와 내부 조직의 염증을 유발하여 안와 지방 조직과 외안근의 부피를 증가시킵니다. 구후 조직 압력 상승으로 안구 돌출이 발생합니다.
안와 지방 조직의 병태: 지방 세포의 비대와 간질의 림프구 침윤이 발생하고, 만성 염증으로 인한 부종과 반흔 형성이 나타납니다. 글리코사미노글리칸(GAG)과 히알루론산 합성 항진이 조직의 체액 저류와 종창을 유발합니다.
외안근의 병태: 횡문근 섬유 사이에 림프구 위주의 염증 세포 침윤이 나타나고, 근섬유는 변성 괴사를 일으킵니다. 간질에는 염증으로 인한 부종과 비후가 발생하고, 근섬유 사이에 결합 조직이 증식하여 외안근 비대가 형성됩니다. 외안근이 침범되는 빈도는 하직근이 가장 많고, 내직근, 상직근, 외직근 순으로 감소합니다. 따라서 상전 장애가 가장 흔하게 나타나고, 다음으로 외전 장애가 많습니다.
두 가지 기전이 복합되어 발생합니다.
①상안검거근의 병태: 염증으로 인해 근세포에 부종이 생겨 안검 부종이 됩니다. 근섬유 사이에는 지방 조직이 침입하고, 근세포는 괴사·반흔화되어 거근 기능이 변화합니다.
②뮐러근의 병태: 교감신경 지배를 받는 평활근인 뮐러근은 갑상선기능항진증에 동반된 교감신경 항진으로 지속적으로 수축하여 안검판을 올리고 안검열을 넓힙니다.
TSH 수용체(TSHR)에 대한 자가항체(TRAb)가 안와 섬유아세포의 TSHR을 활성화하여 하위 신호를 통해 염증성 사이토카인(TNF-α, IL-6, IL-1β)을 생성합니다. CD4+/CD8+ T 세포가 안와 조직에 침윤하여 염증 반응을 증폭시킵니다. 활성화된 섬유아세포는 지방세포와 근섬유아세포로 분화하여 각각 안와 지방 팽창과 외안근 섬유화를 유발합니다3).
IGF-1R은 TSHR과 복합체를 형성하여 안와 섬유아세포 활성화에 상승적으로 관여합니다4). 이 복합체 신호의 차단이 테프로투무맙의 작용 기전입니다.
염증 활동기(보통 1~3년)에서 안정기(비염증기)로 이행하는 자연 경과는 Rundle 곡선으로 개념화되었습니다13). 실제 치료 중재는 활동성과 중증도를 평가한 후 선택합니다1). 활동기에는 염증 억제 치료를 우선하고, 비염증 안정기에 수술 계획을 세웁니다.
FDA 승인 후에도 지속적으로 데이터가 축적되고 있습니다. 5개의 RCT(총 411예) 메타분석4)에서 유효성과 안전성이 확인되었지만, 장기 안전성(청각 장애, 고혈당 등 장기 결과)은 4상 시험 결과가 주목됩니다. 비활동기 TED로의 적응증 확대 가능성도 검토되고 있습니다.
7개 기관, 7명의 술자, 633안을 대상으로 한 다기관 연구11)에서 동일한 수술법을 시행한 경우 술자 간 유의한 차이가 없음이 확인되었습니다. 이는 다기관 RCT의 통계적 타당성을 지지하는 중요한 발견입니다. 내시경적 내측벽 감압술은 개방 수술과 비교하여 내측벽 및 바닥 감압에서 유의하게 더 큰 돌출도 개선(-3.67mm 대 -2.97mm, p=0.008)이 보고되었습니다. 수술 전 안구 돌출도가 수술 후 돌출도 변화와 통계적으로 유의하게 관련(p<0.001)된다는 것도 나타나 수술 전 평가의 중요성이 재확인되었습니다.
TRAb 및 TSAb의 활동기 변동이 CAS와 상관관계가 있는 것으로 알려져 있으며, 바이오마커에 기반한 치료 선택 연구가 진행 중입니다. 토실리주맙(IL-6 억제제)에 대해서도 난치성 증례에 대한 대규모 RCT가 기다려집니다.
Bartalena L, Kahaly GJ, Baldeschi L, et al. The 2021 European Group on Graves’ Orbitopathy (EUGOGO) clinical practice guidelines for the medical management of Graves’ orbitopathy. Eur J Endocrinol. 2021;184(4):G43-G67.
Prummel MF, Wiersinga WM. Smoking and risk of Graves’ disease. JAMA. 1993;269(4):479-482.
Bahn RS. Graves’ ophthalmopathy. N Engl J Med. 2010;362(8):726-738.
Cong X, Pei L, Hu H. Teprotumumab for treating active thyroid eye disease: a meta-analysis. Medicine. 2024;103(18):e38059.
Wang Y, Sharma A, Padnick-Silver L, et al. Physician-perceived impact of thyroid eye disease on patient quality of life in the United States. Ophthalmol Ther. 2021;10(1):75-87.
Mourits MP, Koornneef L, Wiersinga WM, et al. Clinical criteria for the assessment of disease activity in Graves’ ophthalmopathy: a novel approach. Br J Ophthalmol. 1989;73(8):639-644.
Smith TJ, Kahaly GJ, Ezra DG, et al. Teprotumumab for thyroid-associated ophthalmopathy. N Engl J Med. 2017;376(18):1748-1761.
Douglas RS, Kahaly GJ, Patel A, et al. Teprotumumab for the treatment of active thyroid eye disease. N Engl J Med. 2020;382(4):341-352.
Kahaly GJ, Pitz S, Hommel G, et al. Randomized, single blind trial of intravenous versus oral steroid monotherapy in Graves’ orbitopathy. J Clin Endocrinol Metab. 2005;90(9):5234-5240.
Marcocci C, Kahaly GJ, Krassas GE, Bartalena L, Prummel M, Stahl M, et al.; European Group on Graves’ Orbitopathy. Selenium and the course of mild Graves’ orbitopathy. N Engl J Med. 2011;364(20):1920-1931. PMID: 21591944. doi:10.1056/NEJMoa1012985.
Hong A, Shoji MK, Villatoro GA, et al. Intersurgeon variability in proptosis reduction after orbital decompression for thyroid eye disease: a multicenter analysis. Ophthalmic Plast Reconstr Surg. 2024;40(3).
Salvi M, Vannucchi G, Campi I, et al. Rituximab treatment in active moderate-to-severe Graves’ orbitopathy: an international, multicenter, single-blind, randomized placebo-controlled study. J Clin Endocrinol Metab. 2015;100(11):422-431.
Rundle FF, Wilson CW. Development and course of exophthalmos and ophthalmoplegia in Graves’ disease with special reference to the effect of thyroidectomy. Clin Sci. 1945;5(3-4):177-194. PMID: 21011937.