염증기 평가
CAS (Clinical Activity Score)1)
7개 항목: 자발성 구후통, 주시 시 통증, 눈꺼풀 발적, 결막 충혈, 결막 부종, 눈물언덕 종창, 눈꺼풀 부종
CAS≥3/7: 활동기로 판정. 스테로이드 펄스 요법의 적응증.
영상: MRI STIR 시퀀스에서 고신호 (염증 활동성 지표)

안와 감압술(orbital decompression surgery)은 갑상선 안병증(TED)에 동반된 안구돌출 및 압박성 시신경병증에 대해 시행하는 수술입니다. 안와벽(내측벽, 하벽, 외측벽)의 뼈를 제거하고 필요에 따라 안와 내 지방 조직을 절제하여 안와 용적을 확장하고 안구를 후방으로 복위시킵니다.
갑상선 안병증은 갑상선 기능 항진증(Graves병/바세도우병)에 동반되어 발생하는 경우와 갑상선 기능이 정상인 euthyroid ophthalmopathy로 발생하는 경우가 있습니다. 갑상선 안병증은 기본적으로 갑상선 호르몬과 무관하게 진행되며, 갑상선 관련 자가항체가 관여하는 자가면역 질환 중 하나입니다. 안와 지방 조직과 외안근의 용적 증가로 안와 내압이 상승하여 안구돌출이 발생합니다.
안와감압술에는 크게 두 가지 목적이 있습니다.
미용적 목적: 약물 치료로 개선되지 않는 현저한 안구돌출의 감소. 외모 변화와 사회생활의 지장이 적응 판단 기준이 됩니다.
시기능 보존: 비대해진 외안근이 안와 첨부(orbital apex)에서 시신경을 압박하는 압박성 시신경병증(dysthyroid optic neuropathy: DON)의 해소. 응급 적응이 될 수 있는 가장 중요한 수술 목적입니다.
안와감압술은 약물 치료에 반응하지 않는 시신경병증이나 현저한 안구돌출에 대해 시행됩니다. 염증기(활동기)에는 스테로이드 펄스 요법이나 방사선 요법을 우선 시행하는 것이 원칙입니다. 압박성 시신경병증이 심한 경우 염증기라도 응급으로 안와감압술을 시행하지만, 수술 후에도 스테로이드 치료를 지속하여 염증을 가라앉힙니다.
모든 안구돌출에 수술이 필요한 것은 아닙니다. 염증기에는 스테로이드 펄스 요법(메틸프레드니솔론 500~1,000mg/일×3일을 1코스)이나 방사선 요법이 일차 선택이며, 많은 증례에서 염증의 진정과 증상의 개선을 얻을 수 있습니다. 안와감압술은 약물 치료에 반응하지 않는 시신경병증이나 현저한 안구돌출에 대해 시행되는 확립된 치료 선택지입니다.
갑상샘안병증의 임상 증상은 안검 증상, 안구돌출, 복시, 시력 장애의 4가지로 분류됩니다. 젊은 환자에서는 안구돌출이 주가 되고, 고령자에서는 안구운동장애와 복시가 발생하기 쉽습니다.
시력 장애에는 각막 장애로 인한 시력 저하와 비대해진 외안근에 의한 압박성 시신경병증으로 인한 시력 저하의 두 가지가 있습니다. 하직근과 내직근이 이환되는 경우가 많아 상하사시와 내사시를 일으키기 쉽습니다.
| 징후명 | 소견 |
|---|---|
| Graefe 징후 | 하방 주시 시 상안검 하강 지연(lid lag) |
| Dalrymple 징후 | 위눈꺼풀 후퇴로 인한 눈구멍 틈새 확대 |
| Stellwag 징후 | 눈 깜빡임 감소 및 불완전한 눈 감김 |
| Gifford 징후 | 위눈꺼풀 뒤집기 어려움 |
염증기(활동기): 안와 후방 조직의 부종 및 염증이 주를 이룹니다. 스테로이드 펄스 요법과 방사선 요법이 우선시됩니다. 안와 감압술은 압박성 시신경병증이 심한 응급 상황에서만 적응됩니다.
비염증기(만성기): 염증이 가라앉고 고정된 안구 돌출, 안구 운동 장애, 시신경병증이 남아 있는 시기입니다. 이 시기가 안와 감압술의 주된 적응 시기입니다.
CAS(임상 활동성 점수)는 갑상샘 눈병증의 염증 활동성을 평가하는 7개 항목의 점수 체계입니다1). 7개 항목 중 3점 이상이면 활동기로 판정하고 약물 치료의 적응이 됩니다.
EUGOGO(유럽 그레이브스 안병증 그룹)의 중증도 분류는 경증, 중등증~중증, 시력 위협형(sight-threatening)의 3단계로 분류됩니다8). 시력 위협형은 압박성 시신경병증 또는 각막 궤양을 의미하며 응급 개입의 대상이 됩니다.
안와 내 안구 후방 조직의 섬유아세포에 존재하는 TSH 수용체(TSHR)가 항원이 되어 안와 조직에 림프구 침윤을 촉진하고, 대식세포를 활성화시키며, 국소 사이토카인 네트워크를 통해 염증 반응이 활성화됩니다. 이로 인해 안와 내용적이 증가하여 안구 돌출, 안와 내압 상승, 압박성 시신경병증이 발생합니다.
갑상샘눈병증은 그레이브스병 환자의 2550%에서 발생합니다3). 시력을 위협하는 압박시신경병증은 전체 증례의 약 35%에서 발생합니다.
아래곧은근과 안쪽곧은근이 가장 흔하게 침범됩니다. 바깥눈근육 침범은 아래곧은근이 가장 많고, 그다음으로 안쪽곧은근, 위곧은근, 가쪽곧은근 순으로 감소합니다. 따라서 위쪽 주시 장애가 가장 흔하고, 그다음으로 가쪽 주시 장애가 흔합니다.
흡연은 갑상샘눈병증의 가장 큰 위험 인자이며, 발병 위험, 중증도, 치료 저항성 모두와 관련됩니다. 633안, 386명의 환자를 대상으로 한 다기관 연구에서 흡연율은 기관 간에 16.2~71.1%로 널리 분포했습니다. 흡연은 눈병증의 중증도를 악화시키지만, 감압술 후 돌출도 감소 효과 자체에는 유의한 영향을 미치지 않았습니다4).
갑상샘 관련 자가항체 중 하나라도 양성인 경우 진단이 확립됩니다. 측정 대상은 TSH 수용체 항체(TRAb), 갑상샘자극항체(TSAb), 항갑상샘글로불린 항체(TgAb), 항갑상샘과산화효소 항체(TPOAb)입니다. 갑상샘 기능이 정상이더라도, 눈돌출, 눈꺼풀 뒤당김, 복시 소견이 있으면 검사를 시행합니다.
헤르텔 눈돌출계로 눈돌출도를 측정합니다. 일본인의 정상 범위는 10~15mm(평균 13mm)이며, 이를 초과하면 눈돌출로 판정합니다. 좌우 차이는 2mm 이내가 정상입니다. 수술 전후 평가에 표준적으로 사용됩니다.
MRI(일차 선택): T1 강조 영상에서 바깥눈근육의 형태를 평가합니다. STIR(short-TI inversion recovery) 기법은 염증 부위를 고신호 영역으로 나타내어 염증 활동성 평가에 유용합니다. 관상면은 아래빗근을 제외한 모든 바깥눈근육을 동시에 평가할 수 있으므로 필수적입니다.
CT: 바깥눈근육의 비후를 확인합니다(힘줄 비후는 경미하고 근육배가 비후되어 전체적으로 방추형을 나타냄). 눈확벽 평가 및 수술 계획에 골창 CT를 사용합니다. 감압술 전 눈확 단면적(위눈확틈새 앞쪽 약 1.5cm의 관상 CT 단면적) 측정은 수술 후 돌출도 변화 예측에 사용됩니다4).
RAPD(상대구심동공운동장애) 양성, CFF(임계깜빡임빈도) 감소, 색각 이상, 시야 장애는 압박시신경병증의 초기 징후입니다. 이러한 소견이 확인되면 응급 대처가 필요합니다.
염증기 평가
CAS (Clinical Activity Score)1)
7개 항목: 자발성 구후통, 주시 시 통증, 눈꺼풀 발적, 결막 충혈, 결막 부종, 눈물언덕 종창, 눈꺼풀 부종
CAS≥3/7: 활동기로 판정. 스테로이드 펄스 요법의 적응증.
영상: MRI STIR 시퀀스에서 고신호 (염증 활동성 지표)
비염증기 평가
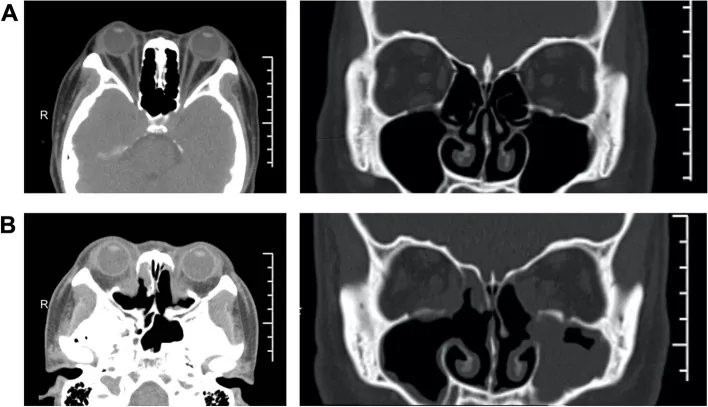
갑상선기능항진증이 있는 경우 갑상선 호르몬 정상화가 필수 전제이며, 내분비내과와의 긴밀한 협력이 필요합니다. 수술은 Rundle 곡선의 안정기(비염증기)에 염증이 가라앉은 후에 계획합니다. 시행 순서는 안와감압술→사시수술→안검수술이며, 선행 수술 결과가 후속 수술 계획에 직접 영향을 미치므로 이 순서를 엄격히 준수합니다.
스테로이드 펄스 요법(1차 선택): 메틸프레드니솔론 5001,000mg/일을 3일간 1쿠르로 시행합니다. 증상을 보면서 1주 간격으로 23쿠르 시행한 후, 정맥주사 또는 경구로 점차 감량합니다.
국소 스테로이드 주사: 비대해진 외안근 주위 테논낭 아래에 스테로이드를 주사합니다. 상안검 부종 및 염증으로 인한 안검 후퇴에는 트리암시놀론 아세토나이드(케나코르트-A® 1앰플)의 국소 주사가 효과적입니다.
방사선 요법: 스테로이드 치료가 불가능하거나 재발한 경우 적응됩니다. 구후 조직에 1.5~2.0Gy/일을 10일간 조사합니다.
테프로투무맙(IGF-1R 항체): 해외에서 안구돌출의 유의한 개선이 보고된 생물학적 제제입니다5). IGF-1 수용체를 억제하고 안와 섬유아세포 활성화를 억제하는 기전을 가집니다. 현재 일본에서는 미승인 상태이며, 연구 단계의 치료 옵션으로 간주됩니다.
안와벽 절제 범위와 지방 절제의 조합에 따라 주로 5가지 수술 방법으로 분류됩니다. 633안의 다기관 연구(7명의 술자)에 의한 수술 방법별 돌출도 감소량은 다음과 같습니다4).
| 수술 방법 | 벽 수 | 돌출도 감소량(평균) |
|---|---|---|
| 내측벽만 | 1벽 | 1.4~2.3mm |
| 지방+외측벽 | 2벽 | 2.9~3.6mm |
| 내측벽 + 하벽 | 2벽 | 2.6~3.7mm |
| 지방 + 외측벽 + 내측벽 | 3벽 | 3.1~3.9mm |
| 지방 + 외측벽 + 내측벽 + 하벽 | 3벽 + 지방 | 4.6~5.0mm (최대 효과) |
벽의 수가 증가함에 따라 돌출도 감소량이 증가합니다. 중증도에 따른 단계적 감압(graded decompression)이 수술 선택의 기본 원칙이며2)6), 미용 목적 또는 시신경 보호 목적에 따라 수술 방식이 결정됩니다. 수술 전 돌출도가 높을수록 수술 후 개선량도 커지는 것이 통계적으로 유의하게 나타났습니다(p<0.001)4).
| 순서 | 수술 | 시기 |
|---|---|---|
| 1 | 안와 감압술 | 비염증기 (압박성 시신경병증에서는 응급 시행도 가능) |
| 2 | 사시 수술 | 감압술 후 사시가 안정된 후 |
| 3 | 안검 수술 | 마지막에 시행 |
사시 수술: 만성기에 고정된 사시에 대해 비후된 직근의 후전술을 주로 시행합니다. 안와 감압술 후 새로운 복시가 나타날 수 있으므로 사시가 안정된 후 수술 계획을 세웁니다.
안검 수술: 안검 후퇴에 대해 염증에 의한 경우 트리암시놀론 아세토니드 국소 주사를 시행합니다. 비염증 안정기의 고정된 안검 후퇴에는 후퇴 교정술(뮐러근 절제술, 상안검거근 후전술)을 시행합니다.
술식에 따라 다릅니다. 1벽 감압(내측벽만)으로 1.42.3mm, 3벽 및 지방 감압(최대 술식)으로 4.65.0mm의 돌출도 감소가 기대됩니다4). 벽 수가 증가함에 따라 효과가 증가하고, 수술 전 돌출도가 높을수록 수술 후 개선량도 커지는 경향이 있습니다. 중증도에 따른 단계적 감압(graded decompression)이 권장됩니다6).
안와 내 구후 조직의 섬유아세포에 존재하는 TSH 수용체가 항원이 되어 안와 조직에 림프구 침윤을 촉진하고, 대식세포를 활성화시키며, 국소 사이토카인 네트워크를 통해 염증 반응이 활성화됩니다. 염증성 사이토카인(IL-1, IL-6, TNF-α)이 생성되고 안와 내용적이 증가합니다.
지방 조직의 변화: 지방 세포의 비대와 간질의 림프구 침윤이 발생하고, 만성 염증으로 인한 부종과 반흔 형성이 나타납니다. 글리코사미노글리칸(GAG) 및 히알루론산 합성 항진이 조직의 체액 저류 및 종창을 유발합니다.
외안근의 변화: 횡문근 섬유 사이에 림프구 위주의 염증 세포 침윤이 관찰되고, 근섬유는 변성 괴사를 일으킵니다. 간질에는 염증으로 인한 부종과 비후가 발생하고, 근섬유 사이에 결합 조직이 증식하여 외안근 비대가 형성됩니다. CT/MRI상 힘줄 비후는 경미하고 근복이 비대하여 전체적으로 방추형을 나타냅니다.
안와 내용적 증가로 인한 안와 내압 상승과 외안근 비후가 안와 첨부(orbital apex)에서 시신경을 압박합니다. RAPD 양성, CFF 감소, 시야 장애가 징후입니다. 이 기전이 안와 감압술(안와 용적 확대)에 의한 시신경 압박 해소의 근거가 됩니다.
IGF-1 수용체(IGF-1R)는 안와 섬유아세포에서 TSHR과 복합체를 형성하여 안와 섬유아세포 활성화에 상승적으로 관여합니다5). 이 복합체 신호의 차단이 테프로투무맙의 작용 기전이며, 해외에서의 안구돌출 개선이라는 치료 성과의 이론적 기반이 됩니다.
안와벽을 제거함으로써 안와와 인접한 부비동(사골동, 상악동, 접형동) 사이의 골격벽이 없어지고, 안와 내 지방이 부비동 쪽으로 탈출하여 안와 내용적이 확대됩니다. 이로 인해 안와 내압이 감소하고 안구가 후방으로 이동합니다. 지방 절제를 병행하면 감압 효과를 더욱 높일 수 있습니다.
Hong 등(2025)의 7개 기관, 7명의 술자, 633안을 대상으로 한 다기관 후향적 연구에서는 동일 술식을 시행한 경우 술자 간 돌출도 감소량에 유의한 차이가 없음이 확인되었습니다4) (표준오차 0.14~0.56mm). 표준화된 술식의 재현성이 다기관 수준에서 입증된 것은 다기관 RCT의 통계적 타당성을 지지하는 중요한 소견입니다.
또한, 수술 전 안구돌출도가 수술 후 돌출도 변화를 예측하는 가장 유의한 인자임이 입증되었으며(p<0.001), 수술 전 평가의 중요성이 재확인되었습니다4).
해당 연구에서는 수술법별로 접근법의 효과도 검토되었습니다. 내측벽+하벽 감압에서는 내시경군이 개방 수술군보다 유의하게 더 큰 돌출도 감소를 보였습니다(-3.67mm vs -2.97mm, p=0.008). 반면, 지방+외측벽+내측벽 감압에서는 내시경과 개방 수술 간에 유의한 차이가 없었습니다4).
테프로투무맙(IGF-1R 항체)은 해외에서 안구돌출의 유의한 개선이 보고된 생물학적 제제입니다5). 일본에서는 현재 승인되지 않았지만, 국제적으로는 활동기 중등도~중증 갑상샘눈병증에 대한 약물 요법으로 자리 잡고 있습니다. 장기 안전성(청각 장애, 고혈당 등)은 4상 시험 결과가 주목됩니다.
감압술 후 새로 발생한 복시 발생을 예측하는 모델이 개발되었으며7), 수술 전 상담 및 수술법 선택에 활용될 것으로 기대됩니다.
흡연은 갑상샘눈병증의 중증도를 악화시키는 가장 큰 위험 인자이지만, 633안 연구에서는 감압술에 의한 돌출도 감소 효과 자체에 흡연이 유의한 영향을 미치지 않았습니다4). 치료 효과 예측에서 흡연의 역할이 정밀화되고 있습니다.
Mourits MP, Prummel MF, Wiersinga WM, et al. Clinical activity score as a guide in the management of patients with Graves’ ophthalmopathy. Clin Endocrinol (Oxf). 1997;47:9-14.
Mourits MP, Bijl H, Altea MA, et al; European Group on Graves’ Orbitopathy (EUGOGO). Outcome of orbital decompression for disfiguring proptosis in patients with Graves’ orbitopathy using various surgical procedures. Br J Ophthalmol. 2009;93:1518-1523.
Bahn RS, Heufelder AE. Pathogenesis of Graves’ ophthalmopathy. N Engl J Med. 1993;329:1468-1475.
Hong A, Shoji MK, Villatoro GA, et al. Intersurgeon variability in proptosis reduction after orbital decompression for thyroid eye disease: a multicenter analysis. Ophthalmic Plast Reconstr Surg. 2025. [Epub ahead of print].
Rootman DB. Orbital decompression for thyroid eye disease. Surv Ophthalmol. 2018;63:86-104.
Kikkawa DO, Pornpanich K, Cruz RC Jr, Levi L, Granet DB. Graded orbital decompression based on severity of proptosis. Ophthalmology. 2002;109(7):1219-1224. doi:10.1016/S0161-6420(02)01068-0.
Nair AA, Ediriwickrema LS, Dolman PJ, et al. Predictive modeling of new-onset postoperative diplopia following orbital decompression for thyroid eye disease. Ophthalmic Plast Reconstr Surg. 2022;38(6):551-557. PMID:35551414. doi:10.1097/IOP.0000000000002196.
Bartalena L, Kahaly GJ, Baldeschi L, Dayan CM, Eckstein A, Marcocci C, et al; EUGOGO. The 2021 European Group on Graves’ orbitopathy (EUGOGO) clinical practice guidelines for the medical management of Graves’ orbitopathy. Eur J Endocrinol. 2021;185(4):G43-G67. PMID:34297684. doi:10.1530/EJE-21-0479.