發炎期評估
CAS(臨床活動性評分)1)
7個項目:自發性球後痛、注視時疼痛、眼瞼發紅、結膜充血、結膜水腫、淚阜腫脹、眼瞼水腫
CAS≥3/7:判定為活動期。適用類固醇脈衝療法。
影像學:MRI STIR序列高訊號(發炎活動性指標)

眼眶減壓術是針對甲狀腺眼病(TED)引起的眼球突出和壓迫性視神經病變進行的手術。通過切除眼眶壁(內側壁、下壁、外側壁)的骨質,並根據需要切除眼眶內脂肪組織,擴大眼眶容積,使眼球向後復位。
甲狀腺眼病可伴隨甲狀腺功能亢進症(Graves病/巴塞多病)發生,也可作為甲狀腺功能正常的甲狀腺眼病發生。甲狀腺眼病基本上獨立於甲狀腺激素進展,是一種涉及甲狀腺相關自體抗體的自體免疫性疾病。眼眶脂肪組織和眼外肌體積增大導致眼眶內壓升高,引起眼球突出。
眼眶減壓手術主要有兩個目的。
美容目的:減輕藥物治療無效的顯著眼球突出。容貌變化和社交障礙是判斷適應症的標準。
保護視功能:解除因肥大的眼外肌在眶尖壓迫視神經引起的壓迫性視神經病變(dysthyroid optic neuropathy: DON)。這是最重要的手術目的,可能成為緊急適應症。
眼眶減壓手術用於對藥物治療無效的視神經病變或顯著眼球突出。在發炎期(活動期),原則上先進行類固醇脈衝療法或放射治療。如果壓迫性視神經病變嚴重,即使在發炎期也可能緊急施行眼眶減壓手術,但術後需繼續類固醇治療以控制發炎。
並非所有眼球突出都需要手術。在發炎期,類固醇脈衝療法(甲基潑尼松龍500-1000mg/日×3天為一個療程)或放射治療是首選,許多病例可獲得發炎消退和症狀改善。眼眶減壓手術是對藥物治療無效的視神經病變或顯著眼球突出的既定治療選擇。
甲狀腺眼病的臨床症狀分為四類:眼瞼症狀、眼球突出、複視和視力障礙。年輕患者以眼球突出為主,老年患者則易出現眼球運動障礙和複視。
視力障礙包括兩種:角膜損傷導致的視力下降和肥大的眼外肌壓迫視神經導致的視力下降。下直肌和內直肌常受累,易導致垂直斜視和內斜視。
| 徵候名稱 | 表現 |
|---|---|
| Graefe徵 | 下視時上眼瞼遲落(lid lag) |
| Dalrymple徵 | 上眼瞼退縮導致瞼裂增寬 |
| Stellwag徵 | 眨眼減少與不完全閉眼 |
| Gifford徵 | 上眼瞼外翻困難 |
發炎期(活動期):以球後組織水腫和發炎為主。優先使用類固醇脈衝治療和放射治療。僅在壓迫性視神經病變嚴重時緊急進行眼眶減壓手術。
非發炎期(慢性期):發炎消退,殘留固定的眼球突出、眼球運動障礙和視神經病變。此期是眼眶減壓手術的主要適應症。
CAS(臨床活動性評分)是評估甲狀腺眼病發炎活動性的7項評分系統1)。7項中≥3分判定為活動期,是藥物治療的適應症。
EUGOGO(歐洲Graves眼病協作組)嚴重程度分級將疾病分為輕度、中重度、視力威脅型三級8)。視力威脅型指壓迫性視神經病變或角膜潰瘍,需緊急干預。
眼眶內球後組織的纖維母細胞上的TSH受體(TSHR)作為抗原,促進淋巴細胞浸潤眼眶組織,激活巨噬細胞,通過局部細胞因子網絡激活發炎反應。這導致眼眶內容積增加,引起眼球突出、眶內壓升高和壓迫性視神經病變。
甲狀腺眼病變發生在25%–50%的葛瑞夫茲病患者中3)。威脅視力的壓迫性視神經病變約占所有病例的3%–5%。
下直肌和內直肌最常受侵犯。眼外肌侵犯以下直肌最多見,其次依序為內直肌、上直肌和外直肌。因此,上轉障礙最常見,其次是外轉障礙。
吸菸是甲狀腺眼病變最大的風險因子,與發病風險、嚴重程度和治療抗性均相關。一項涉及633隻眼、386名患者的多中心研究顯示,吸菸率在不同機構間差異很大,為16.2%–71.1%。雖然吸菸會加重眼病變的嚴重程度,但對減壓術後眼球突出度的減少效果沒有顯著影響4)。
當任何一種甲狀腺相關自體抗體陽性時即可確診。檢測目標包括TSH受體抗體(TRAb)、甲狀腺刺激抗體(TSAb)、抗甲狀腺球蛋白抗體(TgAb)和抗甲狀腺過氧化酶抗體(TPOAb)。即使甲狀腺功能正常,如果存在眼球突出、眼瞼退縮或複視的表現,也應進行檢查。
使用Hertel眼球突出計測量眼球突出度。日本人的正常範圍為10–15 mm(平均13 mm),超過此值判定為眼球突出。雙眼差異在2 mm以內為正常。該檢查常規用於術前和術後評估。
MRI(首選):T1加權像評估眼外肌形態。STIR(短TI反轉恢復)序列可將發炎部位顯示為高信號區域,有助於評估發炎活動性。冠狀切面是必需的,因為它可以同時評估除下斜肌外的所有眼外肌。
CT:確認眼外肌增厚(肌腱增厚輕微,肌腹增厚,整體呈梭形)。使用骨窗CT評估眼眶壁和進行手術規劃。減壓術前測量眼眶橫截面積(上眶裂前方約1.5 cm處的冠狀CT橫截面積)可用於預測術後眼球突出度的變化4)。
RAPD(相對傳入性瞳孔缺損)陽性、CFF(臨界閃爍頻率)降低、色覺異常和視野缺損是壓迫性視神經病變的早期徵象。如果確認存在這些表現,需要緊急處理。
發炎期評估
CAS(臨床活動性評分)1)
7個項目:自發性球後痛、注視時疼痛、眼瞼發紅、結膜充血、結膜水腫、淚阜腫脹、眼瞼水腫
CAS≥3/7:判定為活動期。適用類固醇脈衝療法。
影像學:MRI STIR序列高訊號(發炎活動性指標)
非發炎期評估
它是評估甲狀腺眼病發炎活動性的7項評分系統(0~7分)1)。①自發性球後痛、②注視時疼痛、③眼瞼發紅、④結膜充血、⑤結膜水腫、⑥淚阜腫脹、⑦眼瞼水腫,每項1分,3分及以上判定為活動期。它是判斷發炎活動性和類固醇脈衝療法適應症的重要臨床指標。
如果存在甲狀腺功能亢進症,甲狀腺激素正常化是必要前提,需要與內分泌科緊密協作。手術應在Rundle曲線的穩定期(非炎症期)炎症消退後進行。手術順序為眼眶減壓術→斜視手術→眼瞼手術,必須嚴格遵守此順序,因為前次手術的結果直接影響後續手術計劃。
類固醇脈衝療法(一線治療):甲潑尼龍500~1000毫克/日,連續3天為一個療程。根據症狀,每隔一週進行2~3個療程後,通過靜脈滴注或口服逐漸減量。
局部類固醇注射:在肥大的眼外肌周圍的Tenon囊下進行類固醇注射。對於上眼瞼水腫和炎症引起的眼瞼退縮,局部注射曲安奈德(Kenacort-A® 1安瓿)有效。
放射治療:適用於無法進行類固醇治療或復發的情況。球後組織每日照射1.5~2.0 Gy,共10天。
替妥木單抗(IGF-1R抗體):一種生物製劑,在國外報導可顯著改善眼球突出5)。其機制是抑制IGF-1受體,抑制眼眶纖維母細胞的活化。目前在日本尚未核准,屬於研究階段的治療選擇。
根據眼眶壁切除範圍和脂肪切除的組合,主要分為5種術式。一項633眼的多中心研究(7名術者)按術式分類的突出度減少量如下4)。
| 術式 | 壁數 | 突出度減少量(平均) |
|---|---|---|
| 僅內側壁 | 1壁 | 1.4~2.3毫米 |
| 脂肪+外側壁 | 2壁 | 2.9~3.6毫米 |
| 內側壁+下壁 | 2壁 | 2.6~3.7mm |
| 脂肪+外側壁+內側壁 | 3壁 | 3.1~3.9mm |
| 脂肪+外側壁+內側壁+下壁 | 3壁+脂肪 | 4.6~5.0mm(最大效果) |
隨著壁數增加,突出度減少量增大。根據嚴重程度進行分級減壓(graded decompression)是術式選擇的基本原則2)6),術式也根據是美容目的還是視神經保護目的而決定。術前突出度越高,術後改善量也越大,這在統計學上顯著(p<0.001)4)。
| 順序 | 手術 | 時機 |
|---|---|---|
| 1 | 眼眶減壓術 | 非發炎期(壓迫性視神經病變時緊急施行) |
| 2 | 斜視手術 | 減壓術後斜視穩定後 |
| 3 | 眼瞼手術 | 最後進行 |
斜視手術:針對慢性期已固定的斜視,主要進行肥厚直肌的後徙術。眼眶減壓術後可能出現新的複視,應在斜視穩定後制定手術計畫。
眼瞼手術:對於眼瞼退縮,若由發炎引起,則局部注射曲安奈德。對於非發炎穩定期的固定性眼瞼退縮,進行退縮矯正術(Müller肌切除術或上眼瞼提肌腱膜後徙術)。
因術式而異。單壁減壓(僅內側壁)可減少突出1.4–2.3毫米,三壁加脂肪減壓(最大術式)可減少4.6–5.0毫米4)。隨著減壓壁數增加,效果增強,術前突出度越高,術後改善量越大。建議根據嚴重程度進行分級減壓6)。
眼眶內球後組織的纖維母細胞中存在的TSH受體作為抗原,促進淋巴球浸潤眼眶組織,活化巨噬細胞,並透過局部細胞激素網絡活化發炎反應。產生發炎性細胞激素(IL-1、IL-6、TNF-α),眼眶內容積逐漸增大。
脂肪組織的變化:脂肪細胞腫大,間質出現淋巴球浸潤,慢性發炎導致水腫和疤痕形成。糖胺聚醣(GAG)和玻尿酸合成增加,引起組織液滯留和腫脹。
眼外肌的變化:橫紋肌纖維間出現以淋巴球為主的發炎細胞浸潤,肌纖維發生變性壞死。間質因發炎出現水腫和增厚,肌纖維間結締組織增生,形成眼外肌肥大。CT/MRI上肌腱增厚輕微,肌腹肥大,整體呈紡錘形。
眼眶內容積增大導致眶內壓升高,眼外肌肥厚,在眶尖部壓迫視神經。RAPD陽性、CFF下降、視野缺損為徵象。此機轉是眼眶減壓術(擴大眼眶容積)解除視神經壓迫的依據。
IGF-1受體(IGF-1R)在眼眶纖維母細胞上與TSHR形成複合物,協同參與眼眶纖維母細胞的活化5)。阻斷該複合物訊號是替妥木單抗的作用機轉,也是海外眼球突出改善治療成果的理論基礎。
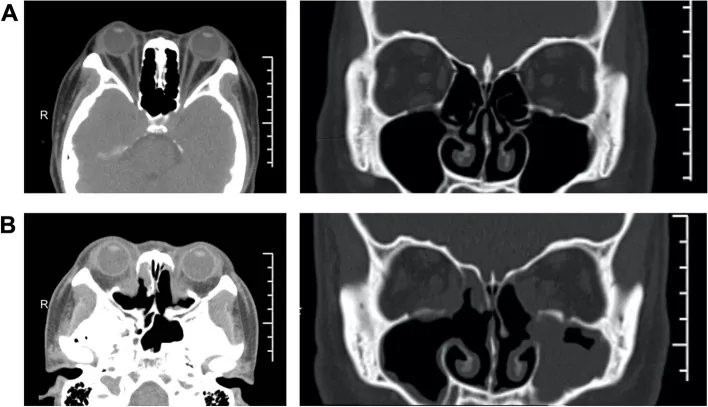
切除眼眶壁後,眼眶與相鄰鼻竇(篩竇、上頷竇、蝶竇)之間的骨隔消失,眶內脂肪向鼻竇側脫出,眼眶容積擴大。這降低了眶內壓,使眼球向後移動。結合脂肪切除可進一步增強減壓效果。
Hong等人(2025年)對7個機構、7位術者、633眼進行的多中心回顧性研究證實,在實施相同術式時,術者間眼球突出度減少量無顯著差異4)(標準誤0.14~0.56mm)。標準化術式的可重複性在多中心層級得到證實,這是支持多中心RCT統計效度的重要發現。
此外,術前眼球突出度被證明是預測術後突出度變化的最顯著因子(p<0.001),再次確認了術前評估的重要性4)。
該研究也按術式探討了入路方法的效果。在內側壁+下壁減壓中,內視鏡組比開放手術組顯示出顯著更大的突出度減少(-3.67mm vs -2.97mm,p=0.008)。而在脂肪+外側壁+內側壁減壓中,內視鏡與開放手術之間無顯著差異4)。
替妥木單抗(IGF-1R抗體)是一種在國外被報導可顯著改善眼球突出的生物製劑5)。目前在日本尚未核准,但在國際上被定位為活動期中重度甲狀腺眼病的藥物治療。長期安全性(聽力障礙、高血糖等)備受關注,期待IV期試驗結果。
已開發出預測減壓術後新發複視的模型7),有望用於術前諮詢和術式選擇。
吸菸是加重甲狀腺眼病嚴重度的最大風險因子,但在633眼的研究中,吸菸對減壓術後突出度減少效果本身無顯著影響4)。吸菸在預測治療效果中的作用正在精細化。
Mourits MP, Prummel MF, Wiersinga WM, et al. Clinical activity score as a guide in the management of patients with Graves’ ophthalmopathy. Clin Endocrinol (Oxf). 1997;47:9-14.
Mourits MP, Bijl H, Altea MA, et al; European Group on Graves’ Orbitopathy (EUGOGO). Outcome of orbital decompression for disfiguring proptosis in patients with Graves’ orbitopathy using various surgical procedures. Br J Ophthalmol. 2009;93:1518-1523.
Bahn RS, Heufelder AE. Pathogenesis of Graves’ ophthalmopathy. N Engl J Med. 1993;329:1468-1475.
Hong A, Shoji MK, Villatoro GA, et al. Intersurgeon variability in proptosis reduction after orbital decompression for thyroid eye disease: a multicenter analysis. Ophthalmic Plast Reconstr Surg. 2025. [Epub ahead of print].
Rootman DB. Orbital decompression for thyroid eye disease. Surv Ophthalmol. 2018;63:86-104.
Kikkawa DO, Pornpanich K, Cruz RC Jr, Levi L, Granet DB. Graded orbital decompression based on severity of proptosis. Ophthalmology. 2002;109(7):1219-1224. doi:10.1016/S0161-6420(02)01068-0.
Nair AA, Ediriwickrema LS, Dolman PJ, et al. Predictive modeling of new-onset postoperative diplopia following orbital decompression for thyroid eye disease. Ophthalmic Plast Reconstr Surg. 2022;38(6):551-557. PMID:35551414. doi:10.1097/IOP.0000000000002196.
Bartalena L, Kahaly GJ, Baldeschi L, Dayan CM, Eckstein A, Marcocci C, et al; EUGOGO. The 2021 European Group on Graves’ orbitopathy (EUGOGO) clinical practice guidelines for the medical management of Graves’ orbitopathy. Eur J Endocrinol. 2021;185(4):G43-G67. PMID:34297684. doi:10.1530/EJE-21-0479.