การผ่าตัดลดความดันในเบ้าตา เป็นหัตถการเพื่อรักษาภาวะตายื่นและโรคเส้นประสาทตาถูกกดทับ ที่เกี่ยวข้องกับโรคตาจากต่อมไทรอยด์ โดยการตัดกระดูกผนังเบ้าตา ออกเพื่อขยายปริมาตรเบ้าตา
ปริมาณการลดตายื่นจะเพิ่มขึ้นตามจำนวนผนังที่ลดความดัน (1 ผนัง: 1.4–2.3 มม., 3 ผนัง + ไขมัน: 4.6–5.0 มม.)
ในระยะอักเสบ การให้สเตียรอยด์ แบบพัลส์เป็นทางเลือกแรก และการผ่าตัดลดความดันจะจำกัดเฉพาะกรณีที่ไม่ตอบสนองต่อยาหรือกรณีฉุกเฉินของโรคเส้นประสาทตาถูกกดทับ
ประเมินตายื่นด้วยเครื่องวัดตายื่น Hertel โดยค่าปกติในคนญี่ปุ่นคือ 10–15 มม. (เฉลี่ย 13 มม.)
ระดับตายื่นก่อนผ่าตัดเป็นปัจจัยที่มีนัยสำคัญที่สุดในการทำนายการเปลี่ยนแปลงของตายื่นหลังผ่าตัด (p<0.001)
สำหรับเทคนิคการผ่าตัดเดียวกัน ไม่มีความแตกต่างอย่างมีนัยสำคัญในผลการลดความดันระหว่างศัลยแพทย์ ซึ่งยืนยันความสามารถในการทำซ้ำของเทคนิคที่ได้มาตรฐาน
การผ่าตัดลดความดันในเบ้าตา (orbital decompression surgery) เป็นหัตถการที่ทำเพื่อรักษาภาวะตายื่นและโรคเส้นประสาทตาถูกกดทับ ที่เกี่ยวข้องกับโรคตาจากต่อมไทรอยด์ (thyroid eye disease: TED) โดยตัดกระดูกผนังเบ้าตา (ผนังด้านใน ด้านล่าง ด้านนอก) ออก และตัดเนื้อเยื่อไขมันในเบ้าตา ออกตามความจำเป็น เพื่อขยายปริมาตรเบ้าตา และทำให้ลูกตากลับไปอยู่ตำแหน่งด้านหลัง
โรคตาจากต่อมไทรอยด์ อาจเกิดขึ้นร่วมกับภาวะต่อมไทรอยด์ทำงานเกิน (โรคเกรฟส์/เบสโดว์) หรือเป็นโรคตาจากต่อมไทรอยด์ ที่การทำงานของต่อมไทรอยด์ปกติ (euthyroid ophthalmopathy) โดยพื้นฐานแล้วโรคตาจากต่อมไทรอยด์ ดำเนินไปโดยไม่ขึ้นกับฮอร์โมนไทรอยด์ และเป็นหนึ่งในโรคภูมิต้านตนเองที่เกี่ยวข้องกับแอนติบอดีต่อต่อมไทรอยด์ การเพิ่มขึ้นของปริมาตรเนื้อเยื่อไขมันในเบ้าตา และกล้ามเนื้อนอกตาทำให้ความดันภายในเบ้าตา สูงขึ้น ส่งผลให้เกิดภาวะตายื่น
การผ่าตัดลดความดันในเบ้าตา มีวัตถุประสงค์หลักสองประการ
วัตถุประสงค์ด้านความสวยงาม : ลดภาวะตายื่นที่เด่นชัดซึ่งไม่ตอบสนองต่อการรักษาด้วยยา การเปลี่ยนแปลงของรูปลักษณ์หรือผลกระทบต่อชีวิตทางสังคมเป็นเกณฑ์ในการพิจารณา
การรักษาการทำงานของการมองเห็น : แก้ไขภาวะเส้นประสาทตา ถูกกดทับ (dysthyroid optic neuropathy: DON) ที่เกิดจากกล้ามเนื้อนอกลูกตา ที่โตขึ้นบริเวณปลายเบ้าตา (orbital apex) นี่คือวัตถุประสงค์การผ่าตัดที่สำคัญที่สุด ซึ่งอาจเป็นข้อบ่งชี้ฉุกเฉิน
การผ่าตัดลดความดันในเบ้าตา ทำในกรณีเส้นประสาทตา ถูกทำลายหรือตายื่นรุนแรงที่ไม่ตอบสนองต่อการรักษาด้วยยา ในระยะอักเสบ (ระยะ active) หลักการคือให้การรักษาด้วยสเตียรอยด์ แบบ pulse หรือการฉายรังสีก่อน หากภาวะเส้นประสาทตา ถูกกดทับรุนแรง อาจต้องผ่าตัดลดความดันในเบ้าตา อย่างฉุกเฉินแม้ในระยะอักเสบ แต่ต้องให้สเตียรอยด์ ต่อเนื่องหลังผ่าตัดเพื่อลดการอักเสบ
Q
ตายื่นจากโรคตาต่อมไทรอยด์ทุกรายจำเป็นต้องผ่าตัดหรือไม่?
A
ไม่ใช่ตายื่นทุกรายที่ต้องผ่าตัด ในระยะอักเสบ การรักษาด้วยสเตียรอยด์ แบบ pulse (methylprednisolone 500-1000 มก./วัน นาน 3 วันเป็น 1 คอร์ส) หรือการฉายรังสีเป็นทางเลือกแรก และในหลายกรณีสามารถลดการอักเสบและทำให้อาการดีขึ้นได้ การผ่าตัดลดความดันในเบ้าตา เป็นทางเลือกการรักษาที่เป็นมาตรฐานสำหรับเส้นประสาทตา ถูกทำลายหรือตายื่นรุนแรงที่ไม่ตอบสนองต่อการรักษาด้วยยา
อาการทางคลินิกของโรคตาต่อมไทรอยด์แบ่งเป็น 4 ประเภท: อาการทางเปลือกตา, ตายื่น, เห็นภาพซ้อน , และความบกพร่องทางการมองเห็น ในผู้ป่วยอายุน้อย ตายื่นเป็นอาการหลัก ส่วนในผู้สูงอายุ มักเกิดความผิดปกติของการเคลื่อนไหวลูกตา และเห็นภาพซ้อน
ความบกพร่องทางการมองเห็น มี 2 ชนิด: การมองเห็น ลดลงจากความเสียหายของกระจกตา และการมองเห็น ลดลงจากเส้นประสาทตา ถูกกดทับโดยกล้ามเนื้อนอกลูกตา ที่โตขึ้น กล้ามเนื้อเรคตัสด้านล่างและเรคตัสด้านในมักได้รับผลกระทบ ทำให้เกิดตาเหล่ แนวตั้งและตาเหล่เข้า ได้ง่าย
ชื่อสัญญาณ ลักษณะที่พบ สัญญาณ Graefe เปลือกตาบนหย่อนลงช้าเมื่อมองลง (lid lag) เครื่องหมาย Dalrymple การเปิดของรอยแยกเปลือกตากว้างขึ้นเนื่องจากการหดรั้งของเปลือกตาบน เครื่องหมาย Stellwag การกระพริบตาลดลงและการปิดเปลือกตาไม่สมบูรณ์ เครื่องหมาย Gifford การพลิกเปลือกตาบนทำได้ยาก
ระยะอักเสบ (ระยะ active) : มีอาการบวมน้ำและอักเสบของเนื้อเยื่อ retrobulbar เป็นหลัก การรักษาด้วยสเตียรอยด์ แบบ pulse และการฉายรังสีเป็นทางเลือกแรก การผ่าตัดลดเบ้าตา จะพิจารณาเฉพาะในกรณีฉุกเฉินที่มีภาวะ optic neuropathy จากการกดทับรุนแรง
ระยะไม่อักเสบ (ระยะเรื้อรัง) : การอักเสบสงบลง แต่ยังคงมีตาโปนคงที่ ความผิดปกติของการเคลื่อนไหวลูกตา และ optic neuropathy ระยะนี้เป็นระยะหลักสำหรับการผ่าตัดลดเบ้าตา
CAS (Clinical Activity Score) เป็นระบบการให้คะแนน 7 รายการเพื่อประเมินการอักเสบของ thyroid eye disease 1) คะแนน 3 จาก 7 รายการขึ้นไปถือเป็นระยะ active และเป็นข้อบ่งชี้ในการรักษาด้วยยา
การจำแนกความรุนแรงของ EUGOGO (European Group on Graves’ Orbitopathy) แบ่งเป็น 3 ระดับ: เล็กน้อย ปานกลางถึงรุนแรง และคุกคามการมองเห็น (sight-threatening) 8) ภาวะคุกคามการมองเห็น หมายถึง compressive optic neuropathy หรือ corneal ulcer ซึ่งต้องได้รับการแทรกแซงฉุกเฉิน
ตัวรับ TSH (TSHR) ที่มีอยู่ใน fibroblast ของเนื้อเยื่อ retrobulbar ในเบ้าตา ทำหน้าที่เป็นแอนติเจน กระตุ้นการแทรกซึมของลิมโฟไซต์เข้าไปในเนื้อเยื่อเบ้าตา กระตุ้นมาโครฟาจ และกระตุ้นปฏิกิริยาการอักเสบผ่านเครือข่ายไซโตไคน์เฉพาะที่ในตา ทำให้ปริมาตรของเนื้อหาในเบ้าตา เพิ่มขึ้น ส่งผลให้ตาโปน ความดันในเบ้าตา เพิ่มขึ้น และ compressive optic neuropathy
โรคตาจากต่อมไทรอยด์ เกิดขึ้นในผู้ป่วยโรคเกรฟส์ (โรคเบสโดว์) ร้อยละ 25-50 3) โรคเส้นประสาทตาถูกกดทับ ซึ่งคุกคามการมองเห็น เกิดขึ้นประมาณร้อยละ 3-5 ของผู้ป่วยทั้งหมด
กล้ามเนื้อเรกตัสด้านล่างและเรกตัสด้านในเป็นกล้ามเนื้อที่ได้รับผลกระทบบ่อยที่สุด การเกี่ยวข้องของกล้ามเนื้อนอกลูกตา พบมากที่สุดในเรกตัสด้านล่าง รองลงมาคือเรกตัสด้านใน เรกตัสด้านบน และเรกตัสด้านนอก ดังนั้นความผิดปกติในการเงยตาขึ้นจึงพบได้บ่อยที่สุด รองลงมาคือความผิดปกติในการกางตา
การสูบบุหรี่เป็นปัจจัยเสี่ยงที่สำคัญที่สุดของโรคตาจากต่อมไทรอยด์ สัมพันธ์กับความเสี่ยงในการเกิดโรค ความรุนแรง และการดื้อต่อการรักษา ในการศึกษาหลายศูนย์ในผู้ป่วย 633 ตาและ 386 ราย อัตราการสูบบุหรี่อยู่ระหว่างร้อยละ 16.2 ถึง 71.1 ในแต่ละศูนย์ แม้ว่าการสูบบุหรี่จะทำให้ความรุนแรงของโรคตาแย่ลง แต่ไม่มีผลอย่างมีนัยสำคัญต่อประสิทธิภาพในการลดตาโปนของการผ่าตัดลดความดันในเบ้าตา 4)
การวินิจฉัยจะได้รับการยืนยันเมื่อตรวจพบแอนติบอดีต่อตนเองที่เกี่ยวข้องกับต่อมไทรอยด์ชนิดใดชนิดหนึ่งเป็นบวก แอนติบอดีที่วัดได้แก่ แอนติบอดีต่อตัวรับ TSH (TRAb), แอนติบอดีกระตุ้นต่อมไทรอยด์ (TSAb), แอนติบอดีต่อไทโรโกลบูลิน (TgAb) และแอนติบอดีต่อไทรอยด์เปอร์ออกซิเดส (TPOAb) แม้ว่าการทำงานของต่อมไทรอยด์จะปกติ ก็ควรทำการตรวจหากมีอาการตาโปน หนังตาหด หรือเห็นภาพซ้อน
วัดระดับตาโปนด้วยเครื่องวัดตาโปน Hertel ค่าปกติในคนญี่ปุ่นคือ 10-15 มม. (เฉลี่ย 13 มม.) และค่าที่เกินกว่านั้นถือว่าตาโปน ความแตกต่างระหว่างตาทั้งสองข้างภายใน 2 มม. ถือว่าปกติ ใช้เป็นมาตรฐานในการประเมินก่อนและหลังการผ่าตัด
MRI (ตัวเลือกแรก) : ประเมินรูปร่างของกล้ามเนื้อนอกลูกตา ในภาพถ่วงน้ำหนัก T1 วิธี STIR (short-TI inversion recovery) แสดงบริเวณที่มีการอักเสบเป็นสัญญาณความเข้มสูง มีประโยชน์ในการประเมินกิจกรรมการอักเสบ ภาพตัดแนวโคโรนัลมีความจำเป็นเพื่อประเมินกล้ามเนื้อนอกลูกตา ทั้งหมดยกเว้นกล้ามเนื้อเฉียงล่างพร้อมกัน
CT : ยืนยันความหนาของกล้ามเนื้อนอกลูกตา (เอ็นหนาเล็กน้อยในขณะที่ท้องกล้ามเนื้อหนาขึ้น ทำให้มีรูปร่างคล้ายกระสวย) ใช้ CT หน้าต่างกระดูกเพื่อประเมินผนังเบ้าตา และวางแผนการผ่าตัด การวัดพื้นที่หน้าตัดของเบ้าตา (ในภาพตัดแนวโคโรนัลประมาณ 1.5 ซม. ด้านหน้ารอยแยกเบ้าตา ส่วนบน) ก่อนการผ่าตัดลดความดันใช้เพื่อทำนายการเปลี่ยนแปลงของตาโปนหลังผ่าตัด 4)
RAPD (ความบกพร่องของรูม่านตา ต่อ afferent แบบสัมพัทธ์) เป็นบวก, CFF (ความถี่ flicker วิกฤต) ลดลง, ความผิดปกติของการมองเห็นสี และความบกพร่องของลานสายตา เป็นสัญญาณเริ่มต้นของโรคเส้นประสาทตาถูกกดทับ หากยืนยันสัญญาณเหล่านี้ จำเป็นต้องได้รับการดูแลอย่างเร่งด่วน
การประเมินระยะอักเสบ
CAS (Clinical Activity Score) 1)
7 รายการ: ปวดหลังลูกตาขณะพัก, ปวดเมื่อกลอกตา, หนังตาลอก, เยื่อบุตา คั่ง, เยื่อบุตา บวม, ต่อมน้ำตาบวม, หนังตาบวม
CAS≥3/7 : ถือว่าอยู่ในระยะ active. บ่งชี้สำหรับการรักษาด้วยสเตียรอยด์ แบบ pulse
ภาพถ่าย : สัญญาณสูงในลำดับ STIR ของ MRI (ตัวบ่งชี้การอักเสบที่ active)
การประเมินระยะไม่อักเสบ
การประเมินตาโปน : Hertel exophthalmometer. ค่าปกติ 10-15 มม. (เฉลี่ย 13 มม.), ความแตกต่าง ≤2 มม.
การประเมินโรคเส้นประสาทตา : RAPD , CFF , การมองเห็น สี, ลานสายตา. ถ้าผลบวก ให้พิจารณาการแทรกแซงฉุกเฉิน
การประเมินตาเหล่ แบบคงที่ : การจำกัดการเคลื่อนไหวของลูกตา, มีภาพซ้อน . วางแผนผ่าตัดตาเหล่ หลังการผ่าตัดลดเบ้าตา
Q
CAS (Clinical Activity Score) คืออะไร?
A
เป็นระบบการให้คะแนน 7 รายการ (0-7 คะแนน) เพื่อประเมินการอักเสบที่ active ของโรคตาจากต่อมไทรอยด์ 1) เจ็ดรายการ: ① ปวดหลังลูกตาขณะพัก, ② ปวดเมื่อกลอกตา, ③ หนังตาลอก, ④ เยื่อบุตา คั่ง, ⑤ เยื่อบุตา บวม, ⑥ ต่อมน้ำตาบวม, ⑦ หนังตาบวม แต่ละรายการ 1 คะแนน คะแนน ≥3 ถือว่าอยู่ในระยะ active เป็นตัวบ่งชี้ทางคลินิกที่สำคัญในการระบุการอักเสบที่ active และการตัดสินใจรักษาด้วยสเตียรอยด์ แบบ pulse
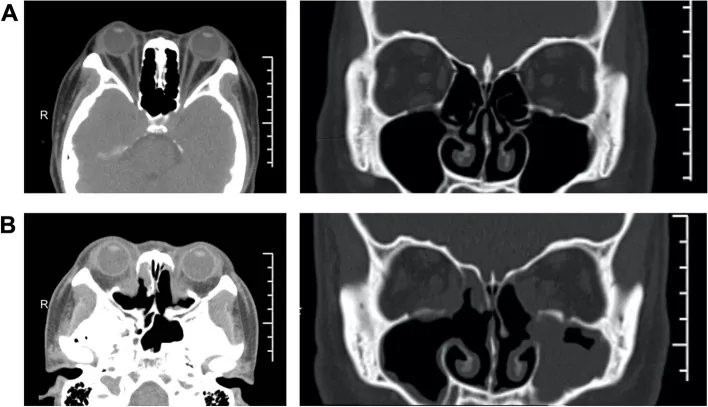
CT ก่อนและหลังผ่าตัดลดเบ้าตา: การเอาผนังด้านในออกและการหดกลับของลูกตา Ye Y, Hu F, Ji Y, et al. The outcomes of endoscopic orbital decompression combined with fat decompression for thyroid-associated ophthalmopathy. BMC Ophthalmol. 2023;23:217. Figure 5. PM
CI D: PMC10186627. DOI: 10.1186/s12886-023-02957-7. License: CC BY 4.0.
CT ตามแนวแกนของผู้ป่วยโรคตาจากต่อมไทรอยด์ ก่อนผ่าตัด (A) แสดงตาโปนทั้งสองข้างและความแออัดของปลายเบ้าตา โดยผนังด้านในยังคงอยู่ หลังผ่าตัด (B) แสดงการหายไปของผนังด้านในส่วนหลังพร้อมกับการขยายช่องเบ้าตา และการหดกลับของตาโปนอย่างชัดเจน สอดคล้องกับการขยายปริมาตรเบ้าตา โดยการลดเบ้าตา ทางกระดูก (การเอาผนังด้านในออก) ที่กล่าวถึงในหัวข้อ “5. การรักษามาตรฐาน”
หากมีภาวะต่อมไทรอยด์ทำงานเกิน การทำให้ฮอร์โมนไทรอยด์กลับสู่ปกติเป็นข้อกำหนดเบื้องต้นที่จำเป็น และต้องมีการประสานงานอย่างใกล้ชิดกับแผนกต่อมไร้ท่อ การผ่าตัดจะวางแผนหลังจากเข้าสู่ระยะคงที่ (ระยะไม่มีการอักเสบ) ของเส้นโค้ง Rundle และการอักเสบสงบลง ลำดับการทำคือ การผ่าตัดลดความดันในเบ้าตา → การผ่าตัดตาเหล่ → การผ่าตัดเปลือกตา และต้องปฏิบัติตามลำดับนี้อย่างเคร่งครัดเนื่องจากผลของการผ่าตัดก่อนหน้าส่งผลโดยตรงต่อแผนการผ่าตัดครั้งต่อไป
การให้สเตียรอยด์ แบบพัลส์ (ทางเลือกแรก) : Methylprednisolone 500-1000 มก./วัน เป็นเวลา 3 วันเป็นหนึ่งคอร์ส หลังจาก 2-3 คอร์ส ห่างกัน 1 สัปดาห์ตามอาการ ให้ลดขนาดยาลงทีละน้อยโดยการให้ทางหลอดเลือดดำหรือรับประทาน
การฉีดสเตียรอยด์ เฉพาะที่ : ฉีดสเตียรอยด์ ใต้แคปซูลเทนอนรอบกล้ามเนื้อนอกลูกตา ที่โต สำหรับภาวะหนังตาบนหดตัวเนื่องจากบวมน้ำและอักเสบ การฉีด triamcinolone acetonide (Kenacort-A® 1 หลอด) เฉพาะที่มีประสิทธิภาพ
การฉายรังสี : บ่งชี้เมื่อไม่สามารถรักษาด้วยสเตียรอยด์ ได้หรือเมื่อเกิดการกลับเป็นซ้ำ ฉายรังสีเนื้อเยื่อหลังลูกตาด้วยขนาด 1.5-2.0 Gy/วัน เป็นเวลา 10 วัน
Teprotumumab (แอนติบอดีต่อ IGF-1R) : ยาชีวภาพที่แสดงให้เห็นการปรับปรุงอย่างมีนัยสำคัญของภาวะตายื่นในต่างประเทศ 5) ยับยั้งตัวรับ IGF-1 และยับยั้งการกระตุ้นไฟโบรบลาสต์ในเบ้าตา ปัจจุบันยังไม่ได้รับการอนุมัติในญี่ปุ่นและถือเป็นทางเลือกในการรักษาในขั้นตอนการวิจัย
จำแนกออกเป็น 5 เทคนิคหลักโดยพิจารณาจากการผสมผสานระหว่างการตัดผนังเบ้าตา และการกำจัดไขมัน ต่อไปนี้คือปริมาณการลดตายื่นตามเทคนิคจากการศึกษาแบบหลายศูนย์ใน 633 ตา (ศัลยแพทย์ 7 คน) 4)
เทคนิค จำนวนผนัง ปริมาณการลดตายื่น (เฉลี่ย) ผนังด้านในเท่านั้น 1 ผนัง 1.4-2.3 มม. ไขมัน + ผนังด้านข้าง 2 ผนัง 2.9-3.6 มม. ผนังด้านใน + ผนังด้านล่าง 2 ผนัง 2.6–3.7 มม. ไขมัน + ผนังด้านนอก + ผนังด้านใน 3 ผนัง 3.1–3.9 มม. ไขมัน + ผนังด้านนอก + ผนังด้านใน + ผนังด้านล่าง 3 ผนัง + ไขมัน 4.6–5.0 มม. (ผลสูงสุด)
ปริมาณการลดการโปนของลูกตาเพิ่มขึ้นตามจำนวนผนังที่เพิ่มขึ้น การลดการกดแบบเป็นขั้น (graded decompression) ตามความรุนแรงเป็นหลักการพื้นฐานในการเลือกเทคนิค2) 6) และเทคนิคยังถูกกำหนดโดยวัตถุประสงค์เพื่อความสวยงามหรือเพื่อปกป้องเส้นประสาทตา มีการแสดงให้เห็นทางสถิติว่าผู้ป่วยที่มีการโปนของลูกตาก่อนผ่าตัดมากกว่าจะมีการปรับปรุงหลังผ่าตัดมากกว่า (p<0.001)4)
ลำดับ การผ่าตัด ระยะเวลา 1 การลดความดันในเบ้าตา ระยะที่ไม่มีการอักเสบ (อาจทำเร่งด่วนในกรณีเส้นประสาทตา ถูกกดทับ) 2 การผ่าตัดตาเหล่ หลังจากตาเหล่ คงที่หลังการผ่าตัดลดความดันในเบ้าตา 3 การผ่าตัดเปลือกตา ทำเป็นลำดับสุดท้าย
การผ่าตัดตาเหล่ : ส่วนใหญ่ทำโดยการเลื่อนกล้ามเนื้อเรกตัสที่หนาตัวกลับในตาเหล่ ที่คงที่ในระยะเรื้อรัง อาจเกิดภาพซ้อน ใหม่หลังการผ่าตัดลดความดันในเบ้าตา และวางแผนการผ่าตัดหลังจากตาเหล่ คงที่
การผ่าตัดเปลือกตา : สำหรับเปลือกตาหดตัวจากการอักเสบ ฉีด triamcinolone acetonide เฉพาะที่ สำหรับเปลือกตาหดตัวคงที่ในระยะไม่อักเสบที่สงบ ทำการผ่าตัดแก้ไขการหดตัว (ตัดกล้ามเนื้อมึลเลอร์หรือเลื่อนกล้ามเนื้อลืมตาบนกลับ)
ภาวะแทรกซ้อนของการผ่าตัดลดความดันในเบ้าตา : ระวังการเกิดภาพซ้อน ใหม่หลังผ่าตัด หากเกิดภาพซ้อน ใหม่ ให้จัดการภายหลังด้วยการผ่าตัดตาเหล่ (เลื่อนกล้ามเนื้อเรกตัสที่หนาตัวกลับ) ต้องปฏิบัติตามลำดับการผ่าตัดอย่างเคร่งครัด (ลดความดันในเบ้าตา → ผ่าตัดตาเหล่ → ผ่าตัดเปลือกตา)
ข้อห้ามในการผ่าตัดในระยะอักเสบ : การผ่าตัดลดความดันในเบ้าตา เพื่อความสวยงามในระยะอักเสบเพิ่มความเสี่ยงต่อการเปลี่ยนแปลงหลังผ่าตัดและการกลับเป็นซ้ำ ยกเว้นกรณีฉุกเฉินของโรคเส้นประสาทตาถูกกดทับ ควรวางแผนผ่าตัดหลังจากอาการอักเสบสงบลง
ข้อควรระวังในการรักษาด้วยสเตียรอยด์ : เพิ่มการจัดการทางการแพทย์ในผู้ป่วยเบาหวาน กระดูกพรุน ความดันโลหิตสูง แนะนำให้ขนาดยาสะสมไม่เกิน 8 กรัม
Q
การผ่าตัดลดความดันในเบ้าตาช่วยลดตาโปนได้มากแค่ไหน?
A
แตกต่างกันตามเทคนิคการผ่าตัด การลดความดันผนังเดียว (เฉพาะผนังด้านใน) คาดว่าลดตาโปนได้ 1.4–2.3 มม. และการลดความดันสามผนังร่วมกับการตัดไขมัน (เทคนิคสูงสุด) ลดได้ 4.6–5.0 มม.4) ผลเพิ่มขึ้นตามจำนวนผนังที่เพิ่มขึ้น และยิ่งตาโปนก่อนผ่าตัดมาก การดีขึ้นหลังผ่าตัดก็ยิ่งมาก แนะนำให้ลดความดันแบบเป็นขั้นตามความรุนแรง (graded decompression)6) .
ตัวรับ TSH ที่มีอยู่ในไฟโบรบลาสต์ของเนื้อเยื่อเรโทรบัลบาร์ภายในเบ้าตา ทำหน้าที่เป็นแอนติเจน กระตุ้นให้เกิดการแทรกซึมของลิมโฟไซต์เข้าไปในเนื้อเยื่อเบ้าตา กระตุ้นมาโครฟาจ และกระตุ้นปฏิกิริยาการอักเสบผ่านเครือข่ายไซโตไคน์เฉพาะที่ในดวงตา มีการผลิตไซโตไคน์ที่ก่อให้เกิดการอักเสบ (IL-1, IL-6, TNF -ɑ) และปริมาตรของเนื้อหาในเบ้าตา เพิ่มขึ้น
การเปลี่ยนแปลงของเนื้อเยื่อไขมัน : เกิดการขยายขนาดของเซลล์ไขมันและการแทรกซึมของลิมโฟไซต์ในเนื้อเยื่อคั่นระหว่างหน้า ร่วมกับอาการบวมน้ำและการเกิดแผลเป็นจากการอักเสบเรื้อรัง การสังเคราะห์ไกลโคซามิโนไกลแคน (GAG) และกรดไฮยาลูโรนิกที่เพิ่มขึ้นทำให้เกิดการกักเก็บของเหลวและเนื้อเยื่อบวม
การเปลี่ยนแปลงของกล้ามเนื้อนอกลูกตา : พบการแทรกซึมของเซลล์อักเสบที่นำโดยลิมโฟไซต์ระหว่างเส้นใยกล้ามเนื้อลาย ทำให้เส้นใยกล้ามเนื้อเสื่อมและตาย เกิดอาการบวมน้ำและหนาตัวขึ้นในเนื้อเยื่อคั่นระหว่างหน้าจากการอักเสบ และมีเนื้อเยื่อเกี่ยวพันเพิ่มขึ้นระหว่างเส้นใยกล้ามเนื้อ ทำให้เกิดการโตเกินของกล้ามเนื้อนอกลูกตา ใน CT/MRI เส้นเอ็นหนาขึ้นเล็กน้อยและท้องกล้ามเนื้อโตขึ้น ทำให้โดยรวมมีรูปร่างคล้ายกระสวย
ความดันภายในเบ้าตา ที่เพิ่มขึ้นจากการเพิ่มขึ้นของปริมาตรเนื้อหาในเบ้าตา และการโตเกินของกล้ามเนื้อนอกลูกตา ไปกดทับเส้นประสาทตา ที่ปลายเบ้าตา (orbital apex) RAPD เป็นบวก CFF ลดลง และความบกพร่องของลานสายตา เป็นสัญญาณ กลไกนี้เป็นพื้นฐานสำหรับการคลายการกดทับเส้นประสาทตา โดยการผ่าตัดลดความดันเบ้าตา (การขยายปริมาตรเบ้าตา )
ตัวรับ IGF-1 (IGF-1R) สร้างสารเชิงซ้อนกับ TSHR บนไฟโบรบลาสต์เบ้าตา และมีส่วนร่วมแบบเสริมฤทธิ์ในการกระตุ้นไฟโบรบลาสต์เบ้าตา 5) การปิดกั้นสัญญาณของสารเชิงซ้อนนี้เป็นกลไกการออกฤทธิ์ของเทโปรทูมูแมบ และเป็นพื้นฐานทางทฤษฎีสำหรับผลการรักษาในการปรับปรุงภาวะตายื่นในต่างประเทศ
โดยการเอาผนังเบ้าตา ออก ผนังกั้นกระดูกระหว่างเบ้าตา และโพรงอากาศข้างจมูก (เอทมอยด์ แม็กซิลลารี สฟีนอยด์) จะหายไป และไขมันภายในเบ้าตา จะยื่นออกไปทางโพรงอากาศ ทำให้ปริมาตรเบ้าตา ขยายใหญ่ขึ้น ซึ่งจะลดความดันภายในเบ้าตา และเคลื่อนลูกตาไปด้านหลัง การตัดไขมันร่วมด้วยสามารถเพิ่มประสิทธิภาพในการลดความดันได้มากขึ้น
เนื้อหาต่อไปนี้รวมถึงข้อมูลที่อยู่ในขั้นตอนการวิจัยหรือยังไม่ได้รับการอนุมัติบางส่วน ในการรักษาจริง ให้ปฏิบัติตามคำแนะนำของแพทย์ผู้รักษา
ในการศึกษาย้อนหลังแบบหลายศูนย์โดย Hong et al. (2025) ใน 7 สถาบัน ศัลยแพทย์ 7 คน และ 633 ตา ยืนยันว่าไม่มีความแตกต่างอย่างมีนัยสำคัญในปริมาณการลดลงของภาวะตายื่นระหว่างศัลยแพทย์เมื่อทำเทคนิคการผ่าตัดเดียวกัน 4) (ค่าความคลาดเคลื่อนมาตรฐาน 0.14–0.56 มม.) ความสามารถในการทำซ้ำของเทคนิคการผ่าตัดที่ได้มาตรฐานในระดับหลายศูนย์เป็นข้อค้นพบที่สำคัญซึ่งสนับสนุนความถูกต้องทางสถิติของ RCT แบบหลายศูนย์
นอกจากนี้ ยังพบว่าระดับของตาโปนก่อนผ่าตัดเป็นปัจจัยที่มีนัยสำคัญที่สุดในการทำนายการเปลี่ยนแปลงของตาโปนหลังผ่าตัด (p<0.001) ซึ่งเป็นการย้ำถึงความสำคัญของการประเมินก่อนผ่าตัด4)
ในการศึกษาเดียวกันนี้ ได้ตรวจสอบผลของวิธีการผ่าตัดตามประเภทของหัตถการด้วย ในการลดแรงกดผนังด้านใน + ผนังด้านล่าง กลุ่มที่ใช้กล้องส่องแสดงการลดลงของตาโปนอย่างมีนัยสำคัญมากกว่าการผ่าตัดแบบเปิด (-3.67 มม. เทียบกับ -2.97 มม., p=0.008) ในขณะที่การลดแรงกดไขมัน + ผนังด้านข้าง + ผนังด้านใน ไม่มีความแตกต่างอย่างมีนัยสำคัญระหว่างการส่องกล้องและการผ่าตัดแบบเปิด4)
Teprotumumab (แอนติบอดีต่อ IGF-1R) เป็นยาชีวภาพที่มีรายงานว่าช่วยปรับปรุงอาการตาโปนได้อย่างมีนัยสำคัญในต่างประเทศ5) ปัจจุบันยังไม่ได้รับการอนุมัติในญี่ปุ่น แต่ในระดับสากลถูกจัดให้เป็นการรักษาด้วยยาสำหรับโรคตาต่อมไทรอยด์ระยะ active ระดับปานกลางถึงรุนแรง ความปลอดภัยในระยะยาว (ความบกพร่องทางการได้ยิน ระดับน้ำตาลในเลือดสูง ฯลฯ) เป็นที่จับตามองจากผลการทดลองระยะที่ 4
ได้มีการพัฒนาแบบจำลองเพื่อทำนายการเกิดภาพซ้อน ใหม่หลังการผ่าตัดลดแรงกด7) และคาดว่าจะนำไปใช้ในการให้คำปรึกษาก่อนผ่าตัดและการเลือกวิธีการผ่าตัด
การสูบบุหรี่เป็นปัจจัยเสี่ยงที่ใหญ่ที่สุดที่ทำให้ความรุนแรงของโรคตาต่อมไทรอยด์แย่ลง แต่ในการศึกษา 633 ตา การสูบบุหรี่ไม่มีผลอย่างมีนัยสำคัญต่อประสิทธิภาพในการลดตาโปนจากการผ่าตัดลดแรงกด4) บทบาทของการสูบบุหรี่ในการทำนายประสิทธิภาพการรักษากำลังถูกปรับให้ละเอียดขึ้น
Mourits MP, Prummel MF, Wiersinga WM, et al. Clinical activity score as a guide in the management of patients with Graves’ ophthalmopathy. Clin Endocrinol (Oxf). 1997;47:9-14.
Mourits MP, Bijl H, Altea MA, et al; European Group on Graves’ Orbitopathy (EUGOGO). Outcome of orbital decompression for disfiguring proptosis in patients with Graves’ orbitopathy using various surgical procedures. Br J Ophthalmol. 2009;93:1518-1523.
Bahn RS, Heufelder AE. Pathogenesis of Graves’ ophthalmopathy. N Engl J Med. 1993;329:1468-1475.
Hong A, Shoji MK, Villatoro GA, et al. Intersurgeon variability in proptosis reduction after orbital decompression for thyroid eye disease: a multicenter analysis. Ophthalmic Plast Reconstr Surg. 2025. [Epub ahead of print].
Rootman DB. Orbital decompression for thyroid eye disease. Surv Ophthalmol. 2018;63:86-104.
Kikkawa DO, Pornpanich K, Cruz RC Jr, Levi L, Granet DB. Graded orbital decompression based on severity of proptosis. Ophthalmology. 2002;109(7):1219-1224. doi:10.1016/S0161-6420(02)01068-0.
Nair AA, Ediriwickrema LS, Dolman PJ, et al. Predictive modeling of new-onset postoperative diplopia following orbital decompression for thyroid eye disease. Ophthalmic Plast Reconstr Surg. 2022;38(6):551-557. PMID:35551414. doi:10.1097/IOP .0000000000002196.
Bartalena L, Kahaly GJ, Baldeschi L, Dayan CM, Eckstein A, Marcocci C, et al; EUGOGO. The 2021 European Group on Graves’ orbitopathy (EUGOGO) clinical practice guidelines for the medical management of Graves’ orbitopathy. Eur J Endocrinol. 2021;185(4):G43-G67. PMID:34297684. doi:10.1530/EJE-21-0479.