โรคตาจากต่อมไทรอยด์ เป็นโรคภูมิคุ้มกันทำลายตนเองของเบ้าตา ที่เกิดจากแอนติบอดีต่อตัวรับ TSH พบร่วมในผู้ป่วยโรคเกรฟส์ร้อยละ 25-50อาจเกิดเป็นโรคตาจากต่อมไทรอยด์ ที่การทำงานของต่อมไทรอยด์ปกติได้เช่นกัน
อาการทางคลินิกแบ่งออกเป็น 4 กลุ่ม ได้แก่ อาการของเปลือกตา ตาโปน ตาเห็นภาพซ้อน และความบกพร่องทางการมองเห็น
กล้ามเนื้อเรกตัสล่างและเรกตัสด้านในมักได้รับผลกระทบ ทำให้เกิดตาเหล่ แนวตั้งและตาเหล่เข้า
ในระยะลุกลาม การรักษาด้วยสเตียรอยด์แบบพัลส์ (เมทิลเพรดนิโซโลน) เป็นทางเลือกแรก
โดยหลักการแล้ว การผ่าตัดจะทำในระยะสงบ ตามลำดับ: ผ่าตัดลดความดันในเบ้าตา → ผ่าตัดแก้ตาเหล่ → ผ่าตัดเปลือกตา
โรคเส้นประสาทตาถูกกดทับ เป็นข้อบ่งชี้ฉุกเฉินสำหรับการผ่าตัดลดความดันในเบ้าตา โรคตาจากต่อมไทรอยด์ (TED) เป็นโรคภูมิคุ้มกันทำลายตนเองของเบ้าตา ที่เกิดจากปฏิกิริยาของแอนติบอดีตนเองที่เกี่ยวข้องกับต่อมไทรอยด์ต่อเนื้อเยื่อในเบ้าตา เรียกอีกชื่อว่า โรคตาที่สัมพันธ์กับต่อมไทรอยด์ (TAO ) หรือ โรคตาเกรฟส์ (GO)
โรคตาอาจเกิดขึ้นร่วมกับภาวะต่อมไทรอยด์ทำงานเกิน (โรคเกรฟส์) หรือเป็นโรคตาจากต่อมไทรอยด์ ที่การทำงานของต่อมไทรอยด์ปกติโดยสมบูรณ์ โรคตาจากต่อมไทรอยด์ โดยพื้นฐานแล้วดำเนินไปโดยอิสระจากฮอร์โมนไทรอยด์ และเป็นหนึ่งในโรคภูมิต้านตนเองที่เกี่ยวข้องกับแอนติบอดีต่อตนเองที่เกี่ยวข้องกับต่อมไทรอยด์
ความชุกของโรคตาจากต่อมไทรอยด์ รายงานที่ 16 ต่อผู้หญิง 100,000 คนต่อปี และ 2.9 ต่อผู้ชาย 100,000 คนต่อปี 6) ผู้ป่วยโรคเกรฟส์ประมาณ 25-50% มีโรคตาร่วมด้วย 5) อายุที่เริ่มมีอาการแสดงการกระจายแบบสองยอดที่ 40-50 ปี และ 60-70 ปี 6) การสูบบุหรี่เป็นปัจจัยเสี่ยงหลักสำหรับการเริ่มต้นและความรุนแรง 12) และการเลิกบุหรี่เป็นพื้นฐานของการรักษา
โรคฮาชิโมโตะ (ต่อมไทรอยด์อักเสบเรื้อรัง) อาจทำให้เกิดอาการทางตาได้เช่นกัน แต่มักแสดงเป็นโรคตาจากต่อมไทรอยด์ ที่การทำงานปกติ กลไกที่แอนติบอดีต่อตนเองที่เกี่ยวข้องกับต่อมไทรอยด์ (anti-TPO, anti-TG) ส่งผลต่อเนื้อเยื่อเบ้าตา มีความคล้ายคลึงกับโรคตาจากเกรฟส์
แนวทาง EUGOGO 2021 1) จำแนกโรคตาจากต่อมไทรอยด์ ออกเป็นสามระยะดังนี้:
ความรุนแรง ลักษณะสำคัญ แผนการรักษา เล็กน้อย เปลือกตาบวม, เปลือกตาหดรั้ง, ตาโปนเล็กน้อย (<3 มม.), ไม่มีภาพซ้อน สังเกตอาการ, รักษาตามอาการ, เสริมซีลีเนียม ปานกลางถึงรุนแรง ตาโปน (≥3 มม.), ภาพซ้อน (เป็นระยะหรือต่อเนื่อง), เปลือกตาหดรั้ง (≥2 มม.), ความเสียหายของกระจกตา การรักษาด้วยสเตียรอยด์แบบพัลส์ , การฉายรังสีเบ้าตา โรคตาจากต่อมไทรอยด์ ที่คุกคามการมองเห็น (DON)โรคเส้นประสาทตาถูกกดทับ หรือกระจกตา เสียหายรุนแรงการผ่าตัดเบ้าตา ฉุกเฉิน / สเตียรอยด์
Q
อาการทางตาสามารถเกิดขึ้นได้แม้ค่าระดับไทรอยด์ปกติหรือไม่?
A
ได้ ภาวะที่เรียกว่า euthyroid ophthalmopathy คือโรคตาที่เกิดขึ้นแม้การทำงานของต่อมไทรอยด์ปกติ เนื่องจากแอนติบอดีที่เกี่ยวข้องกับต่อมไทรอยด์ออกฤทธิ์โดยตรงต่อเนื้อเยื่อในเบ้าตา อาการทางตาจึงปรากฏโดยไม่ขึ้นกับระดับฮอร์โมนไทรอยด์ การวินิจฉัยโรคตาจากต่อมไทรอยด์ ต้องตรวจแอนติบอดีในเลือดและการถ่ายภาพเบ้าตา เป็นสิ่งสำคัญ
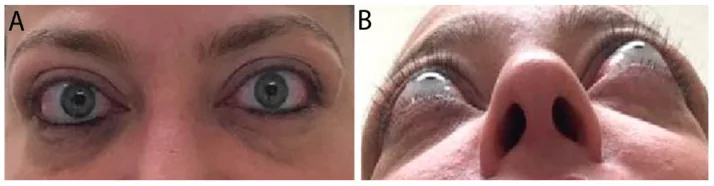
โรคตาจากต่อมไทรอยด์: ภาพสีของตาส่วนนอกแสดงหนังตาบนและล่างหดรั้งและตาโปน Rashad R, Pinto R, Li E, Sohrab M, Distefano AG. Thyroid Eye Disease. Life (Basel). 2022;12(12):2084. Figure 2. PM
CI D: PMC9787503. License: CC BY 4.0.
ภาพสีของตาส่วนนอกของผู้ป่วยโรคตาจากต่อมไทรอยด์ เรื้อรังระดับปานกลาง (A) แสดงหนังตาบนและล่างหดรั้ง ปีกหนังตาบนด้านข้าง และไขมันรอบเบ้าตา โปนระดับปานกลาง และ (B) ในมุมเงยคาง (worm’s eye view) จะเห็นตาโปนทั้งสองข้างชัดเจน ซึ่งสอดคล้องกับหนังตาหดรั้ง และตาโปนที่กล่าวถึงในหัวข้อ “2. อาการหลักและผลการตรวจทางคลินิก”
อาการทางคลินิกโดยทั่วไปแบ่งเป็น 4 กลุ่ม ได้แก่ อาการทางหนังตา ตาโปน เห็นภาพซ้อน และความบกพร่องทางการมองเห็น ตาโปนพบได้บ่อยในผู้ป่วยอายุน้อย ส่วนความผิดปกติของการเคลื่อนไหวตาและเห็นภาพซ้อน พบได้บ่อยในผู้สูงอายุ
อาการทางหนังตา
หนังตาบนหดรั้ง : อาการที่พบบ่อยที่สุด เกิดจากความตื่นตัวของระบบประสาทซิมพาเทติกต่อกล้ามเนื้อมึลเลอร์หรือพังผืดของกล้ามเนื้อลิเวเตอร์
หนังตาตก ค้าง (lid lag)
หนังตาบวม : บวมเนื่องจากหนังตาบวมน้ำหรือไขมันเจริญเกิน ในกรณีที่มีการอักเสบ การฉีดสเตียรอยด์ เฉพาะที่ได้ผลดี
ตาโปน
วัดด้วยเครื่อง Hertel exophthalmometer ค่าปกติน้อยกว่า 18 มม. และในผู้ป่วยโรคตาจากต่อมไทรอยด์ มักเกิน 21 มม.
การเพิ่มขึ้นของเนื้อเยื่อไขมันในเบ้าตา และการโตของกล้ามเนื้อนอกลูกตา ทำให้ลูกตาถูกดันไปข้างหน้า
ความแตกต่างระหว่างสองข้าง (≥2 มม.) เป็นข้อบ่งชี้ในการวินิจฉัย
ภาพซ้อนและความผิดปกติของการเคลื่อนไหวลูกตา
กล้ามเนื้อเรกตัสล่างและเรกตัสด้านใน มักได้รับผลกระทบ ทำให้เกิดตาเหล่ แนวตั้งและตาเหล่เข้า ได้ง่าย
การเปลี่ยนแปลงแบบหดตัวของกล้ามเนื้อนอกลูกตา (โดยคงจุดเกาะเอ็นไว้) เป็นลักษณะเฉพาะ และสามารถยืนยันได้ด้วย CT
การผ่าตัดตาเหล่ โดยหลักจะทำในระยะที่ไม่มีการอักเสบ
ความผิดปกติทางการมองเห็น
ความผิดปกติของกระจกตา : การมองเห็น ลดลงจากตาแห้ง และกระจกตา อักเสบจากการเปิดรับ
โรคเส้นประสาทตาถูกกดทับ (DON)เบ้าตา ที่เพิ่มขึ้นจากกล้ามเนื้อนอกลูกตา ที่โตขึ้นกดทับเส้นประสาทตา เกิดในผู้ป่วยประมาณ 5%5) และต้องได้รับการแทรกแซงฉุกเฉิน
การมองเห็น ลดลงอย่างรวดเร็ว ความผิดปกติของการมองเห็นสี และข้อบกพร่องของลานสายตาเป็นสัญญาณเตือน
ในระยะแรก อาจมีอาการคล้ายตาแห้ง เช่น ตาแห้ง ระคายเคือง น้ำตาไหล และกลัวแสง ต่อมา เปลือกตาบวม ตาโปน และภาพซ้อน ปรากฏชัด เมื่อรุนแรงขึ้น จะเกิดกระจกตา เปิดรับหรือโรคเส้นประสาทตาถูกกดทับ ซึ่งต้องได้รับการรักษาอย่างเร่งด่วน
ดังที่เส้นโค้ง Rundle14) แสดง โรคตาจากต่อมไทรอยด์ ดำเนินเป็นสองระยะ: ระยะ active (อักเสบ) และระยะ inactive (พังผืด/คงที่) ระยะ active มักกินเวลา 1-3 ปี จากนั้นจะคงที่เอง แต่การควบคุมการอักเสบตั้งแต่เนิ่นๆ ด้วยการรักษาที่เหมาะสมเป็นสิ่งสำคัญ
Q
ตาโปนเกี่ยวข้องกับต่อมไทรอยด์หรือไม่?
A
ตาโปนเป็นหนึ่งในอาการหลักของโรคตาจากต่อมไทรอยด์ เกิดจากเนื้อเยื่อไขมันและกล้ามเนื้อนอกลูกตา ในเบ้าตา ขยายใหญ่ขึ้น ดันลูกตาไปข้างหน้า โดยเฉพาะในผู้ป่วยโรคเกรฟส์ หากสังเกตเห็นตาโปน ควรได้รับการประเมินทางจักษุวิทยาทันที วัดด้วย Hertel exophthalmometer และตรวจสภาพเบ้าตา ด้วย CT หรือ MRI
ไฟโบรบลาสต์ในเนื้อเยื่อเรโทรบัลบาร์ของเบ้าตา มีการแสดงออกของตัวรับ TSH ตัวรับ TSH เหล่านี้ทำหน้าที่เป็นแอนติเจนที่กระตุ้นให้ลิมโฟไซต์แทรกซึมเข้าไปในเนื้อเยื่อเบ้าตา กระตุ้นมาโครฟาจ และกระตุ้นการตอบสนองการอักเสบผ่านเครือข่ายไซโตไคน์เฉพาะที่ในดวงตา
การแทรกซึมของเซลล์ภูมิคุ้มกัน (ส่วนใหญ่เป็นเซลล์ T CD4+/CD8+) เข้าสู่เนื้อเยื่อเบ้าตา เป็นตัวกระตุ้นให้เกิดลำดับเหตุการณ์ดังต่อไปนี้ 8) 16) :
แอนติบอดีต่อตัวรับ TSH → การกระตุ้นไฟโบรบลาสต์ในเบ้าตา
การปล่อยไซโตไคน์ที่ก่อให้เกิดการอักเสบ (TNF -α, IL-6, IL-1β)
การสังเคราะห์ไกลโคซามิโนไกลแคน (กรดไฮยาลูโรนิก) มากเกินไป → เนื้อเยื่อบวมน้ำ
การเปลี่ยนแปลงของไฟโบรบลาสต์เป็นเซลล์ไขมันและไมโอไฟโบรบลาสต์ → การขยายตัวของไขมันในเบ้าตา และพังผืดของกล้ามเนื้อนอกลูกตา
ความดันภายในเบ้าตา เพิ่มขึ้น → ตาโปนและการกดทับเส้นประสาทตา
เป็นที่ทราบกันว่าตัวรับ IGF-1 (IGF-1R) และตัวรับ TSH ก่อตัวเป็นสารเชิงซ้อนของตัวรับที่ขยายสัญญาณ 4) และนี่คือเป้าหมายการรักษาของยาเทโปรตูมูแมบที่จะกล่าวถึงในภายหลัง
การสูบบุหรี่ : ปัจจัยปรับเปลี่ยนที่รุนแรงที่สุด เพิ่มความเสี่ยงในการเกิดโรคตาต่อมไทรอยด์ ความเสี่ยงในการดำเนินโรค และการดื้อต่อการรักษาอย่างมีนัยสำคัญ 12) การเลิกสูบบุหรี่ช่วยเพิ่มประสิทธิภาพการรักษาโดยตรงการรักษาด้วยไอโอดีนกัมมันตรังสี (RAI) : โดยเฉพาะอย่างยิ่งเมื่อทำโดยไม่มีการครอบคลุมด้วยสเตียรอยด์ จะเพิ่มความเสี่ยงต่อการแย่ลงของโรคตา 1) ความไม่เสถียรของการทำงานของต่อมไทรอยด์ (ความผันผวนอย่างรุนแรงระหว่างภาวะไทรอยด์ต่ำและไทรอยด์เป็นพิษ)อายุมาก และเพศชาย (มีแนวโน้มที่จะรุนแรงกว่า)ระดับแอนติบอดีต่อตัวรับฮอร์โมนกระตุ้นต่อมไทรอยด์ (TRAb) สูง
Q
การสูบบุหรี่ส่งผลต่อโรคตาจากต่อมไทรอยด์อย่างไร?
A
การสูบบุหรี่เป็นปัจจัยเสี่ยงที่รุนแรงที่สุดของโรคตาจากต่อมไทรอยด์ การสูบบุหรี่เพิ่มความเสี่ยงในการเกิดโรคและความรุนแรงของโรค และลดประสิทธิภาพของการรักษาเช่นสเตียรอยด์ ความเสี่ยงที่โรคจะแย่ลงหลังการรักษาด้วยไอโอดีนกัมมันตรังสีก็สูงขึ้นในผู้สูบบุหรี่ การเลิกบุหรี่ช่วยให้การรักษามีประสิทธิภาพดีขึ้น ดังนั้นการแนะนำให้ผู้ป่วยเลิกบุหรี่จึงเป็นส่วนสำคัญของการรักษา
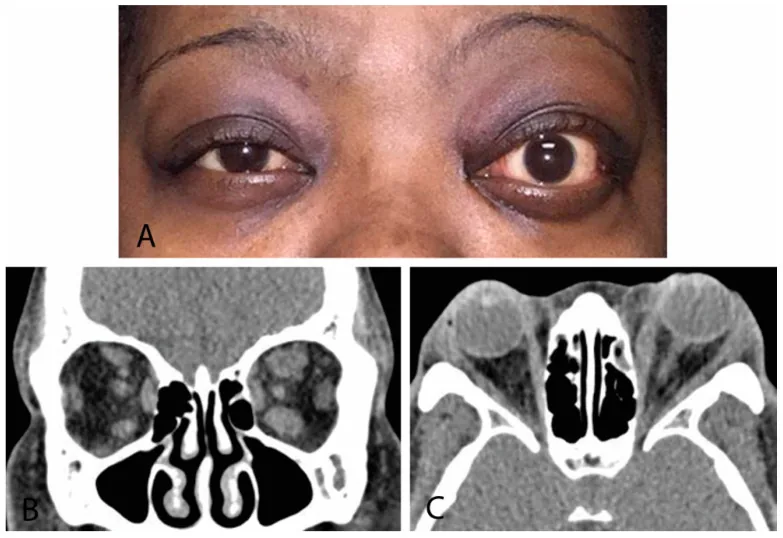
ภาพ CT แนวโคโรนาของเบ้าตาในโรคตาจากต่อมไทรอยด์: กล้ามเนื้อนอกลูกตาหนาตัว (เด่นข้างซ้าย) Rashad R, Pinto R, Li E, Sohrab M, Distefano AG. Thyroid Eye Disease. Life (Basel). 2022;12(12):2084. Figure 4. PM
CI D: PMC9787503. License: CC BY 4.0.
(A) ภาพถ่ายภายนอกตาที่แสดงภาวะตายื่นไม่สมมาตรเด่นข้างซ้าย (B) ภาพ CT แนวโคโรนาของเบ้าตา แสดงการหนาตัวของกลุ่มกล้ามเนื้อเรกตัสเด่นข้างซ้าย (แบบกล้ามเนื้อท้องโตแต่เอ็นยึดปกติ) (C) ภาพ CT แนวทัลของผู้ป่วยรายเดียวกัน การพบว่าเอ็นยึดของกล้ามเนื้อเรกตัสยังปกติเป็นสิ่งสำคัญในการแยกโรคจากโรคที่เกี่ยวข้องกับ IgG4 และกล้ามเนื้อเบ้าตา อักเสบ ซึ่งสอดคล้องกับการประเมินกล้ามเนื้อนอกลูกตา หนาตัวด้วย CT ในหัวข้อ “4. การวินิจฉัยและวิธีการตรวจ”
การวินิจฉัยทางคลินิกเป็นพื้นฐาน การวินิจฉัยเกิดจาการมีหนังตาหดร่น ตายื่น เห็นภาพซ้อน ร่วมกับประวัติโรคต่อมไทรอยด์ ข้อควรระวังสำคัญ: เพื่อการวินิจฉัยโรคตาจากต่อมไทรอยด์ อย่างแน่ชัด ต้องมีความสัมพันธ์ระหว่างกล้ามเนื้อนอกลูกตา หนาตัว/อักเสบ กับการจำกัดการเคลื่อนไหวของตาและตำแหน่งตา
การทำงานของต่อมไทรอยด์ : Free T4, Free T3, TSHแอนติบอดีต่อตัวรับ TSH (TRAb, TSAb) : สูงในโรคเกรฟส์ สัมพันธ์กับกิจกรรมของโรคตาแอนติบอดีต่อ TPO (TPOAb) และต่อ TG (TgAb) : อาจเป็นบวกในโรคฮาชิโมโตะ
CT : ยืนยันการหนาตัวของกล้ามเนื้อนอกลูกตา (โดยเอ็นยึดปกติ ซึ่งเป็นลักษณะสำคัญในการแยกโรค) ยังมีประโยชน์ในการประเมินพื้นเบ้าตา และโครงสร้างกระดูกMRI : ประเมินรูปร่างของกล้ามเนื้อนอกลูกตา ในภาพ T1-weighted และประเมินการอักเสบด้วยวิธี STIR (short-TI inversion recovery) วิธี STIR สามารถแสดงบริเวณที่มีการอักเสบเป็นบริเวณสัญญาณสูงโดยไม่ต้องใช้สารทึบแสง มีประโยชน์ในการประเมินกิจกรรมของโรคตาจากต่อมไทรอยด์ อัลตราซาวนด์แบบ B-scan : ประเมินการโตของกล้ามเนื้อนอกลูกตา และรูปแบบการสะท้อนเสียง
RAPD (relative afferent pupillary defect) positiveรูม่านตา ต่อแสงระหว่างสองตาCFF (ความถี่กระพริบวิกฤต) ลดลงการมองเห็น การตรวจลานสายตา จุดบอดกลาง หรือจุดบอดใกล้กลางการตรวจการมองเห็น สี : การมองเห็น สีลดลงเนื่องจากความเสียหายของเส้นประสาทตา
CAS ที่เสนอโดย Mourits และคณะ9) ถูกใช้อย่างแพร่หลายเป็นตัวบ่งชี้วัตถุประสงค์ในการประเมินกิจกรรมของโรคตาจากต่อมไทรอยด์
รายการประเมิน CAS คะแนน ปวดตา ที่เกิดขึ้นเองหรือรู้สึกกดดันหลังลูกตา1 คะแนน ปวดเมื่อขยับตา 1 คะแนน หนังตาบวมแดง 1 คะแนน เยื่อบุตาอักเสบ (กระจาย)1 คะแนน เปลือกตาบวม 1 คะแนน เยื่อบุตา บวมน้ำ1 คะแนน การอักเสบของต่อมน้ำตาและรอยพับรูปพระจันทร์เสี้ยว 1 คะแนน
ในรายงานต้นฉบับของ Mourits และคณะ ผู้ป่วยที่มีคะแนนกิจกรรมตั้งแต่ 3 ขึ้นไปแสดงการตอบสนองที่ดีต่อการรักษาด้วยยาต้านการอักเสบ ซึ่งมีประโยชน์ในการเลือกการรักษา9) .
เนื้องอกในเบ้าตา (มะเร็งต่อมน้ำเหลือง, เนื้องอกแพร่กระจาย)เซลลูไลติสในเบ้าตา
โรคตาที่เกี่ยวข้องกับ IgG4 การอักเสบของเบ้าตา โดยไม่ทราบสาเหตุ (กล้ามเนื้อเบ้าตา อักเสบ)
ช่องทะลุระหว่างหลอดเลือดแดงคาโรติดกับโพรงเลือดดำคาเวอร์นัส
Q
จะทราบได้อย่างไรว่าโรคตาจากต่อมไทรอยด์อยู่ในระยะ active?
A
ประเมินโดยใช้ Clinical Activity Score (CAS) ให้คะแนน 7 รายการ ได้แก่ ปวดตา ปวดเมื่อขยับตา หนังตาสีแดง เยื่อบุตาอักเสบ หนังตาบวม เยื่อบุตา บวมน้ำ และต่อมน้ำตาอักเสบ คะแนน ≥3 จาก 7 ถือว่าระยะ active การวินิจฉัยระยะ active มีความสำคัญในการตัดสินใจให้การรักษาด้วยภูมิคุ้มกัน เช่น การให้สเตียรอยด์ แบบ pulse การตรวจ MRI ด้วยวิธี STIR ก็มีประโยชน์ในการยืนยันการอักเสบในเบ้าตา
หากมีภาวะต่อมไทรอยด์ทำงานเกิน การทำให้ฮอร์โมนไทรอยด์เป็นปกติเป็นเงื่อนไขที่จำเป็น การทำให้การทำงานของต่อมไทรอยด์เป็นปกติทำได้โดยใช้ยาต้านไทรอยด์ เช่น thiamazole (MMI) อย่างไรก็ตาม การรักษาต่อมไทรอยด์ไม่ได้ช่วยให้โรคตาดีขึ้นโดยตรง และการรักษาโรคตาจะดำเนินการควบคู่กันไป
เนื่องจากการรักษาด้วยไอโอดีนกัมมันตรังสี (RAI) มีความเสี่ยงที่จะทำให้โรคตาแย่ลง จึงควรใช้ด้วยความระมัดระวังในผู้ป่วยโรคตาระยะ active ระดับปานกลางถึงรุนแรง และควรพิจารณาให้สเตียรอยด์ ครอบคลุมหากใช้ 1)
ระดับความรุนแรง ระยะ active (CAS ≥3) ระยะ inactive (CAS <3) เล็กน้อย เสริมซีลีเนียมและการรักษาตามอาการ สังเกตอาการและการรักษาตามอาการ ปานกลางถึงรุนแรง การให้สเตียรอยด์ แบบ pulse (ทางเลือกแรก) ± การฉายรังสีเบ้าตา การผ่าตัด (ผ่าตัดลดเบ้าตา → ผ่าตัดตาเหล่ → ผ่าตัดหนังตา) DON (โรคเส้นประสาทตาถูกกดทับ ) การผ่าตัดเบ้าตา ฉุกเฉิน + สเตียรอยด์ การผ่าตัดเบ้าตา
การเสริมซีลีเนียม : การให้ซีลีโนเมไธโอนีน 100 ไมโครกรัม วันละสองครั้ง นาน 6 เดือน มีประสิทธิภาพในการชะลอการดำเนินของโรคตาจากต่อมไทรอยด์ ชนิดไม่รุนแรง จากการศึกษา RCT (Marcocci 2011 NEJM)13) แนวทาง EUGOGO 20211) แนะนำให้ใช้ในผู้ป่วยอาการน้อย
การรักษาตามอาการ : ปกป้องกระจกตา ด้วยน้ำตาเทียม และยาหยอดตาหล่อลื่น จัดการอาการกลัวแสง ด้วยเลนส์สี แก้ไขภาพซ้อน ด้วยเลนส์ปริซึม
การเลิกบุหรี่ : จำเป็น
ทางเลือกแรก: การให้สเตียรอยด์ แบบพัลส์
ในการศึกษา RCT โดย Kahaly และคณะ การให้ methylprednisolone ทางหลอดเลือดดำ 0.5 กรัม สัปดาห์ละครั้ง นาน 6 สัปดาห์ ตามด้วย 0.25 กรัม สัปดาห์ละครั้ง นาน 6 สัปดาห์ (รวมสะสม 4.5 กรัม) มีประสิทธิภาพมากกว่าและทนได้ดีกว่าการให้ prednisolone ทางปากแบบลดขนาด11)
ในระยะอักเสบ อาจใช้การให้ methylprednisolone 1 กรัม นาน 3 วันเป็นหนึ่งคอร์ส
ทางเลือกที่สอง: การฉายรังสีเบ้าตา
ฉายรังสีครั้งละ 2 Gy สัปดาห์ละ 5 ครั้ง นาน 2 สัปดาห์ (รวม 20 Gy) การใช้ร่วมกับสเตียรอยด์ อาจให้ผลเสริมกัน7) มีประสิทธิภาพสูงสำหรับภาพซ้อน และความผิดปกติของการเคลื่อนไหวตา ควรพิจารณาอย่างระมัดระวังในผู้ป่วยอายุน้อย (<35 ปี) หรือผู้ป่วยเบาหวาน/ความดันโลหิตสูง
การรักษาทางภูมิคุ้มกันอื่นๆ
Rituximab (แอนติบอดีต่อ CD20) : มีรายงานว่าลดกิจกรรมของโรคในผู้ป่วยปานกลางถึงรุนแรงที่ดื้อต่อการรักษา10) Tocilizumab (ยับยั้ง IL-6) : พิจารณาใช้ในกรณีที่ดื้อต่อการรักษา 17)
สำหรับอาการบวมน้ำของเปลือกตาบนจากการอักเสบและการหดรั้งของเปลือกตาบน การฉีด triamcinolone acetonide (Kenacort-A® 1 หลอด) เฉพาะที่มีประสิทธิภาพ
หลักการพื้นฐานคือการผ่าตัดในระยะไม่มีการอักเสบเมื่อการอักเสบสงบเพียงพอ ลำดับมีความสำคัญและต้องปฏิบัติตามลำดับต่อไปนี้ 15) :
การผ่าตัดลดความดันในเบ้าตา (แก้ไขตาโปนและลดความดันเส้นประสาทตา )การผ่าตัดตาเหล่ (แก้ไขภาพซ้อน ) — ต้องรักษาลำดับเพราะตาเหล่ อาจเปลี่ยนหลังผ่าตัดลดความดันเบ้าตา การผ่าตัดเปลือกตา (แก้ไขการหดรั้งของเปลือกตา) — ทำเป็นลำดับสุดท้ายเพื่อปรับสมดุลระหว่างเปลือกตาบนและล่าง
การผ่าตัดลดความดันในเบ้าตา 18) : การเอาส่วนหนึ่งของผนังด้านใน ด้านล่าง และด้านนอกของเบ้าตา ออกเพื่อขยายปริมาตรเบ้าตา ช่วยลดตาโปนและแรงกดบนเส้นประสาทตา วิธีการส่องกล้องแบบรุกรานน้อยที่สุดกำลังเป็นที่นิยม
ในกรณีโรคเส้นประสาทตาถูกกดทับ รุนแรง การผ่าตัดลดความดันเบ้าตา เป็นข้อบ่งชี้ฉุกเฉิน ในระยะอักเสบ ให้ทำการรักษาด้วยสเตียรอยด์ แบบ pulse ก่อน หากไม่ตอบสนองหรือกรณีเร่งด่วนสูง ให้ทำการผ่าตัดลดความดันเบ้าตา ทันที
การพยากรณ์การมองเห็น ดีหากได้รับการแทรกแซงในเวลาที่เหมาะสม อย่างไรก็ตาม ในโรคตาจากต่อมไทรอยด์ ที่เริ่มต้นด้วยโรคเส้นประสาทตาถูกกดทับ การพยากรณ์การมองเห็น อาจไม่ดี ดังนั้นการตรวจพบและการรักษาตั้งแต่เนิ่นๆ จึงสำคัญ 15)
Q
ควรผ่าตัดโรคตาจากต่อมไทรอยด์เมื่อใดดีที่สุด?
A
หลักการคือผ่าตัดในระยะไม่มีการอักเสบเมื่อการอักเสบสงบ ลำดับพื้นฐานคือ: ① ลดความดันเบ้าตา → ② ผ่าตัดตาเหล่ → ③ ผ่าตัดเปลือกตา การรักษาลำดับป้องกันไม่ให้การผ่าตัดก่อนหน้าส่งผลต่อผลลัพธ์ของการผ่าตัดหลัง (เช่น ตาเหล่ เปลี่ยนหลังลดความดันเบ้าตา ) อย่างไรก็ตาม โรคเส้นประสาทตาถูกกดทับ เป็นข้อบ่งชี้ในการผ่าตัดฉุกเฉิน และจะทำการผ่าตัดลดความดันเบ้าตา ทันทีโดยไม่คำนึงถึงระยะอักเสบหรือไม่
ไฟโบรบลาสต์ในเนื้อเยื่อเรโทรบัลบาร์ (retrobulbar) ในเบ้าตา มีการแสดงออกของตัวรับ TSH ซึ่งกลายเป็นเป้าหมายของปฏิกิริยาภูมิคุ้มกันตนเอง แอนติบอดีต่อตัวรับ TSH (TRAb) ที่ผลิตในผู้ป่วยโรคเกรฟส์ (Basedow) จะจับไม่เฉพาะกับต่อมไทรอยด์เท่านั้น แต่ยังจับกับตัวรับ TSH บนไฟโบรบลาสต์ในเบ้าตา ทำให้เกิดการทำงานของระบบอักเสบเฉพาะที่ในเบ้าตา 8)
กลไกการเกิดโรคดำเนินไปตามขั้นตอนต่อไปนี้:
การนำเสนอแอนติเจนและการผลิตออโตแอนติบอดี : เซลล์ทีที่ถูกกระตุ้นจะจดจำตัวรับ TSH เซลล์บีผลิต TRAb และ TSAbการกระตุ้นไฟโบรบลาสต์ในเบ้าตา : TRAb จับกับตัวรับ TSH บนไฟโบรบลาสต์ในเบ้าตา → กระตุ้นการส่งสัญญาณภายในเซลล์การขยายสัญญาณของวิถี IGF-1R 4) : ตัวรับ TSH และตัวรับ IGF-1 (IGF-1R) สร้างสารเชิงซ้อนของตัวรับ ทำให้สัญญาณขยายเพิ่มขึ้น ยาเทโปรทูมูแมบ (Teprotumumab) จะปิดกั้น IGF-1R เพื่อปรับปรุงภาวะจักษุวิทยาการปล่อยไซโตไคน์ที่ก่อให้เกิดการอักเสบ : ไซโตไคน์ที่ก่อให้เกิดการอักเสบ เช่น TNF -α, IL-6 และ IL-1β ถูกปล่อยเฉพาะที่ในเบ้าตา ทำให้เกิดการเพิ่มขึ้นของการซึมผ่านของหลอดเลือด การเกิดอาการบวมน้ำ และการแทรกซึมของเซลล์ภูมิคุ้มกันเพิ่มเติม 16) การสังเคราะห์ไกลโคซามิโนไกลแคน (กรดไฮยาลูโรนิก) มากเกินไป : ไฟโบรบลาสต์ในเบ้าตา ถูกกระตุ้นให้ผลิตไกลโคซามิโนไกลแคน เช่น กรดไฮยาลูโรนิก มากเกินไป ทำให้เกิดการกักเก็บของเหลวและบวมของเนื้อเยื่อในเบ้าตา การเปลี่ยนเป็นเซลล์ไขมัน : ไฟโบรบลาสต์เปลี่ยนเป็นเซลล์ไขมัน (adipogenesis) ทำให้ปริมาณไขมันในเบ้าตา เพิ่มขึ้นการเปลี่ยนแปลงของกล้ามเนื้อนอกลูกตา : ลิมโฟไซต์ พลาสมาเซลล์ และมาโครฟาจแทรกซึมเข้าไปในกล้ามเนื้อนอกลูกตา ทำให้เกิดอาการบวมน้ำและการสะสมของไกลโคซามิโนไกลแคนระหว่างเส้นใยกล้ามเนื้อ ในระยะท้ายของการอักเสบจนถึงระยะไม่ทำงาน การเกิดพังผืดจะดำเนินไป และความสามารถในการเคลื่อนไหวของกล้ามเนื้อลดลง
การเพิ่มจำนวนของไขมันในเบ้าตา และการโตเกินของกล้ามเนื้อนอกลูกตา ทำให้ปริมาตรของเนื้อหาในเบ้าเพิ่มขึ้น ทำให้ความดันภายในเบ้าตา กระดูกที่คงที่ (ปริมาตรเบ้าตา ประมาณ 30 มล.) สูงขึ้น ความดันภายในเบ้าตา ที่เพิ่มขึ้นนี้จะดันลูกตาไปข้างหน้า (ตาโปน) และอาจพัฒนาไปสู่ภาวะเลือดดำคั่ง → การกดทับเส้นประสาทตา (orbital apex syndrome)
การกดทับเส้นประสาทตา ที่ปลายเบ้าตา เป็นกลไกหลักของภาวะเส้นประสาทตา ถูกกดทับ และสามารถยืนยันได้ด้วย CT ว่าเป็นการรวมตัวของกล้ามเนื้อนอกลูกตา ที่ปลายเบ้า (apical crowding)
เส้นโค้ง Rundle 14) เป็นแบบจำลองที่แสดงให้เห็นถึงประวัติธรรมชาติของโรคตาที่เกี่ยวข้องกับต่อมไทรอยด์ โดยแสดงให้เห็นระยะสองระยะ: ระยะ active (การอักเสบ) และระยะ inactive (คงที่/พังผืด) ระยะ active มักกินเวลา 1-3 ปี จากนั้นกิจกรรมของโรคจะลดลงและคงที่ อย่างไรก็ตาม แม้หลังจากเปลี่ยนผ่านไปยังระยะ inactive แล้ว การเปลี่ยนแปลงทางสัณฐานวิทยา เช่น ตาโปน ตาเห็นภาพซ้อน (diplopia) และหนังตาหดรั้ง มักยังคงอยู่ และในระยะนี้จะพิจารณาการผ่าตัดแก้ไข
เทโปรทูมูแมบ (TEPEZ ZA®) เป็นแอนติบอดีชนิดโมโนโคลนอลของมนุษย์ที่กำหนดเป้าหมาย IGF-1R และได้รับการอนุมัติจาก FDA ของสหรัฐอเมริกาในปี 2020 สำหรับโรคตาจากต่อมไทรอยด์ ชนิดออกฤทธิ์ระดับปานกลางถึงรุนแรง 2) 3) .
สูตรการให้ยาคือ 3 มก./กก. สำหรับครั้งแรก, 10 มก./กก. สำหรับครั้งที่สอง, และ 20 มก./กก. (สูงสุด) สำหรับครั้งที่สามเป็นต้นไป ให้โดยการหยดทางหลอดเลือดดำทุก 3 สัปดาห์ รวมทั้งหมด 8 ครั้ง.
ในการวิเคราะห์อภิมานจากการทดลองแบบสุ่มมีกลุ่มควบคุม 5 การทดลอง รวมผู้ป่วย 411 ราย (Cong et al. 2024) 4) เมื่อเทียบกับกลุ่มยาหลอก กลุ่มเทโปรทูมูแมบแสดงให้เห็น:
การปรับปรุงอย่างมีนัยสำคัญของภาวะตายื่น (proptosis)
การปรับปรุงภาพซ้อน (เพิ่มอัตราการตอบสนองของภาพซ้อน อย่างมีนัยสำคัญ)
การลดลงอย่างมีนัยสำคัญของคะแนน CAS (กิจกรรมทางคลินิก)
ไม่มีความแตกต่างอย่างมีนัยสำคัญของอัตราเหตุการณ์ไม่พึงประสงค์ร้ายแรงเมื่อเทียบกับยาหลอก
ได้รับการยืนยันแล้ว เหตุการณ์ไม่พึงประสงค์หลักที่ต้องระวัง ได้แก่ ความบกพร่องทางการได้ยิน (สูญเสียการได้ยินความถี่สูง) ระดับน้ำตาลในเลือดสูง และตะคริวของกล้ามเนื้อ 4) .
ในแถลงการณ์ร่วมของสมาคมต่อมไทรอยด์แห่งอเมริกา (ATA) และสมาคมต่อมไทรอยด์แห่งยุโรป (ETA) แนะนำให้ใช้สำหรับ TED ชนิดออกฤทธิ์ระดับปานกลางถึงรุนแรง.
ริตูซิแมบ (แอนติบอดีต่อต้าน CD20) : กำหนดเป้าหมายเซลล์บี และการทดลองแบบสุ่มมีกลุ่มควบคุมบางรายงานว่ากิจกรรมของโรคตาจากต่อมไทรอยด์ ลดลง 10) โทซิลิซูแมบ (ยับยั้ง IL-6)17)
Bartalena L, Kahaly GJ, Baldeschi L, et al. The 2021 European Group on Graves’ Orbitopathy (EUGOGO) clinical practice guidelines for the medical management of Graves’ orbitopathy. Eur J Endocrinol. 2021;184(4):G43-G67.
Douglas RS, Kahaly GJ, Patel A, et al. Teprotumumab for the treatment of active thyroid eye disease. N Engl J Med. 2020;382(4):341-352.
Smith TJ, Kahaly GJ, Ezra DG, et al. Teprotumumab for thyroid-associated ophthalmopathy. N Engl J Med. 2017;376(18):1748-1761.
Cong X, Pei L, Hu H. Teprotumumab for treating active thyroid eye disease: A meta-analysis. Medicine (Baltimore). 2024;103(xx):eXXXXX.
Bahn RS. Graves’ ophthalmopathy. N Engl J Med. 2010;362(8):726-738.
Wiersinga WM, Bartalena L. Epidemiology and prevention of Graves’ ophthalmopathy. Thyroid. 2002;12(10):855-860.
Stan MN, Salvi M. Management of thyroid eye disease. J Clin Endocrinol Metab. 2017;102(11):4088-4100.
Bahn RS. Pathophysiology of Graves’ ophthalmopathy: the cycle of disease. J Clin Endocrinol Metab. 2003;88(5):1939-1946.
Mourits MP, Koornneef L, Wiersinga WM, et al. Clinical criteria for the assessment of disease activity in Graves’ ophthalmopathy: a novel approach. Br J Ophthalmol. 1989;73(8):639-644.
Salvi M, Vannucchi G, Curro N, Campi I, Covelli D, Dazzi D, et al. Efficacy of B-cell targeted therapy with rituximab in patients with active moderate to severe Graves’ orbitopathy: a randomized controlled study. J Clin Endocrinol Metab. 2015;100(2):422-431. PMCI D: PMC4318899. doi:10.1210/jc.2014-3014.
Kahaly GJ, Pitz S, Hommel G, et al. Randomized, single blind trial of intravenous versus oral steroid monotherapy in Graves’ orbitopathy. J Clin Endocrinol Metab. 2005;90(9):5234-5240.
Prummel MF, Wiersinga WM. Smoking and risk of Graves’ disease. JAMA. 1993;269(4):479-482.
Marcocci C, Kahaly GJ, Krassas GE, et al. Selenium and the course of mild Graves’ orbitopathy. N Engl J Med. 2011;364(20):1920-1931.
Rundle FF, Wilson CW. Development and course of exophthalmos and ophthalmoplegia in Graves’ disease with special reference to the effect of thyroidectomy. Clin Sci. 1945;5:177-194.
Wakelkamp IM, Baldeschi L, Saeed P, et al. Surgical or medical decompression as a first-line treatment of optic neuropathy in Graves’ ophthalmopathy? A randomized controlled trial. Clin Endocrinol. 2005;63(3):323-328.
Garrity JA, Bahn RS. Pathogenesis of Graves’ orbitopathy: implications for prediction, prevention, and treatment. Am J Ophthalmol. 2006;142(1):147-153.
Kabra A, Higuchi K, Sheth A, et al. Tocilizumab in refractory thyroid eye disease: a case series. Ophthalmology. 2018;125(9):1326-1328.
Ugradar S, Rootman DB. Advances in orbital decompression for thyroid eye disease. Curr Opin Ophthalmol. 2021;32(5):454-460.