眼瞼症状
上眼瞼後退:最も頻度が高い徴候。Müller筋への交感神経緊張亢進または挙筋の線維化による。
lid lag(上眼瞼遅れ):下方視で上眼瞼が遅れて追従する。
眼瞼腫脹:眼瞼の浮腫・脂肪増殖による腫脹。炎症性の場合はステロイド局所注射が有効。

甲状腺眼症(Thyroid Eye Disease: TED)は、甲状腺関連自己抗体が眼窩組織に作用して生じる自己免疫性眼窩疾患である。Thyroid-associated ophthalmopathy(TAO)、Graves眼症(GO)とも呼ばれる。
甲状腺機能亢進症(バセドウ病)に伴って眼症を発症する場合と、甲状腺機能が全く正常なeuthyroid ophthalmopathyとして発症する場合がある。甲状腺眼症は基本的には甲状腺ホルモンとは無関係に進行し、甲状腺関連自己抗体が関与する自己免疫疾患の一つである。
甲状腺眼症の有病率は女性で年間16/10万人、男性で年間2.9/10万人と報告されている6)。バセドウ病患者のうち25〜50%に眼症を合併する5)。好発年齢は40〜50歳と60〜70歳の二峰性分布を示す6)。喫煙は発症と重症化の主要なリスク因子であり12)、禁煙指導が治療の基本となる。
橋本病(慢性甲状腺炎)においても眼症状が生じることがあるが、多くはeuthyroid ophthalmopathyとしての発症様式をとる。甲状腺関連自己抗体(抗TPO抗体・抗TG抗体)が眼窩組織に影響を与える機序は、バセドウ病眼症と共通している部分がある。
EUGOGOガイドライン20211)では甲状腺眼症を以下の3段階に分類する。
| 重症度 | 主な特徴 | 治療方針 |
|---|---|---|
| 軽症 | 眼瞼腫脹・眼瞼後退、眼球突出が軽度(<3mm)、複視なし | 経過観察・対症療法・セレン補充 |
| 中等症〜重症 | 眼球突出(≥3mm)、複視(間欠性または持続性)、眼瞼後退(≥2mm)、角膜障害 | ステロイドパルス療法・眼窩放射線 |
| 視力を脅かす甲状腺眼症(DON) | 圧迫性視神経症または重度角膜障害 | 緊急眼窩減圧術・ステロイド |
あります。euthyroid ophthalmopathyとして、甲状腺機能が正常な状態でも眼症を発症することがあります。甲状腺関連自己抗体が眼窩組織に直接作用するため、甲状腺ホルモン値とは独立して眼症状が現れます。甲状腺眼症の診断には血液検査での自己抗体確認と眼窩画像検査が重要です。
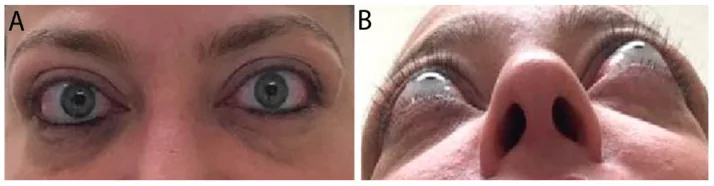
臨床症状は大きく、眼瞼症状・眼球突出・複視・視力障害の4つに分類される。若年者では眼球突出が、高齢者では眼球運動障害・複視が生じやすい。
眼瞼症状
上眼瞼後退:最も頻度が高い徴候。Müller筋への交感神経緊張亢進または挙筋の線維化による。
lid lag(上眼瞼遅れ):下方視で上眼瞼が遅れて追従する。
眼瞼腫脹:眼瞼の浮腫・脂肪増殖による腫脹。炎症性の場合はステロイド局所注射が有効。
眼球突出
複視・眼球運動障害
視力障害
初期には乾燥感・刺激感・流涙・羞明などドライアイ類似の愁訴が先行することがある。その後、眼瞼腫脹・眼球突出・複視などが顕在化する。重症化すると角膜暴露または圧迫性視神経症が生じ、緊急的な治療を要する。
Rundle曲線14)が示すように、甲状腺眼症は活動期(炎症期)と非活動期(線維化・安定期)の二相性経過をたどる。活動期は通常1〜3年続き、その後自然に安定化するが、適切な治療により炎症を早期に制御することが重要である。
眼窩内球後組織の線維芽細胞にはTSH受容体が発現している。このTSH受容体が抗原となって眼窩組織にリンパ球の浸潤を促し、マクロファージを活性化させ、眼局所でのサイトカインネットワークにより炎症反応が活性化する。
免疫細胞の眼窩組織への浸潤(主にCD4+/CD8+ T細胞)が引き金となり、以下のカスケードが進行する8)16):
IGF-1受容体(IGF-1R)とTSH受容体が受容体複合体を形成してシグナル伝達を増幅することが明らかになっており4)、これが後述するテプロツムマブの治療標的となっている。
喫煙は甲状腺眼症の最も強力なリスク因子です。喫煙によって発症リスクと重症化リスクが上昇し、ステロイドなどの治療効果も低下します。放射性ヨード治療後の眼症悪化リスクも喫煙者で高くなります。禁煙により治療効果が改善することが示されており、患者への禁煙指導は治療の重要な一部です。
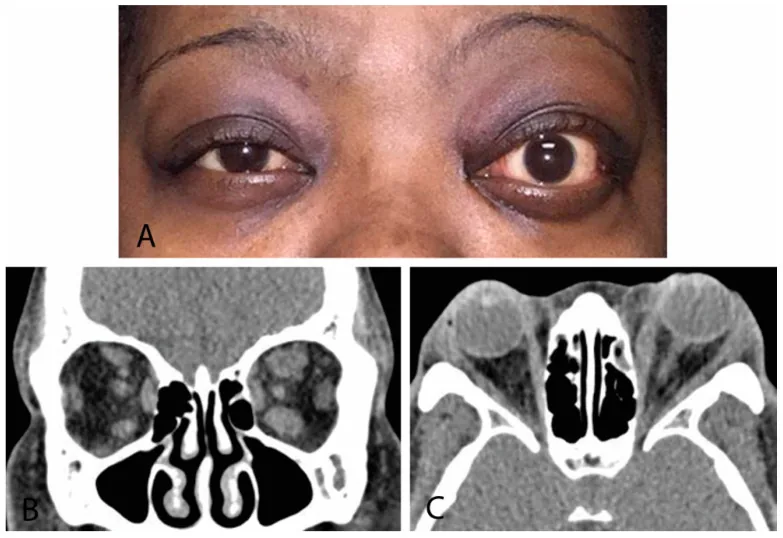
臨床診断が基本となる。眼瞼後退・眼球突出・複視の存在と甲状腺疾患の既往の組み合わせで診断される。重要な注意点として、甲状腺眼症と確定診断するためには外眼筋の肥大・炎症と眼位・眼球運動制限が相関している必要がある。
Mourits らが提唱したCAS9)は甲状腺眼症の活動性を客観的に評価する指標として広く用いられる。
| CAS評価項目 | 点数 |
|---|---|
| 自発的な眼痛または眼球後部の圧迫感 | 1点 |
| 眼球運動による疼痛 | 1点 |
| 眼瞼発赤 | 1点 |
| 結膜充血(びまん性) | 1点 |
| 眼瞼腫脹 | 1点 |
| 球結膜浮腫 | 1点 |
| 涙丘・半月ヒダの炎症 | 1点 |
Mouritsらの原報では、activity score 3点以上の症例で抗炎症治療への良好な反応が示され、治療選択に有用とされた9)。
甲状腺機能亢進症がある場合は、甲状腺ホルモンの正常化が必須の前提条件である。チアマゾール(MMI)などの抗甲状腺薬による甲状腺機能の正常化を図る。ただし甲状腺治療が眼症そのものを直接改善するわけではなく、眼症の治療は並行して進める。
放射性ヨード(RAI)治療は眼症を悪化させるリスクがあるため、中等症以上の活動期眼症患者には慎重に行い、施行する場合はステロイドカバーを考慮する1)。
| 重症度 | 活動期(CAS ≥3) | 非活動期(CAS <3) |
|---|---|---|
| 軽症 | セレン補充・対症療法 | 経過観察・対症療法 |
| 中等症〜重症 | ステロイドパルス療法(第一選択)± 眼窩放射線 | 手術(眼窩減圧術→斜視手術→眼瞼手術) |
| DON(圧迫性視神経症) | 緊急眼窩減圧術 + ステロイド | 眼窩減圧術 |
セレン補充療法:セレンメチオニン100μg 1日2回、6ヶ月間の投与が軽症甲状腺眼症の進行抑制に有効であることがRCT(Marcocci 2011 NEJM)で示されている13)。EUGOGOガイドライン20211)では軽症例への使用を推奨している。
対症療法:人工涙液・潤滑眼軟膏による角膜保護、ティント(着色レンズ)による羞明対策、プリズムレンズによる複視の補正など。
禁煙指導:必須。
第一選択:ステロイドパルス療法
KahalyらのRCTでは、メチルプレドニゾロン0.5gを週1回6週、その後0.25gを週1回6週投与する静脈内投与群(累積4.5g)が、経口プレドニゾロン漸減療法より有効で忍容性が高かった11)。
炎症期には1クールをメチルプレドニゾロン1g×3日間とするパルス療法も用いられる。
第二選択:眼窩放射線照射
1回2Gyを週5回、2週間(計20Gy)照射する。ステロイドとの併用で相乗効果が期待できる7)。複視・眼球運動障害への効果が高い。若年者(35歳未満)や糖尿病・高血圧合併例では照射を慎重に検討する。
その他の免疫療法
炎症性の上眼瞼浮腫・上眼瞼後退症に対しては、トリアムシノロンアセトニド(ケナコルト-A® 1アンプル)の局所注射が有効である。
手術は炎症が十分に鎮静化した非活動期に行うのが基本原則である。施行順序が重要であり、以下の順序を守る15):
眼窩減圧術18):眼窩内壁・下壁・外壁の一部を除去し眼窩容積を拡大することで、眼球突出と視神経圧迫を解除する。内視鏡下での最小侵襲的アプローチが普及している。
圧迫性視神経症が高度な場合は眼窩減圧術が緊急適応となる。炎症期であれば、まずステロイドパルス療法を施行し、奏効しない場合または緊急性が高い場合は速やかに眼窩減圧術を行う。
視機能予後は、適切な時機に介入が行われれば良好である。ただし圧迫性視神経症で発症した甲状腺眼症では視機能予後が不良なこともあり、早期発見・早期治療が重要である15)。
眼窩内球後組織の線維芽細胞にはTSH受容体が発現しており、これが自己免疫反応の標的となる。バセドウ病患者で産生されるTSH受容体抗体(TRAb)が甲状腺だけでなく、眼窩線維芽細胞のTSH受容体にも結合し、眼窩局所での炎症カスケードが開始される8)。
発症機序は以下のステップで進行する:
眼窩脂肪の増殖と外眼筋の肥大が眼窩内容積を増加させ、固定された骨性眼窩(眼窩容積約30mL)内の圧力が上昇する。この眼窩内圧上昇が眼球を前方へ押し出し(眼球突出)、静脈うっ滞→視神経圧迫(orbital apex syndrome)へと進展する場合がある。
眼窩先端部での視神経圧迫は圧迫性視神経症の主要機序であり、CTでは眼窩先端での外眼筋の集積(apical crowding)として確認できる。
Rundle曲線14)は甲状腺眼症の自然経過を図示したモデルで、活動期(炎症期)と非活動期(安定・線維化期)の二相性経過を示す。活動期はおおむね1〜3年続き、その後疾患活動性は低下して安定化する。ただし非活動期に移行しても、眼球突出・複視・眼瞼後退などの形態的変化は残存する場合が多く、この時期に手術的矯正が検討される。
テプロツムマブ(TEPEZZA®)はIGF-1Rを標的とするヒト型モノクローナル抗体であり、2020年に米国FDAが中等症〜重症の活動性甲状腺眼症に対して承認した2)3)。
投与プロトコルは3mg/kgを初回投与後、2回目10mg/kg、3回目以降20mg/kg(最大)を3週ごとに合計8回点滴静注する。
5つのRCT・合計411例を対象とするメタ解析(Cong et al. 2024)4)では、テプロツムマブ群でプラセボ群と比較して:
が確認された。主な有害事象として聴覚障害(高音域の聴力低下)・高血糖・筋痙攣に注意を要する4)。
ATA(米国甲状腺学会)とETA(欧州甲状腺学会)の合同ポジションステートメントでは、活動性中等症〜重症のTEDに対して推奨されている。
Bartalena L, Kahaly GJ, Baldeschi L, et al. The 2021 European Group on Graves’ Orbitopathy (EUGOGO) clinical practice guidelines for the medical management of Graves’ orbitopathy. Eur J Endocrinol. 2021;184(4):G43-G67.
Douglas RS, Kahaly GJ, Patel A, et al. Teprotumumab for the treatment of active thyroid eye disease. N Engl J Med. 2020;382(4):341-352.
Smith TJ, Kahaly GJ, Ezra DG, et al. Teprotumumab for thyroid-associated ophthalmopathy. N Engl J Med. 2017;376(18):1748-1761.
Cong X, Pei L, Hu H. Teprotumumab for treating active thyroid eye disease: A meta-analysis. Medicine (Baltimore). 2024;103(xx):eXXXXX.
Bahn RS. Graves’ ophthalmopathy. N Engl J Med. 2010;362(8):726-738.
Wiersinga WM, Bartalena L. Epidemiology and prevention of Graves’ ophthalmopathy. Thyroid. 2002;12(10):855-860.
Stan MN, Salvi M. Management of thyroid eye disease. J Clin Endocrinol Metab. 2017;102(11):4088-4100.
Bahn RS. Pathophysiology of Graves’ ophthalmopathy: the cycle of disease. J Clin Endocrinol Metab. 2003;88(5):1939-1946.
Mourits MP, Koornneef L, Wiersinga WM, et al. Clinical criteria for the assessment of disease activity in Graves’ ophthalmopathy: a novel approach. Br J Ophthalmol. 1989;73(8):639-644.
Salvi M, Vannucchi G, Curro N, Campi I, Covelli D, Dazzi D, et al. Efficacy of B-cell targeted therapy with rituximab in patients with active moderate to severe Graves’ orbitopathy: a randomized controlled study. J Clin Endocrinol Metab. 2015;100(2):422-431. PMCID: PMC4318899. doi:10.1210/jc.2014-3014.
Kahaly GJ, Pitz S, Hommel G, et al. Randomized, single blind trial of intravenous versus oral steroid monotherapy in Graves’ orbitopathy. J Clin Endocrinol Metab. 2005;90(9):5234-5240.
Prummel MF, Wiersinga WM. Smoking and risk of Graves’ disease. JAMA. 1993;269(4):479-482.
Marcocci C, Kahaly GJ, Krassas GE, et al. Selenium and the course of mild Graves’ orbitopathy. N Engl J Med. 2011;364(20):1920-1931.
Rundle FF, Wilson CW. Development and course of exophthalmos and ophthalmoplegia in Graves’ disease with special reference to the effect of thyroidectomy. Clin Sci. 1945;5:177-194.
Wakelkamp IM, Baldeschi L, Saeed P, et al. Surgical or medical decompression as a first-line treatment of optic neuropathy in Graves’ ophthalmopathy? A randomized controlled trial. Clin Endocrinol. 2005;63(3):323-328.
Garrity JA, Bahn RS. Pathogenesis of Graves’ orbitopathy: implications for prediction, prevention, and treatment. Am J Ophthalmol. 2006;142(1):147-153.
Kabra A, Higuchi K, Sheth A, et al. Tocilizumab in refractory thyroid eye disease: a case series. Ophthalmology. 2018;125(9):1326-1328.
Ugradar S, Rootman DB. Advances in orbital decompression for thyroid eye disease. Curr Opin Ophthalmol. 2021;32(5):454-460.