眼睑症状
上眼睑退缩:最常见的体征。由Müller肌的交感神经过度兴奋或提肌纤维化引起。
眼睑迟落:向下看时上眼睑延迟跟随。
眼睑肿胀:由于眼睑水肿和脂肪增生引起的肿胀。炎症性病例局部注射类固醇有效。

甲状腺眼病(Thyroid Eye Disease: TED)是一种由甲状腺相关自身抗体作用于眼眶组织引起的自身免疫性眼眶疾病。也称为甲状腺相关眼病(TAO)或格雷夫斯眼病(GO)。
甲状腺眼病可伴随甲状腺功能亢进症(格雷夫斯病)发生,也可在甲状腺功能完全正常的情况下作为甲状腺功能正常眼病发生。甲状腺眼病基本独立于甲状腺激素进展,是与甲状腺相关自身抗体有关的自身免疫性疾病之一。
甲状腺眼病的患病率报告为女性每年16/10万人,男性每年2.9/10万人6)。格雷夫斯病患者中25%~50%合并眼病5)。好发年龄呈双峰分布,分别为40~50岁和60~70岁6)。吸烟是发病和重症化的主要危险因素12),戒烟指导是治疗的基础。
桥本病(慢性甲状腺炎)也可能出现眼部症状,但多数表现为甲状腺功能正常眼病。甲状腺相关自身抗体(抗TPO抗体、抗TG抗体)影响眼眶组织的机制与格雷夫斯眼病有共同之处。
EUGOGO指南20211)将甲状腺眼病分为以下三个阶段。
| 严重程度 | 主要特征 | 治疗策略 |
|---|---|---|
| 轻度 | 眼睑肿胀、眼睑退缩、轻度眼球突出(<3mm),无复视 | 观察、对症治疗、补充硒 |
| 中度至重度 | 眼球突出(≥3mm)、复视(间歇性或持续性)、眼睑退缩(≥2mm)、角膜受累 | 类固醇冲击疗法、眼眶放疗 |
| 威胁视力的甲状腺眼病(DON) | 压迫性视神经病变或严重角膜病变 | 紧急眼眶减压术/类固醇 |
会的。作为甲状腺功能正常眼病,即使在甲状腺功能正常的情况下也可能发生眼病。由于甲状腺相关自身抗体直接作用于眼眶组织,眼部症状独立于甲状腺激素水平出现。甲状腺眼病的诊断需要血液检查确认自身抗体和眼眶影像学检查。
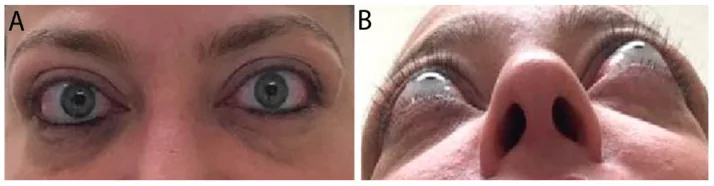
临床症状大致分为四类:眼睑症状、眼球突出、复视和视力障碍。年轻人更容易出现眼球突出,而老年人更容易出现眼球运动障碍和复视。
眼睑症状
上眼睑退缩:最常见的体征。由Müller肌的交感神经过度兴奋或提肌纤维化引起。
眼睑迟落:向下看时上眼睑延迟跟随。
眼睑肿胀:由于眼睑水肿和脂肪增生引起的肿胀。炎症性病例局部注射类固醇有效。
眼球突出
用Hertel眼球突出计测量。正常值小于18毫米,甲状腺眼病患者常超过21毫米。
由于眼眶内脂肪组织增生和外眼肌肥大,眼球被向前推挤。
左右差异(2mm以上)是诊断的线索。
复视和眼球运动障碍
视力障碍
初期可能先出现干燥感、刺激感、流泪、畏光等类似干眼的症状。随后出现眼睑肿胀、眼球突出、复视等。重症化时会出现角膜暴露或压迫性视神经病变,需要紧急治疗。
如Rundle曲线14)所示,甲状腺眼病经历活动期(炎症期)和非活动期(纤维化/稳定期)的双相过程。活动期通常持续1-3年,之后自然稳定,但通过适当治疗早期控制炎症很重要。
眼球突出是甲状腺眼病的主要症状之一。眼眶内的脂肪组织和外眼肌肿大,将眼球向前推挤。特别是格雷夫斯病患者如果自觉眼球突出,需要尽快进行眼科评估。使用Hertel眼球突出计测量,并通过CT或MRI检查眼眶状态。
眼眶球后组织的成纤维细胞表达TSH受体。这些TSH受体作为抗原,促进淋巴细胞浸润眼眶组织,激活巨噬细胞,并通过局部细胞因子网络激活炎症反应。
免疫细胞(主要是CD4+/CD8+ T细胞)浸润眼眶组织触发以下级联反应8)16):
已发现IGF-1受体(IGF-1R)和TSH受体形成受体复合物,放大信号转导4),这是下文所述替妥木单抗的治疗靶点。
吸烟是甲状腺眼病最强的危险因素。吸烟会增加发病风险和严重程度,并降低类固醇等治疗的效果。放射性碘治疗后眼病恶化的风险在吸烟者中也更高。戒烟已被证明可以改善治疗效果,因此对患者进行戒烟指导是治疗的重要组成部分。
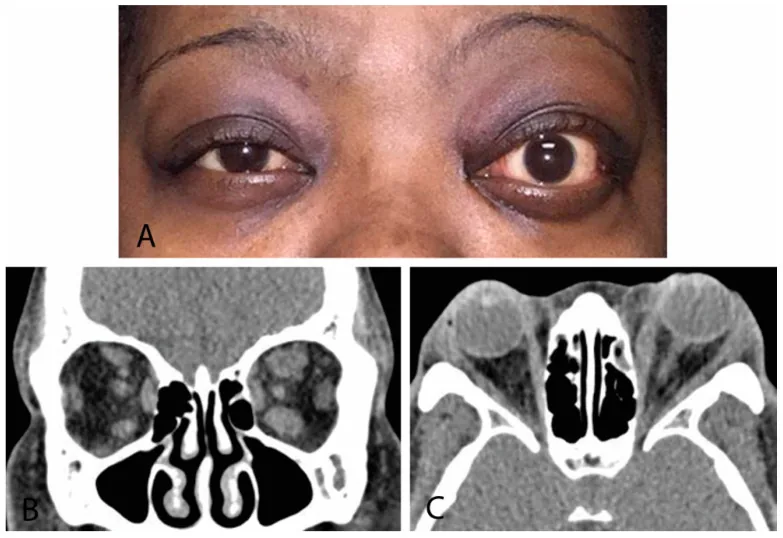
临床诊断是基础。通过眼睑后退、眼球突出、复视的存在以及甲状腺疾病病史的组合来诊断。一个重要注意事项是,要确诊甲状腺眼病,眼外肌的肥大和炎症必须与眼位和眼球运动受限相关。
Mourits等人提出的CAS9)被广泛用作甲状腺眼病活动性的客观评估指标。
| CAS评估项目 | 分数 |
|---|---|
| 自发性眼痛或眼球后压迫感 | 1分 |
| 眼球运动时疼痛 | 1分 |
| 眼睑发红 | 1分 |
| 结膜充血(弥漫性) | 1分 |
| 眼睑肿胀 | 1分 |
| 球结膜水肿 | 1分 |
| 泪阜和半月皱襞炎症 | 1分 |
Mourits等人的原始报告显示,活动评分≥3分的病例对抗炎治疗反应良好,被认为有助于治疗选择9)。
如果存在甲状腺功能亢进症,甲状腺激素正常化是必须的前提条件。使用甲巯咪唑(MMI)等抗甲状腺药物使甲状腺功能恢复正常。但甲状腺治疗本身并不能直接改善眼病,眼病的治疗需同时进行。
放射性碘(RAI)治疗有加重眼病的风险,因此对于中重度活动期眼病患者应谨慎使用,若实施需考虑类固醇覆盖1)。
| 严重程度 | 活动期(CAS ≥3) | 非活动期(CAS <3) |
|---|---|---|
| 轻度 | 补硒、对症治疗 | 观察、对症治疗 |
| 中重度 | 类固醇脉冲疗法(一线)± 眼眶放疗 | 手术(眼眶减压术→斜视手术→眼睑手术) |
| DON(压迫性视神经病变) | 紧急眼眶减压术 + 类固醇 | 眼眶减压术 |
硒补充疗法:硒代蛋氨酸100μg每日两次,持续6个月,已被RCT(Marcocci 2011 NEJM)证明可有效抑制轻度甲状腺眼病的进展13)。EUGOGO指南20211)推荐用于轻度病例。
对症治疗:使用人工泪液和润滑眼膏保护角膜,使用有色眼镜应对畏光,使用棱镜矫正复视。
戒烟指导:必须。
一线治疗:类固醇冲击疗法
Kahaly等人的RCT显示,静脉注射甲泼尼龙0.5g每周一次,持续6周,随后0.25g每周一次,持续6周(累积4.5g),比口服泼尼松龙逐渐减量疗法更有效且耐受性更好11)。
在炎症期,也可使用甲泼尼龙1g×3天的冲击疗法作为一个疗程。
二线治疗:眼眶放射治疗
每次2Gy,每周5次,持续2周(总计20Gy)。与类固醇联合使用可产生协同效应7)。对复视和眼球运动障碍效果显著。年轻患者(35岁以下)或合并糖尿病、高血压的患者应谨慎考虑放疗。
其他免疫疗法
对于炎性上眼睑水肿和上眼睑退缩,局部注射曲安奈德(Kenacort-A® 1安瓿)有效。
手术原则上应在炎症充分消退的非活动期进行。手术顺序很重要,应遵循以下顺序 15):
眼眶减压术 18):切除部分眼眶内壁、下壁和外壁以扩大眼眶容积,缓解眼球突出和视神经压迫。微创内镜入路已广泛普及。
对于严重的压迫性视神经病变,眼眶减压术是紧急适应证。在炎症期,首先进行类固醇冲击疗法;如果无效或紧急程度高,则立即进行眼眶减压术。
如果在适当时机进行干预,视力预后良好。然而,以压迫性视神经病变起病的甲状腺眼病视力预后可能较差,因此早期发现和早期治疗很重要 15)。
手术原则上应在炎症消退的非活动期进行。标准顺序是:①眼眶减压术→②斜视手术→③眼睑手术。遵循此顺序可防止前一次手术影响后一次手术的结果(例如眼眶减压后斜视发生变化)。但压迫性视神经病变是急诊手术适应证,无论活动期还是非活动期,都应立即进行眼眶减压术。
眼眶球后组织的成纤维细胞表达TSH受体,成为自身免疫反应的靶点。格雷夫斯病患者产生的TSH受体抗体(TRAb)不仅与甲状腺TSH受体结合,还与眼眶成纤维细胞的TSH受体结合,从而在眼眶局部启动炎症级联反应8)。
发病机制通过以下步骤进展:
眼眶脂肪增生和眼外肌肥大增加眼眶内容积,使固定的骨性眼眶(眼眶容积约30 mL)内压力升高。这种眶内压升高将眼球向前推(眼球突出),并可能进展为静脉淤滞和视神经压迫(眶尖综合征)。
眶尖部的视神经压迫是压迫性视神经病变的主要机制,CT上可表现为眶尖部眼外肌聚集(眶尖拥挤)。
Rundle曲线14)是展示甲状腺眼病自然病程的模型,显示活动期(炎症期)和非活动期(稳定/纤维化期)的双相过程。活动期通常持续1至3年,之后疾病活动性降低并稳定。然而,即使进入非活动期,眼球突出、复视和眼睑退缩等形态改变往往持续存在,此时期可考虑手术矫正。
替妥木单抗(TEPEZZA®)是一种靶向IGF-1R的人源化单克隆抗体,于2020年获得美国FDA批准用于中重度活动性甲状腺眼病2)3)。
给药方案为:首次剂量3 mg/kg,第二次10 mg/kg,第三次及以后20 mg/kg(最大),每3周静脉输注一次,共8次。
一项纳入5项RCT、共411例患者的荟萃分析(Cong et al. 2024)4)显示,与安慰剂组相比,替妥木单抗组:
主要不良事件包括听力障碍(高频听力下降)、高血糖和肌肉痉挛,需注意监测4)。
美国甲状腺协会(ATA)和欧洲甲状腺协会(ETA)的联合立场声明推荐将其用于活动性中重度TED。
Bartalena L, Kahaly GJ, Baldeschi L, et al. The 2021 European Group on Graves’ Orbitopathy (EUGOGO) clinical practice guidelines for the medical management of Graves’ orbitopathy. Eur J Endocrinol. 2021;184(4):G43-G67.
Douglas RS, Kahaly GJ, Patel A, et al. Teprotumumab for the treatment of active thyroid eye disease. N Engl J Med. 2020;382(4):341-352.
Smith TJ, Kahaly GJ, Ezra DG, et al. Teprotumumab for thyroid-associated ophthalmopathy. N Engl J Med. 2017;376(18):1748-1761.
Cong X, Pei L, Hu H. Teprotumumab for treating active thyroid eye disease: A meta-analysis. Medicine (Baltimore). 2024;103(xx):eXXXXX.
Bahn RS. Graves’ ophthalmopathy. N Engl J Med. 2010;362(8):726-738.
Wiersinga WM, Bartalena L. Epidemiology and prevention of Graves’ ophthalmopathy. Thyroid. 2002;12(10):855-860.
Stan MN, Salvi M. Management of thyroid eye disease. J Clin Endocrinol Metab. 2017;102(11):4088-4100.
Bahn RS. Pathophysiology of Graves’ ophthalmopathy: the cycle of disease. J Clin Endocrinol Metab. 2003;88(5):1939-1946.
Mourits MP, Koornneef L, Wiersinga WM, et al. Clinical criteria for the assessment of disease activity in Graves’ ophthalmopathy: a novel approach. Br J Ophthalmol. 1989;73(8):639-644.
Salvi M, Vannucchi G, Curro N, Campi I, Covelli D, Dazzi D, et al. Efficacy of B-cell targeted therapy with rituximab in patients with active moderate to severe Graves’ orbitopathy: a randomized controlled study. J Clin Endocrinol Metab. 2015;100(2):422-431. PMCID: PMC4318899. doi:10.1210/jc.2014-3014.
Kahaly GJ, Pitz S, Hommel G, et al. Randomized, single blind trial of intravenous versus oral steroid monotherapy in Graves’ orbitopathy. J Clin Endocrinol Metab. 2005;90(9):5234-5240.
Prummel MF, Wiersinga WM. Smoking and risk of Graves’ disease. JAMA. 1993;269(4):479-482.
Marcocci C, Kahaly GJ, Krassas GE, et al. Selenium and the course of mild Graves’ orbitopathy. N Engl J Med. 2011;364(20):1920-1931.
Rundle FF, Wilson CW. Development and course of exophthalmos and ophthalmoplegia in Graves’ disease with special reference to the effect of thyroidectomy. Clin Sci. 1945;5:177-194.
Wakelkamp IM, Baldeschi L, Saeed P, et al. Surgical or medical decompression as a first-line treatment of optic neuropathy in Graves’ ophthalmopathy? A randomized controlled trial. Clin Endocrinol. 2005;63(3):323-328.
Garrity JA, Bahn RS. Pathogenesis of Graves’ orbitopathy: implications for prediction, prevention, and treatment. Am J Ophthalmol. 2006;142(1):147-153.
Kabra A, Higuchi K, Sheth A, et al. Tocilizumab in refractory thyroid eye disease: a case series. Ophthalmology. 2018;125(9):1326-1328.
Ugradar S, Rootman DB. Advances in orbital decompression for thyroid eye disease. Curr Opin Ophthalmol. 2021;32(5):454-460.