眼球突出
特征:缓慢进展、单眼、无痛
方式:因肌锥内肿块,典型表现为轴性突出
测量:使用Hertel眼球突出计评估左右差异。

眼眶海绵状血管瘤(orbital cavernous hemangioma)是一种来源于血管内皮的良性肿瘤,是成人眼眶肿瘤中最具代表性的良性肿块。它形成边界清晰、有包膜的实性肿块,好发于肌锥内(眼眶外眼肌形成的锥形空间内)。
组织学上,血管瘤分为多形性血管瘤(血管壁所有成分均发生肿瘤化)和单形性血管瘤(仅一种成分发生肿瘤化)。海绵状血管瘤属于单形性血管瘤,由海绵状血管腔构成。
从年龄分布来看,不同年龄段的血管性眼眶肿瘤好发类型不同。婴儿期以毛细血管瘤最多见,儿童期常见淋巴管瘤。相比之下,海绵状血管瘤好发于成人,尤其是3050岁。女性略多,男女比例约为1:1.41:2。
在近年国际血管异常研究学会(ISSVA)分类的修订中,有观点提出将传统上归类为“肿瘤”的海绵状血管瘤重新分类为低流量血管畸形(静脉畸形)[1,7]。然而,临床实践中仍广泛使用“海绵状血管瘤”这一名称,因此本文也采用此名称。
它是良性肿瘤,恶性转化极为罕见。它是一个有包膜的边界清晰的肿块,不侵犯周围组织。绝大多数血管瘤在组织学上是良性的,但极少数可能表现出复发或周围组织破坏等恶性特征。适当的诊断和治疗选择可改善预后。完全切除后复发极为罕见,预后通常良好。
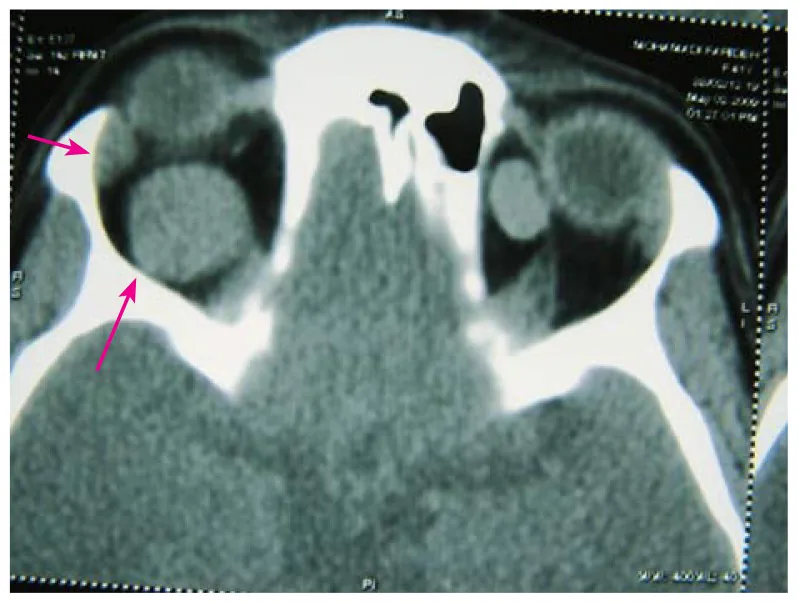
眼眶海绵状血管瘤生长缓慢,症状在数月至数年间逐渐进展。急剧增大罕见,但发生肿瘤内出血时可能导致相对快速的增大。
典型的自觉症状如下:
此外,无症状而在影像检查中偶然发现的病例也不少见。此类病例的基本处理原则是观察。
眼球突出量用Hertel眼球突出计测量。眼底检查时,可能因肿块压迫眼球壁而出现脉络膜皱襞。
眼球突出
特征:缓慢进展、单眼、无痛
方式:因肌锥内肿块,典型表现为轴性突出
测量:使用Hertel眼球突出计评估左右差异。
视力下降和复视
视力下降:由视神经受压引起。在眶尖部肿瘤中尤为明显。
复视:由眼外肌受压和移位引起。
病程:多为缓慢进展型。快速恶化提示肿瘤内出血。
影像学特征
CT:边界清晰、均匀的实性肿块。好发于肌锥内。
MRI动态增强:特征性延迟强化。
超声:包膜高回声,内部连续棘状高回声。
眼眶原发性肿瘤中最常见的是淋巴增殖性疾病,占所有眼眶肿瘤的50%~60%。眼眶海绵状血管瘤是仅次于淋巴增殖性疾病的常见良性眼眶肿瘤,是成人中最常见的良性眼眶肿瘤。
好发年龄为30~50岁,儿童罕见(儿童好发毛细血管瘤和淋巴管瘤)。性别方面,有报道女性略多,但大规模流行病学数据有限。
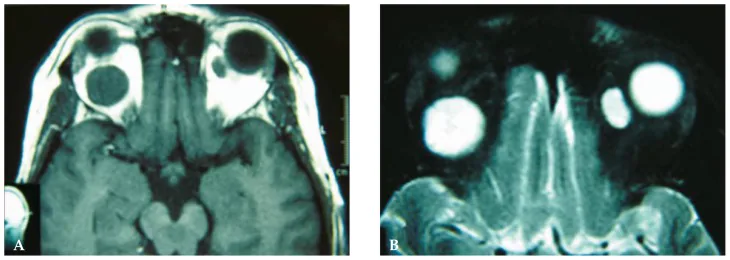
眼眶海绵状血管瘤的诊断主要依靠CT和MRI等影像学检查。影像学检查对于确诊必不可少,需要脑血管造影的病例很少。
影像学上,良性肿瘤通常边界清晰,不侵犯正常组织。而恶性肿瘤和炎性疾病常表现为边界不清和浸润性模式,有助于鉴别。
| 检查方法 | 表现 | 特征与注意事项 |
|---|---|---|
| CT | 边界清晰、均匀的实性肿块 | 好发于肌锥内。钙化罕见。增强CT呈均匀强化。 |
| MRI T1/T2 | T1低至等信号,T2高信号 | 边界清晰、均匀。内部信号强度均匀。 |
| MRI动态增强 | 延迟强化(渐进性强化) | 该病最具特征性。早期不均匀→随时间逐渐均匀强化。 |
| 超声(A型) | 包膜高回声 + 内部连续刺状高回声 | high internal reflectivity with regular pattern |
| 超声(B型) | 边界清晰的实性肿块 | 可观察到包膜回声的高反射 |
MRI动态成像中的延迟强化(gradual enhancement / progressive filling)是眼眶海绵状血管瘤最具特征的影像学表现[3,4,6]。造影剂注射早期,肿瘤内部信号不均匀(强化从一点或一部分开始),部分区域不强化。随时间推移,强化范围扩大,最终整个肿瘤均匀强化。这种延迟模式反映了肿瘤内缓慢的血流,与神经鞘瘤早期广泛强化形成对比,对于与其他眼眶肿瘤的鉴别很重要[3,4]。
在A型超声中,肿瘤前壁可见代表包膜的高反射,肿瘤内部可见连续刺状高反射。这种表现称为high internal reflectivity with regular pattern,是海绵状血管瘤的特征。
以下是眼眶海绵状血管瘤的主要鉴别诊断和鉴别要点。
| 鉴别疾病 | 鉴别要点 |
|---|---|
| 神经鞘瘤 | 在肌锥内难以鉴别。MRI T2加权像上呈不均匀高信号(常有囊性变)。动态MRI上呈早期强化倾向。 |
| 眼眶静脉曲张 | Valsalva动作(屏气)时肿块增大、突出加重。体位改变时变化。 |
| 淋巴管瘤 | 好发于儿童。多房性、可见液平。反复自发性出血。 |
| 泪腺多形性腺瘤 | 局限于泪腺窝(眼眶外上方)。可伴有骨压迫变形。 |
细针穿刺抽吸细胞学检查(FNA)常仅抽吸到血液成分,诊断价值低。
MRI动态增强扫描中的延迟强化(gradual enhancement)是最特征性的表现。造影剂注射早期,肿块内部不均匀,部分不强化,但随时间推移均匀强化。这反映了肿块内部缓慢的血流。A型超声上的包膜高回声加内部刺状高回声的连续模式也具有特征性。结合多种检查手段可提高诊断准确性。
眼眶海绵状血管瘤是良性肿瘤,无症状病例以观察随访为基本原则。定期进行影像学检查(MRI或CT)监测肿瘤是否增大。
手术适应症如下:
在罕见的儿童病例中,若担心影响视力发育,或复视严重干扰日常生活时,应考虑早期手术干预。
外侧开眶术(标准术式)
适应证:肌锥内的肿瘤。适用于大多数病例。
操作:颞部皮肤切口→颞肌剥离→外侧眶壁骨切开→进入肌锥内肿瘤。
要点:完整切除肿瘤(en bloc resection),不破坏包膜。包膜损伤会增加术中出血和不完全切除的风险。
前方/经结膜入路
适应证:位于眼眶前部的小型肿瘤。
特点:创伤相对较小。无需外侧眶壁骨切开。
经结膜入路:对于小型肿瘤,可选择创伤更小的入路。
观察的适应证
条件:无症状,且对视觉功能无影响。
管理:定期影像检查(每6-12个月)确认增大情况。
干预指征:出现视力下降、复视或明显眼球突出时考虑手术。
大多数病例可通过外侧开眶术(lateral orbitotomy)切除肿瘤[2,5]。手术要点如下。
完整保留包膜是最重要的要点。 如果包膜破裂,肿瘤内的血液成分会流出,导致术野不清,难以完全切除。保留包膜可使肿瘤安全地整块切除。
主要并发症包括以下内容:
术后一过性眼球运动障碍多随时间改善[2,5]。术前无视力下降者,术后视功能保持良好。一项164例的大规模队列研究报告,术后视力、视野、复视、眼球突出和眼球运动均有显著改善[2]。
可以。由于是良性肿瘤,若无视力障碍、眼球运动障碍或明显眼球突出,观察是基本方针。当出现增大趋势或对视功能产生影响时,再考虑手术。对于无症状偶然发现的病例,常通过定期影像检查(MRI或CT)确认肿瘤无增大来随访。
若能完整切除而不破坏包膜,复发极为罕见。由于包膜清晰,完全切除率高。但包膜损伤导致的不完全切除是复发风险,因此术中保护包膜至关重要。少数肿瘤可表现为恶性特征如复发或周围组织破坏,建议适当随访。
眼眶海绵状血管瘤是一种来源于血管内皮细胞的良性肿瘤。整个肿瘤被纤维包膜包裹,内部由海绵状扩张的血管腔(海绵状腔隙)集合构成。
血管腔的内壁由血管内皮细胞覆盖,腔内充满血液。血管腔之间的隔膜由纤维结缔组织和平滑肌样细胞组成。这种结构赋予肿瘤特有的柔软橡胶样质地。
肿瘤内的血管腔形成封闭系统,与全身循环的交通有限。因此,造影剂流入肿瘤缓慢,这是动态MRI上观察到延迟强化(渐进性强化)的原因。
造影剂从肿瘤周边逐渐渗透,最终均匀地使整个肿瘤强化。这种“从周边到中心的渐进性强化模式”是海绵状血管瘤的特征,有助于与早期即均匀强化的眼眶肿瘤(如部分神经鞘瘤或转移性肿瘤)鉴别。
通常生长缓慢,被认为是由血液在血管腔内缓慢积聚所致。恶性转化的报道极为罕见。
瘤内出血(内部出血)可导致快速增大。这是因为肿瘤内血管腔破裂导致血液积聚,引起急性眼球突出、视力下降和疼痛。在这种情况下,可能需要紧急手术。
在2018年ISSVA(国际血管异常研究学会)分类修订中,提出将海绵状血管瘤重新分类为“静脉畸形”。这是基于静脉畸形是血管结构的先天性畸形而非血管内皮异常增殖的理解。免疫组织化学研究也报告了提示成人包膜海绵状病变与婴儿血管瘤发病机制不同的发现[7]。这一分类变化可能影响治疗策略和疾病理解,但眼眶“海绵状血管瘤”在临床上是否适合重新分类仍存在争议[1]。
随着ISSVA分类修订,关于将传统上归类为“肿瘤”的眼眶海绵状血管瘤重新分类为“低流量静脉畸形”的讨论仍在继续。这种重新分类是否具有临床意义(例如硬化疗法的适应症)需要在眼眶疾病中进行大规模比较研究。
经鼻内镜入路已被报道为位于眼眶内侧(鼻侧)肿瘤的微创技术。它不需要外侧眼眶壁截骨,术后美容问题较少,但需要内镜手术的技术熟练度,适应症有限。
已有报道尝试使用MRI弥散加权成像(DWI)和表观弥散系数(ADC)值来鉴别眼眶肿瘤的良恶性。海绵状血管瘤被认为具有较高的ADC值,可能有助于与恶性肿瘤鉴别,但在眼眶区域的大规模验证仍不充分。
眼眶海绵状血管瘤的自然消退极为罕见,但有个别病例报告。有研究表明其可能与妊娠后或女性激素波动有关,但机制尚未明确,尚未确立为无症状病例继续观察的依据。
Calandriello L, Grimaldi G, Petrone G, et al. Cavernous venous malformation (cavernous hemangioma) of the orbit: Current concepts and a review of the literature. Surv Ophthalmol. 2017;62(4):393-403. doi:10.1016/j.survophthal.2017.01.004. PMID: 28131871
Strianese D, Bonavolontà G, Iuliano A, et al. Risks and Benefits of Surgical Excision of Orbital Cavernous Venous Malformations (So-Called Cavernous Hemangioma): Factors Influencing the Outcome. Ophthalmic Plast Reconstr Surg. 2021;37(3):248-254. doi:10.1097/IOP.0000000000001767. PMID: 32826827
Tanaka A, Mihara F, Yoshiura T, et al. Differentiation of cavernous hemangioma from schwannoma of the orbit: a dynamic MRI study. AJR Am J Roentgenol. 2004;183(6):1799-1804. doi:10.2214/ajr.183.6.01831799. PMID: 15547232
Xian J, Zhang Z, Wang Z, et al. Evaluation of MR imaging findings differentiating cavernous haemangiomas from schwannomas in the orbit. Eur Radiol. 2010;20(9):2221-2228. doi:10.1007/s00330-010-1774-y. PMCID: PMC2914262
Kim MH, Kim JH, Kim SE, Yang SW. Surgical Outcomes of Intraconal Cavernous Venous Malformation According to Their Location in Four Right-Angled Sectors. J Craniofac Surg. 2019;30(6):1700-1705. doi:10.1097/SCS.0000000000005501. PMID: 30950949
Zhang L, Li X, Tang F, Gan L, Wei X. Diagnostic Imaging Methods and Comparative Analysis of Orbital Cavernous Hemangioma. Front Oncol. 2020;10:577452. doi:10.3389/fonc.2020.577452. PMCID: PMC7539693
Osaki TH, Jakobiec FA, Mendoza PR, Lee Y, Fay AM. Immunohistochemical investigations of orbital infantile hemangiomas and adult encapsulated cavernous venous lesions (malformation versus hemangioma). Ophthalmic Plast Reconstr Surg. 2013;29(3):183-195. doi:10.1097/IOP.0b013e31828b0f1f. PMID: 23584448