Triệu chứng mi mắt
Phù mi trên, co rút mi trên và chậm mi trên là các đặc điểm điển hình.
Dấu hiệu Dalrymple: Khe mi mở rộng do co rút mi trên.
Dấu hiệu von Graefe: chậm hạ mi mắt trên khi nhìn xuống (lid lag).

Bệnh mắt tuyến giáp (thyroid eye disease: TED) là một bệnh tự miễn, trong đó rối loạn chức năng miễn dịch liên quan đến rối loạn chức năng tuyến giáp gây viêm các mô trong hốc mắt, làm tăng thể tích mỡ hốc mắt và cơ ngoại nhãn. Áp lực sau nhãn cầu tăng dẫn đến lồi mắt. Thường xảy ra cùng với cường giáp (bệnh Graves/Basedow), nhưng cũng có thể xảy ra khi chức năng tuyến giáp bình thường (bệnh mắt tuyến giáp với chức năng tuyến giáp bình thường). Bệnh mắt tuyến giáp tiến triển độc lập với hormone tuyến giáp và là một trong những bệnh tự miễn liên quan đến tự kháng thể tuyến giáp.
Khoảng 40-50% bệnh nhân mắc bệnh Graves (Basedow) có triệu chứng mắt. Tổn thương hốc mắt nặng tương đối hiếm, xảy ra ở 5-10% tổng số bệnh nhân Graves.
Tỷ lệ mắc bệnh là 16/100.000 người-năm ở nữ và 2,9/100.000 người-năm ở nam1). Tuổi khởi phát có hai đỉnh: 40-50 tuổi và 60-70 tuổi1). Hút thuốc lá là yếu tố nguy cơ lớn nhất của bệnh mắt tuyến giáp, làm tăng đáng kể nguy cơ mắc bệnh2). Có một mô hình theo tuổi: lồi mắt là triệu chứng chính ở người trẻ, trong khi song thị là triệu chứng chính ở người cao tuổi.
Diễn tiến tự nhiên của bệnh mắt tuyến giáp tuân theo đường cong Rundle, chuyển từ giai đoạn hoạt động (viêm, thường 1-3 năm) sang giai đoạn ổn định (không viêm)3). Thời điểm can thiệp điều trị được xác định dựa trên đường cong này.
Triệu chứng mi mắt
Phù mi trên, co rút mi trên và chậm mi trên là các đặc điểm điển hình.
Dấu hiệu Dalrymple: Khe mi mở rộng do co rút mi trên.
Dấu hiệu von Graefe: chậm hạ mi mắt trên khi nhìn xuống (lid lag).
Lồi mắt
Thường gặp ở người trẻ (tổ chức nâng đỡ hốc mắt yếu).
Được đánh giá bằng thước đo nhãn cầu Hertel. Giá trị bình thường ở người Nhật là 10–15 mm (trung bình 13 mm). Chênh lệch hai mắt trong vòng 2 mm được coi là bình thường.
Song thị
Thường gặp ở người cao tuổi. Nguyên nhân do lác hạn chế vì viêm và xơ hóa cơ ngoại nhãn.
Cơ trực dưới bị ảnh hưởng nhiều nhất → hạn chế đưa mắt lên trên là phổ biến nhất. Tiếp theo là hạn chế đưa mắt ra ngoài do liên quan đến cơ trực trong.
Suy giảm thị lực
Do bệnh lý giác mạc (bệnh lý giác mạc do hở mi) hoặc bệnh thần kinh thị giác do chèn ép (DON).
DON xảy ra ở khoảng 5% tổng số ca1) và cần can thiệp khẩn cấp. Các dấu hiệu bao gồm RAPD dương tính, giảm CFF và khiếm khuyết thị trường.
Có thể xảy ra ngay cả khi chức năng tuyến giáp bình thường, được gọi là bệnh mắt do tuyến giáp thể euthyroid. Bệnh mắt do tuyến giáp là một bệnh tự miễn tiến triển độc lập với nồng độ hormone tuyến giáp và có thể xảy ra nếu tự kháng thể liên quan đến tuyến giáp (TRAb, TSAb) dương tính. Nếu có dấu hiệu co rút mi hoặc lồi mắt, cần xét nghiệm tự kháng thể liên quan đến tuyến giáp ngay cả khi chức năng tuyến giáp bình thường.
Giai đoạn sớm, triệu chứng chính là khô mắt, kích ứng, chảy nước mắt và sợ ánh sáng. Khi bệnh tiến triển, xuất hiện phù quanh hốc mắt, lồi mắt, song thị và co rút mi. Trường hợp nặng có thể dẫn đến loét giác mạc và bệnh thần kinh thị giác do chèn ép.
Dưới đây là các dấu hiệu mi mắt đặc trưng của bệnh mắt do tuyến giáp.
| Tên dấu hiệu | Tên tiếng Anh | Dấu hiệu |
|---|---|---|
| Dấu hiệu Dalrymple | Dấu hiệu Dalrymple | Mở rộng khe mi do co rút mi trên, phần trắng của mắt lộ ra phía trên rìa giác mạc trên |
| Dấu hiệu von Graefe | Lid lag | Hiện tượng mi trên chậm theo kịp khi nhìn xuống |
| Dấu hiệu Stellwag | Dấu hiệu Stellwag | Giảm chớp mắt và nhắm mắt không hoàn toàn |
| Dấu hiệu Gifford | Dấu hiệu Gifford | Khó lật mí mắt trên |
Lồi mắt được đo bằng thước đo nhãn cầu Hertel. Giá trị bình thường ở người Nhật là 10–15 mm (trung bình 13 mm), chênh lệch giữa hai mắt ≤2 mm được coi là bình thường. Giá trị Hertel >18 mm gợi ý lồi mắt1).
Xảy ra do các cơ ngoại nhãn dày lên chèn ép dây thần kinh thị giác tại đỉnh hốc mắt (orbital apex). Gặp ở khoảng 5% tổng số ca1) và là cấp cứu. RAPD (khiếm khuyết đồng tử hướng tâm tương đối) dương tính, giảm CFF (tần số hòa nhập tới hạn) và khiếm khuyết thị trường là các dấu hiệu sớm. Rối loạn sắc giác cũng là một dấu hiệu quan trọng.
Đau, song thị và thay đổi ngoại hình là những yếu tố chính làm giảm chất lượng cuộc sống. Tỷ lệ lo âu và trầm cảm ở bệnh nhân bệnh mắt do tuyến giáp là 36%, gần gấp đôi dân số chung (18,9%) 5). 62% bệnh nhân trung bình và 89% bệnh nhân nặng có suy giảm chất lượng cuộc sống cao (điểm ≥4/7) 5). Sự suy giảm chất lượng cuộc sống tương đương hoặc thấp hơn so với bệnh tiểu đường, khí phế thũng và suy tim đã được báo cáo.
Xảy ra do lác hạn chế gây ra bởi phì đại và co rút các cơ ngoại nhãn (đặc biệt là cơ trực dưới) do viêm và xơ hóa, hạn chế chuyển động mắt bình thường. Cơ trực dưới thường bị ảnh hưởng nhất, do đó rối loạn nâng nhãn cầu là phổ biến nhất. Thứ tự tần suất liên quan của các cơ ngoại nhãn là: cơ trực dưới > cơ trực trong > cơ trực trên > cơ trực ngoài, và thường gặp ở người cao tuổi.
Các bất thường miễn dịch liên quan đến rối loạn chức năng tuyến giáp kích hoạt viêm các mô trong hốc mắt. Các tự kháng thể kháng thụ thể TSH (TRAb) kích hoạt TSHR trên nguyên bào sợi hốc mắt, kích thích sản xuất các cytokine viêm (TNF-α, IL-6, IL-1β, v.v.). Tế bào T CD4+/CD8+ xâm nhập mô hốc mắt và khuếch đại phản ứng viêm.
Các nguyên bào sợi được kích hoạt tăng tổng hợp glycosaminoglycan và axit hyaluronic, gây phù nề mô và giữ nước. Sự biệt hóa của nguyên bào sợi thành tế bào mỡ và nguyên bào sợi cơ dẫn đến mở rộng mỡ hốc mắt và xơ hóa cơ ngoại nhãn3).
Thụ thể IGF-1 (IGF-1R) tạo phức hợp với TSHR và tham gia một cách hiệp đồng vào việc kích hoạt nguyên bào sợi hốc mắt 4). Cơ chế này là mục tiêu điều trị của teprotumumab (thuốc ức chế IGF-1R).
Hút thuốc lá là yếu tố nguy cơ lớn nhất, liên quan đến nguy cơ khởi phát, mức độ nặng và kháng điều trị 2). Ngoài ra, sự bất ổn định chức năng tuyến giáp, giai đoạn cấp sau điều trị i-ốt phóng xạ, tuổi cao và giới tính nam cũng góp phần vào nguy cơ nặng.
Nếu có ba dấu hiệu: co rút mi mắt, lồi mắt và song thị, thì về mặt lâm sàng gợi ý mạnh mẽ bệnh mắt liên quan tuyến giáp (TED). Ngay cả khi chức năng tuyến giáp bình thường, vẫn có thể chẩn đoán TED nếu tự kháng thể liên quan đến tuyến giáp dương tính.
Đo hormone tuyến giáp (FT₄, FT₃), TSH và tự kháng thể tuyến giáp. Các đối tượng đo bao gồm TRAb (kháng thể thụ thể TSH), TSAb (kháng thể kích thích tuyến giáp), kháng thể kháng TG (kháng thể kháng thyroglobulin) và kháng thể kháng TPO (kháng thể kháng peroxidase tuyến giáp). Một trong các kháng thể này sẽ dương tính.
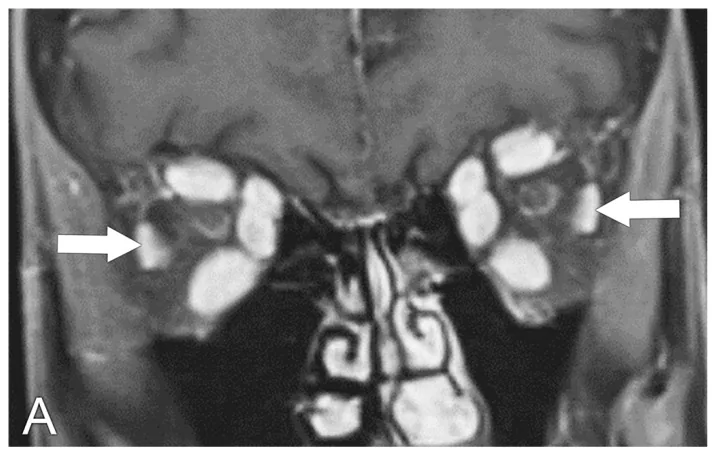
MRI (lựa chọn đầu tiên): Đánh giá hình thái cơ ngoài nhãn cầu trên hình ảnh T1-weighted. Phương pháp STIR (short-TI inversion recovery) mô tả vùng viêm là vùng tín hiệu cao, hữu ích để đánh giá hoạt động viêm. Mặt cắt vành là bắt buộc vì có thể đánh giá đồng thời tất cả các cơ ngoài nhãn cầu ngoại trừ cơ chéo dưới. Mặt cắt ngang đánh giá cơ trực trong và cơ trực ngoài.
CT: Cho thấy phì đại cơ ngoại nhãn (kiểu phì đại bụng cơ trong khi gân được bảo tồn là đặc trưng của TED), và sử dụng cửa sổ xương để đánh giá thành hốc mắt.
Siêu âm B-scan: Được sử dụng hỗ trợ để đánh giá phì đại cơ ngoại nhãn.
Hệ thống tính điểm 7 mục (0-7 điểm) để đánh giá hoạt động viêm do Mourits và cộng sự đề xuất năm 1989 6).
7 mục đánh giá: ① Đau sau nhãn cầu tự phát, ② Đau khi cử động mắt, ③ Đỏ mi mắt, ④ Sưng mi mắt, ⑤ Đỏ kết mạc, ⑥ Phù kết mạc, ⑦ Sưng lệ đạo/nếp bán nguyệt.
CAS ≥ 3/7 được coi là giai đoạn hoạt động và là chỉ định điều trị xung steroid. CAS ≥ 4/7 là tiêu chuẩn đưa vào thử nghiệm lâm sàng ngẫu nhiên của teprotumumab.
| Mức độ nặng | Tiêu chí | Hướng điều trị |
|---|---|---|
| Nhẹ | Ảnh hưởng nhẹ đến sinh hoạt hàng ngày | Bổ sung selen + theo dõi |
| Trung bình đến nặng | Co mi mắt ≥2 mm, lồi mắt ≥3 mm so với bình thường, song thị | Liệu pháp xung steroid, teprotumumab |
| Đe dọa thị lực | Bệnh thần kinh thị giác do chèn ép, loét giác mạc | Phẫu thuật giảm áp hốc mắt khẩn cấp hoặc steroid liều cao |
Phân loại theo EUGOGO (Nhóm Bệnh mắt Graves châu Âu) dựa trên hướng dẫn thực hành lâm sàng năm 2021 1). Phân loại NOSPECS (lớp 0–6) và VISA (Thị lực, Viêm, Lác, Diện mạo) cũng được sử dụng để đánh giá mức độ nặng.
| Bệnh cần phân biệt | Điểm phân biệt | Hình ảnh học |
|---|---|---|
| Bệnh mắt liên quan đến IgG4 | Phì đại tuyến lệ + phì đại cơ ngoại nhãn, IgG4 huyết thanh cao | Phì đại lan tỏa tuyến lệ và cơ ngoại nhãn |
| Viêm cơ ngoài nhãn cầu (viêm cơ hốc mắt) | Khởi phát cấp tính, đau dữ dội | Dày lên ở vùng gân (trong bệnh mắt do tuyến giáp, dày lên ở bụng cơ và gân được bảo tồn) |
| U hốc mắt, u di căn | Một bên, tiến triển | Hình thành khối |
Đây là hệ thống tính điểm 7 mục (0-7 điểm) để đánh giá hoạt động viêm của bệnh mắt tuyến giáp. Bảy mục được đánh giá bao gồm: ① đau sau nhãn cầu tự phát, ② đau khi cử động mắt, ③ đỏ mi mắt, ④ sưng mi mắt, ⑤ đỏ kết mạc, ⑥ phù kết mạc, ⑦ sưng lệ đạo/nếp bán nguyệt. Điểm ≥3 được coi là giai đoạn hoạt động. Đây là chỉ số quan trọng để lựa chọn điều trị, được sử dụng để xác định chỉ định điều trị bằng steroid xung hoặc teprotumumab.
Bình thường hóa chức năng tuyến giáp là điều kiện tiên quyết, và sự phối hợp với khoa nội tiết là không thể thiếu. Tư vấn cai thuốc lá được thực hiện ở tất cả các trường hợp để loại bỏ hút thuốc, yếu tố nguy cơ lớn nhất gây bệnh nặng hơn và kháng điều trị.
Bổ sung selen: Bổ sung selen 200 μg/ngày trong 6 tháng có lợi và được khuyến cáo để cải thiện hoạt động bệnh ở TED nhẹ10).
Bảo vệ giác mạc và bề mặt mắt: Sử dụng thường xuyên nước mắt nhân tạo và thuốc nhỏ bảo vệ giác mạc, đồng thời bôi thuốc mỡ mắt trước khi ngủ là cơ bản. Trong trường hợp mắt hở nặng, cân nhắc khâu mi ngoài (lateral tarsorrhaphy).
Liệu pháp xung steroid (lựa chọn đầu tiên): Tiêm methylprednisolone 500–1000 mg/tuần trong 6–12 tuần1). Steroid đường tĩnh mạch hiệu quả hơn đường uống9). Liều tích lũy khuyến cáo ≤8 g (để giảm nguy cơ tổn thương gan).
Phác đồ chuẩn: Một đợt methylprednisolone 1 g × 3 ngày.
Prednisolone đường uống: Trong trường hợp trung bình đến nặng khó tiêm tĩnh mạch, bắt đầu với 1 mg/kg/ngày.
Tiêm steroid tại chỗ: Đối với phù mi trên và co rút mi viêm, tiêm tại chỗ triamcinolone acetonide (Kenacort-A® 1 ống) có hiệu quả.
Teprotumumab (thuốc ức chế IGF-1R): Là thuốc điều trị có thể cải thiện lồi mắt và song thị ở bệnh nhân TED hoạt động mức độ trung bình đến nặng. Phân tích gộp từ 5 RCT (tổng cộng 411 ca) cho thấy giảm lồi mắt đáng kể, cải thiện tỷ lệ đạt CAS 0–1 ở tuần 24 và cải thiện song thị đáng kể 4), mà không tăng đáng kể các tác dụng phụ nghiêm trọng. Bằng chứng được xây dựng từ hai RCT chính: Smith et al. (2017, 42 ca so với 45 ca) 7) và Douglas et al. (2020, 41 ca so với 42 ca) 8).
Rituximab (kháng thể đơn dòng kháng CD20): Một thử nghiệm ngẫu nhiên đa trung tâm đã chỉ ra khả năng làm giảm hoạt động bệnh ở TED mức độ trung bình đến nặng kháng trị12).
Tocilizumab (thuốc ức chế thụ thể IL-6): Được xem xét sử dụng trong các trường hợp kháng steroid và rituximab.
Trong TED từ trung bình đến nặng, xạ trị hốc mắt được thực hiện kết hợp với liệu pháp ức chế miễn dịch. Thông thường, chiếu 20 Gy/10 phân đoạn trong 2 tuần. Kết hợp với steroid được cho là hiệu quả hơn so với đơn trị liệu.
Phẫu thuật về nguyên tắc được lên kế hoạch sau khi bước vào giai đoạn ổn định của đường cong Rundle và tình trạng viêm đã lắng dịu. Trình tự thực hiện phải được tuân thủ nghiêm ngặt, vì kết quả của phẫu thuật trước ảnh hưởng trực tiếp đến kế hoạch phẫu thuật sau.
Bước 1: Giảm áp Ổ mắt
Chỉ định: Lồi mắt nặng, bệnh thần kinh thị giác do chèn ép (chỉ định cấp cứu)
Kỹ thuật và Kết quả: Có 5 kỹ thuật dựa trên sự kết hợp của thành trong, sàn, thành ngoài và mỡ. Giảm áp một thành giúp cải thiện lồi mắt -1,4 đến -2,3 mm, giảm áp ba thành kèm mỡ giúp cải thiện -4,6 đến -5,0 mm.
Một nghiên cứu đa trung tâm trên 633 mắt xác nhận tính ổn định và khả năng tái lập mà không có sự khác biệt đáng kể giữa các phẫu thuật viên cho cùng một kỹ thuật11).
Bước 2: Phẫu thuật lác
Chỉ định: Song thị và rối loạn vận động nhãn cầu sau khi giai đoạn không viêm ổn định
Kỹ thuật cơ bản: Phẫu thuật lùi cơ thẳng dưới là phổ biến nhất. Lượng phẫu thuật được xác định dựa trên mức độ lác hạn chế.
Cũng được thực hiện để điều trị song thị mới xuất hiện (khoảng 30%) sau phẫu thuật giảm áp hốc mắt.
Bước 3: Phẫu thuật mí mắt
Chỉ định: Co rút mí mắt ở giai đoạn không viêm ổn định, vấn đề chức năng hoặc thẩm mỹ
Kỹ thuật phẫu thuật: Đối với co rút mi trên, lựa chọn cắt cơ Müller hoặc đẩy lùi cơ nâng mi trên. Sự kết hợp giữa cắt cơ Müller và đẩy lùi cơ nâng mi đã được báo cáo cho kết quả tốt.
Lên kế hoạch sau khi các thay đổi sau phẫu thuật giảm áp hốc mắt và phẫu thuật lác đã ổn định.
Phẫu thuật được thực hiện theo thứ tự: giảm áp hốc mắt → phẫu thuật lác → phẫu thuật mí mắt. Điều quan trọng là phải tuân theo thứ tự này vì kết quả của phẫu thuật trước ảnh hưởng đến kế hoạch phẫu thuật sau. Về nguyên tắc, tất cả các phẫu thuật đều được lên kế hoạch sau khi bước vào giai đoạn không viêm (giai đoạn ổn định của đường cong Rundle). Thực hiện phẫu thuật trong giai đoạn viêm làm tăng nguy cơ biến động sau phẫu thuật và tái phát.
Đây là một kháng thể đơn dòng ức chế thụ thể IGF-1 (IGF-1R). Nó ngăn chặn tín hiệu phức hợp IGF-1R và TSHR trên nguyên bào sợi hốc mắt, ức chế viêm và phù nề mô. Một phân tích tổng hợp từ 5 RCT (tổng cộng 411 ca) đã xác nhận cải thiện đáng kể về lồi mắt, song thị và CAS. Không có sự gia tăng đáng kể các tác dụng phụ nghiêm trọng, nhưng độ an toàn lâu dài (rối loạn thính giác, tăng đường huyết, v.v.) vẫn đang được đánh giá.
Rối loạn chức năng miễn dịch liên quan đến rối loạn chức năng tuyến giáp gây viêm các mô trong hốc mắt, làm tăng thể tích mô mỡ hốc mắt và cơ ngoại nhãn. Áp lực sau nhãn cầu tăng dẫn đến lồi mắt.
Bệnh lý mô mỡ hốc mắt: Tế bào mỡ phì đại và thâm nhiễm tế bào lympho ở mô kẽ, kèm phù nề và hình thành sẹo do viêm mạn tính. Tăng tổng hợp glycosaminoglycan (GAG) và axit hyaluronic gây ứ dịch và sưng mô.
Bệnh lý cơ ngoại nhãn: Có thâm nhiễm tế bào viêm chủ yếu là tế bào lympho giữa các sợi cơ vân, gây thoái hóa và hoại tử sợi cơ. Phù nề và dày mô kẽ xảy ra do viêm, và mô liên kết tăng sinh giữa các sợi cơ, dẫn đến phì đại cơ ngoại nhãn. Cơ trực dưới thường bị ảnh hưởng nhất, tiếp theo là cơ trực trong, cơ trực trên và cơ trực ngoài. Do đó, rối loạn vận nhãn lên trên thường gặp nhất, tiếp theo là rối loạn dạng.
Xảy ra do hai cơ chế kết hợp.
① Bệnh lý cơ nâng mi trên: Phù nề tế bào cơ do viêm gây phù mi. Mô mỡ xâm nhập giữa các sợi cơ, và tế bào cơ bị hoại tử và sẹo hóa, làm thay đổi chức năng cơ nâng mi.
②Bệnh lý cơ Müller: Cơ Müller, một cơ trơn được chi phối bởi hệ thần kinh giao cảm, co thắt liên tục do tăng hoạt động giao cảm kèm theo cường giáp, nâng sụn mi và mở rộng khe mi.
Tự kháng thể thụ thể TSH (TRAb) kích hoạt TSHR trên nguyên bào sợi hốc mắt, thông qua tín hiệu xuôi dòng tạo ra các cytokine viêm (TNF-α, IL-6, IL-1β). Tế bào T CD4+/CD8+ xâm nhập mô hốc mắt và khuếch đại phản ứng viêm. Nguyên bào sợi được kích hoạt biệt hóa thành tế bào mỡ và nguyên bào sợi cơ, lần lượt gây giãn mỡ hốc mắt và xơ hóa cơ ngoại nhãn3).
IGF-1R (thụ thể IGF-1) tạo phức hợp với TSHR và tham gia hiệp đồng trong việc kích hoạt nguyên bào sợi hốc mắt4). Sự phong tỏa tín hiệu phức hợp này là cơ chế tác dụng của teprotumumab.
Quá trình chuyển đổi tự nhiên từ giai đoạn viêm hoạt động (thường 1-3 năm) sang giai đoạn ổn định (không viêm) đã được khái niệm hóa thành đường cong Rundle13). Can thiệp điều trị thực tế được lựa chọn sau khi đánh giá hoạt động và mức độ nghiêm trọng1). Trong giai đoạn hoạt động, ưu tiên điều trị ức chế viêm, và phẫu thuật được lên kế hoạch ở giai đoạn ổn định không viêm.
Sau khi được FDA phê duyệt, dữ liệu tiếp tục được tích lũy. Một phân tích tổng hợp từ 5 RCT (tổng cộng 411 ca) 4) đã xác nhận hiệu quả và độ an toàn, nhưng kết quả của thử nghiệm Giai đoạn IV về độ an toàn lâu dài (như suy giảm thính lực, tăng đường huyết) đang được chú ý. Khả năng mở rộng chỉ định cho TED giai đoạn không hoạt động cũng đang được xem xét.
Một nghiên cứu đa trung tâm với 7 cơ sở, 7 phẫu thuật viên và 633 mắt 11) xác nhận rằng không có sự khác biệt đáng kể giữa các phẫu thuật viên khi thực hiện cùng một quy trình. Đây là phát hiện quan trọng hỗ trợ tính hợp lệ thống kê của các RCT đa trung tâm. Giảm áp thành trong nội soi được báo cáo cải thiện độ lồi mắt lớn hơn đáng kể so với phẫu thuật mở trong giảm áp thành trong + sàn (-3,67 mm so với -2,97 mm, p=0,008). Mức độ lồi mắt trước phẫu thuật cũng được chứng minh có liên quan có ý nghĩa thống kê với sự thay đổi độ lồi mắt sau phẫu thuật (p<0,001), khẳng định lại tầm quan trọng của đánh giá trước phẫu thuật.
Sự biến động của TRAb và TSAb trong giai đoạn hoạt động được cho là tương quan với CAS, và nghiên cứu về lựa chọn điều trị dựa trên dấu ấn sinh học đang được tiến hành. Các RCT quy mô lớn về tocilizumab (thuốc ức chế IL-6) cho các trường hợp kháng trị cũng đang được chờ đợi.
Bartalena L, Kahaly GJ, Baldeschi L, et al. The 2021 European Group on Graves’ Orbitopathy (EUGOGO) clinical practice guidelines for the medical management of Graves’ orbitopathy. Eur J Endocrinol. 2021;184(4):G43-G67.
Prummel MF, Wiersinga WM. Smoking and risk of Graves’ disease. JAMA. 1993;269(4):479-482.
Bahn RS. Graves’ ophthalmopathy. N Engl J Med. 2010;362(8):726-738.
Cong X, Pei L, Hu H. Teprotumumab for treating active thyroid eye disease: a meta-analysis. Medicine. 2024;103(18):e38059.
Wang Y, Sharma A, Padnick-Silver L, et al. Physician-perceived impact of thyroid eye disease on patient quality of life in the United States. Ophthalmol Ther. 2021;10(1):75-87.
Mourits MP, Koornneef L, Wiersinga WM, et al. Clinical criteria for the assessment of disease activity in Graves’ ophthalmopathy: a novel approach. Br J Ophthalmol. 1989;73(8):639-644.
Smith TJ, Kahaly GJ, Ezra DG, et al. Teprotumumab for thyroid-associated ophthalmopathy. N Engl J Med. 2017;376(18):1748-1761.
Douglas RS, Kahaly GJ, Patel A, et al. Teprotumumab for the treatment of active thyroid eye disease. N Engl J Med. 2020;382(4):341-352.
Kahaly GJ, Pitz S, Hommel G, et al. Randomized, single blind trial of intravenous versus oral steroid monotherapy in Graves’ orbitopathy. J Clin Endocrinol Metab. 2005;90(9):5234-5240.
Marcocci C, Kahaly GJ, Krassas GE, Bartalena L, Prummel M, Stahl M, et al.; European Group on Graves’ Orbitopathy. Selenium and the course of mild Graves’ orbitopathy. N Engl J Med. 2011;364(20):1920-1931. PMID: 21591944. doi:10.1056/NEJMoa1012985.
Hong A, Shoji MK, Villatoro GA, et al. Intersurgeon variability in proptosis reduction after orbital decompression for thyroid eye disease: a multicenter analysis. Ophthalmic Plast Reconstr Surg. 2024;40(3).
Salvi M, Vannucchi G, Campi I, et al. Rituximab treatment in active moderate-to-severe Graves’ orbitopathy: an international, multicenter, single-blind, randomized placebo-controlled study. J Clin Endocrinol Metab. 2015;100(11):422-431.
Rundle FF, Wilson CW. Development and course of exophthalmos and ophthalmoplegia in Graves’ disease with special reference to the effect of thyroidectomy. Clin Sci. 1945;5(3-4):177-194. PMID: 21011937.