眼瞼症狀
特徵性表現為上眼瞼腫脹、上眼瞼退縮和上眼瞼遲落。
Dalrymple徵:上眼瞼退縮導致眼裂增寬。
von Graefe徵:向下注視時上眼瞼下落遲緩(lid lag)。

甲狀腺眼病(TED)是一種自體免疫疾病,由甲狀腺功能異常相關的免疫功能異常誘發眼眶內部組織發炎,導致眼眶脂肪組織和眼外肌體積增大。球後組織壓力升高引起眼球突出。最常見於甲狀腺功能亢進症(Graves病/巴塞多病),但也可能以甲狀腺功能正常的 euthyroid ophthalmopathy 形式發病。甲狀腺眼病與甲狀腺激素無關,是涉及甲狀腺相關自體抗體的自體免疫疾病之一。
約40-50%的Graves病患者出現眼部症狀。重症眼眶病變在所有Graves病患者中佔5-10%,相對罕見。
據報導,女性患病率為16/100,000人年,男性為2.9/100,000人年1)。發病年齡在40-50歲和60-70歲有兩個高峰1)。吸菸是甲狀腺眼病的最大危險因子,顯著增加發病風險2)。年輕患者以眼球突出為主要表現,老年患者以複視為主要表現,呈現年齡相關模式。
甲狀腺眼病的自然病程遵循Rundle曲線,從活動期(發炎期,通常持續1-3年)過渡到穩定期(非發炎期)3)。治療介入的時機基於該曲線決定。
眼瞼症狀
特徵性表現為上眼瞼腫脹、上眼瞼退縮和上眼瞼遲落。
Dalrymple徵:上眼瞼退縮導致眼裂增寬。
von Graefe徵:向下注視時上眼瞼下落遲緩(lid lag)。
眼球突出
年輕人較多(眼眶支撐組織脆弱)。
使用Hertel眼球突出計評估。日本人正常值為10~15mm(平均13mm)。兩眼差異在2mm以內為正常。
複視
老年人較多。由眼外肌發炎和纖維化導致的限制性斜視引起。
下直肌最常受累 → 上轉障礙最常見。其次為內直肌受累導致的外轉障礙。
視力障礙
即使在甲狀腺功能正常的情況下,也可能作為 euthyroid ophthalmopathy 發生。甲狀腺眼病是一種獨立於甲狀腺激素水平進展的自身免疫性疾病,如果甲狀腺相關自身抗體(TRAb、TSAb)陽性,則可能發病。如果存在眼瞼退縮或眼球突出,即使甲狀腺功能正常,也需要檢查甲狀腺相關自身抗體。
早期以乾燥感、刺激感、流淚、畏光為主。隨著病情進展,出現眼眶周圍腫脹、眼球突出、複視、眼瞼後退,重症病例可導致角膜潰瘍、壓迫性視神經病變。
以下為甲狀腺眼病特徵性的眼瞼所見。
| 徵候名稱 | 英文名稱 | 所見 |
|---|---|---|
| Dalrymple徵 | Dalrymple sign | 上眼瞼退縮導致瞼裂開大,上方角膜緣上方露出鞏膜。 |
| von Graefe徵 | 眼瞼遲滯 | 向下注視時上眼瞼跟隨延遲的現象。 |
| Stellwag徵 | Stellwag徵 | 眨眼減少與不完全閉眼 |
| Gifford徵 | Gifford徵 | 上眼瞼外翻困難 |
眼球突出使用Hertel眼球突出計測量。日本人的正常值為10~15mm(平均13mm),左右差異在2mm以內為正常。Hertel值超過18mm提示眼球突出1)。
肥厚的外眼肌在眼眶尖端壓迫視神經引起。約5%的病例發生1),具有高度緊急性。RAPD(相對性傳入性瞳孔缺損)陽性、CFF(臨界融合頻率)下降、視野缺損是早期徵象。色覺異常也是重要發現。
疼痛、複視和外貌變化是降低生活品質的主要因素。甲狀腺眼病患者焦慮和憂鬱的共病率為36%,約為一般人群(18.9%)的兩倍5)。62%的中度患者和89%的重度患者有較高的生活品質障礙(評分≥4/7分)5)。據報導,生活品質下降程度與糖尿病、肺氣腫和心衰竭相當或更差。
甲狀腺功能異常相關的免疫功能失調會誘發眼眶內部組織的發炎。針對TSH受體(TSHR)的自體抗體(TRAb)激活眼眶纖維母細胞上的TSHR,導致發炎性細胞因子(TNF-α、IL-6、IL-1β等)的產生。CD4+/CD8+ T細胞浸潤眼眶組織並放大發炎反應。
活化的纖維母細胞增加糖胺聚醣(GAG)和玻尿酸的合成,導致組織水腫和保水。纖維母細胞分化為脂肪細胞和肌纖維母細胞,導致眼眶脂肪膨脹和眼外肌纖維化3)。
IGF-1受體(IGF-1R)與TSHR形成複合體,協同參與眼眶纖維母細胞的活化4)。此機制是替妥木單抗(IGF-1R抑制劑)的治療標靶。
吸菸是最大的風險因子,與發病風險、嚴重度及治療抗性均有關聯2)。此外,甲狀腺功能不穩定、放射性碘治療後的急性期、高齡及男性亦與重症風險有關。
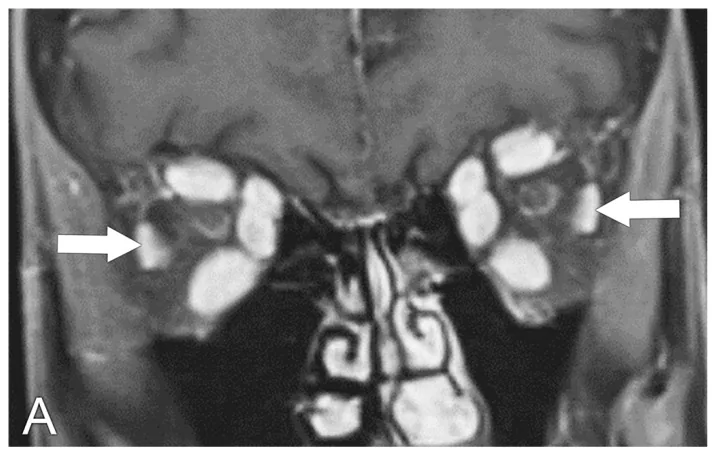
眼瞼退縮、眼球突出和複視三聯徵強烈提示TED。即使甲狀腺功能正常,甲狀腺相關自體抗體陽性也可診斷為TED。
檢測甲狀腺激素(FT₄、FT₃)、TSH和甲狀腺自體抗體。檢測對象包括TRAb(TSH受體抗體)、TSAb(甲狀腺刺激抗體)、抗TG抗體(抗甲狀腺球蛋白抗體)和抗TPO抗體(抗甲狀腺過氧化物酶抗體)。其中至少一項為陽性。
MRI(首選):T1加權像評估眼外肌形態。STIR(短TI反轉恢復)序列顯示炎症區域為高信號,有助於評估炎症活動性。冠狀位是必需的,可同時評估除下斜肌外的所有眼外肌。軸位評估內直肌和外直肌。
CT:確認眼外肌肥厚(肌腱不受影響、肌腹肥大的模式為TED特徵),並使用骨窗評估眼眶骨壁。
B-scan超音波:輔助評估眼外肌肥大。
CAS是Mourits等人於1989年提出的發炎活動性評估7項評分系統(0-7分)6)。
評估7項:①自發性球後疼痛、②眼球運動時疼痛、③眼瞼發紅、④眼瞼腫脹、⑤結膜發紅、⑥結膜水腫、⑦淚阜/半月皺襞腫脹。
CAS≥3/7判定為活動期,適合類固醇脈衝療法。CAS≥4/7是替妥木單抗RCT的納入標準。
| 嚴重度 | 基準 | 治療方針 |
|---|---|---|
| 輕度 | 對日常生活影響輕微 | 補充硒 + 觀察 |
| 中重度 | 眼瞼後退≥2mm、眼球突出超過正常值≥3mm、複視 | 類固醇脈衝療法、替妥木單抗 |
| 視力威脅型 | 壓迫性視神經病變、角膜潰瘍 | 緊急眼眶減壓術或高劑量類固醇 |
根據EUGOGO(歐洲Graves眼症小組)2021年版臨床診療指引的分類1)。NOSPECS分類(0~6級)和VISA分類(視力、發炎、斜視、外觀)也用於嚴重度評估。
| 鑑別疾病 | 鑑別要點 | 影像學發現 |
|---|---|---|
| IgG4相關眼疾 | 淚腺腫大+外眼肌腫大,血清IgG4升高 | 淚腺及外眼肌瀰漫性腫大 |
| 外眼肌炎(眼眶肌炎) | 急性發作,疼痛劇烈 | 肌腱部增厚(甲狀腺眼病變為肌腹增厚,肌腱部不受影響) |
| 眼眶腫瘤/轉移性腫瘤 | 單眼性、進行性 | 腫塊形成 |
它是評估甲狀腺眼病炎症活動性的7項評分系統(0-7分)。評估的7個項目包括:①自發性球後疼痛、②眼球運動時疼痛、③眼瞼發紅、④眼瞼腫脹、⑤結膜發紅、⑥結膜水腫、⑦淚阜/半月皺襞腫脹。3分及以上判定為活動期。它是治療選擇的重要指標,用於判斷是否適合進行類固醇脈衝療法或替妥木單抗治療。
甲狀腺功能正常化是必要條件,與內分泌科的協作不可或缺。戒菸指導在所有病例中實施,以消除吸菸這一導致病情加重和治療抵抗的最大風險因素。
硒補充:對於輕度TED,補充硒200μg/天持續6個月有助於改善疾病活動性,建議使用10)。
角膜與眼表面保護:基本措施包括頻繁使用人工淚液和角膜保護眼藥水,以及睡前塗抹眼藥膏。對於重度兔眼,考慮外側瞼板縫合術。
類固醇脈衝療法(第一線治療):甲基潑尼松龍500–1000 mg/週,持續6–12週1)。靜脈注射類固醇比口服類固醇更有效9)。建議累積劑量不超過8克(以降低肝損傷風險)。
標準方案:甲基潑尼松龍1克×3天作為一個療程。
口服潑尼松龍:對於靜脈給藥困難的中重度病例,從1 mg/kg/天開始。
局部類固醇注射:對於上眼瞼水腫和炎性眼瞼退縮,局部注射曲安奈德(Kenacort-A® 1安瓿)有效。
替普羅妥木單抗(IGF-1R抑制劑):對於活動性中重度TED,這是一種有望改善眼球突出和複視的治療藥物。5項RCT(共411例)的統合分析證實,眼球突出顯著減少、24週時CAS 0~1的達成率顯著改善、複視改善率顯著提高4),且嚴重不良事件未顯著增加。兩項主要RCT——Smith等人(2017年,42例 vs 45例)7)和Douglas等人(2020年,41例 vs 42例)8)——已建立證據基礎。
利妥昔單抗(抗CD20單株抗體):一項多中心隨機試驗顯示,它可能降低難治性中重度TED的疾病活動性12)。
托珠單抗(IL-6受體抑制劑):正在考慮用於對類固醇和利妥昔單抗難治的病例。
對於中重度TED,通常與免疫抑制治療合併使用。通常以20 Gy/10次,在2週內完成照射。與類固醇合併使用被認為比單一治療更有效。
手術原則上應在Rundle曲線進入穩定期、發炎消退後計畫進行。手術順序必須嚴格遵守,因為前次手術的結果直接影響後續手術計畫。
步驟1:眼眶減壓術
適應症:重度眼球突出、壓迫性視神經病變(緊急適應症)
術式與效果:有五種術式,結合內側壁、眶底、外側壁和脂肪。單壁減壓可改善眼球突出-1.4至-2.3毫米,三壁加脂肪減壓可改善-4.6至-5.0毫米。
一項633隻眼的多中心研究證實,同一術式在不同術者之間無顯著差異,具有穩定的可重複性11)。
第2步:斜視手術
第3步:眼瞼手術
適應症:非發炎穩定期的眼瞼後退、功能性和美觀問題
術式:上眼瞼後退選擇Müller肌切除術或上眼瞼提肌後退術。據報告,Müller肌切除與提肌後退合併使用可獲得良好效果。
在眼眶減壓和斜視手術術後變化穩定後再進行計劃。
它是一種抑制IGF-1受體(IGF-1R)的單克隆抗體。它阻斷眼眶成纖維細胞上IGF-1R和TSHR的複合信號,抑制炎症和組織膨脹。五項隨機對照試驗(共411例)的薈萃分析證實了眼球突出、複視和CAS的顯著改善。嚴重不良事件沒有顯著增加,但長期安全性(聽力障礙、高血糖等)仍在評估中。
與甲狀腺功能異常相關的免疫功能異常誘發眼眶內部組織發炎,導致眼眶脂肪組織和眼外肌體積增大。球後組織壓力升高引起眼球突出。
眼眶脂肪組織的病理:脂肪細胞腫大,間質出現淋巴球浸潤,慢性發炎導致水腫和疤痕形成。糖胺聚糖(GAG)和玻尿酸合成增加引起組織液體滯留和腫脹。
眼外肌的病理:橫紋肌纖維間出現以淋巴球為主的發炎細胞浸潤,肌纖維發生變性壞死。間質因發炎出現水腫和增厚,肌纖維間結締組織增生,形成眼外肌肥大。眼外肌受累頻率以下直肌最高,依次為內直肌、上直肌和外直肌。因此,上轉障礙最常見,其次為外轉障礙。
兩種機制共同作用導致。
①上眼瞼提肌的病理:發炎導致肌細胞水腫,引起眼瞼水腫。脂肪組織侵入肌纖維間,肌細胞壞死和疤痕化,提肌功能改變。
②Müller肌的病理:Müller肌是受交感神經支配的平滑肌,因甲狀腺功能亢進症伴隨的交感神經亢進而持續收縮,提舉瞼板,使瞼裂開大。
針對TSH受體(TSHR)的自體抗體(TRAb)激活眼眶纖維母細胞上的TSHR,通過下游信號產生發炎性細胞因子(TNF-α、IL-6、IL-1β)。CD4+/CD8+ T細胞浸潤眼眶組織,放大發炎反應。活化的纖維母細胞分化為脂肪細胞和肌纖維母細胞,分別導致眼眶脂肪膨脹和外眼肌纖維化3)。
IGF-1R與TSHR形成複合物,協同參與眼眶纖維母細胞的活化4)。阻斷該複合物信號是替妥木單抗的作用機制。
從發炎活動期(通常1~3年)到穩定期(非發炎期)的自然病程被概念化為Rundle曲線13)。實際治療干預需在評估活動性和嚴重程度後選擇1)。活動期優先進行抗炎治療,非發炎穩定期制定手術計劃。
FDA核准後數據仍在持續累積。5項RCT(共411例)的統合分析4)已確認其有效性與安全性,但長期安全性(如聽力障礙、高血糖等長期結果)有待第四期試驗結果。同時也在探討將其適應症擴展至非活動期TED的可能性。
一項涉及7個機構、7名術者、633隻眼睛的多中心研究11)證實,當實施相同術式時,術者之間無顯著差異。這是支持多中心RCT統計有效性的重要發現。內視鏡內側壁減壓術與開放手術相比,在內側壁加底壁減壓中報告了顯著更大的突出度改善(-3.67mm vs -2.97mm,p=0.008)。術前眼球突出度與術後突出度變化顯著相關(p<0.001),再次確認了術前評估的重要性。
TRAb和TSAb在活動期的波動與CAS相關,基於生物標誌物的治療選擇研究正在進行中。托珠單抗(IL-6抑制劑)在難治性病例中的大規模RCT值得期待。
Bartalena L, Kahaly GJ, Baldeschi L, et al. The 2021 European Group on Graves’ Orbitopathy (EUGOGO) clinical practice guidelines for the medical management of Graves’ orbitopathy. Eur J Endocrinol. 2021;184(4):G43-G67.
Prummel MF, Wiersinga WM. Smoking and risk of Graves’ disease. JAMA. 1993;269(4):479-482.
Bahn RS. Graves’ ophthalmopathy. N Engl J Med. 2010;362(8):726-738.
Cong X, Pei L, Hu H. Teprotumumab for treating active thyroid eye disease: a meta-analysis. Medicine. 2024;103(18):e38059.
Wang Y, Sharma A, Padnick-Silver L, et al. Physician-perceived impact of thyroid eye disease on patient quality of life in the United States. Ophthalmol Ther. 2021;10(1):75-87.
Mourits MP, Koornneef L, Wiersinga WM, et al. Clinical criteria for the assessment of disease activity in Graves’ ophthalmopathy: a novel approach. Br J Ophthalmol. 1989;73(8):639-644.
Smith TJ, Kahaly GJ, Ezra DG, et al. Teprotumumab for thyroid-associated ophthalmopathy. N Engl J Med. 2017;376(18):1748-1761.
Douglas RS, Kahaly GJ, Patel A, et al. Teprotumumab for the treatment of active thyroid eye disease. N Engl J Med. 2020;382(4):341-352.
Kahaly GJ, Pitz S, Hommel G, et al. Randomized, single blind trial of intravenous versus oral steroid monotherapy in Graves’ orbitopathy. J Clin Endocrinol Metab. 2005;90(9):5234-5240.
Marcocci C, Kahaly GJ, Krassas GE, Bartalena L, Prummel M, Stahl M, et al.; European Group on Graves’ Orbitopathy. Selenium and the course of mild Graves’ orbitopathy. N Engl J Med. 2011;364(20):1920-1931. PMID: 21591944. doi:10.1056/NEJMoa1012985.
Hong A, Shoji MK, Villatoro GA, et al. Intersurgeon variability in proptosis reduction after orbital decompression for thyroid eye disease: a multicenter analysis. Ophthalmic Plast Reconstr Surg. 2024;40(3).
Salvi M, Vannucchi G, Campi I, et al. Rituximab treatment in active moderate-to-severe Graves’ orbitopathy: an international, multicenter, single-blind, randomized placebo-controlled study. J Clin Endocrinol Metab. 2015;100(11):422-431.
Rundle FF, Wilson CW. Development and course of exophthalmos and ophthalmoplegia in Graves’ disease with special reference to the effect of thyroidectomy. Clin Sci. 1945;5(3-4):177-194. PMID: 21011937.