구심성 장애

성인 발병 완만 진행형 자가면역 당뇨병(LADA)의 신경안과적 고찰
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. LADA에서의 신경안과학적 고찰
섹션 제목: “1. LADA에서의 신경안과학적 고찰”LADA (잠재성 성인 자가면역 당뇨병)는 GAD65에 대한 자가항체를 가지면서 T2DM 표현형을 보이는 성인 환자의 하위 범주로 처음 보고된 질환 개념입니다. “1.5형 당뇨병”이라고도 불립니다.
**진단 기준(일본당뇨병학회 IDS)**은 다음 세 가지 항목으로 구성됩니다.
- 발병 연령 30세 이상
- 적어도 한 종류의 췌도 자가항체 양성
- 진단 후 6개월간 인슐린 비의존
유병률은 전체 당뇨병의 212%이며, T2D로 오진되는 비율은 510%로 추정됩니다5). 췌도세포항체(ICA)의 발견은 1974년으로 거슬러 올라가며, 당뇨병 분류에 큰 변화를 가져왔습니다.
신경안과학적 관점에서 만성 고혈당으로 인한 미세혈관 손상은 당뇨망막병증, NAION(비동맥염성 전방허혈시신경병증), 피질 뇌졸중으로 인한 동측반맹, 안구운동신경마비, 안진 등을 유발합니다. LADA 환자의 당뇨망막병증 유병률은 T2D 환자에 비해 유의하게 낮습니다(20.3% 대 26.4%, P < 0.001). 진단 시 망막병증이 있는 경우는 약 12%입니다.
LADA는 자가항체 양성이며 인슐린 의존으로 서서히 진행되는 반면, T2D는 자가항체 음성이며 인슐린 비의존 상태가 오래 지속됩니다. LADA와 T2D의 유전적·임상적 특징을 모두 공유하는 ‘1.5형’으로 분류됩니다.
2. 주요 증상 및 임상 소견
섹션 제목: “2. 주요 증상 및 임상 소견”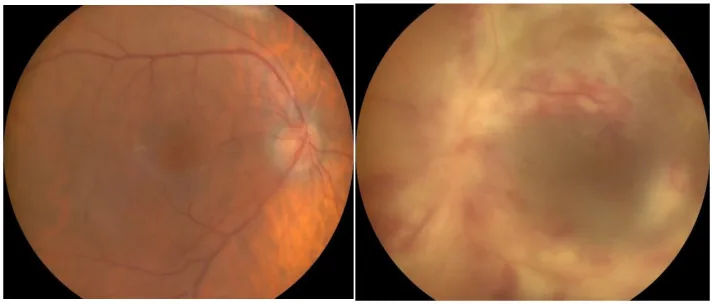
자각 증상
섹션 제목: “자각 증상”- 다뇨, 다식, 다음, 탈수: 고혈당에 따른 전신 증상.
- 시각 증상: 당뇨망막병증, 비동맥염성 전방허혈시신경병증, 피질뇌졸중으로 인한 시력 장애 및 시야 결손.
- DKA 증상: 케톤산증에 따른 경련 및 혼수(T1D와 유사한 급성 발병 사례).
- 소섬유 신경병증: 발에서 시작되는 통증, 작열감, 찌르는 듯한 통증. Aδ섬유와 C섬유의 위축으로 인함.
임상 소견(신경안과적 소견)
섹션 제목: “임상 소견(신경안과적 소견)”원심성 장애
기타 안과적 소견은 다음과 같습니다.
- 각막 이상: 내피세포 크기 부동, 데스메막 주름 형성. 60세 미만에서 데스메막 주름이 관찰되면 당뇨병을 의심합니다.
- 홍채모양체염: 전방에 세포만 보이는 경미한 경우가 많으며, 스테로이드 점안액으로 신속히 호전됩니다.
- 안와 점액곰팡이증: 혈당 조절이 불량한 환자에서 발생합니다. 사망률이 높으며 항진균제로 치료합니다.
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”자가면역 기전
섹션 제목: “자가면역 기전”췌도 베타 세포에 대한 자가항체(GAD65, ICA, IA-2A, IAA)가 생성되어 베타 세포가 파괴됩니다. 인슐린 결핍에 이르는 과정은 T1DM과 T2DM의 기전이 복합적으로 작용합니다.
위험 요인
섹션 제목: “위험 요인”- T1DM 공통 위험 요인: 자가면역 질환의 개인력 또는 가족력, 유전적 소인(HLA-DR4-DQ8, HLA-DR3-DQ2)3)
- T2DM 공통 위험: 비만, 운동 부족, 흡연, 저체중 출생, 가당 음료 섭취, 과도한 알코올 섭취
- 동반 자가면역 질환: 하시모토병(갑상선 질환 유병률 17.7%)5), 쇼그렌 증후군4), 백반증3), 악성 빈혈3)
- COVID-19 관련: SARS-CoV-2가 ACE2 수용체를 통해 췌장 β 세포에 대한 자가면역 반응을 유발할 수 있습니다. 입원한 COVID-19 환자의 20%가 입원 후 새로운 자가항체를 획득했다는 보고가 있습니다1)
- 비만 촉진 인자: GAD65-Ab 양성이더라도 BMI가 안정적이면 3년간 LADA가 발생하지 않는 사례가 있어, 체중 증가가 LADA 발병을 촉진할 가능성이 있습니다4)
COVID-19 이후 IA2 등의 자가항체가 나타난 증례 보고가 있습니다1). ACE2 수용체를 통한 β 세포 손상 메커니즘이 제안되었지만, 현재 인과관계는 확립되지 않았습니다.
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”자가항체 및 대사 검사
섹션 제목: “자가항체 및 대사 검사”- GAD65 항체: 민감도가 가장 높음. LADA 진단의 주요 표지자5)
- 기타 자가항체: ICA, IA-2A, ZnT8A, 테트라스파닌 7
- C-펩타이드 검사: β세포 기능 지표. C-펩타이드 < 0.3 nmol/L은 T1D와 동등한 인슐린 의존 상태를 나타냄
- HbA1c: 반복 측정을 통한 혈당 조절 평가
- CGM(연속혈당측정) : 혈당 변동 파악2)
- 지질 프로파일, eGFR, 혈청 크레아티닌, 시스타틴 C : 합병증 평가
예를 들어, COVID-19 후 LADA 증례에서 GAD65 < 5 nmol/L(정상), C-펩타이드 2.38 ng/mL(정상), IA2 20.6 DK 단위/mL(높음, 정상 < 5.4)의 검사치 패턴이 보고되었습니다1).
안과 검사
섹션 제목: “안과 검사”- 세극등 현미경 검사 : 각막 이상, 홍채모양체염 확인
- 산동 하 안저 검사 : 황반 주변 미세혈관류, 출혈, 삼출물, 부종, 망막 신생혈관, 유리체 세포, 망막 박리 확인
- 당뇨병성 유두증의 감별: RAPD는 음성입니다. 수평 반맹 또는 궁상 암점이 있는 경우 허혈성 시신경병증을 의심합니다. 형광 안저 조영술로 주변부 무혈관 영역 및 신생혈관 유무를 확인합니다.
감별 진단
섹션 제목: “감별 진단”각 당뇨병 유형의 비교는 아래와 같습니다.
| 항목 | LADA | T1D | T2D |
|---|---|---|---|
| 발병 연령 | 30세 이상 | 대부분 35세 미만 | 35세 이후 |
| 자가항체 | 양성 | 양성인 경우가 많음 | 음성 |
| C-펩타이드 | 정상~저치 | 저치 | 정상~고치 |
| 인슐린 의존성 | 서서히 진행 | 발병 직후부터 | 장기간 비의존성 |
기타 감별 질환으로 MODY(강한 가족력, 자가항체 음성), LADY(청년 발병 서서히 진행형 자가면역 당뇨병)가 있습니다.
GAD65 항체(민감도가 가장 높음)와 C-펩타이드 검사의 조합이 진단에 가장 중요합니다. C-펩타이드 저하 및 자가항체 양성이면 LADA를 확진합니다. IDS 분류 기준(발병 연령 30세 이상, 자가항체 양성, 진단 후 6개월간 인슐린 비의존)도 진단에 사용됩니다.
5. 표준 치료법
섹션 제목: “5. 표준 치료법”전신 치료(혈당 조절)
섹션 제목: “전신 치료(혈당 조절)”치료 목표는 베타 세포 기능 보존과 엄격한 혈당 조절입니다.
- C-펩타이드 < 0.3 nmol/L: T1D와 유사한 인슐린 기반 치료 선택
- C-펩타이드 높음: 인슐린 요법에 추가로 다른 혈당 강하제 병용 권장 (국제 전문가 패널 권장)
- GLP-1 작용제(예: 세마글루타이드), DPP-4 억제제(예: 시타글립틴), 메트포르민
- SU 약물은 금기: 베타 세포 부하를 증가시켜 기능 악화 및 혈당 조절 불량 초래5)
- SGLT2 억제제: LADA에서의 유익성은 확립되지 않음
DPP-4 억제제의 보호 효과로, 시타글립틴 100mg/일로 90세 여성의 HbA1c 5.9%를 1년간 유지한 보고가 있음3). 또한, HbA1c가 7.9%에서 11.7%로 악화된 하시모토병 동반 LADA 증례에서 메트포르민, 시타글립틴, 글리클라지드 120mg/일, 다파글리플로진, 둘라글루타이드 모두 무효였으나, 인슐린 기반-식사 볼루스 요법으로 HbA1c 5.7%를 달성한 예가 보고됨5).
안과 치료
섹션 제목: “안과 치료”망막증 치료
국소 레이저: 당뇨병성 황반 부종에 대한 국소 레이저 광응고술.
범망막 광응고술(PRP): 증식성 당뇨망막병증(PDR)의 주요 치료법.
항VEGF 요법: PDR의 대체 또는 보조 요법으로 유리체내 주사.
기타 안구 합병증
SU 약물은 β세포에 직접 작용하여 인슐린 분비를 강제로 촉진하므로 β세포의 부담이 증가하고, 자가면역에 의해 소모되고 있는 잔여 β세포 기능을 더욱 악화시킵니다. LADA에서 SU 약물 사용은 혈당 조절 불량을 초래하는 것으로 보고되어 5) 사용이 금기입니다.
6. 병태생리학 및 상세한 발병 기전
섹션 제목: “6. 병태생리학 및 상세한 발병 기전”자가항체의 종류와 역할
섹션 제목: “자가항체의 종류와 역할”LADA에서 자가항체의 특징은 다음과 같습니다.
| 항체 | 특징 |
|---|---|
| GAD65 | T1DM과 LADA 모두에서 가장 흔함 |
| ICA | T1DM과 LADA 모두에서 양성률 높음 |
| IA-2A 및 IAA | T1DM 단독에서 양성률 높음 |
GAD65는 췌장 섬뿐만 아니라 갑상선, 뇌, 뇌하수체, 신장, 간, 부신, 난소, 고환에도 존재합니다4). 따라서 고역가의 GAD65 항체는 갑상선 자가면역 위험 증가와 관련이 있으며, LADA 환자의 갑상선 질환 유병률은 17.7%에 이릅니다5).
발병 기전
섹션 제목: “발병 기전”T1DM 측의 기전은 유전적 소인 → 면역학적 인자 → 자가항체에 의한 베타세포 세포사멸 → 인슐린 결핍의 경로가 기본입니다. T2DM 측의 기전은 비만 → 내장지방 축적 → 경미한 염증 → 자가면역 → 베타세포 기능 부전이 추가됩니다.
COVID-19와 베타세포 손상의 기전
섹션 제목: “COVID-19와 베타세포 손상의 기전”Lee 등(2023)은 T2DM 병력이 있는 46세 남성이 COVID-19 감염 후 IA2 항체(20.6 DK 단위/mL, 정상 < 5.4) 양성으로 나타나 LADA로 진단된 사례를 보고했습니다1). ACE2 수용체는 췌장 외분비선과 췌도 세포에서 발현되며, SARS-CoV-2 스파이크 단백질이 ACE2에 결합하고 TMPRSS2에 의해 프라이밍되어 세포 내로 침투합니다. ACE2 억제 → 안지오텐신 II 상승 → NHE2 지속적 활성화 → 활성산소종 증가 → 산화 스트레스 → 인슐린 저항성 및 β세포 손상이라는 일련의 기전이 제안되었습니다.
미세혈관 손상 및 신경병증의 메커니즘
섹션 제목: “미세혈관 손상 및 신경병증의 메커니즘”만성 고혈당은 망막 혈관을 가장 일찍 그리고 가장 빈번하게 손상시켜 당뇨병성 망막병증을 유발합니다. 신경병증에서는 대사 관련 손상으로 인한 Aδ 섬유 및 C 섬유의 위축(소섬유 신경병증)이 발에서 시작되는 통증과 작열감을 유발합니다.
자가면역 연쇄(쇼그렌 증후군 및 하시모토 갑상선염과의 연관성)
섹션 제목: “자가면역 연쇄(쇼그렌 증후군 및 하시모토 갑상선염과의 연관성)”Wen 등(2021)은 쇼그렌 증후군(SS)과 하시모토 갑상선염(HT)을 가진 중년 여성 2명에서 GAD65 항체 또는 IAA 항체 양성임에도 불구하고 3년간의 OGTT에서 정상 혈당이 유지되었음을 보고했습니다4). 자가항체 양성이 즉시 LADA로의 진행을 의미하는 것은 아니며, 비만과 같은 촉진 요인이 추가되어야 발병합니다.
7. 최신 연구와 향후 전망 (연구 단계 보고)
섹션 제목: “7. 최신 연구와 향후 전망 (연구 단계 보고)”테플리주맙 (T1DM 발병 지연 면역 요법)
섹션 제목: “테플리주맙 (T1DM 발병 지연 면역 요법)”테플리주맙은 2022년 11월 FDA가 승인한 항CD3 단클론항체입니다. T세포 표면의 CD3에 결합하여 자가반응성 T세포를 불활성화함으로써 T1DM 발병을 지연시킵니다. LADA에 대해서는 승인되지 않았고 연구되지 않았지만, 자가면역 메커니즘의 공통성으로 인해 발병 지연 가능성이 기대됩니다.
세마글루타이드와 비동맥염성 전방 허혈성 시신경병증 위험
섹션 제목: “세마글루타이드와 비동맥염성 전방 허혈성 시신경병증 위험”Hathaway 등(2024)은 T2DM 환자에서 semaglutide 사용군의 비동맥염성 전방허혈시신경병증 위험이 HR 4.28(95% CI 1.62-11.29, P < 0.001)로 유의하게 높다고 보고했습니다6). LADA에서 GLP-1RA를 사용할 때는 비동맥염성 전방허혈시신경병증 발생에 주의해야 합니다.
semaglutide와 당뇨망막병증 악화
섹션 제목: “semaglutide와 당뇨망막병증 악화”HbA1c가 급격히 감소할 때 당뇨망막병증 악화 위험이 증가하며, 증식망막병증 진행 및 황반부종 새로 발생 위험이 상승합니다. semaglutide를 포함한 GLP-1RA 사용 시작 시 안과적 모니터링이 중요합니다.
DPP-4 억제제의 베타세포 보호
섹션 제목: “DPP-4 억제제의 베타세포 보호”Marcon 등(2022)은 GAD65 > 250 U/ml 양성인 90세 여성에게 sitagliptin 100 mg/일을 투여하여 1년 동안 HbA1c 5.9%를 유지한 증례를 보고했습니다3). DPP-4 억제제가 LADA의 베타세포 파괴를 지연시킬 가능성이 시사되지만, 추가 RCT가 필요합니다.
CGM이 정신 건강에 미치는 영향
섹션 제목: “CGM이 정신 건강에 미치는 영향”Gupta 등(2023)은 DKA로 진단된 LADA 환자(44세 남성)에게 CGM을 도입한 후 혈당이 80-408 mg/dL로 변동하여 기존 OCD가 악화되고 자살에 이른 사례를 보고했습니다2). DM 환자는 우울증 위험이 약 2배이며, CGM 사용 전 정신과적 평가의 중요성이 제시되었습니다.
COVID-19 후 자가면역 연구의 과제
섹션 제목: “COVID-19 후 자가면역 연구의 과제”COVID-19 환자에서 췌도 자가항체(IA2, GAD65, ICA) 발생률에 대한 대규모 연구가 필요합니다1). 또한 SS/HT를 가진 GAD65-Ab 양성 비당뇨병 환자가 향후 LADA로 진행하는지에 대한 장기 추적 연구도 요구됩니다4).
현재 T1DM에만 FDA 승인되었습니다. LADA도 유사한 자가면역 기전을 가지므로 이론적으로 효과적일 가능성이 있지만, 연구 및 승인 모두 이루어지지 않았습니다. 향후 임상 시험의 전개가 기대됩니다.
8. 참고문헌
섹션 제목: “8. 참고문헌”- Lee N, Prabhu P, Swaminath S, et al. Development of Islet Antigen 2 (IA2) Antibodies Post-COVID-19 Infection: A Sign of Autoimmunity or Latent Autoimmune Diabetes Mellitus in Adults (LADA)? Cureus. 2023;15(6):e40971.
- Gupta R, Edupuganti S, Zamir I, et al. Latent Autoimmune Diabetes in Adults and a Continuous Glucose Monitoring Device: An Unfortunate Outcome. Cureus. 2023;15(11):e49141.
- Marcon LMR, Fanelli CG, Calafiore R. Type 1 Diabetes (T1D) and Latent Autoimmune Diabetes in Adults (LADA): The Difference Between a Honeymoon and a Holiday. Case Reports in Endocrinology. 2022;2022:9363543.
- Wen S, Jiang W, Zhou L. Islet Autoantibodies in the Patients with Sjogren’s Syndrome and Thyroid Disease and Risk of Progression to Latent Autoimmune Diabetes in Adults: A Case Series. Diabetes Metab Syndr Obes. 2021;14:1025-1033.
- Ibrahim A, Ahmed Mohmed MH, Darwish H, et al. A Case of Persistent Hyperglycemia: Autoimmune Link Between Hashimoto’s Thyroiditis and Latent Autoimmune Diabetes in Adults. Cureus. 2025;17(8):e91219.
- Hathaway JT, Shah MP, Hathaway DB, et al. Risk of Nonarteritic Anterior Ischemic Optic Neuropathy in Patients Prescribed Semaglutide. JAMA Ophthalmol. 2024.
