眼肌麻痺
頻率:CIDP中最常見的眼部併發症,見於3%–8%的病例1)
受影響神經:外展神經(VI)最常見,動眼神經(III)也可能受影響
特點:可能雙側發生,抗硫脂IgM抗體陽性病例中更常見
預後:透過適當的免疫治療可望改善

慢性發炎性脫髓鞘性多發性神經根神經病變(CIDP)是一種周邊神經髓鞘被免疫介導機制損害的疾病。盛行率為每10萬人0.8至8.9人,可發生於所有年齡層,男性略多。日本(鳥取縣)的盛行率報告為每10萬人0.8人。
CIDP本質上是一種以四肢肌無力和感覺障礙為主的多發性神經病變,但也可波及腦神經。約15%的病例出現腦神經受累1),其中與眼相關的症狀作為神經眼科臨床表現尤為重要。
如果眼科醫師漏診CIDP的神經眼科併發症,可能會延誤適當的全身治療,導致不可逆的視功能損害。因此,準確理解CIDP的眼科併發症特徵在臨床上極為重要。
CIDP的神經眼科併發症中,患者主訴的主要自覺症狀如下。
複視是最常見的眼科主訴,由眼外肌或其支配神經的損傷引起。眼瞼下垂由動眼神經(第三對腦神經)功能障礙引起,可能先於複視或與之同時發生。視力下降和視野缺損見於視神經病變或嚴重的視乳頭水腫,若不治療可能導致永久性視功能損害。眼球突出可能由眼眶內神經肥大或發炎引起的佔位效應導致,雖然罕見但有報告。
CIDP的神經眼科臨床表現主要分為五類。
眼肌麻痺
頻率:CIDP中最常見的眼部併發症,見於3%–8%的病例1)
受影響神經:外展神經(VI)最常見,動眼神經(III)也可能受影響
特點:可能雙側發生,抗硫脂IgM抗體陽性病例中更常見
預後:透過適當的免疫治療可望改善
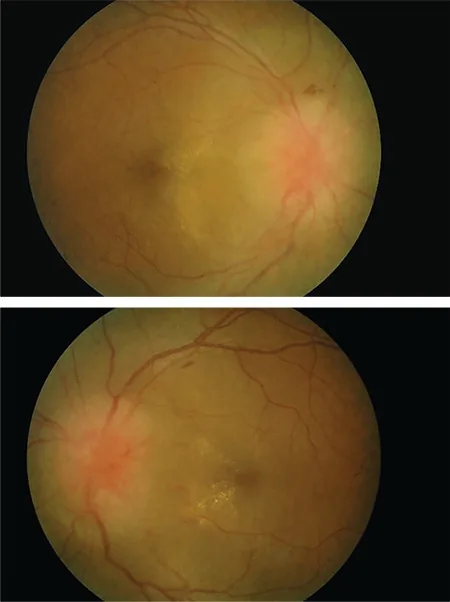
視乳頭水腫
視神經病變
眼球突出和瞳孔異常
CIDP的發病機轉是自體免疫性脫髓鞘,涉及T細胞媒介和抗體媒介的機制。針對髓鞘相關蛋白(P0、P2、PMP22)的自體免疫反應是病理基礎。
CIDP的診斷基於2021年EAN/PNS診斷標準,綜合臨床、電生理、實驗室和神經影像學檢查結果4)。2021年標準的敏感性為74%–83%,特異性為94%–98%,與2010年標準相比,診斷類別更加簡化4)。
在CIDP確診後,或確診前出現神經眼科症狀時,以下檢查至關重要。
| 檢查 | 目的 | 所見 |
|---|---|---|
| 腦脊髓液檢查 | 確認蛋白質升高 | 蛋白質升高(典型為細胞數正常);Bahramy 2024案例中蛋白質210 mg/dL2) |
| 神經傳導檢查 | 脫髓鞘的電生理證據 | 傳導速度減慢、傳導阻滯、遠端潛時延長 |
| 神經超音波/MRI | 確認神經肥大 | 頸部和臂神經叢肥大對CIDP幾乎具有特異性4) |
| 眼眶MRI | 評估眼球突出和神經肥大 | 評估視神經和外眼肌的變化 |
| 眼底檢查和光學同調斷層掃描(OCT) | 評估視乳頭水腫和視神經萎縮 | 確認視乳頭隆起和視網膜神經纖維層變薄 |
| 血液檢查 | 抗體和基礎疾病的詳細檢查 | 抗神經病變抗體、抗硫脂抗體、血糖、腫瘤標記 |
在2021年EAN/PNS診斷標準中,神經超音波和MRI被明確列為不符合電生理學標準病例的輔助診斷標準4)。周邊神經顯著肥大對CIDP和CMT1型具有高度特異性,確認這些表現有助於提高敏感性。眼眶MRI可評估視神經和眼眶內神經的肥大或浸潤,對眼球突出的鑑別診斷有幫助。
CIDP神經眼科併發症的治療基本原則是透過全身免疫療法控制基礎疾病。治療應在神經內科醫師和眼科醫師的密切合作下進行。
第一線治療包括以下三種已確立的方案。
皮質類固醇如口服潑尼松龍或靜脈注射甲潑尼龍,通過抗炎和免疫抑制作用抑制脫髓鞘。長期使用需注意白內障、青光眼和感染風險,建議定期眼科檢查。
靜脈注射免疫球蛋白(IVIg)標準劑量為2 g/kg(分5天給藥),可有效改善急性期神經症狀1)。Chen 2023報告的眼肌麻痺病例中,IVIg與糖皮質激素聯合使用在3個月內實現完全恢復1)。
血漿置換療法用於對上述治療無反應的病例,旨在清除自身抗體。
對於難治性或復發性病例,使用利妥昔單抗、硼替佐米、硫唑嘌呤和環孢素等免疫抑制劑。Kim 2023報告的COVID-19疫苗接種後CIDP病例中,採用潑尼松龍、硫唑嘌呤和IVIg三聯治療3)。
對於難治性視乳頭水腫,可能需要使用乙酰唑胺降低顱內壓,以及視神經鞘開窗術以保護視功能。
CIDP中神經眼科併發症的發病機制與周邊神經病變相同。自體免疫性T細胞和自體抗體作用於動眼神經和視神經的髓鞘或軸突,導致功能障礙。
Chen L等人(J Int Med Res. 2023)分析了14例患者,包括伴有眼肌麻痺的CIDP患者,顯示抗硫脂IgM抗體陽性與眼肌麻痺相關。該研究中,14例患者中有8例(57%)確認有頸部和臂神經叢肥大,神經肥大組的病程平均為15.9年,顯著長於無肥大組的3.3年1)。
Bahramy MA等人(BMC Neurol. 2024)報告了一例接種國藥(不活化)疫苗後發生CIDP的病例。腦脊髓液蛋白顯著升高至210 mg/dL(正常值<45 mg/dL),白血球計數為4/μL,在正常範圍內2)。
Kim S等人(J Korean Med Sci. 2023)報告了兩例接種mRNA-1273疫苗和Ad26.COV2.S疫苗後發生CIDP的病例3)。兩例均在接種後數週內出現症狀,但因果關係尚未確定。COVID-19疫苗後CIDP的機制可能涉及分子擬態、佐劑效應和免疫活化,但目前尚不能排除偶然關聯。
Rathore H, Thaker N(Indian J Nucl Med. 2023)報告了一例因CIDP樣症狀被追蹤的患者最終被診斷為POEMS症候群的病例5)。視乳頭水腫是POEMS診斷標準中的次要項目,鑑別CIDP和POEMS必須評估血清M蛋白、VEGF和器官腫大。
2021年EAN/PNS診斷標準是對2010年標準的修訂,經驗證診斷靈敏度為74–83%,特異度為94–98% 4)。主要改進是將神經超音波和MRI正式納入輔助診斷標準。周邊神經顯著肥大對CIDP和CMT1型具有高度特異性,有助於提高不符合電生理標準病例的診斷靈敏度 4)。
全球已報告多例COVID-19疫苗接種後發生CIDP的病例,涉及病毒載體疫苗、mRNA疫苗和滅活疫苗 2, 3)。然而,確立因果關係需要流行病學發生率比較和生物學機制的闡明;目前尚不能排除偶然關聯。
Chen L, Dong W, Li J, et al. Chronic inflammatory demyelinating polyneuropathy with ophthalmoplegia and anti-sulfatide IgM antibody positivity: a case report and literature review. J Int Med Res. 2023;51(9):3000605231198994.
Bahramy MA, Moridnejad M, Shariati M, et al. Chronic inflammatory demyelinating polyneuropathy following COVID-19 vaccination: a case report. BMC Neurol. 2024;24(1):294.
Kim S, Kim HJ, Kim SM, et al. Two Case Reports of Chronic Inflammatory Demyelinating Polyneuropathy After COVID-19 Vaccination. J Korean Med Sci. 2023;38(9):e73.
Kuwabara S, Suichi T. Validation of the 2021 EAN/PNS diagnostic criteria for chronic inflammatory demyelinating polyneuropathy. J Neurol Neurosurg Psychiatry. 2022;93(12):1237-1238.
Rathore H, Thaker N. POEMS Syndrome Masquerading as Chronic Inflammatory Demyelinating Polyneuropathy. Indian J Nucl Med. 2023;38(1):59-62.