眼肌麻痹
频率:CIDP中最常见的眼部并发症,见于3%–8%的病例1)
受累神经:外展神经(VI)最常见,动眼神经(III)也可受累
特点:可双侧发生,抗硫脂IgM抗体阳性病例中更常见
预后:通过适当的免疫治疗有望改善

慢性炎性脱髓鞘性多发性神经根神经病(CIDP)是一种外周神经髓鞘被免疫介导机制损害的疾病。患病率为每10万人0.8至8.9人,可发生于所有年龄段,男性略多。日本(鸟取县)的患病率报告为每10万人0.8人。
CIDP本质上是一种以四肢肌无力和感觉障碍为主的多发性神经病,但也可波及脑神经。约15%的病例出现脑神经受累1),其中与眼相关的症状作为神经眼科临床表现尤为重要。
如果眼科医生漏诊CIDP的神经眼科并发症,可能会延误适当的全身治疗,导致不可逆的视功能损害。因此,准确理解CIDP的眼科并发症特征在临床上极为重要。
CIDP的神经眼科并发症中,患者主诉的主要自觉症状如下。
复视是最常见的眼部主诉,由眼外肌或其支配神经的损伤引起。上睑下垂由动眼神经(第三脑神经)功能障碍引起,可能先于复视或与之同时发生。视力下降和视野缺损见于视神经病变或严重的视乳头水肿,若不治疗可导致永久性视功能损害。眼球突出可能由眶内神经肥大或炎症引起的占位效应导致,虽然罕见但有报道。
CIDP的神经眼科临床表现主要分为五类。
眼肌麻痹
频率:CIDP中最常见的眼部并发症,见于3%–8%的病例1)
受累神经:外展神经(VI)最常见,动眼神经(III)也可受累
特点:可双侧发生,抗硫脂IgM抗体阳性病例中更常见
预后:通过适当的免疫治疗有望改善
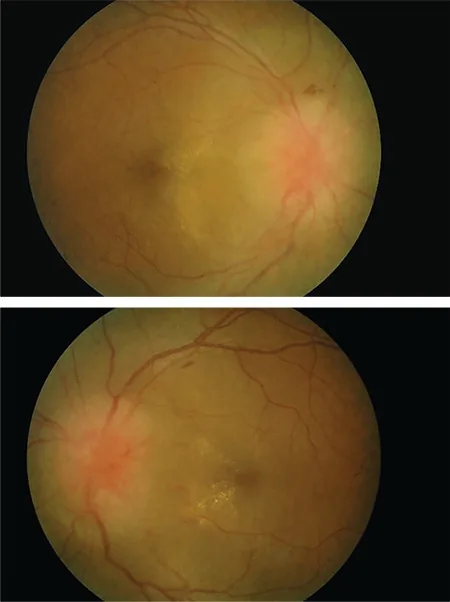
视乳头水肿
视神经病变
眼球突出和瞳孔异常
CIDP的发病机制是自身免疫性脱髓鞘,涉及T细胞介导和抗体介导的机制。针对髓鞘相关蛋白(P0、P2、PMP22)的自身免疫反应是病理基础。
CIDP的诊断基于2021年EAN/PNS诊断标准,综合临床、电生理、实验室和神经影像学检查结果4)。2021年标准的敏感性为74%–83%,特异性为94%–98%,与2010年标准相比,诊断类别更加简化4)。
在CIDP确诊后,或确诊前出现神经眼科症状时,以下检查至关重要。
| 检查 | 目的 | 所见 |
|---|---|---|
| 脑脊液检查 | 确认蛋白升高 | 蛋白升高(典型表现为细胞数正常);Bahramy 2024病例中蛋白210 mg/dL2) |
| 神经传导检查 | 脱髓鞘的电生理证据 | 传导速度减慢、传导阻滞、远端潜伏期延长 |
| 神经超声/MRI | 确认神经肥大 | 颈部和臂丛神经肥大对CIDP几乎具有特异性4) |
| 眼眶MRI | 评估眼球突出和神经肥大 | 评估视神经和外眼肌的变化 |
| 眼底检查和光学相干断层扫描(OCT) | 评估视乳头水肿和视神经萎缩 | 确认视乳头隆起和视网膜神经纤维层变薄 |
| 血液检查 | 抗体和基础疾病的详细检查 | 抗神经病变抗体、抗硫脂抗体、血糖、肿瘤标志物 |
在2021年EAN/PNS诊断标准中,神经超声和MRI被明确列为不符合电生理学标准病例的辅助诊断标准4)。周围神经显著肥大对CIDP和CMT1型具有高度特异性,确认这些表现有助于提高敏感性。眼眶MRI可评估视神经和眶内神经的肥大或浸润,对眼球突出的鉴别诊断有用。
CIDP神经眼科并发症的治疗基本原则是通过全身免疫疗法控制基础疾病。治疗应在神经内科医生和眼科医生的密切合作下进行。
一线治疗包括以下三种已确立的方案。
皮质类固醇如口服泼尼松龙或静脉注射甲泼尼龙,通过抗炎和免疫抑制作用抑制脱髓鞘。长期使用需注意白内障、青光眼和感染风险,建议定期眼科检查。
静脉注射免疫球蛋白(IVIg)标准剂量为2 g/kg(分5天给药),可有效改善急性期神经症状1)。Chen 2023报道的眼肌麻痹病例中,IVIg与糖皮质激素联合使用在3个月内实现完全恢复1)。
血浆置换疗法用于对上述治疗无反应的病例,旨在清除自身抗体。
对于难治性或复发性病例,使用利妥昔单抗、硼替佐米、硫唑嘌呤和环孢素等免疫抑制剂。Kim 2023报道的COVID-19疫苗接种后CIDP病例中,采用泼尼松龙、硫唑嘌呤和IVIg三联治疗3)。
对于难治性视乳头水肿,可能需要使用乙酰唑胺降低颅内压,以及视神经鞘开窗术以保护视功能。
CIDP中神经眼科并发症的发病机制与周围神经病变相同。自身免疫性T细胞和自身抗体作用于动眼神经和视神经的髓鞘或轴突,导致功能障碍。
Chen L等人(J Int Med Res. 2023)分析了14例患者,包括伴有眼肌麻痹的CIDP患者,显示抗硫脂IgM抗体阳性与眼肌麻痹相关。该研究中,14例患者中有8例(57%)确认有颈部和臂丛神经肥大,神经肥大组的病程平均为15.9年,显著长于无肥大组的3.3年1)。
Bahramy MA等人(BMC Neurol. 2024)报告了一例接种国药(灭活)疫苗后发生CIDP的病例。脑脊液蛋白显著升高至210 mg/dL(正常值<45 mg/dL),白细胞计数为4/μL,在正常范围内2)。
Kim S等人(J Korean Med Sci. 2023)报告了两例接种mRNA-1273疫苗和Ad26.COV2.S疫苗后发生CIDP的病例3)。两例均在接种后数周内出现症状,但因果关系尚未确定。COVID-19疫苗后CIDP的机制可能涉及分子模拟、佐剂效应和免疫激活,但目前尚不能排除偶然关联。
Rathore H, Thaker N(Indian J Nucl Med. 2023)报告了一例因CIDP样症状被随访的患者最终被诊断为POEMS综合征的病例5)。视乳头水肿是POEMS诊断标准中的次要项目,鉴别CIDP和POEMS必须评估血清M蛋白、VEGF和器官肿大。
2021年EAN/PNS诊断标准是对2010年标准的修订,经验证诊断灵敏度为74–83%,特异度为94–98% 4)。主要改进是将神经超声和MRI正式纳入辅助诊断标准。周围神经显著肥大对CIDP和CMT1型具有高度特异性,有助于提高不符合电生理标准病例的诊断灵敏度 4)。
全球已报告多例COVID-19疫苗接种后发生CIDP的病例,涉及病毒载体疫苗、mRNA疫苗和灭活疫苗 2, 3)。然而,确立因果关系需要流行病学发病率比较和生物学机制的阐明;目前尚不能排除偶然关联。
Chen L, Dong W, Li J, et al. Chronic inflammatory demyelinating polyneuropathy with ophthalmoplegia and anti-sulfatide IgM antibody positivity: a case report and literature review. J Int Med Res. 2023;51(9):3000605231198994.
Bahramy MA, Moridnejad M, Shariati M, et al. Chronic inflammatory demyelinating polyneuropathy following COVID-19 vaccination: a case report. BMC Neurol. 2024;24(1):294.
Kim S, Kim HJ, Kim SM, et al. Two Case Reports of Chronic Inflammatory Demyelinating Polyneuropathy After COVID-19 Vaccination. J Korean Med Sci. 2023;38(9):e73.
Kuwabara S, Suichi T. Validation of the 2021 EAN/PNS diagnostic criteria for chronic inflammatory demyelinating polyneuropathy. J Neurol Neurosurg Psychiatry. 2022;93(12):1237-1238.
Rathore H, Thaker N. POEMS Syndrome Masquerading as Chronic Inflammatory Demyelinating Polyneuropathy. Indian J Nucl Med. 2023;38(1):59-62.