眼筋麻痺
頻度:CIDPの3〜8%に認められる最多の眼科合併症1)
侵される神経:外転神経(第VI)が最多、動眼神経(第III)も関与
特徴:両側性に生じることがあり、抗硫脂質IgM抗体陽性例で多い
予後:適切な免疫療法により改善が期待できる
慢性炎症性脱髄性多発根神経炎(CIDP)は、末梢神経の髄鞘が免疫介在性に障害される疾患である。有病率は10万人あたり0.8〜8.9人であり、あらゆる年齢層に発症するが、男性にやや多い傾向がある。日本(鳥取県)の有病率は10万人あたり0.8人と報告されている。
CIDPは本来、四肢の筋力低下や感覚障害を主体とする多発ニューロパチーであるが、脳神経にも波及することがある。脳神経障害は約15%の症例に認められ1)、その中でも眼に関連する症状は神経眼科的臨床像として特に重要視される。
眼科医がCIDPの神経眼科的合併症を見逃すと、適切な全身治療の開始が遅れ、不可逆的な視機能障害を招く可能性がある。したがって、CIDPにおける眼科的合併症の特徴を正確に理解することは臨床上きわめて重要である。
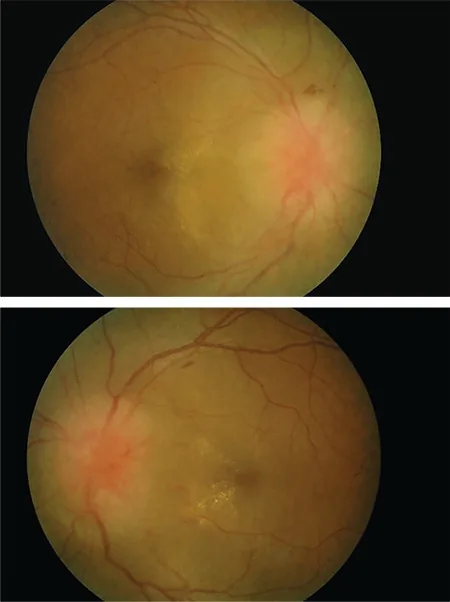
CIDPの神経眼科的合併症として患者が訴える主な自覚症状は以下のとおりである。
複視は最も多い眼科的愁訴であり、外眼筋あるいはその支配神経の障害によって生じる。眼瞼下垂は動眼神経(第III脳神経)の障害で起こり、複視に先行または併発することがある。視力低下や視野障害は視神経症あるいは重篤な乳頭浮腫で認められ、放置すると永続的な視機能障害につながる。眼球突出は眼窩内の神経肥大や炎症による空間占拠で生じる場合があり、まれではあるが報告されている。
CIDPの神経眼科的臨床像は主に5つのカテゴリに分類される。
眼筋麻痺
頻度:CIDPの3〜8%に認められる最多の眼科合併症1)
侵される神経:外転神経(第VI)が最多、動眼神経(第III)も関与
特徴:両側性に生じることがあり、抗硫脂質IgM抗体陽性例で多い
予後:適切な免疫療法により改善が期待できる
乳頭浮腫
視神経症
眼球突出・瞳孔異常
CIDPの発症機序は自己免疫性の脱髄であり、T細胞介在性および抗体介在性の機序が関与する。髄鞘関連蛋白(P0・P2・PMP22)に対する自己免疫反応が病理の基盤となっている。
CIDPの診断は2021年EAN/PNS診断基準に基づき、臨床・電気生理・検査・神経画像所見を総合して行う4)。2021年基準の感度は74〜83%、特異度は94〜98%であり、2010年基準と比較して診断カテゴリが簡略化された4)。
CIDPの確定診断後、あるいは確定前に神経眼科的症状が出現した場合、以下の検査が重要となる。
| 検査 | 目的 | 所見 |
|---|---|---|
| 脳脊髄液検査 | 蛋白上昇の確認 | 蛋白上昇(細胞数正常が典型);Bahramy 2024例では蛋白210 mg/dL2) |
| 神経伝導検査 | 脱髄の電気生理的証拠 | 伝導速度低下・伝導ブロック・末梢潜時延長 |
| 神経超音波・MRI | 神経肥大の確認 | 頸部・腕神経叢の肥大はCIDPにほぼ特異的4) |
| 眼窩MRI | 眼球突出・神経肥大の評価 | 視神経・外眼筋の変化を評価 |
| 眼底検査・光干渉断層計(OCT) | 乳頭浮腫・視神経萎縮の評価 | 乳頭隆起・網膜神経線維層菲薄化を確認 |
| 血液検査 | 抗体・基礎疾患の精査 | 抗ノドパシー抗体・抗硫脂質抗体・血糖・腫瘍マーカー |
2021年EAN/PNS診断基準では、神経超音波およびMRIが電気生理学的基準を満たさない症例に対する補助的診断基準として明記されている4)。末梢神経の著明な肥大はCIDPとCMT1型に特異性が高く、これらが確認されれば感度の向上に貢献する。眼窩MRIは視神経や眼窩内神経の肥大・浸潤を評価し、眼球突出の鑑別診断に有用である。
CIDPの神経眼科的合併症に対する治療の基本方針は、全身免疫療法による基礎疾患のコントロールである。神経内科医と眼科医の緊密な連携のもとで治療を進める。
第一選択治療として以下の3つが確立されている。
副腎皮質ステロイドはプレドニゾロン経口投与またはメチルプレドニゾロン静脈投与が用いられ、抗炎症・免疫抑制効果によって脱髄を抑制する。長期使用では白内障・緑内障・感染症リスクに注意が必要であり、眼科定期検診が推奨される。
免疫グロブリン静注療法(IVIg)は2 g/kg(5日間分割投与)が標準的であり1)、急性期の神経症状改善に有効である。Chen 2023の眼筋麻痺症例では、IVIgとグルココルチコイドの併用により3か月での完全回復が得られた1)。
血漿浄化療法(血漿交換)は上記に反応しない症例に使用され、自己抗体の除去が目的である。
難治性・再発性症例に対してはリツキシマブ・ボルテゾミブ・アザチオプリン・シクロスポリンなどの免疫抑制薬が使用される。Kim 2023のCOVID-19ワクチン後CIDP例では、プレドニゾロン・アザチオプリン・IVIgの三剤併用で治療が行われた3)。
難治性乳頭浮腫に対しては、アセタゾラミドによる頭蓋内圧降下療法、および視神経鞘切開術(optic nerve sheath fenestration)が視機能温存のために必要となる場合がある。
CIDPにおける神経眼科的合併症の発症機序は、末梢神経障害の機序と同一である。自己免疫性T細胞と自己抗体が眼球運動神経・視神経の髄鞘または軸索に作用し、機能障害をきたす。
Chen L et al.(J Int Med Res. 2023)は、眼筋麻痺を呈したCIDP患者を含む14例を解析し、抗硫脂質IgM抗体陽性と眼筋麻痺との関連を示した。同研究によれば、患者14例中8例(57%)に頸部・腕神経叢の肥大が確認され、神経肥大を有する群では病歴が平均15.9年と、肥大なし群の3.3年より有意に長かった1)。
Bahramy MA et al.(BMC Neurol. 2024)は、Sinopharm(不活化)ワクチン接種後にCIDPを発症した症例を報告した。脳脊髄液蛋白は210 mg/dL(正常値 < 45 mg/dL)と著明に上昇し、白血球数4/μLと細胞数は正常範囲内であった2)。
Kim S et al.(J Korean Med Sci. 2023)は、mRNA-1273ワクチンおよびAd26.COV2.Sワクチン接種後にCIDPを発症した2例を報告した3)。いずれも接種から症状発現まで数週間以内であったが、因果関係の確立には至っていない。COVID-19ワクチン後のCIDPは分子相同性・アジュバント効果・免疫活性化などが考えられているが、現時点では偶発的関連が否定できない段階にある。
Rathore H, Thaker N(Indian J Nucl Med. 2023)は、CIDP様症状で経過観察されていた患者がPOEMS症候群であったと判明した症例を報告した5)。乳頭浮腫はPOEMSの診断基準マイナー項目に含まれており、CIDPとPOEMSの鑑別には血清M蛋白・VEGF・臓器肥大の評価が不可欠である。
2021年EAN/PNS診断基準は2010年基準を改訂したものであり、感度74〜83%・特異度94〜98%という診断精度が検証されている4)。神経超音波とMRIが補助診断基準として正式に組み込まれた点が大きな改良点である。末梢神経の著明な肥大はCIDPとCMT1型に特異性が高く、電気生理基準を満たさない症例での診断感度向上に寄与する4)。
COVID-19ワクチン接種後のCIDP発症例は世界各地から報告されており、ウイルスベクターワクチン・mRNAワクチン・不活化ワクチンの種別を問わず症例が集積しつつある2, 3)。しかしながら、因果関係の確立には疫学的な発症率比較や生物学的機序の解明が必要であり、現時点では偶発的関連が否定できない段階にある。
Chen L, Dong W, Li J, et al. Chronic inflammatory demyelinating polyneuropathy with ophthalmoplegia and anti-sulfatide IgM antibody positivity: a case report and literature review. J Int Med Res. 2023;51(9):3000605231198994.
Bahramy MA, Moridnejad M, Shariati M, et al. Chronic inflammatory demyelinating polyneuropathy following COVID-19 vaccination: a case report. BMC Neurol. 2024;24(1):294.
Kim S, Lee EK, Sohn E. Two Case Reports of Chronic Inflammatory Demyelinating Polyneuropathy After COVID-19 Vaccination. Journal of Korean medical science. 2023;38(8):e57. doi:10.3346/jkms.2023.38.e57. PMID:36852853; PMCID:PMC9970789.
Kuwabara S, Suichi T. Validation of the 2021 EAN/PNS diagnostic criteria for chronic inflammatory demyelinating polyneuropathy. J Neurol Neurosurg Psychiatry. 2022;93(12):1237-1238.
Rathore H, Thaker N. POEMS Syndrome Masquerading as Chronic Inflammatory Demyelinating Polyneuropathy. Indian J Nucl Med. 2023;38(1):59-62.