偏头痛 在15岁以上人群中发病率为8.4%,女性(12.9%)约为男性(3.6%)的3倍。闪光暗点是双眼性、同向性的,锯齿状的光从中心向周边在20-30分钟内扩大并消失。
超过90%有先兆的病例出现视觉先兆,典型病例在闪光暗点之后出现头痛。
一过性黑蒙 是单眼性、持续1-5分钟的阴性症状,与闪光暗点的鉴别很重要。亚型包括视网膜 性偏头痛 、偏瘫性偏头痛 和复发性疼痛性眼肌麻痹性神经病(RP ON)。
急性期使用曲普坦类药物和非甾体抗炎药,预防使用洛美利嗪盐酸盐、β受体阻滞剂 和托吡酯。
有先兆的偏头痛 是脑卒中的危险因素,RP ON的MRI显示动眼神经增强。
偏头痛 是一种血管性头痛,是由颈外动脉分支扩张引起的发作性头痛疾病。反复出现搏动性头痛,分为有先兆和无先兆两大类。闪烁暗点是偏头痛 前典型的视觉先兆,传统上解释为由血管痉挛导致枕叶视觉区域一过性缺血引起的锯齿状光。目前,皮质扩散性抑制(CSD)被理解为主要发病机制(参见§6)。
伴有恶心、畏光 、畏声和视觉先兆,持续4至72小时。分为发作性(每月少于15天)和慢性(每月15天以上,持续3个月以上)。
15岁以上人口中8.4%患有偏头痛 。
男性3.6%,女性12.9%,30多岁发病率最高。
估计终生患病率为16%,女性约为男性的2倍1) 。
它是全球第三大常见疾病,也是50岁以下人群致残的首要原因1) 。
以下是国际头痛分类第三版(ICHD-3)中偏头痛 的亚型。
1.1 无先兆偏头痛 :最常见的亚型。不伴有视觉先兆。1.2 有先兆偏头痛 :
1.2.1 伴典型先兆的偏头痛 (1.2.1.1 伴头痛、1.2.1.2 不伴头痛)
1.2.2 伴脑干先兆的偏头痛
1.2.3 偏瘫型偏头痛 (1.2.3.1 家族性偏瘫型偏头痛 FHM)
1.2.4 视网膜 型偏头痛
1.3 慢性偏头痛 :每月头痛≥15天,持续>3个月。1.4 偏头痛 并发症 :包括偏头痛 性脑梗死(1.4.3)在内的严重并发症。1.6 与偏头痛 相关的周期性综合征 :儿童周期性呕吐等。
无头痛的视觉先兆 :多见于老年偏头痛 患者。需与TIA和枕叶癫痫 鉴别。基底型偏头痛 (伴脑干先兆的偏头痛 ) :伴有眩晕、共济失调、耳鸣和复视 。视网膜 偏头痛 视网膜 动脉缺血。偏瘫型偏头痛 :先兆伴可逆性运动无力。患病率0.01%。分为家族性(CACNA1A、ATP1A2、SCN1A基因突变)和散发性2) 。
复发性疼痛性眼肌麻痹性神经病(Recurrent Painful Ophthalmoplegic Neuropathy:RP ON),旧称“眼肌麻痹性偏头痛 ”,在ICHD-3中更名。更名的原因是其更符合脱髓鞘性炎性神经病的特征,而非偏头痛 。
这是一种罕见的疾病,以反复发作的头痛和同侧眼肌麻痹为特征,发病率为每百万人0.7例。主要发生于10岁以下儿童,中位发病年龄为8岁。也有成人发病的报道,一项对165例病例的汇总分析显示,平均发病年龄为22.1岁,34.2%的患者在18岁或以上发病6) 。动眼神经(III)最常受累,其次是外展神经(VI)和滑车神经(IV)。
Q
为什么偏头痛会出现眼部症状?
A
皮质扩散性抑制(CSD)和三叉神经 血管系统的参与是主要原因。CSD是从枕叶视觉皮层开始的神经元去极化波,引起闪光暗点。此外,三叉神经 血管系统的激活释放CGRP 、P物质等炎症物质,导致血管扩张和神经源性炎症,引起畏光 和头痛。
畏光 (光敏感)偏头痛 患者最常见的眼部症状。光线会使头痛加重。几乎总是双侧性。视觉先兆(闪光暗点) :锯齿状、锯齿状或新月形的闪烁光从视野中心向周边扩展和移动。20-30分钟内消失,之后常出现搏动性头痛。特征为双眼性和同向性。90%以上的先兆病例存在视觉先兆。发作频率 :患者之间差异很大,从每月一次到每周两次。疼痛在1-2小时内达到高峰,常伴有恶心和呕吐。视觉残留(视像滞留) :视野中消失的物体留下残像。常见于有先兆的偏头痛 。视觉雪 :像电视雪花一样的小颗粒遍布整个视野。可持续数年。60%的视觉雪综合征 (VSS )患者合并偏头痛 。爱丽丝梦游仙境综合征 (AIWS)良性发作性单侧瞳孔 散大(BEUM) :伴有间歇性视物模糊 和“头脑昏沉”的感觉。
Q
闪光暗点和一过性黑蒙有什么区别?
A
主要区别在于视觉症状的性质、单侧性和持续时间三点。闪光暗点是锯齿状光线的阳性症状,双眼性,持续20-30分钟(最长60分钟)。一过性黑蒙 是变暗、变灰的阴性症状,单眼性,在1-5分钟(最长10分钟)内短暂消失。一过性黑蒙 可能由颈动脉或眼动脉栓塞引起,不可忽视。
以下显示呈现眼科体征的各亚型的临床所见。
视网膜偏头痛
单眼视力 丧失 :可逆的单眼视力 下降或消失。
暗点 :C字形、着色、闪烁、扩大的暗点。至少发作2次方可诊断。
排除TMVL :必须鉴别严重病因(动脉炎、栓塞)。
偏瘫性偏头痛
运动无力 :单侧可逆的运动麻痹作为先兆出现。
多种先兆 :伴有视觉、感觉和语言症状。每种症状持续5至60分钟。
ICHD-3标准 :在≥5分钟内发展,头痛在先兆期间或之后60分钟内出现2) 。
RPON(眼肌麻痹性神经病变)
第三脑神经麻痹 :动眼神经最常受累(儿童)。上睑下垂 、眼球运动障碍 、瞳孔 散大。
MRI表现 :急性期动眼神经局部强化和增厚。一项52例文献综述报告MRI第三神经强化率为75%,神经肿胀率为76%6) 。
复发性 :需要两次或以上发作才能确诊。有些病例随着反复发作,恢复变得不完全9) 。
基底型偏头痛
脑干症状 :伴有眩晕、构音障碍、共济失调、耳鸣和听力丧失。
复视
晕厥 :严重病例可能出现短暂意识丧失。
头痛 :单侧性,眼眶 周围或眼眶 后部最剧烈。通常持续数天至1周左右,比典型偏头痛 (<72小时)更长的倾向。不一定具有偏头痛 样特征(ICHD-III标准)。多达1/3的患者没有偏头痛 的典型特征。伴随症状 :畏光 65%,恶心66%,呕吐69%(Gelfand等人的系统综述)。复视 和上睑下垂 无先兆 :未报告视觉、感觉或语言先兆,是与典型偏头痛 的重要鉴别点。
从头痛发作到眼肌麻痹出现,有即刻至最长14天的时间差。眼肌麻痹通常在2周至3个月内自然消失,但反复发作后可能出现不完全恢复。长期复发的病例中,54%出现持续性眼运动麻痹9) 。
动眼神经(第III对)
上睑下垂
眼球运动受限 :内转、上转、下转受限。
瞳孔 散大及对光反射减弱瞳孔 运动纤维常受累。但McMillan等人对39例病例的回顾显示,23%的患者瞳孔 未受累。
外展神经(第VI对)
外展麻痹 :因外展受限导致的内斜视 。
在成人中,这是RP ON最常受累的脑神经。
滑车神经(第IV对)
下转和内旋受限 :主要症状为垂直复视 。
可见代偿性对侧头位倾斜。受累相对罕见。
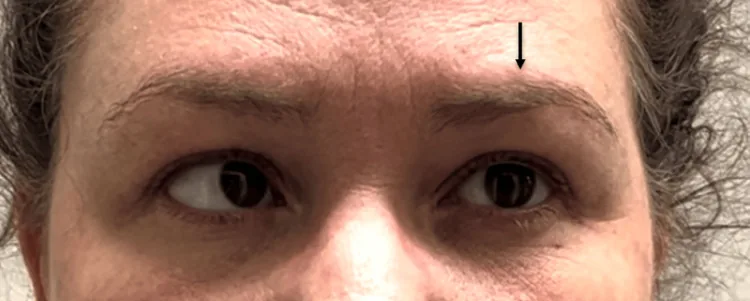
疼痛性眼肌麻痹性神经病变外展缺陷 Nonpharmacologic Management of Recurrent Painful Ophthalmoplegic Neuropathy: A Case Report. Cureus. 2025 May 28; 17(5):e84387. Figure 2. PM
CI D: PMC12178448. License: CC BY.
尝试向左注视。由于左侧第六脑神经(外展神经)麻痹,左眼保持中立位,而右眼完全内收。图像经患者同意获取并展示。添加箭头以强调
典型偏头痛 的眼科检查(包括视野检查 )通常正常。偏头痛 发作期间进行OCTA (光学相干断层扫描 血管成像)可显示脉络膜 血管密度显著降低和黄斑 中心凹 无血管区(FA Z)扩大。
Q
眼肌麻痹多久能好?
A
通常2周至3个月内自行消失,但反复发作后部分病例恢复不完全。据报道,长期复发病例中54%出现持续性眼运动麻痹9) 。发病后自然改善,但每次发作持续时间可能延长,部分病例可永久化。
生活习惯 :月经周期(月经相关偏头痛 )、压力、睡眠不规律。饮食 :酒精(尤其是红酒、啤酒)、味精、咖啡因、陈年奶酪、阿斯巴甜、巧克力。药物 :口服避孕药、雌激素疗法、鼻塞缓解药、阿片类药物、SSRI。感觉刺激 :天气变化、特定声音、气味、光线。光线是加重急性偏头痛 最常见的诱因。
人口统计学因素 :女性、肥胖、糖尿病、头部外伤、压力。慢性化风险 :急性期药物过度使用(镇痛药≥15天/月、曲普坦≥10天/月)、急性期治疗不足。遗传因素 :家族性偏瘫性偏头痛 中,CACNA1A、ATP1A2、SCN1A基因突变(常染色体显性遗传 )2) 。卒中风险 :有先兆的偏头痛 是卒中的危险因素。在45岁以下同时使用口服避孕药和吸烟的女性中风险尤其高。
偏头痛 病史偏头痛 病史常见。感染前驱 :有报道在病毒性胃肠炎后10) 和鼓膜炎后8) 发病的病例。感染可能诱发免疫介导的神经病变。妊娠 :有报道在妊娠19周发病、产后第5天自然缓解的病例,提示与激素和生理变化相关7) 。地域差异与遗传多样性 :在尼日利亚人群中,已报告与异常血红蛋白存在关联。
记录头痛日记,记下诱因、频率和持续时间。
识别并避免个人诱因,如过量饮酒、咖啡因或特定食物。
保持规律作息,管理压力。
由于闪光暗点不一定伴随头痛,长期管理很重要,不要过度拘泥于偏头痛 的诊断。
过度使用急性期治疗药物会使头痛更容易慢性化。请遵守用法用量使用。
Q
有哪些食物或药物会加重偏头痛?
A
食物方面,红葡萄酒、啤酒、巧克力、陈年奶酪、味精(谷氨酸钠)、阿斯巴甜等已知为诱因。药物方面,口服避孕药、雌激素疗法、鼻塞缓解药、阿片类药物、SSRI可能诱发或加重偏头痛 。诱因个体差异很大,因此通过头痛日记进行自我观察很重要。
偏头痛 的诊断基于病史、体格检查和ICHD-3标准。典型症状无需影像学检查。诊断辅助工具有ID-Migraine、VARS、MIDAS问卷和MS Q 2.11) 。
如果怀疑偏头痛 ,首先通过CT或MRI排除脑血管疾病或肿瘤性疾病等器质性疾病。然后开具抑制血管痉挛的药物,确认发作能否被该药物终止,从而做出诊断。
影像学检查(脑MRI/CT)的适应症仅限于以下情况:
无法解释的异常神经学体征
40岁以后新发或进行性恶化
怀疑偏头痛 性脑梗死
突发剧烈头痛(需排除蛛网膜下腔出血)
进行全面的眼科检查(视力 、视野、眼球运动、对光反射、眼底检查 、裂隙灯 检查)。在RP ON中,MRI显示脑神经的局限性增厚和强化是特征性表现3) 。
通过比较以下三点可以进行鉴别。
项目 闪光暗点 一过性黑矇 视觉症状的性质 阳性(锯齿状闪光) 阴性(变暗/变灰) 眼的单侧性 双眼性、同侧性 多为单眼性 持续时间 20~30分钟(60分钟以内) 1~5分钟(10分钟以内)
RP ON 的国际头痛分类第三版(ICHD-III)诊断标准如下。
A . 至少2次发作符合标准BB . (1) 单侧头痛,(2) 伴有同侧第III、IV、VI脑神经中一条或多条的不全麻痹C . 通过适当检查排除眼眶 、鞍旁或后颅窝病变D . 不能用其他ICHD-3诊断更好地解释
MRI是诊断最重要的检查。特征性表现为动眼神经脑池段的局部强化和增厚。文献综述52例中,MRI显示第III神经强化75%、神经肿胀76%10) 。但急性期25-81%的病例MRI可能正常。强化通常在7-9周内消失,但部分病例可持续2-4年。
首次发作即推荐进行包括TOF-MRA在内的完整MRI评估5) 。在涉及瞳孔 运动功能的动眼神经麻痹 中,MRA对于排除大脑后动脉(PCA)动脉瘤尤为重要。
与表现类似症状的疾病进行鉴别很重要。
疾病 鉴别要点 Tolosa-Hunt综合征(THS ) MRI显示海绵窦 壁增厚。对类固醇 反应显著。 动眼神经施万瘤 造影增强持续12周以上(RP ON在12周内消失)11) 重症肌无力 日间波动和疲劳性。冰袋试验和抗AChR抗体 后交通动脉瘤 伴有瞳孔 散大的动眼神经麻痹 。紧急行MRA/CTA评估 有先兆偏头痛 眼肌麻痹在72小时内消失(RP ON持续≥2周)
紧张型头痛和丛集性头痛 :根据头痛性质和伴随症状进行鉴别。TIA・枕叶癫痫 :与无头痛的视觉先兆鉴别。外伤、感染、先天性疾病继发的头痛 :需排除继发性头痛。
临床检查包括脑脊液检查(通常正常,用于与恶性肿瘤和多发性硬化鉴别)5) ,以及血液检查以排除糖尿病、感染、炎症和自身免疫性疾病。
Q
MRI正常时是否可能患有RPON?
A
有可能。急性期25–81%的病例MRI可能正常5) 。对于MRI正常的RP ON,有报道采用NSAID观察反应的方法。但反复发作或持续发作的病例必须复查MRI以排除其他器质性病变。
偏头痛 的治疗包括预防药物、先兆期(出现先兆时)使用的药物以及发作期使用的药物,需区分使用。
轻度发作可使用非甾体抗炎药(NSAIDs)、双氢麦角胺甲磺酸盐和口服曲普坦类药物。重度发作则使用口服曲普坦类药物。
非甾体抗炎药(布洛芬、阿司匹林) :副作用比曲普坦轻微。曲普坦(舒马曲普坦25~100毫克) :比非甾体抗炎药更有效。曲普坦联合非甾体抗炎药比单药治疗的2小时疼痛消失率更高1) 。舒马曲普坦有口服、皮下注射和鼻喷雾剂可用。双氢麦角胺甲磺酸盐(Dihydergot) :对轻度至中度发作有效。拉米地坦 :5-HT1F受体激动剂。急性期治疗的新型药物1) 。
出现先兆时,应尽早使用双氢麦角胺甲磺酸盐。由于在偏头痛 发作早期给药可提高疗效,因此在感知到先兆时迅速给药非常重要。
洛美利嗪盐酸盐(Migsis) :钙拮抗剂。广泛用作预防药物。双氢麦角胺甲磺酸盐(Dihydergot) :也用作预防药物。β受体阻滞剂 1) 。托吡酯 :有报告称可减少发作频率并改善生活质量1) 。阿米替林 :有分析认为其效果优于普萘洛尔和托吡酯1) 。丙戊酸、维拉帕米、加巴喷丁 :有报告显示预防效果1) 。肉毒杆菌毒素 :对慢性偏头痛 的疗效优于安慰剂1) 。核黄素(维生素B2)、镁、辅酶Q10 :针对氧化应激 和神经兴奋性过高的补充疗法1) 。
偏瘫型偏头痛 2) :
尚无标准化的治疗指南。急性期使用非甾体抗炎药和非麻醉性镇痛药。预防用药包括β受体阻滞剂 、钙通道阻滞剂、三环类抗抑郁药和抗癫痫药 。对于频繁发作,可使用长效维拉帕米或拉莫三嗪。
发病后症状可自然改善,但部分发作持续时间延长并可能永久化,因此建议积极进行抗炎治疗。
皮质类固醇 是最常见的急性期治疗。汇总分析显示,76例接受类固醇 治疗的患者中96.2%迅速改善6) 。对于动眼神经麻痹 的炎性病变,首先给予泼尼松龙50-60mg/日,连用3天,然后逐渐减量,注意避免复发。
主要类固醇 治疗方案如下所示。
方案 用法用量 报告 甲泼尼龙(儿童) 25–30 mg/kg/天(最大1 g/天)×5天 Frattini 20235) 、Nandana 20219) 甲泼尼龙(成人) 250 mg 每日4次,共3天 → 泼尼松60 mg逐渐减量 Koo 20246) 地塞米松(静脉注射) 13.2 mg 共12天 Takemoto 20218)
对类固醇 的反应通常不如Tolosa-Hunt综合征那样显著。
对于MRI正常的RP ON,一种选择是使用NSAID(布洛芬10 mg/kg/次,每日3次)进行观察。有报道称使用布洛芬后48小时内完全恢复5) 。
如果频繁复发,考虑以下预防药物。
钙拮抗剂 :氟桂利嗪5 mg/日9) ,维拉帕米β受体阻滞剂 三环类抗抑郁药 :阿米替林25 mg+丙戊酸钠500 mg联合使用,有报告称一年内无复发6) 抗癫痫药 10)
注意托吡酯诱发的急性闭角(TiAAC) :用于偏头痛 的处方占59.7%。75.3%为女性,平均发病时间为开始服用托吡酯后14.1天(平均眼压 41 mmHg)。由睫状体 脉络膜 渗出导致晶状体 虹膜 隔前移引起。发病时立即停用托吡酯,并给予局部降眼压 药和散瞳药 。平均恢复时间为3.9天4) 。偏瘫型偏头痛 禁用曲普坦类和麦角胺类药物 :因其血管收缩作用会增加卒中风险,不得使用2) 。RP ON 类固醇 治疗期间注意眼压 升高眼压 升高至22 mmHg,使用0.5%马来酸噻吗洛尔滴眼液后改善8) 。长期使用类固醇 的病例需要定期测量眼压 。
Q
预防药物托吡酯有眼部副作用吗?
A
托吡酯广泛用于偏头痛 预防,但在开始用药后约2周可能引起急性闭角(TiAAC)。睫状体 脉络膜 渗出导致晶状体 虹膜 隔前移,眼压 急剧升高。如果出现眼痛 、视力 下降或视物模糊 ,应立即就诊眼科并联系处方医生4) 。
Q
RPON有预防药物吗?
A
氟桂利嗪、维拉帕米等钙拮抗剂,普萘洛尔等β受体阻滞剂 ,以及丙戊酸、加巴喷丁、托吡酯等抗癫痫药 物被用作预防药物。由于有30%的永久性后遗症风险,在频繁复发的情况下,考虑积极的预防治疗非常重要6) 。
偏头痛 的基本机制是脑膜、血管和三叉神经 支配区域的刺激,由颈外动脉分支的扩张触发1) 。
压力、食物、激素等诱因 → 脑干血管调节异常 → 外周血管扩张 → 三叉神经 元的牵拉信号 → CGRP 、白细胞介素等炎症和血管活性物质的产生 → 进一步扩张和血管通透性增加 → 组织水肿形成级联反应1) 。
涉及的神经递质包括P物质、一氧化氮和CGRP 。中脑导水管周围灰质(PAG)、蓝斑核(LC)和中缝核(DRN)被认为是参与偏头痛 病理生理的脑区。
传统上认为脑血管痉挛导致枕叶视觉区一过性缺血,从而引起闪光暗点。目前,皮质扩散性抑制(CSD)被广泛认为是视觉先兆的主要机制2) 。
起源于枕部的神经元去极化波向前传播。去极化使钾浓度升高,兴奋性氨基酸的释放进一步增强扩散。CSD导致枕部视觉皮层暂时功能障碍,对应闪光暗点的发生。
基底型偏头痛 :涉及脑干的CSD。视网膜 偏头痛 视网膜 中的CSD(但也有很多证据提示皮质机制,有观点指出“视网膜 偏头痛 ”是误称)。偏瘫性偏头痛 :软脑膜血管的血管源性渗漏刺激三叉神经 血管系统,引起作为先兆的偏瘫2) 。畏光 视锥细胞 驱动的视网膜 通路 → 光敏感丘脑神经元加皮质过度兴奋的机制。AIWS和视觉雪 :AIWS由视觉通路的短暂缺血引起。视觉雪与次级视觉皮层(舌回、布罗德曼19区)的高代谢有关。
关于RP ON的发病机制,已提出多种假说,目前仍在讨论中。
脱髓鞘/炎症学说(主流)
Lance & Zagami :复发性脱髓鞘性神经病/神经炎学说。MRI动眼神经增强被认为是其依据。
Carlow假说 :三叉神经 眼支的神经肽级联反应诱发Willis环的无菌性炎症性血管反应。反复脱髓鞘和再髓鞘化导致施万细胞洋葱球样增生8) 。
缺血学说
Ambrosetto等 :偏头痛 时神经滋养血管痉挛→血-神经屏障可逆性缺血性破坏→血管源性水肿(解释MRI增强和增厚)。
Vijayan等 :ICA壁水肿→小血管开口闭塞→分水岭梗死型损伤。Shin等人的SPECT研究证实了PCA穿支区域的可逆性同侧缺血。
神经血管压迫学说
Bui等人 报告了一例13岁男孩,MRA显示左侧大脑后动脉(PCA)的锐利环压迫动眼神经出口处10) 。
反对压迫学说的论据:(1) 23%的病例瞳孔 保留,(2) 发作期颈动脉造影未证实血管狭窄,(3) RP ON的恢复比解除压迫后更缓慢。
在这些假说中,脱髓鞘/炎症学说目前是主流。已指出与CI DP、MS 和MOGAD 的复发缓解型模式相似,但脑脊液检查通常正常,且未获得病毒感染或免疫介导神经病变的直接证据。
在自发性偏头痛 发作期间,OCTA 显示脉络膜 血管密度显著降低和无血管区(FA Z)扩大。这些发现表明发作期间脉络膜 循环比视网膜 循环更脆弱。
已知与家族性偏瘫性偏头痛 相关的基因有三种:CACNA1A(钙通道)、ATP1A2(钠钾泵)和SCN1A(钠通道)2) 。TREK基因(双孔钾通道)的突变与静息膜电位调节障碍和神经过度兴奋有关1) 。
Fremanezumab、erenumab和galcanezumab是FDA批准的慢性偏头痛 预防药物1) 。
抗CGRP 单克隆抗体的荟萃分析显示,50%应答率显著改善,每月偏头痛 天数和急性期药物使用量减少。广泛认为其获益-风险特征优于普萘洛尔和托吡酯1) 。
Galcanezumab采用240mg皮下注射负荷剂量,随后每月120mg持续5个月的方案,改善了头痛的严重程度、频率和持续时间。主要副作用包括注射部位瘙痒和皮疹1) 。
Ubrogepant于2019年获得FDA批准,是一种口服急性治疗药物,可用于有或无先兆的偏头痛 1) 。Atogepant正在开发为口服预防药物。
托那博沙是一种新型苯并吡喃分子,通过抑制胶质细胞-神经元间隙连接通讯来抑制CSD。一项39例RCT(Goadsby等人,2009年)显示其对预防先兆偏头痛 有效,但目前尚未获得FDA批准1) 。
双孔钾通道(TREK)突变导致静息膜电位调节障碍,引起神经元过度兴奋。针对TREK激活/抑制的治疗研究正在进行中1) 。
Takemoto等人(2021年)报告了一例14岁女性患者,因类固醇 诱导的眼压 升高使用0.5%马来酸噻吗洛尔滴眼液后,复视 在数天内显著改善,上睑下垂 和眼球运动障碍 完全消失8) 。推测局部噻吗洛尔可能通过三叉神经 血管系统的神经肽介导抑制对RP ON发挥效果。即使没有眼压 升高,β受体阻滞剂 滴眼液也可能有效,期待未来的探索性研究。
Koo等人(2024年)基于Liu等人的汇总分析,提出了修订诊断标准:“至少2次单侧头痛发作(几乎与眼肌麻痹同时或之前15天内)”+“脑神经麻痹的临床表现或MRI增强”6) 。关于纳入成人发病和非典型病例的讨论仍在继续。
Castillo-Guerrero等人(2024年)报告了一例妊娠期内眼肌麻痹性偏头痛 (仅双侧瞳孔 散大,无外眼肌麻痹)7) 。确认产后第5天自然缓解,提示激素和生理变化可能参与发病。
已有报道其与抗GQ1b抗体综合征相关,对于类固醇 迅速起效的复发病例,建议检查非典型抗GQ1b抗体综合征5) 。此外,高分辨率MRA评估神经血管压迫在小儿RP ON诊断中的重要性日益增加,部分病例已确认PCA压迫动眼神经出口处10) 。
Okobi OE, Boms MG, Ijeh JC, et al. Migraine and Current Pharmacologic Management. Cureus. 2022;14(10):e29833.
Kana T, Mehjabeen S, Patel N, et al. Sporadic Hemiplegic Migraine. Cureus. 2023;15(5):e38930.
Falsaperla R, Presti S, Lo Bianco M, et al. Diagnostic controversies in recurrent painful ophthalmoplegic neuropathy: single case report with a systematic review. Ital J Pediatr. 2022;48:82.
Al Owaifeer AM, AlSultan ZM, Badawi AH. Topiramate-induced acute angle closure: A systematic review of case reports and case series. Indian J Ophthalmol. 2022;70:1491-501.
Frattini D, Iodice A, Spagnoli C, et al. Tolosa-Hunt syndrome and recurrent painful ophthalmoplegic neuropathy, case reports: what to do and when? Ital J Pediatr. 2023;49:157.
Koo H, Tsai K, Lee C, et al. A Case of Adult-Onset Recurrent Painful Ophthalmoplegic Neuropathy With Bilateral Ophthalmoplegia. Cureus. 2024;16(2):e54683.
Castillo-Guerrero B, Londoño-Juliao G, Pianetta Y, et al. Internal Ophthalmoplegic Migraine During Pregnancy: A Clinical Case. Neurol Int. 2024;16:1779-1787.
Takemoto D, Ohkubo S, Udagawa S, et al. A Case of Recurrent Painful Ophthalmoplegic Neuropathy Successfully Treated with Beta-blocker Eye Drop Instillation. Neuro-Ophthalmology. 2021;45(5):320-323.
Nandana J, Nair SS, Girdhar S, et al. Recurrent painful ophthalmoplegic neuropathy: a cause for recurrent third nerve palsy in a child. BMJ Case Rep. 2021;14:e246179.
Bui LT, Mainali G, Naik S, et al. Role of Neurovascular Compression of Oculomotor Nerve in Ophthalmoplegic Migraine. Cureus. 2022;14(3):e22919.
Mrabet S, Nasri A, Kessentini N, et al. Recurrent painful ophthalmoplegic neuropathy revealing oculomotor nerve schwannoma. La Tunisie Medicale. 2021;99(08/09):919-923.