Dégénérescence cornéenne en bande
Fréquence : environ 32 % des cas
Dépôts de calcium au centre de la cornée dus à une inflammation chronique. Cause de troubles visuels. Traitement par chélation à l’EDTA ou laser excimer.

L’arthrite juvénile idiopathique (AJI) est un terme générique désignant une arthrite chronique de cause inconnue survenant chez les enfants de moins de 16 ans. Autrefois appelée arthrite rhumatoïde juvénile. Selon les critères ILAR de la Ligue internationale des associations de rhumatologie, elle est classée en 7 sous-types (systémique, oligoarticulaire, polyarticulaire FR négatif, polyarticulaire FR positif, arthrite psoriasique, arthrite associée à l’enthésite, et indifférenciée). Parmi ceux-ci, les quatre sous-types systémique, oligoarticulaire, polyarticulaire FR négatif et polyarticulaire FR positif correspondent à l’ancienne arthrite rhumatoïde juvénile (ARJ) et représentent 94 % des cas d’AJI.
L’uvéite chronique est la complication oculaire la plus importante de l’AJI et la cause la plus fréquente d’uvéite chez l’enfant. Elle représente 41 à 47 % de toutes les uvéites pédiatriques. 1) L’uvéite survient le plus souvent après l’apparition de l’arthrite, mais dans 3 à 7 % des cas, elle précède l’arthrite. Le délai médian d’apparition est de 5,5 mois, et elle survient généralement dans les 5 à 7 ans suivant le début de l’arthrite, en particulier 82 à 90 % des cas dans les 4 premières années. 3)
Le taux d’uvéite varie considérablement selon le sous-type d’AJI.
| Sous-type d’AJI | Taux d’uvéite | Risque |
|---|---|---|
| Oligoarthrite persistante | 41 à 46 % | Élevé |
| Polyarthrite RF négative | 5 à 23 % | Moyen à élevé |
| Arthrite psoriasique | 10 à 36 % | Moyen |
| Arthrite liée à l’enthésite | 7 à 25 % | Moyen |
| Forme systémique | 0 % | Faible |
On observe une uvéite chez environ 20 % des patients atteints de la forme oligoarticulaire et chez environ 5 % de la forme polyarticulaire, mais elle ne survient pas dans la forme systémique. Dans la cohorte nordique, il a été confirmé que 10 à 22 % de tous les patients atteints d’AJI développent une uvéite. 3)
Au début, il n’y a presque pas de symptômes subjectifs tels que rougeur, douleur ou photophobie, et elle progresse silencieusement, au point d’être décrite comme une « uvéite blanche ». En particulier chez les jeunes enfants, les plaintes subjectives sont rares et l’examen peut être difficile. Il est très difficile de la détecter sans un dépistage régulier à la lampe à fente.
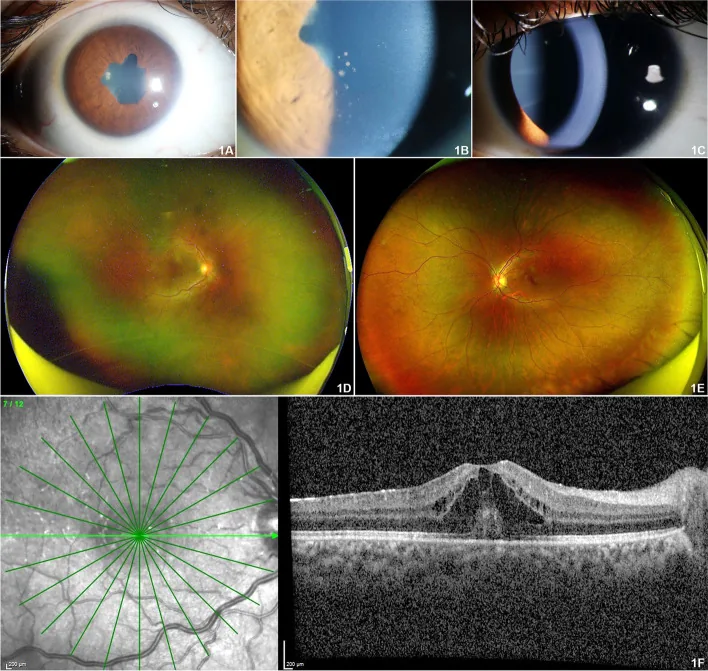
La caractéristique la plus importante de l’uvéite associée à l’AJI est son asymptomaticité précoce.
97,8 % des uvéites associées à l’AJI sont des uvéites antérieures (iridocyclite), typiquement bilatérales et non granulomateuses. 2) Lors de la consultation ophtalmologique, de nombreuses complications sont souvent déjà présentes.
Dégénérescence cornéenne en bande
Fréquence : environ 32 % des cas
Dépôts de calcium au centre de la cornée dus à une inflammation chronique. Cause de troubles visuels. Traitement par chélation à l’EDTA ou laser excimer.
Synéchies postérieures de l'iris
Fréquence : environ 28 % des cas
Adhérences entre l’iris et le cristallin. Souvent présentes dès la découverte, elles peuvent provoquer un bloc pupillaire. La prévention par mydriatiques est importante.
Cataracte compliquée
Incidence cumulée : 0,05/œil-année
Survient en raison d’une inflammation prolongée et de l’utilisation de stéroïdes (environ 22 %). Une chirurgie de la cataracte sous contrôle de l’inflammation active est nécessaire.
Glaucome secondaire
Incidence cumulée : 0,03/œil-année
Observé dans 15 % des cas. Plus fréquent dans l’uvéite associée à l’AJI que dans l’uvéite idiopathique. Principal facteur de mauvais pronostic visuel. 2)
D’autres manifestations incluent des cellules inflammatoires dans le vitré antérieur, un œdème maculaire cystoïde (3 %), une hypotonie (9 %), une névrite optique et une vascularite rétinienne. Une grande cohorte rapporte qu’un tiers des patients présentent déjà une déficience visuelle lors de la première consultation. Les complications telles que la dégénérescence cornéenne en bande, la cataracte secondaire et le glaucome surviennent cumulativement chez environ 67 % des cas.
Laisser faire risque de conduire à une perte de vision. L’uvéite associée au JIA est typiquement une « uvéite indolore » (uvéite blanche), où l’inflammation persiste sans symptômes, entraînant une progression de la dégénérescence cornéenne en bandelette, de la cataracte et du glaucome. Même en l’absence de symptômes, des consultations ophtalmologiques régulières sont le seul moyen de préserver la vision.
L’uvéite associée au JIA est une maladie inflammatoire chronique d’origine auto-immune, dont le développement implique des facteurs environnementaux et l’interaction de plusieurs gènes. La surproduction de cytokines inflammatoires (IL-1, IL-6, TNF-α) joue un rôle central dans la pathogenèse. Dans la synoviale articulaire, un tissu de granulation appelé pannus se forme, et une cascade inflammatoire similaire est activée de manière persistante dans l’uvée.
Facteurs de risque de développement de l’uvéite (Nordic guideline 2023)3) :
Facteurs protecteurs (réduisant significativement le risque d’uvéite)3) :
Le diagnostic de l’uvéite chez les patients atteints d’AJI est souvent posé lors d’un examen de dépistage. La détection à un stade asymptomatique est directement liée à l’amélioration du pronostic visuel.
Les critères de stratification du risque combinent le sous-type d’AJI, la positivité des ANA, l’âge de début et la durée de la maladie. 3, 4)
| Niveau de risque | Critères principaux | Fréquence de dépistage |
|---|---|---|
| Risque élevé | Oligoarthrite + ANA positif + âge de début ≤ 6 ans + durée de la maladie < 4 ans | Tous les 3 mois |
| Risque moyen | Répond partiellement aux critères ci-dessus | Tous les 6 mois |
| Risque faible | Forme systémique, polyarthrite RF positif, ERA, âge de début > 6 ans | Tous les 12 mois (pendant 2 ans seulement) |
Les maladies associant arthrite et uvéite à différencier comprennent : spondylarthrite ankylosante, syndrome de Reiter, rhumatisme psoriasique, sarcoïdose, maladies inflammatoires de l’intestin, sarcoïdose juvénile (EOS), syndrome de Blau, syndrome TINU.
Cela dépend du risque. Pour les patients à haut risque (oligoarthrite, ANA positif, début avant 6 ans, durée de la maladie < 4 ans), un dépistage tous les 3 mois est recommandé. 3, 4) Pour le risque moyen, tous les 6 mois ; pour le faible risque (forme systémique, polyarthrite RF positif, etc.), une observation tous les 12 mois pendant 2 ans est suggérée. Il est important de définir l’intervalle individuellement en collaboration avec le rhumatologue pédiatrique et l’ophtalmologiste.
La prise en charge de l’uvéite associée à l’AJI nécessite généralement une collaboration entre le rhumatologue pédiatrique et l’ophtalmologiste. Le contrôle à long terme de l’inflammation est essentiel pour prévenir les complications et protéger la vision. Les directives pour l’uvéite recommandent de commencer par un traitement local, puis d’introduire progressivement un traitement immunomodulateur et des agents biologiques en cas de résistance. 8)
| Médicament | Posologie et administration | Place dans le traitement |
|---|---|---|
| Méthotrexate (MTX) | 10–15 mg/m²/semaine (sous-cutané ou oral) | Première intention. Risque d’uvéite HR 0,14–0,63 |
| Adalimumab | Poids <30 kg : 20 mg/2 semaines, ≥30 kg : 40 mg/2 semaines (sous-cutané) | Deuxième intention en cas d’échec du MTX. Efficacité établie par l’essai SYCAMORE |
| Infliximab | 5 mg/kg, à 0/2/6 semaines puis toutes les 8 semaines (perfusion) | Option pour les cas réfractaires |
| Tocilizumab (anti-IL-6) | Approuvé pour l’arthrite juvénile idiopathique | Preuves en cours d’accumulation pour l’uvéite |
| Étanercept | — | Inefficace pour l’uvéite (car inhibiteur du récepteur du TNF) |
Le méthotrexate (MTX) est le traitement de première intention de l’immunomodulation pour l’uvéite associée à l’arthrite juvénile idiopathique. 5) L’effet apparaît en 4 à 12 semaines. Dans 27 à 48 % des cas, le MTX seul ne permet pas un contrôle suffisant de l’inflammation, et 20 % des patients présentent des effets secondaires (vomissements, troubles hépatiques). 2)
L’adalimumab est indiqué en deuxième intention en cas d’échec du MTX. L’essai SYCAMORE (Ramanan 2017) est un essai randomisé contrôlé en double aveugle qui a montré une réduction significative du taux d’échec thérapeutique de 60 % à 27 % dans le groupe MTX+adalimumab par rapport au groupe MTX seul (P<0,0001). 6) Il est approuvé pour l’uvéite non infectieuse chez l’enfant. En tant qu’anticorps monoclonal anti-TNF, il a un effet protecteur sur l’uvéite, contrairement à l’étanercept, un inhibiteur du récepteur du TNF. 3)
L’essai ADJUVITE (Quartier 2018) est un essai randomisé contrôlé en double aveugle sur l’adalimumab dans l’uvéite antérieure chronique précoce associée à l’AJI. 7) Il est considéré comme une étude démontrant l’avantage d’une introduction précoce.
Avant d’instaurer un inhibiteur du TNF, il est impératif de réaliser un dépistage de la tuberculose, du VHB et une évaluation des infections. L’administration et la gestion doivent être effectuées en collaboration avec un ophtalmologiste membre de la Société d’inflammation oculaire. 9)
Pas nécessairement, mais l’essai SYCAMORE (Ramanan 2017) a montré une forte réduction du taux d’échec thérapeutique de 60 % avec le MTX seul à 27 % avec l’adalimumab en association. 6) L’approche standard actuelle est d’utiliser d’abord le MTX, puis d’envisager l’adalimumab si le contrôle de l’inflammation est insuffisant. Pour protéger la vision future de l’enfant, un traitement agressif est recommandé si nécessaire.
La pathogénie de l’uvéite associée à l’AJI n’est pas entièrement comprise, mais on pense qu’elle est principalement d’origine immunologique.
Immunité cellulaire : Les lymphocytes T CD4+ (prédominance Th17) infiltrent le tissu uvéal et produisent de l’IL-17, de l’IL-6 et du TNF-α. La surproduction de cytokines inflammatoires augmente la perméabilité endothéliale vasculaire, entraînant un œdème de l’iris et du corps ciliaire et une infiltration persistante de cellules inflammatoires. Dans la synoviale articulaire, la formation de pannus conduit à la destruction du cartilage et de l’os, mais des symptômes systémiques tels que fièvre, fatigue, anémie et retard de croissance sont également induits.
Association avec les auto-anticorps : La positivité des anticorps antinucléaires (AAN) est observée dans environ 80 % des cas d’uvéite associée. Des associations avec HLA-DR5 (DRB1*1101) et HLA-DR11 ont été rapportées dans la forme oligoarticulaire. La réaction des lymphocytes T spécifiques aux auto-antigènes et l’activation de la voie classique du complément sont également impliquées.
Dissociation pathologique avec l’arthrite : L’uvéite peut persister indépendamment même après l’apaisement des symptômes articulaires. Comme elle se maintient par des voies inflammatoires différentes, une surveillance ophtalmologique continue est nécessaire même si l’arthrite est calme.
Principales modifications tissulaires résultant de l’inflammation chronique :
L’essai randomisé contrôlé en double aveugle de Ramanan et al. (2017) a montré que le groupe MTX+adalimumab réduisait le taux d’échec thérapeutique à 27 % contre 60 % dans le groupe MTX seul (P<0,0001). 6) Cet essai a servi de base à l’approbation de l’adalimumab pour l’uvéite non infectieuse pédiatrique. Des données de suivi à long terme sont également accumulées avec des critères d’arrêt de l’essai.
Dans une étude rétrospective menée par Cann et al. (2018) dans la région de Bristol, portant sur 166 enfants atteints d’uvéite non infectieuse, le taux d’utilisation des biothérapies a atteint 35 %, avec un taux de perte de vision (logMAR > 0,3) de 0,05/œil-année et une perte de vision sévère (logMAR ≥ 1,0) de 0,01/œil-année. 2) Cela représente une amélioration par rapport au taux de 0,10/œil-année avant l’introduction des biothérapies, démontrant les progrès thérapeutiques.
Les dernières recommandations du groupe de travail multinational (MIWGUC) par Foeldvari et al. (2023) recommandent clairement l’introduction précoce de l’adalimumab en cas d’uvéite associée à l’AJI réfractaire au MTX, et déconseillent l’étanercept comme traitement de l’uvéite. 10)
L’efficacité des inhibiteurs de JAK tels que le ruxolitinib et le tofacitinib dans l’uvéite réfractaire associée à l’AJI a été rapportée dans des séries de cas et des petites séries, mais aucune preuve définitive n’est disponible à ce jour.
Dans la cohorte nordique, des cas d’apparition après l’âge de 16 ans ont été confirmés (12 nouveaux cas sur 434 à 23 ans), soulignant la nécessité d’une transition fluide de l’enfance à l’âge adulte. 3) Le MTX et le MMF étant tératogènes, l’adalimumab est considéré comme une option relativement sûre pour les femmes en âge de procréer.