Queratopatía en banda
Frecuencia: Aproximadamente el 32% de los casos
Depósito de calcio en la córnea central debido a inflamación crónica, causando deterioro visual. Se trata con quelación con EDTA o láser excímero.

La artritis idiopática juvenil (AIJ) es un término general para la artritis crónica de causa desconocida que se desarrolla en niños menores de 16 años. Anteriormente se denominaba artritis reumatoide juvenil. Según los criterios de la ILAR (Liga Internacional de Asociaciones de Reumatología), la AIJ se clasifica en siete subtipos: sistémico, oligoarticular, poliarticular FR negativo, poliarticular FR positivo, artritis psoriásica, artritis relacionada con entesitis y artritis indiferenciada. De estos, los cuatro subtipos (sistémico, oligoarticular, poliarticular FR negativo y poliarticular FR positivo) corresponden a la antigua artritis reumatoide juvenil (ARJ) y representan el 94% de los casos de AIJ.
La uveítis crónica es la complicación ocular más importante de la AIJ y es la causa más frecuente de uveítis en niños. Representa del 41 al 47% de todas las uveítis pediátricas. 1) La uveítis suele aparecer después del inicio de la artritis, pero en el 3–7% de los casos precede a la artritis. La mediana de tiempo hasta la aparición es de 5.5 meses, y a menudo se desarrolla dentro de los 5–7 años posteriores al inicio de la artritis; en particular, el 82–90% ocurre dentro de los primeros 4 años. 3)
La tasa de uveítis varía considerablemente según el subtipo de AIJ.
| Subtipo de AIJ | Tasa de uveítis | Riesgo |
|---|---|---|
| Oligoartritis persistente | 41–46% | Alto |
| Poliartritis FR negativa | 5–23% | Moderado a alto |
| Artritis psoriásica | 10–36% | Moderado |
| Artritis relacionada con entesitis | 7–25% | Moderado |
| Artritis sistémica | 0% | Bajo |
Se observa en aproximadamente el 20% del tipo oligoarticular y en aproximadamente el 5% del tipo poliarticular, y no se considera que ocurra en el tipo sistémico. En la cohorte nórdica, se confirmó que la uveítis complica del 10 al 22% de todos los pacientes con JIA. 3)
En la etapa inicial, casi no hay síntomas subjetivos como enrojecimiento, dolor o fotofobia, y progresa silenciosamente, a menudo descrita como “uveítis blanca”. Especialmente en niños pequeños, las quejas subjetivas son escasas y el examen puede ser difícil. Es extremadamente difícil de detectar sin un cribado regular con lámpara de hendidura.
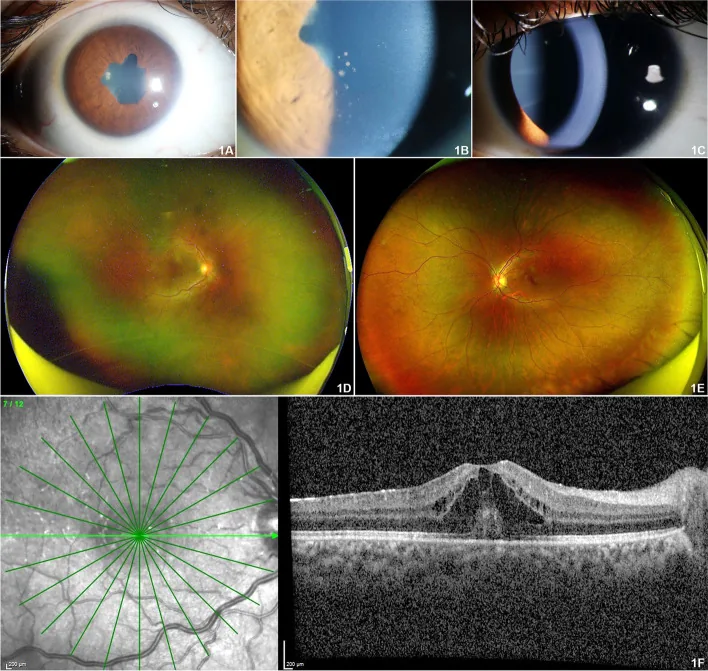
La característica más destacada de la uveítis asociada a JIA es su naturaleza inicial asintomática.
El 97.8% de las uveítis asociadas a JIA se presentan como uveítis anterior (iridociclitis), típicamente bilateral y no granulomatosa. 2) Al momento de la evaluación oftalmológica, muchos pacientes ya presentan múltiples complicaciones.
Queratopatía en banda
Frecuencia: Aproximadamente el 32% de los casos
Depósito de calcio en la córnea central debido a inflamación crónica, causando deterioro visual. Se trata con quelación con EDTA o láser excímero.
Sinequias posteriores
Frecuencia: Aproximadamente el 28% de los casos
Adhesión entre el iris y el cristalino. A menudo presente desde el diagnóstico inicial y puede causar bloqueo pupilar. La profilaxis con midriáticos es importante.
Catarata complicada
Incidencia acumulada: 0.05 por ojo-año
Se desarrolla debido a inflamación crónica y uso de esteroides (aproximadamente 22%). Se requiere cirugía de catarata bajo control de la inflamación activa.
Glaucoma secundario
Incidencia acumulada: 0.03 por ojo-año
Presente en el 15% de los casos. Más frecuente en la uveítis asociada a JIA que en la uveítis idiopática. Es una causa principal de mal pronóstico visual. 2)
Otros hallazgos incluyen células inflamatorias en el vítreo anterior, edema macular quístico (3%), hipotonía (9%), neuritis óptica y vasculitis retiniana. Estudios de cohortes grandes reportan que un tercio de los pacientes ya tienen deterioro visual en la primera visita. Las complicaciones como queratopatía en banda, opacificación capsular posterior y glaucoma se desarrollan acumulativamente en aproximadamente el 67% de los casos.
Dejarla sin tratamiento puede provocar pérdida de visión. La uveítis asociada a AIJ es un ejemplo clásico de “uveítis indolora” (uveítis blanca), donde la inflamación persiste sin síntomas, causando degeneración corneal en banda, cataratas y glaucoma. Incluso sin síntomas, las visitas regulares al oftalmólogo son la única forma de proteger la visión.
La uveítis asociada a AIJ es una enfermedad inflamatoria crónica mediada por mecanismos autoinmunes, que involucra la interacción de factores ambientales y múltiples genes. La sobreproducción de citocinas inflamatorias (IL-1, IL-6, TNF-α) juega un papel central en la patogénesis. En la membrana sinovial articular se forma tejido de granulación llamado pannus, y en la úvea se activa continuamente una cascada inflamatoria similar.
Factores de riesgo para desarrollar uveítis (Guía nórdica 2023)3):
Factores protectores (reducen significativamente el riesgo de desarrollar uveítis)3):
El diagnóstico de uveítis en pacientes con AIJ a menudo se realiza durante los exámenes de detección. La detección en una etapa asintomática se relaciona directamente con una mejoría en el pronóstico visual.
Los criterios de estratificación de riesgo combinan el subtipo de JIA, la positividad de ANA, la edad de inicio y la duración de la enfermedad. 3, 4)
| Nivel de riesgo | Criterios principales | Frecuencia de cribado |
|---|---|---|
| Alto riesgo | Oligoartritis + ANA positivo + inicio ≤6 años + duración <4 años | Cada 3 meses |
| Riesgo moderado | Cumple algunos de los anteriores | Cada 6 meses |
| Bajo riesgo | Tipo sistémico, poliartritis FR positiva, ERA, inicio >6 años | Cada 12 meses (solo durante 2 años) |
Las enfermedades que combinan artritis y uveítis incluyen las siguientes: espondilitis anquilosante, síndrome de Reiter, artritis psoriásica, sarcoidosis, enfermedad inflamatoria intestinal, sarcoidosis de inicio temprano (EOS), síndrome de Blau y síndrome TINU.
Depende del riesgo. Para alto riesgo (tipo oligoarticular, ANA positivo, inicio antes de los 6 años, duración de la enfermedad menor de 4 años), se recomienda un cribado cada 3 meses. 3, 4) Para riesgo moderado, cada 6 meses; para bajo riesgo (tipo sistémico, poliartritis FR positiva, etc.), la observación cada 12 meses durante 2 años es una guía. Es importante establecer el intervalo individualmente en colaboración con el reumatólogo pediátrico y el oftalmólogo.
El manejo de la uveítis asociada a AIJ generalmente requiere el manejo conjunto de un reumatólogo pediátrico y un oftalmólogo. El control a largo plazo de la inflamación es fundamental para prevenir complicaciones y proteger la visión. Las guías de práctica clínica para uveítis recomiendan comenzar con tratamiento local y, para casos refractarios, la introducción gradual de terapia inmunomoduladora y agentes biológicos. 8)
| Fármaco | Dosis y administración | Posición |
|---|---|---|
| Metotrexato (MTX) | 10–15 mg/m²/semana (subcutáneo u oral) | Primera línea. Riesgo de uveítis HR 0.14–0.63 |
| Adalimumab | Peso <30 kg: 20 mg/2 semanas, ≥30 kg: 40 mg/2 semanas (subcutáneo) | Segunda línea en casos refractarios a MTX. Eficacia establecida en el ensayo SYCAMORE |
| Infliximab | 5 mg/kg en las semanas 0, 2, 6, luego cada 8 semanas (intravenoso) | Opción para casos refractarios |
| Tocilizumab (inhibidor de IL-6) | Aprobado para artritis JIA en Japón | Evidencia en acumulación para uveítis |
| Etanercept | — | Ineficaz para uveítis (por ser inhibidor del receptor de TNF) |
Metotrexato (MTX) es el tratamiento de primera línea en la terapia inmunomoduladora para la uveítis asociada a artritis idiopática juvenil. 5) Su efecto tarda de 4 a 12 semanas en manifestarse. En el 27-48% de los casos, el MTX solo no controla adecuadamente la inflamación, y el 20% experimenta efectos secundarios (vómitos, disfunción hepática). 2)
Adalimumab se posiciona como una opción de segunda línea para casos refractarios a MTX. El ensayo SYCAMORE (Ramanan 2017), un ECA doble ciego, mostró que la tasa de fracaso del tratamiento se redujo significativamente del 60% en el grupo de MTX solo al 27% en el grupo de combinación MTX+adalimumab (P<0.0001). 6) Está aprobado para uveítis no infecciosa pediátrica. Como anticuerpo monoclonal anti-TNF, tiene un efecto protector sobre la uveítis, a diferencia del inhibidor del receptor de TNF etanercept. 3)
El ensayo ADJUVITE (Quartier 2018) es un ECA doble ciego de adalimumab para la uveítis anterior crónica temprana asociada a AIJ. 7) Se posiciona como un estudio que demuestra los beneficios de la introducción temprana.
Antes de iniciar inhibidores del TNF, es esencial realizar pruebas de detección de tuberculosis y VHB, y evaluación de infecciones. Se requiere administración y manejo en colaboración con un oftalmólogo miembro de la Sociedad de Inflamación Ocular. 9)
No necesariamente, pero existe evidencia sólida del ensayo SYCAMORE (Ramanan 2017) de que la tasa de fracaso del tratamiento se redujo significativamente del 60% con MTX solo al 27% con la terapia combinada. 6) El enfoque estándar actual es una estrategia escalonada: primero usar MTX, y si no se logra un control adecuado de la inflamación, considerar agregar adalimumab. Para proteger la visión futura del niño, se recomienda un tratamiento agresivo cuando se considere necesario.
La patogenia de la uveítis asociada a AIJ no se comprende completamente, pero se cree que los mecanismos inmunológicos son los principales.
Inmunidad celular: Los linfocitos T CD4+ (predominio Th17) infiltran el tejido uveal y producen IL-17, IL-6 y TNF-α. La sobreproducción de citocinas inflamatorias aumenta la permeabilidad endotelial vascular, manteniendo el edema y la infiltración de células inflamatorias en el iris y el cuerpo ciliar. En la membrana sinovial articular, la formación de pannus conduce a la destrucción del cartílago y el hueso, y también se inducen síntomas sistémicos como fiebre, malestar, anemia y trastornos del crecimiento.
Asociación con autoanticuerpos: La positividad para anticuerpos antinucleares (ANA) se encuentra en aproximadamente el 80% de los pacientes con uveítis. Se han reportado asociaciones con HLA-DR5 (DRB1*1101) y HLA-DR11 en el tipo oligoarticular. También están implicadas las respuestas de linfocitos T específicos de autoantígenos y la activación de la vía clásica del complemento.
Disociación de la artritis: La uveítis puede persistir de forma independiente incluso después de que los síntomas de la artritis hayan remitido. Dado que continúa a través de diferentes vías inflamatorias, es necesario un seguimiento oftalmológico continuo incluso cuando la artritis está inactiva.
Principales cambios tisulares resultantes de la inflamación crónica:
Ramanan et al. (2017) realizaron un ECA doble ciego comparando MTX solo vs. MTX + adalimumab, mostrando que el grupo de adalimumab redujo la tasa de fracaso del tratamiento al 27% frente al 60% (P<0.0001). 6) Este ensayo proporcionó la base para la aprobación de adalimumab para la uveítis no infecciosa pediátrica. Se están acumulando datos de seguimiento a largo plazo con criterios de interrupción predefinidos.
En un estudio retrospectivo del área de Bristol realizado por Cann et al. (2018), en 166 niños con uveítis no infecciosa, la tasa de uso de biológicos alcanzó el 35%, con una incidencia de pérdida visual (logMAR > 0.3) de 0.05/ojo-año y pérdida visual severa (logMAR ≥ 1.0) de 0.01/ojo-año. 2) Esto representa una mejora con respecto a 0.10/ojo-año antes de la introducción de los biológicos, lo que demuestra el progreso del tratamiento.
Las recomendaciones más recientes del Grupo de Trabajo Multinacional Interdisciplinario para la Uveítis en la Infancia (MIWGUC) por Foeldvari et al. (2023) recomiendan claramente la introducción temprana de adalimumab para la uveítis asociada a AIJ refractaria a MTX y aconsejan no seleccionar etanercept para el tratamiento de la uveítis. 10)
La eficacia de los inhibidores de JAK como ruxolitinib y tofacitinib para la uveítis asociada a AIJ refractaria se ha informado en reportes de casos y series pequeñas, pero no se dispone de evidencia definitiva en este momento.
En la cohorte nórdica, se observaron casos de inicio incluso después de la transición a la atención de adultos después de los 16 años (12 de 434 casos fueron de inicio nuevo a los 23 años), lo que destaca el desafío de una colaboración fluida desde la infancia hasta la edad adulta. 3) Dado que MTX y MMF son teratogénicos, el adalimumab se considera una opción relativamente segura para mujeres en edad fértil al seleccionar medicamentos.