Bandförmige Keratopathie
Häufigkeit : etwa 32 % der Fälle
Kalziumablagerungen im zentralen Bereich der Hornhaut aufgrund chronischer Entzündung. Ursache für Sehbehinderung. Behandlung mit EDTA-Chelatbildung oder Excimer-Laser.

Die juvenile idiopathische Arthritis (JIA) ist ein Sammelbegriff für chronische Arthritis unbekannter Ursache bei Kindern unter 16 Jahren. Früher wurde sie auch als juvenile rheumatoide Arthritis bezeichnet. Nach den ILAR-Kriterien der Internationalen Liga gegen Rheumatismus wird sie in 7 Subtypen unterteilt (systemisch, oligoartikulär, RF-negative Polyarthritis, RF-positive Polyarthritis, Psoriasis-Arthritis, Enthesitis-assoziierte Arthritis, undifferenziert). Von diesen entsprechen die vier Subtypen systemisch, oligoartikulär, RF-negative Polyarthritis und RF-positive Polyarthritis der früheren juvenilen rheumatoiden Arthritis (JRA) und machen 94 % der JIA aus.
Die chronische Uveitis ist die wichtigste Augenkomplikation der JIA und die häufigste Ursache für Uveitis bei Kindern. Sie macht 41–47 % aller pädiatrischen Uveitiden aus. 1) Die Uveitis tritt meist nach Beginn der Arthritis auf, in 3–7 % der Fälle jedoch vor der Arthritis. Die mediane Zeit bis zum Auftreten beträgt 5,5 Monate, und sie tritt in der Regel innerhalb von 5–7 Jahren nach Arthritisbeginn auf, insbesondere 82–90 % innerhalb der ersten 4 Jahre. 3)
Die Uveitisrate variiert stark je nach JIA-Subtyp.
| JIA-Subtyp | Uveitisrate | Risiko |
|---|---|---|
| Persistierende Oligoarthritis | 41–46 % | Hoch |
| RF-negative Polyarthritis | 5–23 % | Mittel bis hoch |
| Psoriasisarthritis | 10–36 % | Mittel |
| Enthesitis-assoziierte Arthritis | 7–25 % | Mittel |
| Systemische Form | 0 % | Niedrig |
Bei der oligoartikulären Form tritt sie bei etwa 20 % auf, bei der polyartikulären Form bei etwa 5 %, und bei der systemischen Form tritt sie nicht auf. In der nordischen Kohorte wurde bestätigt, dass 10–22 % aller JIA-Patienten eine Uveitis entwickeln. 3)
Zu Beginn gibt es kaum subjektive Symptome wie Rötung, Schmerzen oder Lichtscheu, und sie schreitet so leise voran, dass sie als „weiße Uveitis“ beschrieben wird. Besonders bei Kleinkindern sind subjektive Beschwerden selten, und die Untersuchung kann schwierig sein. Ohne regelmäßiges Screening mit der Spaltlampe ist sie sehr schwer zu entdecken.
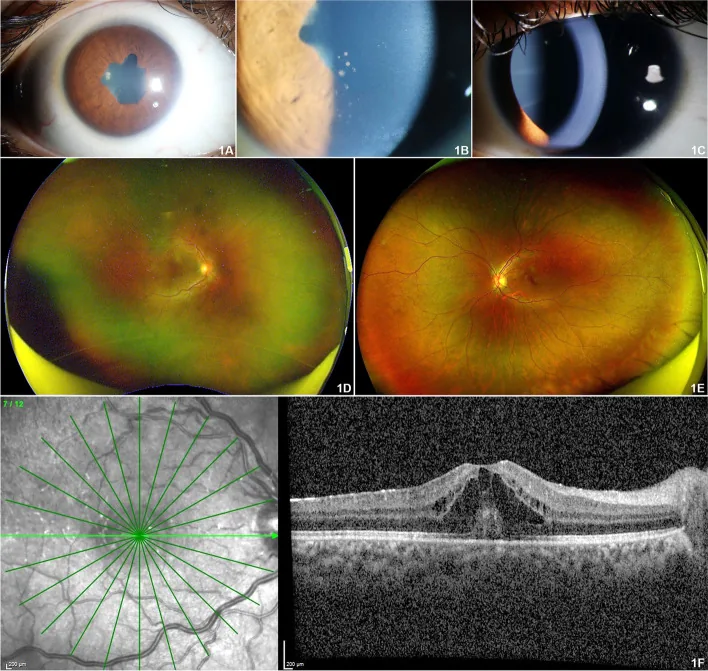
Das Hauptmerkmal der JIA-assoziierten Uveitis ist die frühe Symptomlosigkeit.
97,8 % der JIA-assoziierten Uveitiden sind anteriore Uveitiden (Iridozyklitis), typischerweise bilateral und nicht granulomatös. 2) Zum Zeitpunkt der ophthalmologischen Untersuchung liegen häufig bereits viele Komplikationen vor.
Bandförmige Keratopathie
Häufigkeit : etwa 32 % der Fälle
Kalziumablagerungen im zentralen Bereich der Hornhaut aufgrund chronischer Entzündung. Ursache für Sehbehinderung. Behandlung mit EDTA-Chelatbildung oder Excimer-Laser.
Hintere Synechien
Häufigkeit : etwa 28 % der Fälle
Verwachsungen zwischen Iris und Linse. Oft bereits bei Diagnose vorhanden, können einen Pupillarblock verursachen. Vorbeugung durch Mydriatika ist wichtig.
Komplizierte Katarakt
Kumulative Inzidenz : 0,05/Augenjahr
Tritt aufgrund langanhaltender Entzündung und Steroidgebrauch auf (etwa 22 %). Kataraktoperation unter Kontrolle der aktiven Entzündung erforderlich.
Sekundärglaukom
Kumulative Inzidenz : 0,03/Augenjahr
Tritt bei 15 % auf. Häufiger bei JIA-assoziierter Uveitis als bei idiopathischer Uveitis. Hauptfaktor für schlechte Sehprognose. 2)
Weitere Befunde umfassen Entzündungszellen im vorderen Glaskörper, zystoides Makulaödem (3 %), Hypotonie (9 %), Optikusneuritis und retinale Vaskulitis. Eine große Kohorte berichtet, dass bereits bei der Erstvorstellung ein Drittel der Patienten eine Sehbehinderung aufwies. Bandförmige Keratopathie, Katarakt und Glaukom treten kumulativ bei etwa 67 % der Fälle auf.
Das Ignorieren birgt das Risiko des Sehverlusts. Die JIA-assoziierte Uveitis ist die klassische „schmerzlose Uveitis“ (weiße Uveitis), bei der die Entzündung ohne Symptome fortschreitet und zu bandförmiger Keratopathie, Katarakt und Glaukom führt. Auch ohne Symptome sind regelmäßige augenärztliche Kontrollen der einzige Weg, das Sehvermögen zu schützen.
Die JIA-assoziierte Uveitis ist eine chronische Entzündungskrankheit mit autoimmuner Genese, an deren Entstehung Umweltfaktoren und das Zusammenspiel mehrerer Gene beteiligt sind. Die Überproduktion von Entzündungszytokinen (IL-1, IL-6, TNF-α) spielt eine zentrale Rolle in der Pathogenese. Im Gelenksynovium bildet sich Granulationsgewebe, genannt Pannus, und in der Uvea wird eine ähnliche Entzündungskaskade dauerhaft aktiviert.
Risikofaktoren für die Entwicklung einer Uveitis (Nordic guideline 2023)3):
Schutzfaktoren (senken das Uveitisrisiko signifikant)3):
Die Diagnose einer Uveitis bei JIA-Patienten wird häufig während einer Screening-Untersuchung gestellt. Die Entdeckung im asymptomatischen Stadium ist direkt mit einer Verbesserung der Sehprognose verbunden.
Die Kriterien für die Risikostratifizierung kombinieren den JIA-Subtyp, ANA-Positivität, Erkrankungsalter und Krankheitsdauer. 3, 4)
| Risikostufe | Hauptkriterien | Screening-Häufigkeit |
|---|---|---|
| Hohes Risiko | Oligoarthritis + ANA-positiv + Erkrankungsalter ≤ 6 Jahre + Krankheitsdauer < 4 Jahre | Alle 3 Monate |
| Mittleres Risiko | Erfüllt teilweise die obigen Kriterien | Alle 6 Monate |
| Niedriges Risiko | Systemische Form, RF-positive Polyarthritis, ERA, Erkrankungsalter > 6 Jahre | Alle 12 Monate (nur für 2 Jahre) |
Zu den Erkrankungen, die mit Arthritis und Uveitis einhergehen, gehören: Spondylitis ankylosans, Reiter-Syndrom, Psoriasis-Arthritis, Sarkoidose, entzündliche Darmerkrankungen, juvenile Sarkoidose (EOS), Blau-Syndrom, TINU-Syndrom.
Das hängt vom Risiko ab. Bei hohem Risiko (Oligoarthritis, ANA-positiv, Beginn vor dem 6. Lebensjahr, Krankheitsdauer < 4 Jahre) wird ein Screening alle 3 Monate empfohlen. 3, 4) Bei mittlerem Risiko alle 6 Monate, bei niedrigem Risiko (systemischer Typ, RF-positive Polyarthritis usw.) eine Beobachtung alle 12 Monate für 2 Jahre. Es ist wichtig, das Intervall individuell in Absprache mit dem pädiatrischen Rheumatologen und Augenarzt festzulegen.
Die Behandlung der JIA-assoziierten Uveitis erfordert in der Regel eine Zusammenarbeit zwischen pädiatrischem Rheumatologen und Augenarzt. Die langfristige Kontrolle der Entzündung ist die Grundlage zur Vermeidung von Komplikationen und zum Schutz des Sehvermögens. Die Leitlinien zur Uveitis-Behandlung empfehlen, mit einer lokalen Therapie zu beginnen und bei refraktären Fällen schrittweise immunmodulatorische Therapien und Biologika einzusetzen. 8)
| Medikament | Dosierung und Anwendung | Stellenwert |
|---|---|---|
| Methotrexat (MTX) | 10–15 mg/m²/Woche (subkutan oder oral) | Erste Wahl. Uveitis-Risiko HR 0,14–0,63 |
| Adalimumab | Gewicht <30 kg: 20 mg/2 Wochen, ≥30 kg: 40 mg/2 Wochen (subkutan) | Zweite Wahl bei MTX-Versagen. Wirksamkeit in SYCAMORE-Studie belegt |
| Infliximab | 5 mg/kg, in Woche 0/2/6, dann alle 8 Wochen (Infusion) | Option für therapierefraktäre Fälle |
| Tocilizumab (IL-6-Hemmer) | Für JIA-Arthritis zugelassen | Evidenz für Uveitis wird noch gesammelt |
| Etanercept | — | Unwirksam bei Uveitis (da TNF-Rezeptor-Inhibitor) |
Methotrexat (MTX) ist die erste Wahl der immunmodulatorischen Therapie für Uveitis im Zusammenhang mit juveniler idiopathischer Arthritis. 5) Der Wirkungseintritt dauert 4–12 Wochen. Bei 27–48 % der Fälle reicht MTX allein nicht aus, um die Entzündung zu kontrollieren, und 20 % erleben Nebenwirkungen (Erbrechen, Leberfunktionsstörungen). 2)
Adalimumab wird als Zweitlinientherapie bei MTX-Versagen eingesetzt. Die SYCAMORE-Studie (Ramanan 2017) war eine doppelblinde RCT, die die Therapieversagensrate von 60 % in der MTX-Monotherapie-Gruppe auf 27 % in der MTX+Adalimumab-Kombinationsgruppe signifikant senkte (P<0,0001). 6) Es ist für nichtinfektiöse Uveitis bei Kindern zugelassen. Als monoklonaler TNF-Antikörper hat es im Gegensatz zum TNF-Rezeptor-Inhibitor Etanercept einen schützenden Effekt auf die Uveitis. 3)
Die ADJUVITE-Studie (Quartier 2018) ist eine doppelblinde RCT zu Adalimumab bei früher chronischer JIA-assoziierter anteriorer Uveitis. 7) Sie gilt als Studie, die den Vorteil einer frühen Einführung zeigt.
Vor der Einleitung eines TNF-Inhibitors sind ein Tuberkulose-Screening, HBV-Screening und eine Infektionsbeurteilung obligatorisch. Die Verabreichung und Überwachung sollte in Zusammenarbeit mit einem Augenarzt erfolgen, der Mitglied der Ocular Inflammation Society ist. 9)
Nicht unbedingt, aber die SYCAMORE-Studie (Ramanan 2017) zeigte eine starke Reduktion der Therapieversagensrate von 60 % unter MTX allein auf 27 % unter Adalimumab-Kombination. 6) Der aktuelle Standardansatz ist, zunächst MTX einzusetzen und bei unzureichender Entzündungskontrolle die Zugabe von Adalimumab zu erwägen. Um das zukünftige Sehvermögen des Kindes zu schützen, wird bei Bedarf eine aggressive Therapie empfohlen.
Die Pathogenese der JIA-assoziierten Uveitis ist nicht vollständig geklärt, aber es wird angenommen, dass immunologische Mechanismen im Vordergrund stehen.
Zelluläre Immunität: CD4+ T-Zellen (Th17-dominant) infiltrieren das Uveagewebe und produzieren IL-17, IL-6 und TNF-α. Die Überproduktion entzündlicher Zytokine erhöht die Gefäßendothelpermeabilität und führt zu Ödemen der Iris und des Ziliarkörpers sowie zu anhaltender Infiltration von Entzündungszellen. Im Gelenksynovium führt die Pannusbildung zur Zerstörung von Knorpel und Knochen, aber es werden auch systemische Symptome wie Fieber, Müdigkeit, Anämie und Wachstumsstörungen induziert.
Zusammenhang mit Autoantikörpern: Eine Positivität für antinukleäre Antikörper (ANA) wird bei etwa 80 % der Fälle mit Uveitis beobachtet. Assoziationen mit HLA-DR5 (DRB1*1101) und HLA-DR11 wurden bei der oligoartikulären Form berichtet. Auch die Autoantigen-spezifische T-Zell-Reaktion und die Aktivierung des klassischen Komplementwegs sind beteiligt.
Pathologische Dissoziation von der Arthritis: Die Uveitis kann auch nach Abklingen der Gelenksymptome unabhängig persistieren. Da sie über unterschiedliche Entzündungswege aufrechterhalten wird, ist eine kontinuierliche augenärztliche Überwachung erforderlich, auch wenn die Arthritis ruhig ist.
Wichtigste Gewebeveränderungen als Folge chronischer Entzündung:
Die doppelblinde RCT von Ramanan et al. (2017) zeigte, dass die MTX+Adalimumab-Gruppe die Therapieversagensrate auf 27 % vs. 60 % in der MTX-Monotherapie-Gruppe senkte (P<0,0001). 6) Diese Studie war die Grundlage für die Zulassung von Adalimumab bei pädiatrischer nichtinfektiöser Uveitis. Es werden auch Langzeit-Follow-up-Daten mit festgelegten Studienabbruchkriterien gesammelt.
In einer retrospektiven Studie von Cann et al. (2018) aus der Region Bristol erreichte die Anwendungsrate von Biologika bei 166 Kindern mit nichtinfektiöser Uveitis 35 %, mit einer Inzidenz von Sehverlust (logMAR > 0,3) von 0,05/Augenjahr und schwerem Sehverlust (logMAR ≥ 1,0) von 0,01/Augenjahr. 2) Dies stellt eine Verbesserung gegenüber der Rate von 0,10/Augenjahr vor Einführung der Biologika dar und zeigt den Fortschritt der Behandlung.
Die neuesten Empfehlungen der multinationalen Arbeitsgruppe (MIWGUC) von Foeldvari et al. (2023) empfehlen klar die frühzeitige Einleitung von Adalimumab bei MTX-refraktärer JIA-assoziierter Uveitis und raten davon ab, Etanercept als Uveitis-Therapie zu wählen. 10)
Die Wirksamkeit von JAK-Inhibitoren wie Ruxolitinib und Tofacitinib bei refraktärer JIA-assoziierter Uveitis wurde in Fallberichten und kleinen Serien beschrieben, jedoch liegen derzeit keine endgültigen Belege vor.
In der nordischen Kohorte wurden auch nach dem Übergang ins Erwachsenenalter ab 16 Jahren neue Fälle bei JIA-Patienten bestätigt (12 von 434 Fällen mit Neuerkrankung im Alter von 23 Jahren), was die Notwendigkeit einer nahtlosen Zusammenarbeit zwischen Kinder- und Erwachsenenmedizin unterstreicht. 3) Da MTX und MMF teratogen sind, gilt Adalimumab bei Frauen im gebärfähigen Alter als relativ sichere Option.