前部型
主要所見:水晶體後囊的纖維增生膜(Mittendorf斑)、後囊下白內障、後部水晶體圓錐
治療適應症:病變侷限於水晶體後部且眼底正常時,有手術適應症
預後:三型中最好。中位視力20/100(視力20/200以上佔54%)1)

永存原始玻璃體增生症(persistent fetal vasculature, PFV)是一種先天性眼疾,由胚胎期玻璃體血管系統退化不全引起。舊稱永存原始玻璃體增生症(persistent hyperplastic primary vitreous, PHPV)。1997年,Goldberg提出PFV這一名稱,以包括水晶體周圍的血管纖維組織殘留 12),目前已被廣泛接受。
玻璃體血管系統包括從視盤發出的玻璃體動脈和前方的水晶體血管膜。間質細胞在胚胎第5-6週通過胚裂進入玻璃體腔,於第10週達到高峰。隨後從第13-15週開始從周邊退化,在胎兒晚期消退。PFV中這種退化不全,導致血管周圍組織發育異常。
PFV通常為單眼、非遺傳性,尚未明確特定的致病基因。典型病例表現為伴有小眼球的白色瞳孔,但也可能因斜視或弱視而診斷。
據報導,PFV合併於約20%的嬰幼兒白內障 2)3)。在兒科眼病研究者小組(PEDIG)的白內障登記中,994例中有64例(6.4%)為PFV合併白內障 1);其中75%作為無水晶體眼手術(手術時中位月齡2個月),25%作為人工水晶體眼手術(手術時中位年齡29個月)1)。28%存在後段異常(玻璃體、視網膜或視神經異常)1),僅有4-6%有家族史 1)。
本質上是同一疾病的新舊名稱差異。PHPV是舊稱,側重於玻璃體血管(原始玻璃體)的增生和殘留。1997年,Goldberg提出了PFV(persistent fetal vasculature)這個名稱,以涵蓋水晶體周圍血管纖維組織的殘留。PFV能表達更廣泛的病變譜,因此現在是標準名稱。
PFV幾乎總是單眼發病,且為非遺傳性。在PEDIG研究中,僅3例雙側PFV被排除1)。雙側病例需要與家族性滲出性玻璃體視網膜病變(FEVR)和Norrie病鑑別,建議進行包括基因檢測在內的詳細檢查。
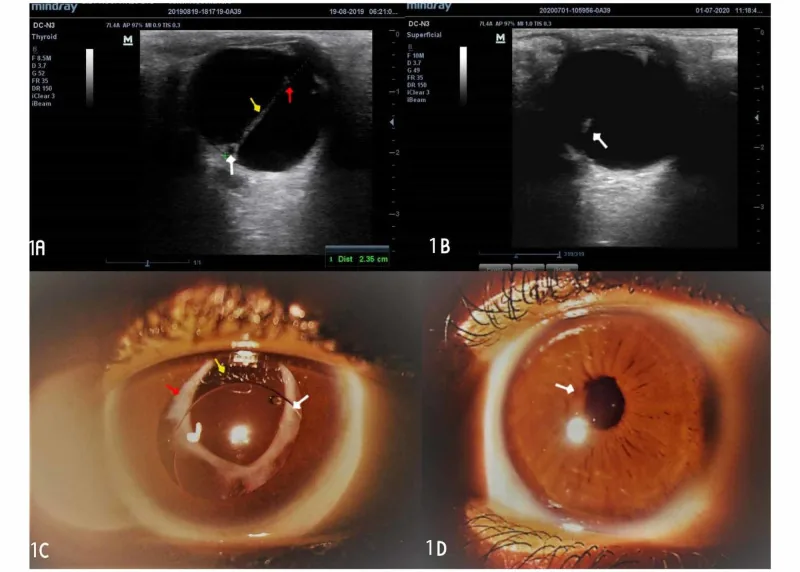
PFV根據病變優勢部位分為前部型、後部型和混合型三型。
前部型
主要所見:水晶體後囊的纖維增生膜(Mittendorf斑)、後囊下白內障、後部水晶體圓錐
治療適應症:病變侷限於水晶體後部且眼底正常時,有手術適應症
預後:三型中最好。中位視力20/100(視力20/200以上佔54%)1)
後部型
混合型
主要發現:前部型與後部型的發現混合存在。常伴隨小眼症。
治療適應症:根據個別病變範圍謹慎判斷。
預後:重度混合型中,可測量視力僅19%,61%無光覺8)
| 病型 | 主要發現 | 可能合併的異常 |
|---|---|---|
| 1. 玻璃體血管(動脈)殘留 | 視乳頭→玻璃體後部中央的白色至灰色索狀物+Mittendorf斑 | 後囊下白內障、後部圓錐形水晶體 |
| 2. 玻璃體血管主幹型 | 從視乳頭發出粗大索狀物 | 視乳頭周圍視網膜牽引 |
| 3. 視盤局限型 | 視盤上白色組織 | 周圍視網膜牽引 |
| 4. 視盤視網膜皺襞 | 眼底周邊部增殖組織牽引 | 周邊視網膜異常 |
| 5. 玻璃體腔占位型 | 廣泛增殖、全視網膜剝離、視網膜發育不良 | 多伴小眼球 |
| 6. 水晶體後纖維增生為主型 | 局限於水晶體後,眼底大致正常 | 有治療適應症 |
| 7. 水晶體前型 | 水晶體血管膜增殖導致的前方纖維增生 | 瞳孔變形、閉鎖 |
主要所見包括單眼小眼球、水晶體後囊混濁(Mittendorf斑)、視網膜血管走向異常、視網膜發育不良、睫狀突延長,以及從水晶體後囊向視神經乳頭延伸的索狀物。索狀物可能導致牽引,經由延長睫狀突引起低眼壓。乳頭附近的索狀組織可能牽扯視網膜。嚴重程度取決於玻璃體血管退化的程度。
在PEDIG研究中,PFV白內障的28%(18/64眼)存在後段異常1),人工水晶體眼的46%有後段病變(與無水晶體眼的28%相比,年齡校正OR為4.47)1)。無水晶體PFV眼中96%在白內障手術時進行了前部玻璃體切除1)。
在玻璃體血管系統的正常發育中,間質細胞在胚胎第5-6週通過胚裂進入玻璃體腔,形成玻璃體血管系統。在胚胎第10週達到頂峰,隨後從周邊開始退化。具體而言,退化始於胚胎第13-15週,在胚胎晚期消退。
在PFV中,玻璃體血管退化不全,導致血管周圍組織發育異常。這被認為會導致水晶體混濁、視網膜發育不良和小眼球。此外,殘留組織的牽引導致睫狀突延長和視網膜皺襞。
PFV被認為是單眼性、非遺傳性的,尚未確定特定的致病基因。僅有4-6%有家族史1),大多數為散發性。雙眼病例需與FEVR(NDP、LRP5、FZD4基因突變)和Norrie病(NDP基因突變)進行遺傳學鑑別。
尚未顯示與低出生體重或早產有明確關聯,但嚴重的玻璃體血管殘留罕見地可能呈現類似早產兒視網膜病變的所見。
與引起白瞳症的疾病進行鑑別是最重要的任務。特別是與視網膜母細胞瘤的鑑別直接關係到生命預後。
與視網膜母細胞瘤的鑑別
與FEVR和Norrie病的鑑別
雙眼病例中重要
雙眼全視網膜剝離或水晶體後纖維增生時,需要與FEVR或Norrie病鑑別。家族史和基因異常檢查有參考價值。利用次世代定序(NGS)檢測是有用的。
| 疾病 | 側別 | 小眼症 | 遺傳性 | CT鈣化 | 特徵性表現 |
|---|---|---|---|---|---|
| PFV | 幾乎均為單眼 | 有 | 非遺傳性 | 無 | 水晶體後纖維血管索、視乳頭纖維血管膜 |
| 視網膜母細胞瘤 | 70%單眼 | 無 | RB1突變(35–45%) | 有(特徵性) | 白色隆起腫塊、玻璃體播種 |
| FEVR | 雙眼 | 無 | 有(FZD4等) | 無 | 周邊視網膜無血管區、牽引性視網膜剝離 |
| Norrie病 | 雙眼性 | 可能 | X染色體隱性遺傳(NDP) | 無 | 玻璃體出血、視網膜剝離、智能障礙 |
| 早產兒視網膜病變 | 雙眼性 | 無 | 無 | 無 | 周邊視網膜無血管區、血管增生 |
透光體的混濁處理與白內障相同。如果混濁侷限於水晶體後部且眼底正常,則按照先天性白內障進行水晶體切除和纖維增殖膜切除。如果水晶體後方的索狀物偏心且不影響視軸,則不一定需要手術。如果眼底受累,通常不進行手術。對於視網膜剝離或牽引,如果ERG/VEP反應良好,可作為外科介入的依據。如果前部增殖導致瞳孔變形或閉鎖,則進行瞳孔成形術。
水晶體去除後進行屈光矯正和弱視治療。手術方式參照先天性白內障。PEDIG研究中,96%的無水晶體PFV眼在白內障手術時同時進行了前部玻璃體切除術1),初次手術時進行前部玻璃體切除術的視軸混濁發生率為18%,而未進行者高達60%1)。
術後進行屈光矯正(隱形眼鏡或眼鏡)和健眼遮蓋(眼罩)相結合的弱視治療。單眼PFV的弱視治療遵從性決定視力預後。治療需要在視覺發育關鍵期(出生後至10歲左右)積極進行。
| 指標 | 無水晶體PFV眼 | 人工水晶體PFV眼 |
|---|---|---|
| 手術時年齡(中位數) | 2個月 | 29個月 |
| 5年時中位視力 | 20/100(IQR 20/50–20/320) | 20/400(IQR 20/200–<20/800) |
| 視力20/200或以上 | 59%(95%CI 39–76%) | 23%(95%CI 5–54%) |
| 達到年齡正常視力 | 10%(95%CI 2–27%) | 8%(95%CI 0–36%) |
| 青光眼相關不良事件(5年累積) | 24%(95%CI 9–37%) | 7%(95%CI 0–20%) |
| 視軸混濁 | 15%(95%CI 5–25%) | 45%(95%CI 13–66%) |
| 視網膜剝離 | 4%(95%CI 0–10%) | 7%(95%CI 0–19%) |
整體視力結果:42隻眼中,4隻眼(10%,95%CI 3–23%)達到年齡正常視力,48%(95%CI 32–64%)達到20/200或以上視力1)。人工水晶體眼PFV眼的20/200以上視力達成率(23%)顯著低於非PFV人工水晶體眼(68%)(年齡校正OR=0.14,P=0.005)1)。無水晶體眼PFV眼與非PFV無水晶體眼相比,結果相當(年齡校正OR=1.90,P=0.14)1)。
依類型分,前部型的中位視力為20/100(20/200以上佔54%),而後部型的中位視力較差,為20/800(20/200以上佔36%),相差4個logMAR行(P=0.09)1)。
其他報告包括:Bata等人的20年單中心研究(58隻無水晶體眼PFV眼)中33%達到20/200以上(平均追蹤6.7年)4);Anteby等人的報告(30隻無水晶體眼PFV眼)中16.7%達到20/200以上(平均追蹤8.5年)5);de Saint Sauveur等人的36例重度混合型PFV病例中,僅19%有可測量視力,61%無光感8)。
其他主要併發症包括視軸混濁(人工水晶體眼PFV眼45%,無水晶體眼15%),人工水晶體眼PFV眼需要視軸清晰化手術的累積發生率高達40%1)。此外,13%(95%CI 2–22%)的無水晶體眼PFV眼在5年內需要二次IOL植入手術1)。
視網膜發育不良沒有有效的治療方法。後部型PFV通常無法預期視力發育。對於明顯的小眼球,出於美觀考量,應早期佩戴義眼。義眼佩戴也有助於眼眶發育。
前部型(水晶體後局部型)術後5年中位視力為20/100,20/200以上達成率為54%1)。但只有10%的眼能達到年齡正常視力。後部型中位視力較差,為20/8001)。視力預後受病型、後段病變有無、手術年齡和弱視治療遵從性的顯著影響。
青光眼相關不良事件最為常見,無水晶體PFV眼的5年累積發生率達24%1)。視軸混濁也是重要的併發症,假水晶體眼中45%會發生1)。初次手術時施行前部玻璃體切除對預防視軸混濁很重要(有施行18% vs 無施行60%)1)。術後也需要長期定期進行眼壓管理、視軸評估和屈光矯正。
在胎齡第5-6週,間質細胞從視裂進入玻璃體腔,形成由玻璃體動脈和水晶體血管膜組成的玻璃體血管系統。該血管系統為發育中的水晶體和眼前段提供氧氣和營養,扮演重要角色。
胎齡第10週為發育高峰期,此後從周邊開始退化。胎齡13-15週退化全面開始,至胎兒後期幾乎完全消退。正常分娩時玻璃體血管系統幾乎不可見,但有時會殘留如Mittendorf斑(水晶體後囊上的小白點)等痕跡。
在PFV中,玻璃體血管退化不全,導致血管周圍纖維增殖組織發生異常。殘留的血管周圍間質組織增殖並纖維化,呈現各種臨床表現。
具體結果如下:
單眼性、非遺傳性的原因被認為是,胚胎期玻璃體血管退化受局部血管新生和退化信號調控,這種調控機制僅在一隻眼發生障礙。但具體的分子機制尚未闡明。
雖然PFV的特定致病基因尚未確定,但動物模型已報告FZD4、LRP5、NDP等Wnt信號傳導路徑相關基因的突變表現出PFV樣表型(玻璃體血管殘留)。這些也是FEVR和Norrie病的致病基因,提示PFV與相關疾病之間存在遺傳連續性。次世代定序(NGS)面板檢測在PFV鑑別診斷中的臨床應用也在進展中。
使用25G和27G微切口玻璃體手術(MIVS)處理後部型PFV的方法正在嘗試中。針對新生兒和嬰兒的小切口手術據說具有最小化創傷和減少術後發炎的優點11)。
嬰兒期一期IOL植入與無水晶體管理後二期IOL植入的長期結果比較是PFV研究的重要課題。PEDIG研究的延長追蹤數據有望建立PFV特有的IOL植入適應症標準6)7)。
使用廣角眼底相機和前段OCT對PFV進行非侵入性評估正在進步。特別是前段OCT對於後部圓錐形水晶體和後囊下白內障的形態評估以及術前規劃非常有用。