전방형

원발성 유리체 증식증 (PFV)
1. 지속태아혈관증(PFV)이란?
섹션 제목: “1. 지속태아혈관증(PFV)이란?”지속태아혈관증(persistent fetal vasculature: PFV)은 태생기 유리체 혈관계의 퇴축 부전으로 발생하는 선천성 안질환이다. 구칭은 지속원발유리체증식증(persistent hyperplastic primary vitreous: PHPV)이라고 불렸다. 1997년 Goldberg가 수정체 주변의 혈관섬유조직 잔류도 포함하여 PFV라는 명칭을 제안하였고 12), 현재 널리 받아들여지고 있다.
유리체 혈관계는 시신경 유두에서 발원하는 유리체 동맥(hyaloid artery)과 전방의 수정체 혈관막(tunica vasculosa lentis)으로 구성된다. 태생 제56주에 간엽세포가 태생열에서 유리체강으로 진입하여 형성되며, 태생 제10주에 최성기가 된다. 이후 태생 1315주부터 말초에서 퇴축이 시작되어 태생 후기에는 소실된다. PFV에서는 이 퇴축 부전이 발생하여 혈관 주변 조직의 발생 이상이 초래된다.
단안성이며 비유전성으로 알려져 있으며, 원인이 되는 특정 유전자는 밝혀지지 않았다. 전형적인 예는 소안구를 동반한 백색동공으로 발견되지만, 사시나 약시를 계기로 진단되는 경우도 있다.
PFV는 영유아·소아 백내장의 약 20%에 합병된다고 보고된다 2)3). Pediatric Eye Disease Investigator Group(PEDIG)의 백내장 등록 994예 중 64예(6.4%)가 PFV 합병 백내장이었으며 1), 75%가 무수정체로 수술(수술 시 월령 중앙값 2개월), 25%가 위수정체로 수술(수술 시 연령 중앙값 29개월)되었다 1). 28%에서 후안부 이상(유리체·망막·시신경 이상)을 인정하였고 1), 가족력을 가진 것은 4~6%에 불과하다 1).
PFV는 거의 항상 단안성이며 비유전성입니다. PEDIG 연구에서도 양측 PFV는 3예만 제외되었습니다1). 양안성인 경우 가족성 삼출성 유리체망막병증(FEVR)이나 Norrie병과의 감별이 필요하며, 유전자 검사를 포함한 정밀 검사가 권장됩니다.
2. 주요 증상과 임상 소견
섹션 제목: “2. 주요 증상과 임상 소견”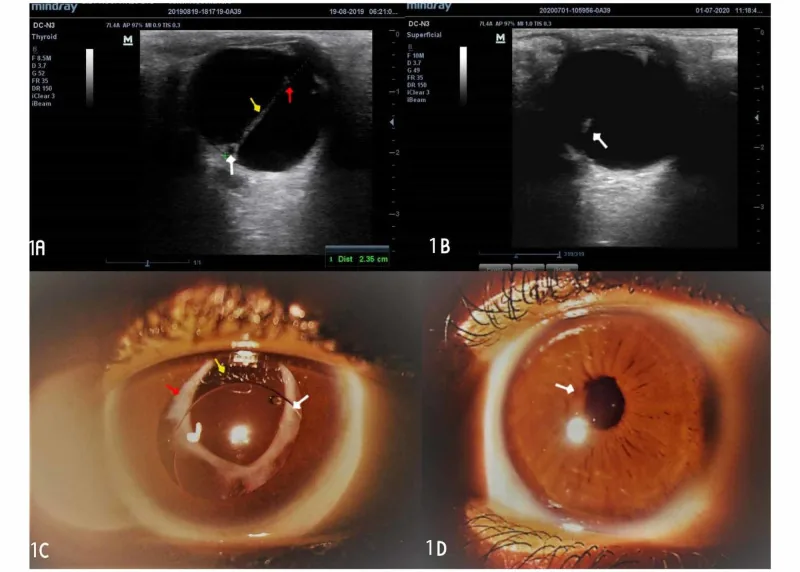
병형 분류
섹션 제목: “병형 분류”PFV는 병변 부위의 우세에 따라 전방형, 후방형, 혼합형의 3형으로 분류됩니다.
후방형
혼합형
주요 소견: 전방형과 후방형의 소견이 혼재합니다. 소안구증을 동반하는 경우가 많습니다.
치료 적응증: 개별 병변 범위에 따라 신중히 판단합니다.
예후: 중증 혼합형에서는 측정 가능 시력이 19%에 불과하며, 61%가 광각 없음 8)
소아 안과학 세부 7형 분류
섹션 제목: “소아 안과학 세부 7형 분류”| 병형 | 주요 소견 | 합병 가능한 이상 |
|---|---|---|
| 1. 유리체 혈관 (동맥) 잔류 | 유두→유리체 후부 중앙의 백색~회색 삭상물 + Mittendorf 반점 | 후낭하 백내장, 후부 수정체 원추 |
| 2. 유리체 혈관 본간 주체형 | 유두에서 굵은 삭상물이 솟아오름 | 유두 주위 망막 견인 |
| 3. 시신경 유두 국한형 | 유두 위의 백색 조직 | 주변 망막 견인 |
| 4. 유두에서 발생한 망막 주름 | 안저 주변부 증식 조직의 견인 | 주변부 망막 이상 |
| 5. 유리체강 전체 점유형 | 광범위 증식, 전망막박리, 망막 이형성 | 소안구증이 많음 |
| 6. 수정체 후 섬유증식 주체형 | 수정체 후방에 국한, 안저 거의 정상 | 치료 적응증 있음 |
| 7. 수정체 전방형 | 수정체 혈관막 증식에 의한 전방 섬유증식 | 동공 변형, 폐쇄 |
주요 임상 소견
섹션 제목: “주요 임상 소견”주요 소견으로는 한쪽 눈의 소안구증, 수정체 후면 혼탁(Mittendorf 반점), 망막 혈관 주행 이상, 망막 이형성, 연장된 섬모체 돌기, 수정체 후면에서 시신경 유두로 뻗어 있는 끈 모양의 구조물이 관찰됩니다. 끈 모양 구조물은 견인을 유발하여 섬모체 돌기의 연장을 통해 저안압을 초래합니다. 유두 부근의 끈 조직에 망막이 포함되기도 합니다. 유리체 혈관 퇴축 정도에 따라 중증도가 다릅니다.
PEDIG 연구에서 PFV 백내장의 28%(18/64안)에서 후안부 이상이 발견되었고1), 인공수정체안의 46%에서 후안부 병변이 있었습니다(무수정체안 28%와 비교 시 연령 보정 OR 4.47)1). 무수정체 PFV안의 96%에서 백내장 수술 시 전방 유리체 절제술이 시행되었습니다1).
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”발생학적 배경
섹션 제목: “발생학적 배경”유리체 혈관계의 정상 발달에서는 태생 제56주에 간엽 세포가 태생열에서 유리체강으로 진입하여 유리체 혈관계가 형성됩니다. 태생 제10주에 절정에 이르며, 이후 말초에서 퇴축이 시작됩니다. 구체적으로 태생 1315주부터 퇴축이 시작되어 태생 후기에는 소멸됩니다.
PFV에서는 유리체 혈관의 퇴축 부전이 발생하여 혈관 주변 조직의 발생 이상이 유발됩니다. 그 결과 수정체 혼탁, 망막 형성 이상, 소안구증이 발생하는 것으로 생각됩니다. 또한 잔류 조직의 견인으로 인해 섬모체 돌기의 연장이나 망막 주름이 발생합니다.
유전적 배경
섹션 제목: “유전적 배경”PFV는 단안성, 비유전성으로 간주되며, 원인이 되는 특정 유전자는 동정되지 않았습니다. 가족력이 있는 경우는 4~6%에 불과하며1), 대부분이 산발성입니다. 양안성인 경우 FEVR(NDP, LRP5, FZD4 유전자 변이)이나 Norrie병(NDP 유전자 변이)과의 유전적 감별이 중요합니다.
주산기 위험 요인
섹션 제목: “주산기 위험 요인”저체중 출생이나 조산과의 명확한 연관성은 입증되지 않았지만, 중증의 유리체 혈관 잔류는 드물게 미숙아 망막병증과 유사한 소견을 보일 수 있습니다.
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”진단 검사
섹션 제목: “진단 검사”- 초음파 검사(B-스캔): 수정체 후낭에서 유래한 끈 모양 구조물을 시각화합니다. 소안구증 평가와 유리체강 평가에 유용합니다. 중간 투명체가 혼탁하여 후극부를 직접 볼 수 없는 경우 특히 중요합니다.
- CT: 안내 석회화 유무를 검출합니다. 망막모세포종은 석회화를 동반하지만 PFV는 석회화가 없으므로 두 질환의 감별에 가장 유용한 검사입니다.
- MRI: 끈 모양 구조물, 후안부 이상, 시신경 침윤 평가에 탁월합니다.
- ERG/VEP(망막전위도/시각유발전위): 망막 기능 평가. 수술 전 시기능을 평가하여 외과적 중재의 적절성을 판단하는 근거가 됩니다.
감별 진단
섹션 제목: “감별 진단”백색 동공을 유발하는 질환과의 감별이 가장 중요한 과제입니다. 특히 망막모세포종과의 감별은 생명 예후에 직결됩니다.
망막모세포종과의 감별
FEVR 및 Norrie병과의 감별
양안성인 경우 중요
양안의 망막전체박리나 수정체후방섬유증식이 있는 경우 FEVR이나 Norrie병과의 감별이 필요합니다. 가족력 및 유전자 이상 검사가 참고가 됩니다. 차세대염기서열분석(NGS) 패널 검사의 활용이 유용합니다.
| 질환 | 측성 | 소안구증 | 유전성 | CT 석회화 | 특징적 소견 |
|---|---|---|---|---|---|
| PFV | 거의 항상 단안 | 있음 | 비유전성 | 없음 | 수정체 뒤 섬유혈관성 줄기, 시신경유두로의 섬유혈관막 |
| 망막모세포종 | 70% 단안 | 없음 | RB1 돌연변이 (35–45%) | 있음 (특징적) | 백색 융기 종괴, 유리체 파종 |
| FEVR | 양안 | 없음 | 있음 (FZD4 등) | 없음 | 주변부 망막 무혈관 영역, 견인성 망막박리 |
| Norrie병 | 양안성 | 가능함 | X-연관 열성 (NDP) | 없음 | 유리체 출혈, 망막박리, 지적 장애 |
| 미숙아 망막병증 | 양안성 | 없음 | 없음 | 없음 | 주변부 망막 무혈관 영역, 혈관 증식 |
5. 표준 치료법
섹션 제목: “5. 표준 치료법”수술 적응증 판단
섹션 제목: “수술 적응증 판단”투명체의 혼탁은 백내장과 동일하게 대처합니다. 혼탁이 수정체 후부에 국한되고 안저에 이상이 없으면 선천백내장에 준하여 수정체 절제 및 섬유증식막 절제를 시행합니다. 수정체 후방의 끈 모양 구조가 시축에 걸리지 않고 편심되어 있으면 반드시 수술이 필요하지 않습니다. 안저에 병변이 있는 경우 일반적으로 수술 대상이 아닙니다. 망막박리나 견인이 있는 경우 ERG/VEP 반응이 양호하면 외과적 개입의 근거가 됩니다. 수정체 전부의 증식으로 동공 변형이나 폐쇄가 있는 경우 동공성형술을 시행합니다.
백내장 수술
섹션 제목: “백내장 수술”수정체 제거 후 굴절 교정과 약시 치료를 시행합니다. 수술 방식은 선천백내장에 준합니다. PEDIG 연구에서는 무수정체 PFV안의 96%에서 백내장 수술 시 전방 유리체 절제술이 시행되었으며1), 첫 수술 시 전방 유리체 절제술을 시행한 경우 시축 혼탁 발생률이 18%인 반면, 시행하지 않은 경우 60%에 달합니다1).
수술 후 약시 치료
섹션 제목: “수술 후 약시 치료”수술 후에는 굴절 교정(콘택트렌즈 또는 안경)과 건안 가림(안대)을 병용한 약시 치료를 시행합니다. 단안성 PFV에서는 약시 치료 순응도가 시력 예후를 좌우합니다. 치료는 시각 발달의 결정적 시기(출생 후부터 10세경까지)에 적극적으로 시행해야 합니다.
수술 성적 (PEDIG PFV 백내장 5년 성적)
섹션 제목: “수술 성적 (PEDIG PFV 백내장 5년 성적)”| 지표 | 무수정체 PFV안 | 인공수정체 PFV안 |
|---|---|---|
| 수술 시 연령 (중앙값) | 생후 2개월 | 생후 29개월 |
| 5년 시점 중앙 시력 | 20/100 (IQR 20/50–20/320) | 20/400 (IQR 20/200–<20/800) |
| 시력 20/200 이상 | 59% (95% CI 39–76%) | 23% (95% CI 5–54%) |
| 연령 정상 시력 달성 | 10% (95% CI 2–27%) | 8% (95% CI 0–36%) |
| 녹내장 관련 이상 반응 (5년 누적) | 24% (95% CI 9–37%) | 7% (95% CI 0–20%) |
| 시축 혼탁 | 15% (95% CI 5–25%) | 45% (95% CI 13–66%) |
| 망막 박리 | 4% (95% CI 0–10%) | 7% (95% CI 0–19%) |
전체 시력 결과: 42안 중 4안(10%, 95% CI 3–23%)이 연령 정상 시력을 달성했고, 48%(95% CI 32–64%)가 20/200 이상의 시력을 달성했습니다1). 인공수정체 PFV안의 20/200 이상 시력 달성률(23%)은 비PFV 인공수정체안(68%)에 비해 유의하게 낮았습니다(연령 보정 OR=0.14, P=0.005)1). 무수정체 PFV안은 비PFV 무수정체안과 비교하여 유사한 결과를 보였습니다(연령 보정 OR=1.90, P=0.14)1).
병형별로, 전방형의 중앙 시력은 20/100(20/200 이상 54%)인 반면, 후방형의 중앙 시력은 20/800(20/200 이상 36%)로 더 나빴으며, 차이는 4 logMAR 라인(P=0.09)이었습니다1).
다른 보고로는 Bata 등의 20년 단일 기관 연구(무수정체 PFV 58안)에서 33%가 20/200 이상(평균 추적 6.7년)4), Anteby 등의 보고(무수정체 PFV 30안)에서 16.7%가 20/200 이상(평균 추적 8.5년)5), de Saint Sauveur 등의 중증 혼합형 PFV 36예에서 측정 가능 시력은 19%에 불과하고 61%가 광각 없음으로 보고되었습니다8).
합병증 관리
섹션 제목: “합병증 관리”녹내장 외 주요 합병증으로 시축 혼탁(인공수정체 PFV안의 45%, 무수정체안의 15%)이 있으며, 시축 청명화 수술의 누적 발생률은 인공수정체 PFV안에서 40%에 달합니다1). 또한, 무수정체 PFV안의 13%(95% CI 2–22%)가 5년 내에 이차 IOL 삽입 수술을 필요로 합니다1).
중증 예후 및 후방형 관리
섹션 제목: “중증 예후 및 후방형 관리”망막 이형성에는 효과적인 치료 방법이 없습니다. 후안부형에서는 시력 발달이 기대되지 않는 경우가 많습니다. 현저한 소안구증에 대해서는 미용적 측면을 고려하여 조기에 의안을 착용합니다. 의안 착용은 안와 발달 촉진에도 기여합니다.
전방형(수정체 후방 국한)에서는 수술 후 5년째 중앙 시력 20/100, 20/200 이상 달성률 54%로 보고됩니다1). 그러나 연령 정상 시력을 달성하는 것은 전체의 10%에 불과합니다. 후방형에서는 중앙 시력 20/800로 좋지 않습니다1). 시력 예후는 병형, 후안부 병변 유무, 수술 연령, 약시 치료 순응도에 크게 영향을 받습니다.
녹내장 관련 이상 반응이 가장 흔하며, 무수정체 PFV 안에서 5년 누적 발생률이 24%에 이릅니다1). 시축 혼탁도 중요한 합병증으로, 인공수정체 안에서 45%에서 발생합니다1). 초회 수술 시 전방 유리체 절제술을 시행하는 것이 시축 혼탁 예방에 중요합니다(시행 시 18% vs 미시행 시 60%)1). 수술 후에도 장기적인 정기적 안압 관리, 시축 평가, 굴절 교정이 필요합니다.
6. 병태생리학 및 상세 발병 기전
섹션 제목: “6. 병태생리학 및 상세 발병 기전”유리체 혈관계의 정상 발달과 퇴축
섹션 제목: “유리체 혈관계의 정상 발달과 퇴축”태생 5~6주에 간엽 세포가 시각열에서 유리체강으로 진입하여 유리체 동맥과 수정체 혈관막으로 구성된 유리체 혈관계가 형성됩니다. 이 혈관계는 발달 중인 수정체와 안구 전절에 산소와 영양을 공급하는 중요한 역할을 합니다.
태생 10주에 발달이 최고조에 이르며, 이후 말초에서부터 퇴축이 시작됩니다. 태생 13~15주부터 퇴축이 본격화되고, 태생 후기에는 거의 소실됩니다. 정상 분만 시 유리체 혈관계는 거의 관찰되지 않지만, Mittendorf 반점(수정체 후면에 남아 있는 작은 흰 점)으로 흔적이 남을 수 있습니다.
PFV의 발생 기전
섹션 제목: “PFV의 발생 기전”PFV에서는 유리체 혈관의 퇴축 부전이 발생하여 혈관 주변의 섬유 증식 조직의 발생 이상이 유발됩니다. 잔존한 혈관 주변 간엽 조직은 증식 및 섬유화되어 다양한 임상 소견을 나타냅니다.
구체적인 결과로 다음이 발생합니다.
- 수정체 혼탁(후낭하 백내장, 후부 수정체 원추): 잔존 섬유 조직의 수정체 후면 부착
- 소안구증: 혈관 주위 조직의 발생 이상으로 인한 안구 전체의 발육 장애
- 망막 형성 이상: 후부형에서 견인 및 허혈로 인한 망막의 이형성
- 모양체 돌기의 연장과 저안압: 삭상물에 의한 견인
- 망막 주름: 후부 병변 조직의 견인으로 인한 변형
단안성, 비유전성인 이유는 태생기 유리체 혈관 퇴축이 국소 혈관 신생 및 퇴축 신호에 의해 조절되며, 이 조절 기전의 한쪽 눈만의 장애가 가정되기 때문입니다. 그러나 구체적인 분자 기전은 아직 밝혀지지 않았습니다.
7. 최신 연구와 향후 전망
섹션 제목: “7. 최신 연구와 향후 전망”PFV의 유전적 병태 생리
섹션 제목: “PFV의 유전적 병태 생리”PFV의 특정 원인 유전자는 아직 확인되지 않았지만, 동물 모델에서 FZD4, LRP5, NDP 등 Wnt 신호 전달 경로 관련 유전자의 돌연변이가 PFV 유사 표현형(유리체 혈관 잔류)을 나타내는 것으로 보고되었습니다. 이들은 FEVR 및 Norrie병의 원인 유전자이기도 하며, PFV와 관련 질환 간의 유전적 연속성을 시사합니다. 차세대 염기서열 분석(NGS) 패널 검사의 PFV 감별 진단에 대한 임상 적용도 진행되고 있습니다.
수술 기법의 개선
섹션 제목: “수술 기법의 개선”25게이지 및 27게이지 미세 절개 유리체 절제술(MIVS)을 통한 후방형 PFV 접근이 시도되고 있습니다. 신생아 및 영유아를 대상으로 한 소절개 수술은 침습성을 최소화하고 수술 후 염증을 억제하는 장점이 있다고 알려져 있습니다11).
IOL 삽입의 최적 시기
섹션 제목: “IOL 삽입의 최적 시기”영아기의 일차 IOL 삽입 대 무수정체 관리 후 이차 IOL 삽입의 장기 결과 비교는 PFV 연구의 중요한 과제입니다. PEDIG 연구의 연장 추적 데이터를 통해 PFV 특유의 IOL 삽입 적응 기준 확립이 기대됩니다6)7).
영상 진단의 발전
섹션 제목: “영상 진단의 발전”광각 안저 카메라 및 전안부 OCT를 이용한 PFV의 비침습적 평가가 발전하고 있습니다. 특히 전안부 OCT는 후부 수정체 원추 및 후낭하 백내장의 형태 평가와 수술 전 계획에 유용합니다.
8. 참고 문헌
섹션 제목: “8. 참고 문헌”- Haider KM, Repka MX, Sutherland DR, et al. Outcomes and complications 5 years after surgery for pediatric cataract associated with persistent fetal vasculature. Am J Ophthalmol. 2024;(online ahead of print).
- Wilson ME, Trivedi RH, Morrison DG, et al. The Infant Aphakia Treatment Study: evaluation of cataract morphology in eyes with monocular cataracts. J AAPOS. 2011;15(5):421-426.
- Solebo AL, Russell-Eggitt I, Cumberland P, Rahi JS. Congenital cataract associated with persistent fetal vasculature: findings from IoLunder2. Eye (Lond). 2016;30(9):1204-1209.
- Bata BM, Chiu HH, Mireskandari K, Ali A, Lam WC, Wan MJ. Long-term visual and anatomic outcomes following early surgery for persistent fetal vasculature: a single-center, 20-year review. J AAPOS. 2019;23(6):327.e1-327.e5.
- Anteby I, Cohen E, Karshai I, BenEzra D. Unilateral persistent hyperplastic primary vitreous: course and outcome. J AAPOS. 2002;6(2):92-99.
- Repka MX, Dean TW, Lazar EL, et al. Cataract surgery in children from birth to less than 13 years of age: baseline characteristics of the cohort. Ophthalmology. 2016;123(12):2462-2473.
- Pediatric Eye Disease Investigator Group. Visual acuity and ophthalmic outcomes 5 years after cataract surgery among children younger than 13 years. JAMA Ophthalmol. 2022;140(3):269-276.
- de Saint Sauveur G, Chapron T, Abdelmassih Y, et al. Management and outcomes of posterior persistent fetal vasculature. Ophthalmology. 2023;130(8):844-853.
- Khandwala N, Besirli C, Bohnsack BL. Outcomes and surgical management of persistent fetal vasculature. BMJ Open Ophthalmol. 2021;6(1):e000656.
- Hunt A, Rowe N, Lam A, Martin F. Outcomes in persistent hyperplastic primary vitreous. Br J Ophthalmol. 2005;89(7):859-863.
- Bata BM, Khalili S, Ali A, Wan MJ, Mireskandari K. Late surgery for unilateral persistent fetal vasculature: long-term visual and anatomic outcomes. J AAPOS. 2022;26(6):296.e1-296.e5.
- Goldberg MF. Persistent fetal vasculature (PFV): an integrated interpretation of signs and symptoms associated with persistent hyperplastic primary vitreous (PHPV). Am J Ophthalmol. 1997;124(5):587-626.
