前部型
主要所见:晶状体后囊的纤维增生膜(Mittendorf斑)、后囊下白内障、后部晶状体圆锥
治疗适应症:病变局限于晶状体后部且眼底正常时,有手术适应症
预后:三型中最好。中位视力20/100(视力20/200以上占54%)1)

永存原始玻璃体增生症(persistent fetal vasculature, PFV)是一种先天性眼病,由胚胎期玻璃体血管系统退化不全引起。旧称永存原始玻璃体增生症(persistent hyperplastic primary vitreous, PHPV)。1997年,Goldberg提出PFV这一名称,以包括晶状体周围的血管纤维组织残留 12),目前已被广泛接受。
玻璃体血管系统包括从视盘发出的玻璃体动脉和前方的晶状体血管膜。间充质细胞在胚胎第5-6周通过胚裂进入玻璃体腔,于第10周达到高峰。随后从第13-15周开始从周边退化,在胎儿晚期消退。PFV中这种退化不全,导致血管周围组织发育异常。
PFV通常为单眼、非遗传性,尚未明确特定的致病基因。典型病例表现为伴有小眼球的白色瞳孔,但也可能因斜视或弱视而诊断。
据报道,PFV合并于约20%的婴幼儿白内障 2)3)。在儿科眼病研究者小组(PEDIG)的白内障登记中,994例中有64例(6.4%)为PFV合并白内障 1);其中75%作为无晶状体眼手术(手术时中位月龄2个月),25%作为人工晶状体眼手术(手术时中位年龄29个月)1)。28%存在后段异常(玻璃体、视网膜或视神经异常)1),仅有4-6%有家族史 1)。
本质上是同一疾病的新旧名称差异。PHPV是旧称,侧重于玻璃体血管(原始玻璃体)的增生和残留。1997年,Goldberg提出了PFV(persistent fetal vasculature)这一名称,以涵盖晶状体周围血管纤维组织的残留。PFV能表达更广泛的病变谱,因此现在是标准名称。
PFV几乎总是单眼发病,且为非遗传性。在PEDIG研究中,仅3例双侧PFV被排除1)。双侧病例需要与家族性渗出性玻璃体视网膜病变(FEVR)和Norrie病鉴别,建议进行包括基因检测在内的详细检查。
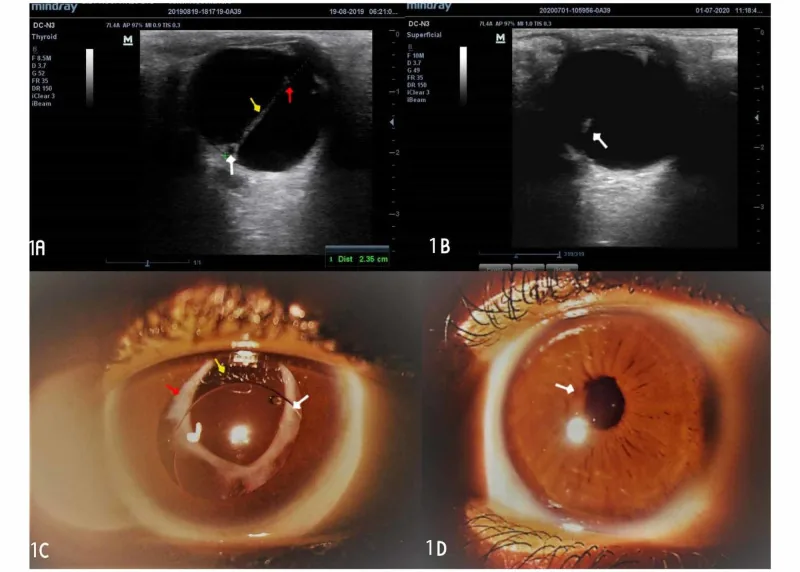
PFV根据病变优势部位分为前部型、后部型和混合型三型。
前部型
主要所见:晶状体后囊的纤维增生膜(Mittendorf斑)、后囊下白内障、后部晶状体圆锥
治疗适应症:病变局限于晶状体后部且眼底正常时,有手术适应症
预后:三型中最好。中位视力20/100(视力20/200以上占54%)1)
后部型
混合型
主要表现:前部型和后部型表现混合存在。常伴有小眼球。
治疗适应症:根据个体病变范围谨慎判断。
预后:重度混合型中,可测量视力仅19%,61%无光感8)
| 类型 | 主要表现 | 可能合并的异常 |
|---|---|---|
| 1. 玻璃体血管(动脉)残留 | 视乳头→玻璃体后部中央的白色至灰色索状物+Mittendorf斑 | 后囊下白内障、后部圆锥形晶状体 |
| 2. 玻璃体血管主干型 | 从视乳头发出粗大索状物 | 视乳头周围视网膜牵引 |
| 3. 视盘局限型 | 视盘上白色组织 | 周围视网膜牵引 |
| 4. 视盘视网膜皱襞 | 眼底周边部增殖组织牵引 | 周边视网膜异常 |
| 5. 玻璃体腔占位型 | 广泛增殖、全视网膜脱离、视网膜发育不良 | 多伴小眼球 |
| 6. 晶状体后纤维增生为主型 | 局限于晶状体后,眼底大致正常 | 有治疗指征 |
| 7. 晶状体前型 | 晶状体血管膜增殖导致的前方纤维增生 | 瞳孔变形、闭锁 |
主要所见包括单眼小眼球、晶状体后囊混浊(Mittendorf斑)、视网膜血管走行异常、视网膜发育不良、睫状突延长,以及从晶状体后囊向视乳头延伸的条索状物。条索状物可导致牵引,通过延长睫状突引起低眼压。视乳头附近的条索组织可能牵拉视网膜。严重程度取决于玻璃体血管退化的程度。
在PEDIG研究中,PFV白内障的28%(18/64眼)存在后段异常1),人工晶状体眼的46%有后段病变(与无晶状体眼的28%相比,年龄校正OR为4.47)1)。无晶状体PFV眼中96%在白内障手术时进行了前部玻璃体切除1)。
在玻璃体血管系统的正常发育中,间充质细胞在胚胎第5-6周通过胚裂进入玻璃体腔,形成玻璃体血管系统。在胚胎第10周达到顶峰,随后从周边开始退化。具体而言,退化始于胚胎第13-15周,在胚胎晚期消退。
在PFV中,玻璃体血管退化不全,导致血管周围组织发育异常。这被认为会导致晶状体混浊、视网膜发育不良和小眼球。此外,残留组织的牵引导致睫状突延长和视网膜皱襞。
PFV被认为是单眼性、非遗传性的,尚未确定特定的致病基因。仅有4-6%有家族史1),大多数为散发性。双眼病例需与FEVR(NDP、LRP5、FZD4基因突变)和Norrie病(NDP基因突变)进行遗传学鉴别。
尚未显示与低出生体重或早产有明确关联,但严重的玻璃体血管残留罕见地可能呈现类似早产儿视网膜病变的所见。
与引起白瞳症的疾病进行鉴别是最重要的任务。特别是与视网膜母细胞瘤的鉴别直接关系到生命预后。
与视网膜母细胞瘤的鉴别
与FEVR和Norrie病的鉴别
双眼病例中重要
双眼全视网膜脱离或晶状体后纤维增生时,需要与FEVR或Norrie病鉴别。家族史和基因异常检查有参考价值。利用下一代测序(NGS)面板检测是有用的。
| 疾病 | 侧别 | 小眼球 | 遗传性 | CT钙化 | 特征性表现 |
|---|---|---|---|---|---|
| PFV | 几乎均为单眼 | 有 | 非遗传性 | 无 | 晶状体后纤维血管索、视乳头纤维血管膜 |
| 视网膜母细胞瘤 | 70%单眼 | 无 | RB1突变(35–45%) | 有(特征性) | 白色隆起肿块、玻璃体种植 |
| FEVR | 双眼 | 无 | 有(FZD4等) | 无 | 周边视网膜无血管区、牵拉性视网膜脱离 |
| Norrie病 | 双眼性 | 可能 | X连锁隐性遗传(NDP) | 无 | 玻璃体出血、视网膜脱离、智力障碍 |
| 早产儿视网膜病变 | 双眼性 | 无 | 无 | 无 | 周边视网膜无血管区、血管增殖 |
透光体的混浊处理与白内障相同。如果混浊局限于晶状体后部且眼底正常,则按照先天性白内障进行晶状体切除和纤维增殖膜切除。如果晶状体后方的索状物偏心且不影响视轴,则不一定需要手术。如果眼底受累,通常不进行手术。对于视网膜脱离或牵拉,如果ERG/VEP反应良好,可作为外科干预的依据。如果前部增殖导致瞳孔变形或闭锁,则进行瞳孔成形术。
晶状体去除后进行屈光矫正和弱视治疗。手术方式参照先天性白内障。PEDIG研究中,96%的无晶状体PFV眼在白内障手术时同时进行了前部玻璃体切除术1),初次手术时进行前部玻璃体切除术的视轴混浊发生率为18%,而未进行者高达60%1)。
术后进行屈光矫正(隐形眼镜或眼镜)和健眼遮盖(眼罩)相结合的弱视治疗。单眼PFV的弱视治疗依从性决定视力预后。治疗需要在视觉发育关键期(出生后至10岁左右)积极进行。
| 指标 | 无晶状体PFV眼 | 人工晶状体PFV眼 |
|---|---|---|
| 手术时年龄(中位数) | 2个月 | 29个月 |
| 5年时中位视力 | 20/100(IQR 20/50–20/320) | 20/400(IQR 20/200–<20/800) |
| 视力20/200或以上 | 59%(95%CI 39–76%) | 23%(95%CI 5–54%) |
| 达到年龄正常视力 | 10%(95%CI 2–27%) | 8%(95%CI 0–36%) |
| 青光眼相关不良事件(5年累积) | 24%(95%CI 9–37%) | 7%(95%CI 0–20%) |
| 视轴混浊 | 15%(95%CI 5–25%) | 45%(95%CI 13–66%) |
| 视网膜脱离 | 4%(95%CI 0–10%) | 7%(95%CI 0–19%) |
总体视力结局:42只眼中,4只眼(10%,95%CI 3–23%)达到年龄正常视力,48%(95%CI 32–64%)达到20/200或以上视力1)。人工晶体眼PFV眼的20/200以上视力达成率(23%)显著低于非PFV人工晶体眼(68%)(年龄校正OR=0.14,P=0.005)1)。无晶体眼PFV眼与非PFV无晶体眼相比,结果相当(年龄校正OR=1.90,P=0.14)1)。
按类型分,前部型的中位视力为20/100(20/200以上占54%),而后部型的中位视力较差,为20/800(20/200以上占36%),相差4个logMAR行(P=0.09)1)。
其他报告包括:Bata等人的20年单中心研究(58只无晶体眼PFV眼)中33%达到20/200以上(平均随访6.7年)4);Anteby等人的报告(30只无晶体眼PFV眼)中16.7%达到20/200以上(平均随访8.5年)5);de Saint Sauveur等人的36例重度混合型PFV病例中,仅19%有可测量视力,61%无光感8)。
其他主要并发症包括视轴混浊(人工晶体眼PFV眼45%,无晶体眼15%),人工晶体眼PFV眼需要视轴清晰化手术的累积发生率高达40%1)。此外,13%(95%CI 2–22%)的无晶体眼PFV眼在5年内需要二次IOL植入手术1)。
视网膜发育不良没有有效的治疗方法。后部型PFV通常无法预期视力发育。对于明显的小眼球,出于美容考虑,应早期佩戴义眼。义眼佩戴也有助于眼眶发育。
前部型(晶状体后局限型)术后5年中位视力为20/100,20/200以上达成率为54%1)。但只有10%的眼能达到年龄正常视力。后部型中位视力较差,为20/8001)。视力预后受病型、后段病变有无、手术年龄和弱视治疗依从性的显著影响。
青光眼相关不良事件最为常见,无晶状体PFV眼的5年累积发病率达24%1)。视轴混浊也是重要的并发症,假晶状体眼中45%发生1)。初次手术时行前部玻璃体切除对预防视轴混浊很重要(施行组18% vs 未施行组60%)1)。术后也需要长期定期进行眼压管理、视轴评估和屈光矫正。
在胎龄第5-6周,间充质细胞从视裂进入玻璃体腔,形成由玻璃体动脉和晶状体血管膜组成的玻璃体血管系统。该血管系统为发育中的晶状体和眼前节提供氧气和营养,发挥重要作用。
胎龄第10周为发育高峰期,此后从外周开始退化。胎龄13-15周退化全面开始,至胎儿后期几乎完全消退。正常分娩时玻璃体血管系统几乎不可见,但有时会残留如Mittendorf斑(晶状体后囊上的小白点)等痕迹。
在PFV中,玻璃体血管退化不全,导致血管周围纤维增殖组织发生异常。残留的血管周围间充质组织增殖并纤维化,呈现各种临床表现。
具体结果如下:
单眼性、非遗传性的原因被认为是,胚胎期玻璃体血管退化受局部血管新生和退化信号调控,这种调控机制仅在一只眼发生障碍。但具体的分子机制尚未阐明。
虽然PFV的特定致病基因尚未确定,但动物模型已报告FZD4、LRP5、NDP等Wnt信号通路相关基因的突变表现出PFV样表型(玻璃体血管残留)。这些也是FEVR和Norrie病的致病基因,提示PFV与相关疾病之间存在遗传连续性。下一代测序(NGS)面板检测在PFV鉴别诊断中的临床应用也在推进中。
使用25G和27G微切口玻璃体手术(MIVS)处理后部型PFV的方法正在尝试中。针对新生儿和婴儿的小切口手术据说具有最小化创伤和减少术后炎症的优势11)。
婴儿期一期IOL植入与无晶状体管理后二期IOL植入的长期结果比较是PFV研究的重要课题。PEDIG研究的延长随访数据有望建立PFV特有的IOL植入适应症标准6)7)。
使用广角眼底相机和前段OCT对PFV进行无创评估正在进步。特别是前段OCT对于后部圆锥形晶状体和后囊下白内障的形态评估以及术前规划非常有用。