Persistent fetal vasculature (PFV ) เป็นโรคตาที่เกิดแต่กำเนิดจากการถดถอยที่ไม่สมบูรณ์ของระบบหลอดเลือดวุ้นตา ในระยะตัวอ่อน เดิมเรียกว่า persistent hyperplastic primary vitreous (PHPV ) ในปี 1997 Goldberg เสนอชื่อ PFV เพื่อรวมเนื้อเยื่อเส้นใยหลอดเลือดที่เหลืออยู่รอบเลนส์ 12) และปัจจุบันเป็นที่ยอมรับอย่างกว้างขวาง
ระบบหลอดเลือดวุ้นตา ประกอบด้วยหลอดเลือดแดงไฮยาลอยด์ (hyaloid artery) ที่ออกจากจานประสาทตา และทูนิกา วาสคูโลซา เลนทิส (tunica vasculosa lentis) ด้านหน้า ก่อตัวขึ้นในสัปดาห์ที่ 5-6 ของการตั้งครรภ์เมื่อเซลล์มีเซนไคม์เข้าสู่ช่องวุ้นตา ผ่านรอยแยกของตัวอ่อน และเจริญเต็มที่ในสัปดาห์ที่ 10 หลังจากนั้นการถดถอยเริ่มจากส่วนปลายในสัปดาห์ที่ 13-15 และหายไปในช่วงท้ายของการตั้งครรภ์ ใน PFV การถดถอยนี้ล้มเหลว ทำให้เกิดความผิดปกติของเนื้อเยื่อรอบหลอดเลือด
ถือว่าเป็นโรคข้างเดียวและไม่ถ่ายทอดทางพันธุกรรม ยังไม่มีการระบุยีนที่จำเพาะ กรณีทั่วไปพบด้วยรูม่านตาขาว ร่วมกับตาเล็ก แต่บางครั้งวินิจฉัยเมื่อพบตาเหล่ หรือตามัว
PFV ประมาณว่าพบร่วมกับต้อกระจก ในทารกและเด็กประมาณ 20% 2) 3) ในทะเบียนต้อกระจก ของ Pediatric Eye Disease Investigator Group (PED IG) จำนวน 994 ราย มี 64 ราย (6.4%) เป็นต้อกระจก ร่วมกับ PFV 1) โดย 75% ผ่าตัดแบบไม่มีเลนส์แก้วตาเทียม (อายุผ่าตัดมัธยฐาน 2 เดือน) และ 25% ผ่าตัดแบบมีเลนส์แก้วตาเทียม (อายุผ่าตัดมัธยฐาน 29 เดือน) 1) พบความผิดปกติของส่วนหลัง (วุ้นตา จอประสาทตา เส้นประสาทตา ) ใน 28% 1) และมีประวัติครอบครัวเพียง 4-6% 1)
Q
PFV และ PHPV แตกต่างกันอย่างไร?
A
โดยพื้นฐานแล้วเป็นโรคเดียวกันแต่เป็นชื่อเก่าและใหม่ PHPV เป็นชื่อเดิม ซึ่งเน้นที่การเจริญเกินและการคงอยู่ของหลอดเลือดแก้วตา (แก้วตาปฐมภูมิ) ในปี 1997 Goldberg เสนอชื่อ PFV (persistent fetal vasculature) เพื่อรวมถึงการคงอยู่ของเนื้อเยื่อเส้นใยหลอดเลือดรอบเลนส์ด้วย เนื่องจาก PFV สามารถแสดงสเปกตรัมรอยโรคที่กว้างกว่า จึงกลายเป็นชื่อมาตรฐานในปัจจุบัน
Q
PFV เกิดขึ้นทั้งสองตาหรือไม่?
A
PFV มักเป็นข้างเดียว (unilateral) และไม่ถ่ายทอดทางพันธุกรรม ในการศึกษา PED IG มีเพียง 3 รายของ PFV สองข้างที่ถูกคัดออก 1) ในกรณีสองข้าง จำเป็นต้องแยกจาก familial exudative vitreoretinopathy (FEVR ) และโรค Norrie และแนะนำให้ตรวจอย่างละเอียดรวมถึงการตรวจทางพันธุกรรม
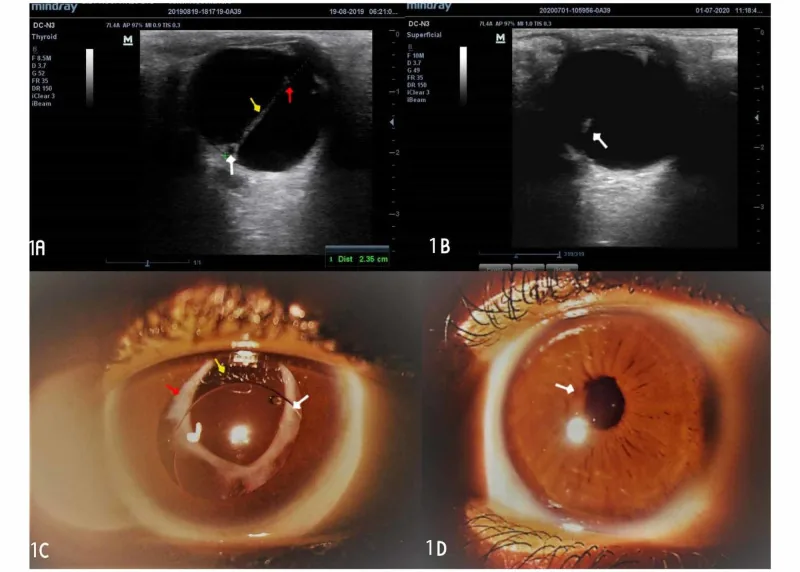
ภาพอัลตราซาวนด์ลูกตาและภาพถ่ายส่วนหน้าของตาใน PFV พบรอยโรคคล้ายเส้นในแก้วตา และเยื่อเส้นใยหลอดเลือดสีขาวด้านหลังรูม่านตา Egbu E The Outcome of Manual Small Incision Cataract Surgery and Anterior Vitrectomy for Persistent Fetal Vasculature in an 18-Year-Old Woman: A One-Year Follow-Up. Cureus. 2020. Figure 1. PM
CI D: PMC7584328. License: CC BY.
อัลตราซาวนด์ลูกตาแสดงรอยโรคสะท้อนเสียงสูงคล้ายเส้นที่พาดผ่านแก้วตา และภาพถ่ายส่วนหน้าขณะขยาย
ม่านตา แสดงเนื้อเยื่อเส้นใยหลอดเลือดสีขาวด้านหลัง
รูม่านตา ผลการตรวจเหล่านี้เหมาะสมกับส่วนอาการหลักและผลการตรวจทางคลินิก ซึ่งเป็นลักษณะเฉพาะของเยื่อเส้นใยหลอดเลือดหลังเลนส์และเส้นในแก้วตาใน
PFV PFV แบ่งเป็น 3 ชนิดตามตำแหน่งรอยโรคที่เด่น: ชนิดหน้า, ชนิดหลัง, และชนิดผสม
ชนิดหน้า
ผลการตรวจหลัก : เยื่อเจริญเส้นใยที่ผิวหลังเลนส์ (Mittendorf dot), ต้อกระจก ใต้แคปซูลหลัง, เลนส์รูปกรวยหลัง
ข้อบ่งชี้การรักษา : หากรอยโรคจำกัดอยู่ที่ส่วนหลังของเลนส์และจอประสาทตา ปกติ ก็มีข้อบ่งชี้ในการผ่าตัด
พยากรณ์โรค : ดีที่สุดในสามชนิด ค่ามัธยฐานการมองเห็น 20/100 (54% มีการมองเห็น 20/200 หรือดีกว่า) 1)
ชนิดหลัง
ผลการตรวจหลัก : เส้นจากจานประสาทตา ไปยังแก้วตา, รอยพับจอประสาทตา , จอประสาทตาลอก , จอประสาทตา ผิดปกติ
ข้อบ่งชี้ในการรักษา : หาก ERG /VEP ดี ให้พิจารณาการผ่าตัด ไม่มีการรักษาที่ได้ผลสำหรับจอประสาทตา ผิดปกติ
การพยากรณ์โรค : ไม่ดี ค่ามัธยฐานของการมองเห็น 20/800 (การมองเห็น 20/200 หรือดีกว่า 36%) 1)
ชนิดผสม
ลักษณะสำคัญ : ผสมผสานลักษณะของชนิดหน้าและชนิดหลัง มักมีตาเล็ก (microphthalmos) ร่วมด้วย
ข้อบ่งชี้ในการรักษา : ตัดสินใจอย่างระมัดระวังตามขอบเขตของรอยโรคแต่ละราย
การพยากรณ์โรค : ในชนิดผสมรุนแรง มีเพียง 19% ที่มีการมองเห็น ที่วัดได้ 61% ไม่มีการรับรู้แสง 8)
ชนิด ลักษณะสำคัญ ความผิดปกติที่อาจร่วมด้วย 1. การคงอยู่ของหลอดเลือดแดงไฮยาลอยด์ (หลอดเลือดแก้วตา) เส้นสีขาวถึงเทาจากหัวประสาทตาไปยังกลางแก้วตาส่วนหลัง + จุดมิทเทนดอร์ฟ ต้อกระจก ใต้แคปซูลด้านหลัง, กรวยเลนส์ด้านหลัง2. ชนิดลำตัวหลักของหลอดเลือดแดงไฮยาลอยด์เด่น เส้นหนาโผล่ขึ้นจากหัวประสาทตา การดึงรั้งจอประสาทตา รอบหัวประสาทตา 3. ชนิดจำกัดเฉพาะที่เหนือจานประสาทตา เนื้อเยื่อสีขาวบนจานประสาทตา การดึงรั้งจอประสาทตา ส่วนปลาย 4. รอยพับจอประสาทตา จากจานประสาทตา การดึงรั้งของเนื้อเยื่อเจริญบริเวณรอบนอกของอวัยวะรับภาพ ความผิดปกติของจอประสาทตา ส่วนปลาย 5. ชนิดที่เต็มช่องว่างแก้วตา การเจริญแพร่กระจายเป็นบริเวณกว้าง จอประสาทตาลอก ทั้งหมด จอประสาทตา ผิดรูป ตาลูกเล็กพบได้บ่อย 6. ชนิดที่มีการเจริญของเนื้อเยื่อเส้นใยหลังเลนส์เป็นหลัก จำกัดเฉพาะที่หลังเลนส์ อวัยวะรับภาพเกือบปกติ มีข้อบ่งชี้ในการรักษา 7. ชนิดหน้าต่อเลนส์ การเจริญของเนื้อเยื่อเส้นใยด้านหน้าจากการเจริญของเยื่อหุ้มหลอดเลือดเลนส์ รูม่านตา ผิดรูป ปิด
อาการแสดงที่สำคัญ ได้แก่ ตาเล็กข้างเดียว (microphthalmos) ความขุ่นที่ผิวหลังของเลนส์แก้วตา (Mittendorf spot) ความผิดปกติของแนวเส้นเลือดจอประสาทตา จอประสาทตา ผิดรูป (retinal dysplasia) ซิลิอารีบอดี ที่ยืดยาว และเส้นใยที่ยื่นจากผิวหลังของเลนส์แก้วตา ไปยังหัวประสาทตา เส้นใยนี้สามารถทำให้เกิดการดึงรั้ง นำไปสู่ความดันลูกตาต่ำ ผ่านการยืดของซิลิอารีบอดี จอประสาทตา อาจถูกดึงเข้าไปในเนื้อเยื่อเส้นใยใกล้หัวประสาทตา ความรุนแรงแตกต่างกันไปตามระดับการถดถอยของหลอดเลือดวุ้นตา
ในการศึกษา PED IG พบความผิดปกติของส่วนหลังของตาใน 28% (18/64 ตา) ของต้อกระจก จาก PFV 1) และ 46% ของตาที่มีเลนส์แก้วตาเทียม มีรอยโรคที่ส่วนหลัง (เทียบกับ 28% ในตาที่ไม่มีเลนส์แก้วตา OR ที่ปรับตามอายุ 4.47) 1) การตัดวุ้นตา ส่วนหน้าทำใน 96% ของตา PFV ที่ไม่มีเลนส์แก้วตา ระหว่างการผ่าตัดต้อกระจก 1)
ในชนิดหน้าที่จำกัดอยู่ที่ผิวหลังของเลนส์แก้วตา โดยไม่มีความผิดปกติของจอตา สามารถคาดหวังการมองเห็น ที่ดีขึ้นหลังการผ่าตัด สิ่งสำคัญคือการเพิ่มโอกาสในการรักษาภาวะตาขี้เกียจ ให้สูงสุดผ่านการตรวจพบและการผ่าตัดตั้งแต่เนิ่นๆ
ในการพัฒนาปกติของระบบหลอดเลือดวุ้นตา เซลล์มีเซนไคม์จะเข้าสู่ช่องวุ้นตา จากรอยแยกของคัพภะในสัปดาห์ที่ 5-6 ของการตั้งครรภ์ ก่อตัวเป็นระบบหลอดเลือดวุ้นตา ระบบนี้จะเจริญเต็มที่ในสัปดาห์ที่ 10 จากนั้นการถดถอยจะเริ่มจากส่วนปลาย โดยเฉพาะอย่างยิ่ง การถดถอยเริ่มประมาณสัปดาห์ที่ 13-15 และหายไปในช่วงท้ายของการตั้งครรภ์
ใน PFV เกิดการถดถอยของหลอดเลือดวุ้นตา ที่ไม่สมบูรณ์ ทำให้เกิดความผิดปกติของเนื้อเยื่อรอบหลอดเลือด เชื่อว่าส่งผลให้เกิดความขุ่นของเลนส์แก้วตา จอประสาทตา ผิดรูป และตาเล็ก นอกจากนี้ การดึงรั้งของเนื้อเยื่อที่เหลืออยู่ทำให้ซิลิอารีบอดี ยืดยาวและเกิดรอยพับของจอประสาทตา
PFV ถือเป็นโรคข้างเดียวและไม่ถ่ายทอดทางพันธุกรรม และยังไม่มีการระบุยีนก่อโรคที่จำเพาะ มีเพียง 4-6% ที่มีประวัติครอบครัว 1) และส่วนใหญ่เป็นแบบประปราย ในกรณีที่เป็นสองข้าง การแยกโรคทางพันธุกรรมจาก FEVR (การกลายพันธุ์ของยีน NDP, LRP 5, FZD4) และโรค Norrie (การกลายพันธุ์ของยีน NDP) เป็นสิ่งสำคัญ
ไม่มีความสัมพันธ์ชัดเจนกับน้ำหนักแรกเกิดน้อยหรือการคลอดก่อนกำหนด แต่ในบางกรณีที่พบไม่บ่อย หลอดเลือดวุ้นตา ที่เหลืออยู่มากอาจแสดงลักษณะคล้ายกับจอประสาทตา ในทารกคลอดก่อนกำหนด
อัลตราซาวนด์ (B-scan) : แสดงโครงสร้างคล้ายเส้นจากด้านหลังเลนส์ มีประโยชน์ในการประเมินภาวะลูกตาเล็กและการประเมินช่องวุ้นตา สำคัญอย่างยิ่งเมื่อสื่อโปร่งใสขุ่นมัวจนไม่สามารถมองเห็นขั้วหลังได้โดยตรงซีทีสแกน : ตรวจหาการมีหินปูนในลูกตา เรติโนบลาสโตมามีหินปูน ในขณะที่ PFV ไม่มี ดังนั้นจึงเป็นการตรวจที่มีประโยชน์มากที่สุดในการแยกโรคทั้งสองเอ็มอาร์ไอ : ดีเยี่ยมในการประเมินโครงสร้างคล้ายเส้น ความผิดปกติของส่วนหลัง และการลุกลามของเส้นประสาทตา ERG และ VEP (คลื่นไฟฟ้าจอตาและศักย์ evoked ทางการเห็น)การมองเห็น ก่อนผ่าตัดเพื่อพิจารณาความเหมาะสมของการผ่าตัด
การแยกโรคจากโรคที่ทำให้เกิดม่านตา ขาวเป็นประเด็นสำคัญที่สุด โดยเฉพาะการแยกจากเรติโนบลาสโตมาซึ่งเกี่ยวข้องโดยตรงกับการพยากรณ์โรคเพื่อการอยู่รอด
การแยกจากเรติโนบลาสโตมา
โรคที่ต้องตัดออกเป็นลำดับแรก
PFV มักมีภาวะลูกตาเล็กร่วมด้วย แต่เรติโนบลาสโตมาไม่มี การตรวจหาหินปูนในลูกตาด้วยซีทีสแกนมีประโยชน์ หินปูนเป็นลักษณะเฉพาะของเรติโนบลาสโตมาและไม่พบใน PFV
การแยกจาก FEVR และโรค Norrie
สำคัญในกรณีที่เป็นสองข้าง
ในกรณีจอตาลอกทั้งหมดสองข้างหรือพังผืดหลังเลนส์ ต้องแยกจาก FEVR และโรค Norrie ประวัติครอบครัวและการค้นหาความผิดปกติทางพันธุกรรมมีประโยชน์ การใช้ชุดตรวจ NGS มีประโยชน์
โรค ข้าง ลูกตาเล็ก ถ่ายทอดทางพันธุกรรม หินปูนในซีที ลักษณะเฉพาะ PFV เกือบข้างเดียวเสมอ มี ไม่ถ่ายทอดทางพันธุกรรม ไม่มี เส้นใยหลังเลนส์แก้วตา , เยื่อเส้นใยไปยังหัวประสาทตา เรติโนบลาสโตมา 70% ข้างเดียว ไม่มี การกลายพันธุ์ RB1 (35–45%) มี (ลักษณะเฉพาะ) ก้อนสีขาวนูน, การกระจายในวุ้นตา FEVR สองข้าง ไม่มี มี (FZD4 เป็นต้น) ไม่มี บริเวณจอประสาทตา ส่วนปลายไร้หลอดเลือด, จอประสาทตาลอก แบบดึงรั้ง โรค Norrie สองตา เป็นไปได้ ถ่ายทอดแบบด้อยเชื่อมโยงโครโมโซม X (NDP) ไม่มี เลือดออกในวุ้นตา จอประสาทตาลอก ภาวะบกพร่องทางสติปัญญา จอประสาทตาผิดปกติในทารกคลอดก่อนกำหนด สองตา ไม่มี ไม่มี ไม่มี บริเวณจอประสาทตา ส่วนปลายไร้หลอดเลือด การเจริญของหลอดเลือดผิดปกติ
Q
เมื่อพบรูม่านตาสีขาว โรคใดที่ควรแยกออกเป็นอันดับแรก?
A
เรติโนบลาสโตมา เป็นเนื้องอกร้ายภายในลูกตาที่พบบ่อยที่สุดในเด็ก ต้องแยกออกอย่างรวดเร็วเนื่องจากส่งผลโดยตรงต่อการพยากรณ์โรค PFV มักมีลูกตาเล็ก ในขณะที่เรติโนบลาสโตมามักไม่มีลูกตาเล็ก การตรวจ CT เพื่อหาการกลายเป็นปูนภายในลูกตาเป็นขั้นตอนการแยกโรคที่สำคัญที่สุด หากยืนยันว่ามีการกลายเป็นปูน ให้สงสัยเรติโนบลาสโตมาอย่างมาก และจำเป็นต้องส่งต่อผู้ป่วยไปยังสถานพยาบาลเฉพาะทาง
ความขุ่นของสื่อโปร่งใสได้รับการจัดการเช่นเดียวกับต้อกระจก หากจำกัดอยู่ที่ส่วนหลังของเลนส์และไม่มีสิ่งผิดปกติที่จอตา ให้ทำการตัดเลนส์และตัดเยื่อพังผืดหลอดเลือดที่เจริญผิดปกติตามแนวทางของต้อกระจกแต่กำเนิด หากเส้นใยที่ผิวหลังเลนส์ไม่กระทบต่อแนวสายตาและอยู่เยื้องศูนย์ อาจไม่จำเป็นต้องผ่าตัด หากโรคขยายไปถึงจอตา โดยทั่วไปแล้วไม่ใช่ข้อบ่งชี้ในการผ่าตัด สำหรับจอตาลอกหรือแรงดึง หากการตอบสนองของ ERG /VEP ดี ก็เป็นพื้นฐานสำหรับการผ่าตัด หากมีการเจริญผิดปกติของเลนส์ส่วนหน้าทำให้รูม่านตา ผิดรูปหรือปิด ให้ทำการสร้างรูม่านตา ใหม่
หลังการนำเลนส์ออก ให้ทำการแก้ไขสายตาผิดปกติและรักษาภาวะตาขี้เกียจ เทคนิคการผ่าตัดเป็นไปตามแนวทางของต้อกระจกแต่กำเนิด ในการศึกษา PED IG มีการตัดน้ำวุ้นตา ส่วนหน้าใน 96% ของตา PFV ที่ไม่มีเลนส์ระหว่างการผ่าตัดต้อกระจก 1) และอุบัติการณ์ของความขุ่นของแนวสายตาคือ 18% เมื่อทำการตัดน้ำวุ้นตา ส่วนหน้าในการผ่าตัดครั้งแรก เทียบกับ 60% เมื่อไม่ได้ทำ 1)
หลังผ่าตัด ให้รักษาภาวะตาขี้เกียจ โดยการรวมการแก้ไขสายตาผิดปกติ (คอนแทคเลนส์หรือแว่นตา) และการปิดตาข้างดี (แผ่นปิดตา) ใน PFV ข้างเดียว การปฏิบัติตามการรักษา ภาวะตาขี้เกียจ เป็นตัวกำหนดพยากรณ์โรคทางสายตา การรักษาควรทำอย่างจริงจังในช่วงวิกฤตของการพัฒนาการมองเห็น (ตั้งแต่แรกเกิดจนถึงประมาณ 10 ปี)
ตัวชี้วัด ตา PFV ที่ไม่มีเลนส์ ตา PFV ที่มีเลนส์เทียม อายุขณะผ่าตัด (มัธยฐาน) 2 เดือน 29 เดือน ค่ามัธยฐานการมองเห็น ที่ 5 ปี 20/100 (IQR 20/50–20/320) 20/400 (IQR 20/200–<20/800) การมองเห็น 20/200 หรือดีกว่า59% (ช่วงความเชื่อมั่น 95%: 39–76%) 23% (ช่วงความเชื่อมั่น 95%: 5–54%) การบรรลุการมองเห็น ปกติตามอายุ 10% (ช่วงความเชื่อมั่น 95%: 2–27%) 8% (ช่วงความเชื่อมั่น 95%: 0–36%) เหตุการณ์ไม่พึงประสงค์ที่เกี่ยวข้องกับต้อหิน (สะสม 5 ปี) 24% (ช่วงความเชื่อมั่น 95%: 9–37%) 7% (ช่วงความเชื่อมั่น 95%: 0–20%) ความขุ่นของแนวการมองเห็น 15% (ช่วงความเชื่อมั่น 95%: 5–25%) 45% (ช่วงความเชื่อมั่น 95%: 13–66%) จอประสาทตาลอก 4% (ช่วงความเชื่อมั่น 95%: 0–10%) 7% (ช่วงความเชื่อมั่น 95%: 0–19%)
ในแง่ของผลลัพธ์การมองเห็น โดยรวม จาก 42 ตา มี 4 ตา (10%, ช่วงความเชื่อมั่น 95% 3–23%) ที่บรรลุการมองเห็น ปกติตามอายุ และ 48% (ช่วงความเชื่อมั่น 95% 32–64%) บรรลุการมองเห็น 20/200 หรือดีกว่า 1) อัตราการบรรลุการมองเห็น 20/200 หรือดีกว่าในตา PFV ชนิดมีเลนส์แก้วตาเทียม (23%) แย่กว่าอย่างมีนัยสำคัญเมื่อเทียบกับตาชนิดมีเลนส์แก้วตาเทียม ที่ไม่ใช่ PFV (68%) (อัตราส่วนออดส์ที่ปรับตามอายุ = 0.14, P = 0.005) 1) ตา PFV ชนิดไม่มีเลนส์แก้วตาเทียม มีผลลัพธ์เทียบเท่ากับตาชนิดไม่มีเลนส์แก้วตาเทียม ที่ไม่ใช่ PFV (อัตราส่วนออดส์ที่ปรับตามอายุ = 1.90, P = 0.14) 1)
จำแนกตามชนิด ค่ากลางของการมองเห็น ในชนิดด้านหน้าคือ 20/100 (54% มีการมองเห็น 20/200 หรือดีกว่า) ในขณะที่ชนิดด้านหลัง ค่ากลางของการมองเห็น คือ 20/800 (36% มีการมองเห็น 20/200 หรือดีกว่า) โดยมีความแตกต่าง 4 เส้น logMAR (P = 0.09) 1)
ในรายงานอื่นๆ การศึกษา 20 ปีในสถาบันเดียวโดย Bata และคณะ (ตา PFV ชนิดไม่มีเลนส์แก้วตาเทียม 58 ตา) พบว่า 33% บรรลุการมองเห็น 20/200 หรือดีกว่า (ติดตามเฉลี่ย 6.7 ปี) 4) รายงานของ Anteby และคณะ (ตา PFV ชนิดไม่มีเลนส์แก้วตาเทียม 30 ตา) พบว่า 16.7% บรรลุ 20/200 หรือดีกว่า (ติดตามเฉลี่ย 8.5 ปี) 5) และในผู้ป่วย PFV ชนิดผสมรุนแรง 36 รายของ de Saint Sauveur และคณะ มีเพียง 19% ที่มีการมองเห็น ที่วัดได้ 61% รายงานว่าไม่มีการรับรู้แสง 8)
PFV
ภาวะแทรกซ้อนที่พบบ่อยที่สุดหลังผ่าตัดต้อกระจก PFV คือโรคต้อหิน ซึ่งเกิดขึ้นใน 24% ของตาชนิดไม่มีเลนส์แก้วตาเทียม ภายใน 5 ปี 1) การติดตามความดันลูกตา ระยะยาวเป็นสิ่งจำเป็นไม่ว่าจะผ่าตัดหรือไม่ก็ตาม แม้ในตา PFV ที่ไม่ได้รับการผ่าตัด ความเสี่ยงของโรคต้อหิน ประมาณ 7–15% 9) 10)
ภาวะแทรกซ้อนหลักอื่นๆ นอกเหนือจากโรคต้อหิน ได้แก่ ความขุ่นของแกนการมองเห็น (45% ในตา PFV ชนิดมีเลนส์แก้วตาเทียม , 15% ในตาชนิดไม่มีเลนส์แก้วตาเทียม ) และอัตราการเกิดสะสมของการผ่าตัดเพื่อทำให้แกนการมองเห็น ใสสูงถึง 40% ในตา PFV ชนิดมีเลนส์แก้วตาเทียม 1) นอกจากนี้ 13% ของตา PFV ชนิดไม่มีเลนส์แก้วตาเทียม (ช่วงความเชื่อมั่น 95% 2–22%) จำเป็นต้องผ่าตัดใส่เลนส์แก้วตาเทียม ครั้งที่สองภายใน 5 ปี 1)
ไม่มีการรักษาที่มีประสิทธิภาพสำหรับจอประสาทตา ผิดปกติ ในชนิดด้านหลัง มักไม่สามารถคาดหวังการพัฒนาการมองเห็น ได้ ในกรณีตาลูกเล็กอย่างมีนัยสำคัญ จะมีการใส่ตาเทียม ตั้งแต่เนิ่นๆ เพื่อเหตุผลด้านความสวยงาม การใส่ตาเทียม ยังช่วยส่งเสริมการเจริญเติบโตของเบ้าตา
Q
การผ่าตัด PFV สามารถคาดหวังการมองเห็นได้มากเพียงใด?
A
ในชนิดด้านหน้า (จำกัดอยู่หลังเลนส์) ค่ากลางของการมองเห็น 5 ปีหลังผ่าตัดคือ 20/100 และอัตราการบรรลุการมองเห็น 20/200 หรือดีกว่าคือ 54% 1) อย่างไรก็ตาม มีเพียง 10% ของทั้งหมดที่บรรลุการมองเห็น ปกติตามอายุ ในชนิดด้านหลัง ค่ากลางของการมองเห็น คือ 20/800 ซึ่งแย่ 1) การพยากรณ์การมองเห็น ขึ้นอยู่กับชนิดของโรค การมีรอยโรคของส่วนหลังของลูกตา อายุขณะผ่าตัด และการปฏิบัติตามการรักษา ภาวะตาขี้เกียจ อย่างมาก
Q
ภาวะแทรกซ้อนใดที่ควรระวังมากที่สุดหลังผ่าตัด PFV?
A
ภาวะแทรกซ้อนที่เกี่ยวข้องกับโรคต้อหิน พบได้บ่อยที่สุด โดยมีอัตราการเกิดสะสม 5 ปีสูงถึง 24% ในดวงตาที่ไม่มีเลนส์แก้วตาเทียม ใน PFV 1) การขุ่นของแนวแกนสายตาก็เป็นภาวะแทรกซ้อนที่สำคัญ โดยเกิดขึ้นใน 45% ของดวงตาที่มีเลนส์แก้วตาเทียม 1) การทำ vitrectomy ส่วนหน้าในการผ่าตัดครั้งแรกมีความสำคัญในการป้องกันการขุ่นของแนวแกนสายตา (18% เมื่อทำเทียบกับ 60% เมื่อไม่ทำ) 1) หลังการผ่าตัด จำเป็นต้องมีการติดตามความดันลูกตา อย่างสม่ำเสมอในระยะยาว การประเมินแนวแกนสายตา และการแก้ไขค่าสายตา
ในสัปดาห์ที่ 5-6 ของการตั้งครรภ์ เซลล์มีเซนไคม์จะเข้าสู่ช่องวุ้นตา ผ่านรอยแยกของแก้วตา (optic fissure) ก่อตัวเป็นระบบหลอดเลือดวุ้นตา ซึ่งประกอบด้วยหลอดเลือดแดงไฮยาลอยด์ (hyaloid artery) และทูนิกา วาสคูโลซา เลนทิส (tunica vasculosa lentis) ระบบหลอดเลือดนี้มีบทบาทสำคัญในการให้ออกซิเจนและสารอาหารแก่เลนส์ที่กำลังพัฒนาและส่วนหน้าของลูกตา
การพัฒนาสูงสุดเกิดขึ้นในสัปดาห์ที่ 10 ของการตั้งครรภ์ หลังจากนั้นการถดถอยจะเริ่มจากส่วนปลาย การถดถอยที่แท้จริงเริ่มตั้งแต่สัปดาห์ที่ 13-15 ของการตั้งครรภ์ และเกือบจะหายไปในช่วงท้ายของการตั้งครรภ์ ในการคลอดปกติ ระบบหลอดเลือดวุ้นตา แทบจะไม่เห็น แต่จุด Mittendorf (จุดสีขาวเล็กๆ บนผิวด้านหลังของเลนส์) อาจยังคงอยู่เป็นร่องรอย
ใน PFV เกิดความล้มเหลวในการถดถอยของหลอดเลือดวุ้นตา ทำให้เกิดความผิดปกติในการพัฒนาเนื้อเยื่อเส้นใยที่มีการเจริญ proliferative รอบหลอดเลือด เนื้อเยื่อมีเซนไคม์ที่เหลืออยู่รอบหลอดเลือดจะเจริญ proliferative และเกิดพังผืด ทำให้เกิดอาการทางคลินิกต่างๆ
ผลที่ตามมาโดยเฉพาะมีดังนี้:
เลนส์ขุ่น (ต้อกระจก ใต้แคปซูลด้านหลัง, เลนส์รูปกรวยด้านหลัง): การยึดเกาะของเนื้อเยื่อเส้นใยที่เหลือกับผิวด้านหลังของเลนส์
ลูกตาเล็ก (microphthalmia): ความผิดปกติของการพัฒนาเนื้อเยื่อรอบหลอดเลือดทำให้การเจริญเติบโตของลูกตาทั้งหมดช้าลง
จอประสาทตา ผิดปกติ (retinal dysplasia): ในชนิดหลัง เกิดจอประสาทตา ผิดปกติเนื่องจากการดึงรั้งและขาดเลือดซิลิอารีบอดี ้ยาวและความดันลูกตาต่ำ : เนื่องจากการดึงรั้งโดยเส้นใยจอประสาทตา พับ (retinal fold): การเสียรูปเนื่องจากการดึงรั้งของเนื้อเยื่อพยาธิสภาพด้านหลัง
สาเหตุที่ PFV เป็นข้างเดียวและไม่ถ่ายทอดทางพันธุกรรม เนื่องจากการถดถอยของหลอดเลือดวุ้นตา ของทารกในครรภ์ถูกควบคุมโดยสัญญาณการสร้างหลอดเลือดและการถดถอยเฉพาะที่ และสันนิษฐานว่าเกิดความผิดปกติในกลไกการควบคุมนี้เพียงข้างเดียว อย่างไรก็ตาม กลไกระดับโมเลกุลที่แน่ชัดยังไม่เป็นที่ทราบ
ยังไม่มีการระบุยีนก่อโรคเฉพาะของ PFV แต่ในแบบจำลองสัตว์มีรายงานว่าการกลายพันธุ์ในยีนที่เกี่ยวข้องกับวิถีสัญญาณ Wnt เช่น FZD4, LRP 5 และ NDP แสดงฟีโนไทป์คล้าย PFV (การคงอยู่ของหลอดเลือดแก้วตา) ยีนเหล่านี้ยังเป็นสาเหตุของ FEVR และโรค Norrie ซึ่งบ่งชี้ถึงความต่อเนื่องทางพันธุกรรมระหว่าง PFV และโรคที่เกี่ยวข้อง การตรวจแผงการหาลำดับรุ่นใหม่ (NGS) ก็มีความก้าวหน้าในการประยุกต์ใช้ทางคลินิกเพื่อการวินิจฉัยแยกโรค PFV
กำลังมีการทดลองวิธีการเข้าถึง PFV ชนิดหลังโดยใช้การผ่าตัดแก้วตาแบบแผลเล็กมาก (MIVS) ด้วยเข็มขนาด 25 และ 27 เกจ การผ่าตัดแผลเล็กในทารกแรกเกิดและทารกมีข้อดีคือลดการบาดเจ็บและลดการอักเสบหลังผ่าตัด 11)
การเปรียบเทียบผลลัพธ์ระยะยาวระหว่างการใส่ IOL ระยะแรกในวัยทารกกับการใส่ IOL ระยะที่สองหลังการจัดการภาวะไม่มีเลนส์ตาเป็นประเด็นสำคัญในการวิจัย PFV ข้อมูลการติดตามผลระยะยาวจากการศึกษา PED IG คาดว่าจะช่วยกำหนดเกณฑ์บ่งชี้การใส่ IOL เฉพาะสำหรับ PFV 6) 7)
การประเมิน PFV แบบไม่รุกล้ำด้วยกล้องถ่ายภาพจอประสาทตามุมกว้าง และ OCT ส่วนหน้าดำเนินไปอย่างก้าวหน้า โดยเฉพาะ OCT ส่วนหน้ามีประโยชน์ในการประเมินสัณฐานของกรวยเลนส์ตาด้านหลังและต้อกระจก ใต้แคปซูลด้านหลัง รวมถึงการวางแผนก่อนผ่าตัด
Haider KM, Repka MX, Sutherland DR, et al. Outcomes and complications 5 years after surgery for pediatric cataract associated with persistent fetal vasculature. Am J Ophthalmol. 2024;(online ahead of print).
Wilson ME, Trivedi RH, Morrison DG, et al. The Infant Aphakia Treatment Study: evaluation of cataract morphology in eyes with monocular cataracts. J AAPOS. 2011;15(5):421-426.
Solebo AL, Russell-Eggitt I, Cumberland P, Rahi JS. Congenital cataract associated with persistent fetal vasculature: findings from IoLunder2. Eye (Lond). 2016;30(9):1204-1209.
Bata BM, Chiu HH, Mireskandari K, Ali A, Lam WC, Wan MJ. Long-term visual and anatomic outcomes following early surgery for persistent fetal vasculature: a single-center, 20-year review. J AAPOS. 2019;23(6):327.e1-327.e5.
Anteby I, Cohen E, Karshai I, BenEzra D. Unilateral persistent hyperplastic primary vitreous: course and outcome. J AAPOS. 2002;6(2):92-99.
Repka MX, Dean TW, Lazar EL, et al. Cataract surgery in children from birth to less than 13 years of age: baseline characteristics of the cohort. Ophthalmology. 2016;123(12):2462-2473.
Pediatric Eye Disease Investigator Group. Visual acuity and ophthalmic outcomes 5 years after cataract surgery among children younger than 13 years. JAMA Ophthalmol. 2022;140(3):269-276.
de Saint Sauveur G, Chapron T, Abdelmassih Y, et al. Management and outcomes of posterior persistent fetal vasculature. Ophthalmology. 2023;130(8):844-853.
Khandwala N, Besirli C, Bohnsack BL. Outcomes and surgical management of persistent fetal vasculature. BMJ Open Ophthalmol. 2021;6(1):e000656.
Hunt A, Rowe N, Lam A, Martin F. Outcomes in persistent hyperplastic primary vitreous. Br J Ophthalmol. 2005;89(7):859-863.
Bata BM, Khalili S, Ali A, Wan MJ, Mireskandari K. Late surgery for unilateral persistent fetal vasculature: long-term visual and anatomic outcomes. J AAPOS. 2022;26(6):296.e1-296.e5.
Goldberg MF. Persistent fetal vasculature (PFV ): an integrated interpretation of signs and symptoms associated with persistent hyperplastic primary vitreous (PHPV ). Am J Ophthalmol. 1997;124(5):587-626.