顺应型
定义:光感受器外节与RPE(视网膜色素上皮)之间无分离的类型。
特征:凹陷内光感受器与RPE紧密贴合一起下沉。通常病程相对稳定。
OCT表现:凹陷处的RPE和光感受器层整体向脉络膜侧移位。

局限性脉络膜凹陷(Focal Choroidal Excavation; FCE)是一种通过光学相干断层扫描(OCT)检测到的脉络膜局限性凹陷性改变。其特点是不伴有后巩膜葡萄肿或巩膜扩张。2006年由Jampol首次报道,2011年由Margolis等人命名。
FCE的形态大致分为两型。
顺应型
定义:光感受器外节与RPE(视网膜色素上皮)之间无分离的类型。
特征:凹陷内光感受器与RPE紧密贴合一起下沉。通常病程相对稳定。
OCT表现:凹陷处的RPE和光感受器层整体向脉络膜侧移位。
非适应型
定义:光感受器外节与RPE之间存在间隙(视网膜下液或高反射物质)的类型。
特征:合并黄斑新生血管(脉络膜新生血管)和浆液性视网膜脱离的风险较高。
OCT表现:凹陷内的RPE与光感受器层之间可见液体潴留或高反射物质。
也采用按形状分类(圆锥型、碗型、混合型)和按部位分类(中心窝型、中心窝外型)。
Capellan等人根据病因将FCE分为3型:1型(近视性)、2型(先天性)和3型(获得性/炎症性)。3型中CNV(脉络膜新生血管)合并率高达40%7)。
40岁以下人群的患病率为0.18%(1697只眼中3只眼)1)。中心性浆液性脉络膜视网膜病变(CSC)患者中FCE的患病率为2.8%~7.8%,高于一般人群1)。随着OCT检查的普及,检出例数正在增加。
近年来,FCE有被排除在厚脉络膜疾病谱之外的趋势。它被认为是炎症导致Bruch膜缺损和局限性脉络膜变薄的结果,是一种独立的病理状态8)。
多数无症状,在OCT检查时偶然发现。有症状病例表现为以下情况。
在32例FCE系列中,60%至77%的患者主诉某种视觉障碍。
无症状且不伴有黄斑新生血管或浆液性视网膜脱离时,基本以观察为主。但由于存在合并黄斑新生血管的风险,建议定期进行OCT和OCTA检查监测(详见“标准治疗方法”章节)。
FCE的发病机制尚未完全阐明,目前提出了多种假说。
与FCE相关的主要疾病和风险因素如下所示。
| 类别 | 疾病/因素 | 备注 |
|---|---|---|
| 遗传性眼病 | Best病 | 6%合并FCE3) |
| 遗传性眼病 | ABCA4相关视网膜病变 | 进行性加深的报告7) |
| 全身性疾病 | Alagille综合征 | JAG1基因突变6) |
| 脉络膜疾病 | 中心性浆液性脉络膜视网膜病变/息肉状脉络膜血管病变 | 患病率2.8%~7.8%1) |
| 生活习惯 | 吸烟 | 氧化应激→Bruch膜缺损4) |
其他风险因素包括近视、女性和亚洲人种。双眼发病在18例中有7例(38.89%)1)。
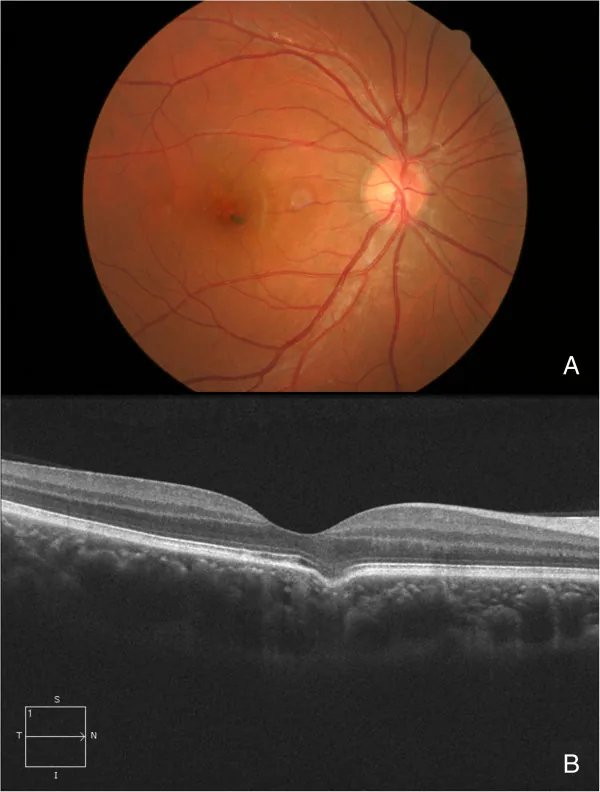
OCT对于诊断FCE不可或缺。通过结合以下检查进行诊断和评估。
OCT
作用:诊断的金标准。
所见:脉络膜的局限性凹陷。可区分适合型和非适合型。同时测量形状(圆锥型、碗型、混合型)和深度。
OCTA
作用:无创检测黄斑新生血管。无需造影剂即可诊断2)。
所见:FCE区域的脉络膜毛细血管层出现暗区血流信号缺失。合并黄斑新生血管时,可见花环状新生血管网2)。
荧光素眼底血管造影(FA)与吲哚青绿血管造影(ICGA)
其他辅助检查包括FAF(评估RPE健康状况)和B型超声(用于与后巩膜葡萄肿鉴别)。
与以下疾病的鉴别诊断很重要。
对于无症状、不伴有黄斑新生血管或浆液性视网膜脱离的病例,定期随访是基本方针。建议终身进行OCT和OCTA监测1)。
在一例FCE合并CSC的双眼病例中,采用局灶激光(光斑大小50μm,功率70mW,照射时间0.1秒)与SML(阈下微脉冲激光)联合治疗,5个月后浆液性视网膜脱离消失1)。
合并黄斑新生血管的病例,抗VEGF治疗是一线选择。主要治疗结果如下所示。
| 报告 | 药物 | 治疗结果 |
|---|---|---|
| Duke 20252) | 贝伐珠单抗 1.25mg/0.05mL | 3次给药后20/40→20/20 |
| Sato 20214) | 阿柏西普 每月1次×3个月 | CNV消失+FCE消失,12个月无复发 |
| 文献汇总4) | 抗VEGF总体 | 76眼中54眼(71%)显示良好的解剖学反应 |
Duke RCT等人(2025)报告了一例30岁女性中心凹下黄斑新生血管合并FCE的病例,给予贝伐珠单抗三次注射后,OCTA上花网状黄斑新生血管消退,BCVA从20/40改善至20/202)。
Sato等人(2021)报告了一例每月注射阿柏西普三次后CNV消失且FCE本身也消失的病例4)。随访12个月未见CNV和FCE复发。推测FCE消失是由于抗VEGF治疗后纤维血管瘢痕桥接了Bruch膜缺损处。
抗VEGF治疗有效,据报道76只眼中54只眼(71%)获得了良好的解剖学反应4)。部分病例中FCE本身也可能消失4)。但由于存在复发风险,治疗后仍需持续监测。
目前最受支持的是Bruch膜缺损假说。在Bruch膜脆弱或缺损的部位,由于眼内压(IOP)的作用,RPE-Bruch膜复合体的外层向外突出。内界膜(ILM)不发生移位。这与OCT观察到的FCE形态特征一致4)。
Benson等人(2022)在ABCA4相关视网膜病变患者中通过8年连续OCT记录了以下过程7)。
这一观察是适应型和非适应型存在于一个谱系中并可逐步进展的直接证据7)。
OCTA分析显示,FCE区域的脉络膜毛细血管层存在暗流信号空白区1)。这表明FCE部位的脉络膜毛细血管血流减少,局部缺血可能导致炎症、Bruch膜脆弱化和黄斑新生血管形成2)。
推测的路径为:脉络膜凹陷→局部脉络膜变薄→缺血/慢性炎症→Bruch膜脆弱化→黄斑新生血管2)。在3型FCE中,CNV合并率据报道可达40%7),因此FCE的分型对临床风险评估很重要。
Alagille综合征(AGS)是一种由JAG1基因突变(超过97%)引起的多器官疾病。在Notch信号通路异常导致的脉络膜视网膜萎缩背景下,已有报道FCE和黄斑裂孔合并发生6)。
传统上,FCE有时被归入厚脉络膜疾病谱,但近年的大规模综述推动了重新分类。Cheung等人(2024)提出将FCE从厚脉络膜疾病谱中排除,并将其定位为以炎症性Bruch膜缺损和局部脉络膜变薄为病因的独立病理状态8)。
Benson等人通过连续OCT对ABCA4相关视网膜病变中的FCE进行了8年追踪,并首次记录了顺应型FCE转变为非顺应型FCE并最终发展为黄斑裂孔的自然病程7)。这一观察对于理解FCE的进展具有重要意义。
据报道,结合OCTA(光学相干断层血管成像)和SD-OCT(频域OCT)可以在不使用造影剂(荧光素、ICGA)的情况下诊断FCE合并黄斑新生血管2)。这可能减少对有创造影检查的依赖。
Sato等人(2021年)首次报告了阿柏西普给药后FCE本身消失的病例4)。推测纤维血管瘢痕对Bruch膜缺损的桥接是FCE消失的机制,表明抗VEGF治疗也可能影响FCE的形态变化。
Capellan等人的三型分类(1型:近视性,2型:先天性,3型:获得性/炎症性)作为风险评估和治疗决策的有用框架受到关注7)。期待未来前瞻性大规模研究的验证。
大多数FCE病程稳定,但长期随访中黄斑新生血管的发生率约为16%2)。在伴有ABCA4相关视网膜病变等进行性视网膜变性的病例中,有报告显示从适应型逐步加深至非适应型,最终导致黄斑裂孔7)。建议终身监测1)。