FES

阻塞性睡眠呼吸暂停综合征的眼科体征
一目了然的要点
Section titled “一目了然的要点”1. 阻塞性睡眠呼吸暂停综合征的眼部体征
Section titled “1. 阻塞性睡眠呼吸暂停综合征的眼部体征”阻塞性睡眠呼吸暂停综合征(OSA)是一种常见的睡眠障碍,睡眠期间上气道反复部分或完全阻塞。阻塞导致低氧血症和再氧合循环反复发生,对全身产生多种影响。
**呼吸暂停低通气指数(AHI)**指每小时睡眠中呼吸暂停和低通气事件的数量。OSA定义为AHI >5且伴有日间嗜睡、疲劳或认知功能障碍。呼吸暂停指气流完全停止至少10秒,低通气指气流相对减少并伴有低氧血症或觉醒。
患病率男性为3-7%,女性为2-5%,但美国队列报告男性为17-31%,女性为6.5-9%。65岁以上人群患病率增加2-3倍。儿童中常见于扁桃体和腺样体肥大,非裔美国人中发病率较高。
OSA被认为是眼病的独立危险因素,已有报道其与六种疾病相关:眼睑松弛综合征、青光眼、非动脉炎性前部缺血性视神经病变、视乳头水肿、圆锥角膜和中心性浆液性脉络膜视网膜病变(Huon 2016 [PMID 27230013], Bulloch 2024 [PMID 37227479])。参与OSA患者诊疗的眼科医生应牢记这些并发症。
与OSA相关的主要眼科并发症有六种:眼睑松弛综合征、青光眼、非动脉炎性前部缺血性视神经病变(NAION)、视乳头水肿、圆锥角膜和中心性浆液性脉络膜视网膜病变。间歇性缺氧、交感神经过度刺激和氧化应激是共同的病理生理机制。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”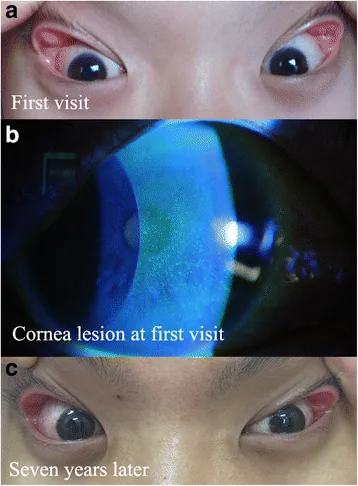
自觉症状(OSA的全身症状)
Section titled “自觉症状(OSA的全身症状)”OSA的症状通常隐匿起病,患者往往在数年后才就医。体重增加、衰老和绝经会使其加重。
日间症状:
- 嗜睡:影响日常生活的困倦
- 晨起头痛:早晨出现的头痛
- 口干和过敏:与睡眠碎片化相关的症状
- 健忘和抑郁:对认知功能和情绪的影响
夜间症状:
- 打鼾:上气道狭窄引起的振动声
- 窒息感、喘息或鼻音:气道阻塞的觉醒反应
- 失眠和夜尿:由于睡眠碎片化
临床所见(眼科体征)
Section titled “临床所见(眼科体征)”与OSA相关的眼科并发症如下所示。
非动脉炎性前部缺血性视神经病变
青光眼和视盘水肿
青光眼:OSA患者患病率为2%~27%。夜间眼压升高和缺氧后的氧化应激参与其中。
视盘水肿:因颅内压升高导致的双侧视盘肿胀。对于无特发性颅内压增高症危险因素的患者,应考虑OSA的鉴别诊断(Thurtell 2013 [PMID 23412355])。
角膜和视网膜
圆锥角膜:圆锥角膜患者的OSA患病率高于一般人群,荟萃分析显示存在显著关联(Pellegrini 2020 [PMID 31895272])。多见于高BMI或有OSA家族史的男性。睡眠中对角膜的机械性损伤被认为是原因之一。
中心性浆液性脉络膜视网膜病变(CSCR):约三分之二的CSCR患者合并OSA。氧化应激导致的血管内皮损伤和血管收缩参与其中。
受影响的眼睛往往与患者通常睡觉时朝向的一侧一致。侧卧时,下方的眼睑受到枕头或寝具的压迫,产生机械刺激,导致该侧的眼表症状更为明显。
3. 原因和风险因素
Section titled “3. 原因和风险因素”OSA的风险因素
Section titled “OSA的风险因素”以下列出OSA发病的主要风险因素。
- 肥胖:最重要的风险因素。体重增加10%会使OSA发病风险升高6倍。
- 男性:男性患病率高于女性。
- 高龄:65岁以上人群患病率增加2~3倍。
- 解剖因素:扁桃体/舌体肥大、下颌后缩、舌骨下移。
- 咽周脂肪堆积:肺容量减少→咽部塌陷性增加
- 儿童:常见于伴有扁桃体和腺样体肥大的病例
- 种族:非裔美国人中更常见
全身相关疾病
Section titled “全身相关疾病”OSA还与以下全身疾病相关:高血压、代谢综合征、糖尿病、心力衰竭、冠状动脉疾病、心律失常、中风、肺动脉高压、神经认知障碍和情绪障碍。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”OSA的诊断标准
Section titled “OSA的诊断标准”通过以下A至C进行诊断。满足A或B且C时确诊。无论症状如何,AHI ≥15/小时也确诊。
- A:无法用其他因素解释的日间过度嗜睡
- B:以下两项或以上:睡眠中窒息或喘气、反复觉醒、缺乏熟睡感、日间疲劳、注意力下降
- C:每小时睡眠出现5次或以上阻塞性呼吸事件
严重程度分级
Section titled “严重程度分级”基于AHI的严重程度分级如下。
| 严重程度 | AHI(次/小时) |
|---|---|
| 轻度 | 5~14 |
| 中度 | 15~29 |
| 重度 | ≥30 |
- STOP-Bang问卷(SBQ):8个项目:打鼾、疲劳、观察到的呼吸暂停、高血压、BMI、年龄、颈围、性别
- Epworth嗜睡量表(ESS):日间嗜睡的定量评估。FES患者评分>10时,需进行整夜PSG
- 柏林问卷:从3个类别评估:打鼾、日间嗜睡、高血压、肥胖
整夜多导睡眠监测(PSG)是金标准。虽然存在便携式简易睡眠检测设备,但最终确诊仍推荐PSG。
眼科医生筛查的作用
Section titled “眼科医生筛查的作用”- 建议FES患者进行整夜PSG
- 对OSA患者进行全面眼科检查时积极筛查FES
- 临床检查眼睑是否容易翻转是FES诊断的关键
- 在非动脉炎性前部缺血性视神经病变患者的问诊中,需确认血管风险因素、手术史、吸烟史、用药史(如PDE5抑制剂)、OSA症状及巨细胞动脉炎症状。
确诊的金标准是整夜多导睡眠监测(PSG)。门诊筛查可使用STOP-Bang问卷、Epworth嗜睡量表和柏林问卷。FES患者ESS评分>10时推荐进行PSG。
5. 标准治疗方法
Section titled “5. 标准治疗方法”OSA本身的治疗
Section titled “OSA本身的治疗”OSA治疗有助于从根本上管理眼科并发症。
- 减重:最基本的治疗。体重减轻可改善AHI。
- CPAP(持续气道正压通气)疗法:防止睡眠中气道塌陷。OSA的一线治疗,有效减轻症状和并发症。
- 口腔矫治器(牙套):适用于轻度OSA或不能耐受CPAP的患者。通过前移下颌或固定舌体扩大气道。
- 手术治疗:适用于颅面畸形或明确阻塞性病变。
- 舌下神经电刺激疗法(HSN):适用于内科治疗无效的患者。据报道可降低AHI和ESS评分,改善觉醒水平。
- 侧卧位睡眠:通过改变体位的保守治疗。
FES的治疗
Section titled “FES的治疗”- 眼科护理:使用人工泪液和眼膏滴眼
- 眼睑胶带/眼罩:防止睡眠时眼睑外翻
- 避免侧卧和俯卧:指导患者不要患侧朝下睡觉
- 抗炎眼药水:仅在眼表炎症严重时短期使用
- CPAP疗法:McNab报告称,开始CPAP治疗后,乳头状结膜炎消失,眼睑松弛恢复正常。中重度OSA患者使用CPAP 18个月后,FES分级、OSDI评分(干眼症状)、泪液功能检查(TBUT、Schirmer I)和角膜荧光素染色均有统计学显著改善。
适用于保守治疗和CPAP无效的病例。
- 外侧睑板条固定术(LTS):70例中报告91%症状改善,97.5%长期稳定。
- 全层楔形切除术(FTWE):FTWE的复发率往往高于LTS。
- Moorfields眼科医院的长期研究(71例)显示复发率为25.6–60.6%,内、外眼角缝合术和LTS的生存结果优于FTWE。
非动脉炎性前部缺血性视神经病变的预防性管理
Section titled “非动脉炎性前部缺血性视神经病变的预防性管理”- 识别并管理可改变的风险因素(高血压、糖尿病、高脂血症、OSAS)
- 建议戒烟、减重和运动
- 避免睡前服用夜间降压药(夜间低血压是非动脉炎性前部缺血性视神经病变的易感因素)
- 指导患者避免患侧卧位
- 如果眼压处于临界或升高状态,考虑降眼压治疗
- 确认PDE5抑制剂使用史(与非动脉炎性前部缺血性视神经病变风险相关)
- 谨慎进行玻璃体内注射(急剧的眼压升高可能导致ONH循环障碍,增加对侧眼非动脉炎性前部缺血性视神经病变的风险)
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”OSA的上气道阻塞机制
Section titled “OSA的上气道阻塞机制”OSA的阻塞由解剖因素和神经肌肉因素的相互作用引起。
- 解剖因素:扁桃体及舌体肥大、下颌后缩、舌骨下移
- 神经肌肉因素:睡眠期间咽部扩张肌活动减少
- 肥胖的影响:咽周脂肪堆积→肺容量减少→咽部塌陷性增加
全身性方面,血氧饱和度变化激活交感神经系统,导致血压升高、胰岛素抵抗、心律失常、血管内皮功能障碍、全身炎症标志物升高和血小板聚集增强。
眼科并发症的主要机制
Section titled “眼科并发症的主要机制”OSA引起眼科并发症的主要途径有以下四种。
- 间歇性低氧:反复的血氧饱和度降低和再氧合导致组织损伤
- 交感神经过度刺激:对眼压升高和视神经血流的影响
- 氧化应激:再氧合时自由基产生导致的血管内皮损伤
- 内皮素-1(ET-1)的有害作用:具有强烈血管收缩作用的肽过度产生
FES的病理生理学
Section titled “FES的病理生理学”关于FES的发病机制有多种假说。
机械理论:侧卧睡眠时眼睑内翻,眼表面与枕头或寝具直接接触。醒来时症状最严重支持这一理论。
局部缺血-再灌注理论(Culbertson & Tseng):提出了侧卧位或俯卧位时眼睑压迫缺血,加上OSA导致的全身间歇性低氧,体位改变或觉醒时再灌注,引起氧化应激和自由基损伤,结缔组织变性,最终导致眼睑松弛的机制。
高瘦素血症与基质金属蛋白酶(MMPs):与OSA严重程度相关的高瘦素血症以剂量依赖性方式调节MMP-9的表达。MMP-7和MMP-9的升高参与睑板细胞外基质的变性。组织学上可见睑板弹性蛋白含量降低和胶原变性。
非动脉炎性前部缺血性视神经病变的病理生理
Section titled “非动脉炎性前部缺血性视神经病变的病理生理”非动脉炎性前部缺血性视神经病变被认为同时涉及以下三种机制。
- 一过性低氧:呼吸暂停事件导致的视神经乳头(ONH)缺血
- 血流自动调节障碍:ONH血流自动调节能力下降
- 颅内压升高:呼吸暂停发作期间ICP升高→视神经乳头水平灌注压降低
青光眼与CSCR的病理生理
Section titled “青光眼与CSCR的病理生理”青光眼:血管因素(缺氧后再灌注时的氧化应激)和机械因素(交感神经紧张亢进导致的夜间眼压升高)均参与其中。
CSCR:氧化应激增加导致血管内皮损伤和血管收缩,引起脉络膜循环障碍。肥胖可能作为共同风险因素参与其中。
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”舌下神经电刺激疗法(HSN)
Section titled “舌下神经电刺激疗法(HSN)”作为药物治疗无效患者的新选择,相关研究正在推进中。
目前的报告显示,HSN疗法可降低AHI和ESS评分,改善觉醒水平,缩短入睡后觉醒时间。正在考虑将其用于不耐受CPAP的中重度OSA患者。
OSA手术与FES的关系
Section titled “OSA手术与FES的关系”Bayir等人报告,在轻至中度OSA患者接受前腭成形术后,术后3个月FES患病率和分级显著降低,氧饱和度指数也有所改善。这一发现提示OSA本身的外科治疗可能改善FES。
CPAP与非动脉炎性前部缺血性视神经病变发病风险
Section titled “CPAP与非动脉炎性前部缺血性视神经病变发病风险”CPAP治疗是否能降低非动脉炎性前部缺血性视神经病变的首发或对侧眼发病风险目前尚未确定。关于OSA管理与非动脉炎性前部缺血性视神经病变预防的关系,需要进一步积累证据。
视神经鞘减压术
Section titled “视神经鞘减压术”Sergott等人(1989)报告,在“进行性”非动脉炎性前部缺血性视神经病变病例中,通过在视神经周围组织上开窗或切口以引流脑脊液并解除间隔综合征的视神经鞘减压术,可能带来视力改善的可能性。然而,该手术尚未确立为标准治疗,仍处于研究阶段。
8. 参考文献
Section titled “8. 参考文献”本記事は以下の文献を参考に作成した(いずれもPubMed/PMCで実在を確認済み)。
- Farahvash A, Micieli JA. Neuro-Ophthalmological Manifestations of Obstructive Sleep Apnea: Current Perspectives. Eye Brain. 2020;12:61-71. doi:10.2147/EB.S247121. PMID: 32753994; PMCID: PMC7353992.
- Bulloch G, Seth I, Zhu Z, Sukumar S, McNab A. Ocular manifestations of obstructive sleep apnea: a systematic review and meta-analysis. Graefes Arch Clin Exp Ophthalmol. 2024;262(1):19-32. doi:10.1007/s00417-023-06103-3. PMID: 37227479; PMCID: PMC10806133.
- Huon LK, Liu SY, Camacho M, Guilleminault C. The association between ophthalmologic diseases and obstructive sleep apnea: a systematic review and meta-analysis. Sleep Breath. 2016;20(4):1145-1154. doi:10.1007/s11325-016-1358-4. PMID: 27230013.
- Cheong AJY, Ho OTW, Wang SKX, et al. Association between obstructive sleep apnea and floppy eyelid syndrome: A systematic review and meta-analysis. Surv Ophthalmol. 2023;68(2):257-264. doi:10.1016/j.survophthal.2022.11.006. PMID: 36427560.
- Cristescu Teodor R, Mihaltan FD. Eyelid laxity and sleep apnea syndrome: a review. Rom J Ophthalmol. 2019;63(1):2-9. PMID: 31198891; PMCID: PMC6531778.
- Pellegrini M, Bernabei F, Friehmann A, Giannaccare G. Obstructive Sleep Apnea and Keratoconus: A Systematic Review and Meta-analysis. Optom Vis Sci. 2020;97(1):9-14. doi:10.1097/OPX.0000000000001467. PMID: 31895272.
- Thurtell MJ, Trotti LM, Bixler EO, et al. Obstructive sleep apnea in idiopathic intracranial hypertension: comparison with matched population data. J Neurol. 2013;260(7):1748-1751. doi:10.1007/s00415-013-6858-6. PMID: 23412355; PMCID: PMC3707935.
