FES

阻塞性睡眠呼吸暫停症候群的眼科徵候
一目瞭然的要點
Section titled “一目瞭然的要點”1. 阻塞性睡眠呼吸中止症候群的眼科徵兆
Section titled “1. 阻塞性睡眠呼吸中止症候群的眼科徵兆”阻塞性睡眠呼吸中止症候群(OSA)是一種常見的睡眠障礙,睡眠期間上呼吸道反覆部分或完全阻塞。阻塞導致低血氧症和再氧合循環反覆發生,對全身產生多種影響。
**呼吸中止低通氣指數(AHI)**指每小時睡眠中呼吸中止和低通氣事件的次數。OSA定義為AHI >5且伴有日間嗜睡、疲勞或認知功能障礙。呼吸中止指氣流完全停止至少10秒,低通氣指氣流相對減少並伴有低血氧症或覺醒。
盛行率男性為3-7%,女性為2-5%,但美國隊列報告男性為17-31%,女性為6.5-9%。65歲以上族群盛行率增加2-3倍。兒童中常見於扁桃體和腺樣體肥大,非裔美國人中發生率較高。
OSA被認為是眼疾的獨立風險因子,已有報告指出其與六種疾病相關:眼瞼鬆弛症候群、青光眼、非動脈炎性前部缺血性視神經病變、視乳頭水腫、圓錐角膜和中心性漿液性脈絡膜視網膜病變(Huon 2016 [PMID 27230013], Bulloch 2024 [PMID 37227479])。參與OSA患者診療的眼科醫師應牢記這些併發症。
2. 主要症狀與臨床所見
Section titled “2. 主要症狀與臨床所見”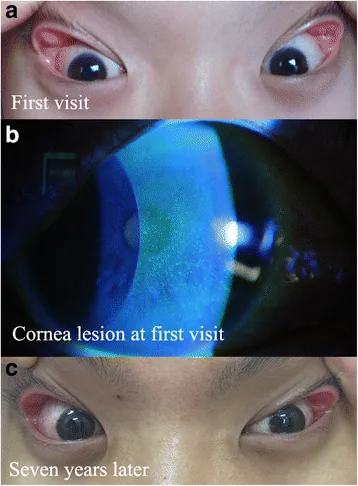
自覺症狀(OSA的全身症狀)
Section titled “自覺症狀(OSA的全身症狀)”OSA的症狀通常隱匿發生,患者往往在數年後才就醫。體重增加、老化及停經會使其惡化。
日間症狀:
- 嗜睡:影響日常生活的睏倦
- 晨起頭痛:早晨出現的頭痛
- 口乾和過敏:與睡眠片段化相關的症狀
- 健忘與憂鬱:對認知功能與情緒的影響
夜間症狀:
- 打鼾:上呼吸道狹窄引起的振動聲
- 窒息感、喘息或鼻音:氣道阻塞的甦醒反應
- 失眠與夜尿:因睡眠片段化所致
臨床所見(眼科徵象)
Section titled “臨床所見(眼科徵象)”與OSA相關的眼科併發症如下所示。
非動脈炎性前部缺血性視神經病變
非動脈炎性前部缺血性視神經病變:表現為突然無痛性單眼視力下降、視神經盤水腫和RAPD(相對性傳入性瞳孔缺陷)。
關聯強度:OSA患者發生非動脈炎性前部缺血性視神經病變的風險高16%。71%~89%的非動脈炎性前部缺血性視神經病變患者合併OSA。OSA使非動脈炎性前部缺血性視神經病變風險增加1.7~3.8倍(Farahvash 2020 [PMID 32753994])。
對側眼風險:合併OSA的病例中,對側眼發生非動脈炎性前部缺血性視神經病變的風險也升高。
青光眼和視神經盤水腫
青光眼:OSA患者患病率為2%~27%。夜間眼壓升高和缺氧後的氧化壓力參與其中。
視神經盤水腫:因顱內壓升高導致的雙側視神經盤腫脹。對於無特發性顱內壓增高症危險因素的患者,應考慮OSA的鑑別診斷(Thurtell 2013 [PMID 23412355])。
角膜與視網膜
受影響的眼睛往往與患者通常睡覺時朝向的一側一致。側臥時,下方的眼瞼受到枕頭或寢具的壓迫,產生機械刺激,導致該側的眼表症狀更明顯。
3. 原因與風險因素
Section titled “3. 原因與風險因素”OSA的風險因子
Section titled “OSA的風險因子”以下列出OSA發病的主要風險因子。
- 肥胖:最重要的風險因子。體重增加10%會使OSA發病風險升高6倍。
- 男性:男性患病率高於女性。
- 高齡:65歲以上族群患病率增加2~3倍。
- 解剖因素:扁桃體/舌頭肥大、下頜後縮、舌骨下移。
- 咽部周圍脂肪堆積:肺容量減少→咽部塌陷性增加
- 兒童:常見於伴有扁桃體和腺樣體肥大的病例
- 種族:非裔美國人中更常見
全身相關疾病
Section titled “全身相關疾病”OSA也與以下全身疾病相關:高血壓、代謝症候群、糖尿病、心衰竭、冠狀動脈疾病、心律不整、中風、肺動脈高壓、神經認知障礙和情緒障礙。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”OSA的診斷標準
Section titled “OSA的診斷標準”透過以下A至C進行診斷。滿足A或B且C時確診。無論症狀如何,AHI ≥15/小時也確診。
- A:無法用其他因素解釋的日間過度嗜睡
- B:以下兩項或以上:睡眠中窒息或喘氣、反覆覺醒、缺乏熟睡感、日間疲勞、注意力下降
- C:每小時睡眠出現5次或以上阻塞性呼吸事件
嚴重程度分級
Section titled “嚴重程度分級”基於AHI的嚴重程度分級如下。
| 嚴重程度 | AHI(次/小時) |
|---|---|
| 輕度 | 5~14 |
| 中度 | 15~29 |
| 重度 | ≥30 |
- STOP-Bang問卷(SBQ):8個項目:打鼾、疲勞、觀察到呼吸暫停、高血壓、BMI、年齡、頸圍、性別
- Epworth嗜睡量表(ESS):日間嗜睡的定量評估。FES患者分數>10時,需進行整夜PSG
- 柏林問卷:從3個類別評估:打鼾、日間嗜睡、高血壓、肥胖
整夜多項睡眠生理檢查(PSG)是黃金標準。雖然有攜帶式簡易睡眠檢查裝置,但最終確診仍建議使用PSG。
眼科醫師篩檢的角色
Section titled “眼科醫師篩檢的角色”- 建議FES患者進行整夜PSG
- 對OSA患者進行全面眼科檢查時積極篩檢FES
- 臨床上檢查眼瞼是否容易外翻是FES診斷的關鍵
- 在非動脈炎性前部缺血性視神經病變患者的問診中,需確認血管風險因子、手術史、吸菸史、藥物史(如PDE5抑制劑)、OSA症狀及巨細胞動脈炎症狀。
確診的黃金標準是整夜多導睡眠圖(PSG)。門診篩查可使用STOP-Bang問卷、Epworth嗜睡量表和柏林問卷。FES患者ESS評分>10時建議進行PSG。
5. 標準治療方法
Section titled “5. 標準治療方法”OSA本身的治療
Section titled “OSA本身的治療”OSA治療有助於從根本上管理眼科併發症。
- 減重:最基本的治療。體重減輕可改善AHI。
- CPAP(持續氣道正壓通氣)療法:防止睡眠中氣道塌陷。OSA的第一線治療,有效減輕症狀和併發症。
- 口腔矯治器(牙套):適用於輕度OSA或無法耐受CPAP的患者。透過前移下頜或固定舌體擴大氣道。
- 手術治療:適用於顱顏畸形或明確阻塞性病變。
- 舌下神經電刺激療法(HSN):適用於內科治療無效的患者。據報導可降低AHI和ESS評分,改善覺醒水平。
- 側臥位睡眠:透過改變體位的保守治療。
FES的治療
Section titled “FES的治療”- 眼科護理:使用人工淚液和眼藥膏點眼
- 眼瞼貼布/眼罩:防止睡眠時眼瞼外翻
- 避免側臥和俯臥:指導患者不要患側朝下睡覺
- 抗發炎眼藥水:僅在眼表發炎嚴重時短期使用
- CPAP療法:McNab報告指出,開始CPAP治療後,乳頭狀結膜炎消失,眼瞼鬆弛恢復正常。中重度OSA患者使用CPAP 18個月後,FES分級、OSDI評分(乾眼症狀)、淚液功能檢查(TBUT、Schirmer I)和角膜螢光素染色均有統計學顯著改善。
適用於保守治療和CPAP無效的病例。
- 外側瞼板條固定術(LTS):70例中報告91%症狀改善,97.5%長期穩定。
- 全層楔形切除術(FTWE):FTWE的復發率往往高於LTS。
- Moorfields眼科醫院的長期研究(71例)顯示復發率為25.6–60.6%,內、外眼角縫合術和LTS的存活結果優於FTWE。
非動脈炎性前部缺血性視神經病變的預防性管理
Section titled “非動脈炎性前部缺血性視神經病變的預防性管理”- 識別並管理可改變的風險因子(高血壓、糖尿病、高血脂症、OSAS)
- 建議戒菸、減重和運動
- 避免睡前服用夜間降壓藥(夜間低血壓是非動脈炎性前部缺血性視神經病變的易感因素)
- 指導患者避免患側臥位
- 如果眼壓處於臨界或升高狀態,考慮降眼壓治療
- 確認PDE5抑制劑使用史(與非動脈炎性前部缺血性視神經病變風險相關)
- 謹慎進行玻璃體內注射(急劇的眼壓升高可能導致ONH循環障礙,增加對側眼非動脈炎性前部缺血性視神經病變的風險)
6. 病理生理學與詳細發病機制
Section titled “6. 病理生理學與詳細發病機制”OSA的上呼吸道阻塞機制
Section titled “OSA的上呼吸道阻塞機制”OSA的阻塞由解剖因素和神經肌肉因素的相互作用引起。
- 解剖因素:扁桃體及舌體肥大、下頜後縮、舌骨下移
- 神經肌肉因素:睡眠期間咽部擴張肌活動減少
- 肥胖的影響:咽周脂肪堆積→肺容量減少→咽部塌陷性增加
全身性方面,血氧飽和度變化激活交感神經系統,導致血壓升高、胰島素阻抗、心律不整、血管內皮功能障礙、全身發炎標誌物升高和血小板聚集增強。
眼科併發症的主要機制
Section titled “眼科併發症的主要機制”OSA引起眼科併發症的主要途徑有以下四種。
- 間歇性低氧:反覆的血氧飽和度降低和再氧合導致組織損傷
- 交感神經過度刺激:對眼壓升高和視神經血流的影響
- 氧化壓力:再氧合時自由基產生導致的血管內皮損傷
- 內皮素-1(ET-1)的有害作用:具有強烈血管收縮作用的肽過度產生
FES的病理生理學
Section titled “FES的病理生理學”關於FES的發病機制有多種假說。
機械理論:側臥睡眠時眼瞼內翻,眼表面與枕頭或寢具直接接觸。醒來時症狀最嚴重支持這一理論。
局部缺血-再灌注理論(Culbertson & Tseng):提出了側臥或俯臥時眼瞼壓迫缺血,加上OSA導致的全身間歇性低氧,體位改變或醒來時再灌注,引起氧化壓力和自由基損傷,結締組織變性,最終導致眼瞼鬆弛的機制。
高瘦素血症與基質金屬蛋白酶(MMPs):與OSA嚴重程度相關的高瘦素血症以劑量依賴性方式調節MMP-9的表達。MMP-7和MMP-9的升高參與瞼板細胞外基質的變性。組織學上可見瞼板彈性蛋白含量降低和膠原變性。
非動脈炎性前部缺血性視神經病變的病理生理
Section titled “非動脈炎性前部缺血性視神經病變的病理生理”非動脈炎性前部缺血性視神經病變被認為同時涉及以下三種機制。
- 一過性低氧:呼吸暫停事件導致的視神經乳頭(ONH)缺血
- 血流自動調節障礙:ONH血流自動調節能力下降
- 顱內壓升高:呼吸暫停發作期間ICP升高→視神經乳頭水平灌流壓降低
青光眼與CSCR的病理生理
Section titled “青光眼與CSCR的病理生理”青光眼:血管因素(缺氧後再灌注時的氧化壓力)和機械因素(交感神經緊張亢進導致的夜間眼壓升高)兩者皆參與其中。
CSCR:氧化壓力增加導致血管內皮損傷和血管收縮,引起脈絡膜循環障礙。肥胖可能作為共同風險因子參與其中。
7. 最新研究與未來展望(研究階段報告)
Section titled “7. 最新研究與未來展望(研究階段報告)”舌下神經電刺激療法(HSN)
Section titled “舌下神經電刺激療法(HSN)”作為藥物治療無效患者的新選擇,相關研究正在推進中。
目前的報告顯示,HSN療法可降低AHI和ESS評分,改善覺醒水平,縮短入睡後覺醒時間。正在考慮將其用於不耐受CPAP的中重度OSA患者。
OSA手術與FES的關係
Section titled “OSA手術與FES的關係”Bayir等人報告,在輕度至中度OSA患者接受前顎成形術後,術後3個月FES盛行率和分級顯著降低,氧飽和度指數也有所改善。此發現提示OSA本身的外科治療可能改善FES。
CPAP與非動脈炎性前部缺血性視神經病變發病風險
Section titled “CPAP與非動脈炎性前部缺血性視神經病變發病風險”CPAP治療是否能降低非動脈炎性前部缺血性視神經病變的首發或對側眼發病風險目前尚未確定。關於OSA管理與非動脈炎性前部缺血性視神經病變預防的關係,需要進一步累積證據。
視神經鞘減壓術
Section titled “視神經鞘減壓術”Sergott等人(1989)報告,在「進行性」非動脈炎性前部缺血性視神經病變病例中,透過在視神經周圍組織上開窗或切口以引流腦脊液並解除間隔症候群的視神經鞘減壓術,可能帶來視力改善的可能性。然而,此手術尚未確立為標準治療,仍處於研究階段。
8. 參考文獻
Section titled “8. 參考文獻”本記事は以下の文献を参考に作成した(いずれもPubMed/PMCで実在を確認済み)。
- Farahvash A, Micieli JA. Neuro-Ophthalmological Manifestations of Obstructive Sleep Apnea: Current Perspectives. Eye Brain. 2020;12:61-71. doi:10.2147/EB.S247121. PMID: 32753994; PMCID: PMC7353992.
- Bulloch G, Seth I, Zhu Z, Sukumar S, McNab A. Ocular manifestations of obstructive sleep apnea: a systematic review and meta-analysis. Graefes Arch Clin Exp Ophthalmol. 2024;262(1):19-32. doi:10.1007/s00417-023-06103-3. PMID: 37227479; PMCID: PMC10806133.
- Huon LK, Liu SY, Camacho M, Guilleminault C. The association between ophthalmologic diseases and obstructive sleep apnea: a systematic review and meta-analysis. Sleep Breath. 2016;20(4):1145-1154. doi:10.1007/s11325-016-1358-4. PMID: 27230013.
- Cheong AJY, Ho OTW, Wang SKX, et al. Association between obstructive sleep apnea and floppy eyelid syndrome: A systematic review and meta-analysis. Surv Ophthalmol. 2023;68(2):257-264. doi:10.1016/j.survophthal.2022.11.006. PMID: 36427560.
- Cristescu Teodor R, Mihaltan FD. Eyelid laxity and sleep apnea syndrome: a review. Rom J Ophthalmol. 2019;63(1):2-9. PMID: 31198891; PMCID: PMC6531778.
- Pellegrini M, Bernabei F, Friehmann A, Giannaccare G. Obstructive Sleep Apnea and Keratoconus: A Systematic Review and Meta-analysis. Optom Vis Sci. 2020;97(1):9-14. doi:10.1097/OPX.0000000000001467. PMID: 31895272.
- Thurtell MJ, Trotti LM, Bixler EO, et al. Obstructive sleep apnea in idiopathic intracranial hypertension: comparison with matched population data. J Neurol. 2013;260(7):1748-1751. doi:10.1007/s00415-013-6858-6. PMID: 23412355; PMCID: PMC3707935.
