نوع I (ادم پاپی)
ضایعه: عروق ناحیه لامینا کریبروزا قدامی
مکانیسم: استاز وریدی ناشی از التهاب غیراختصاصی
ویژگی: ادم پاپی غالب است. گزارشهایی از اثربخشی استروئیدها وجود دارد

پاپیلوفلبیت (Papillophlebitis) یک زیرگروه بالینی (نوع ناقص) انسداد ورید مرکزی شبکیه (CRVO) است که در بزرگسالان جوان سالم زیر ۴۵ سال رخ میدهد و نادر است1, 2). به آن «واسکولیت دیسک بینایی» نیز گفته میشود.
پاپیلیت بینایی (نوریت پاپی) در مقابل CRVO در میانسالی که با افزایش سن، فشار خون بالا و تصلب شرایین همراه است، در افراد جوان سالم ۲۰ تا ۳۵ ساله، به ویژه زنان، شایعتر است. هایره (۱۹۷۲) این بیماری را به دو نوع زیر طبقهبندی کرد:
نوع I (ادم پاپی)
ضایعه: عروق ناحیه لامینا کریبروزا قدامی
مکانیسم: استاز وریدی ناشی از التهاب غیراختصاصی
ویژگی: ادم پاپی غالب است. گزارشهایی از اثربخشی استروئیدها وجود دارد
نوع II (انسداد ورید مرکزی)
محل ضایعه: ناحیه سر عصب بینایی یا پشت صفحه کریبریفرم
مکانیسم: التهاب ورید مرکزی شبکیه
ویژگیها: همراه با گشاد شدن ورید، پیچ خوردگی و خونریزی شبکیه. برخی گزارشها حاکی از عدم پاسخ به استروئید است
CRVO بیشتر در افراد میانسال و مسن با عوامل خطر مانند فشار خون بالا، دیابت و تصلب شرایین دیده میشود و در نوع ایسکمیک، اختلال شدید بینایی شایع است. در مقابل، پاپیلفلبیت در جوانان سالم رخ میدهد، بینایی معمولاً نسبتاً حفظ میشود و بیماری با پیشآگهی خوب طی ۶ تا ۱۲ ماه خودبهخود消退 مییابد. با این حال، در CRVO جوانان، افتراق از پاپیلفلبیت مهم است و ممکن است نیاز به تجویز استروئید سیستمیک باشد.
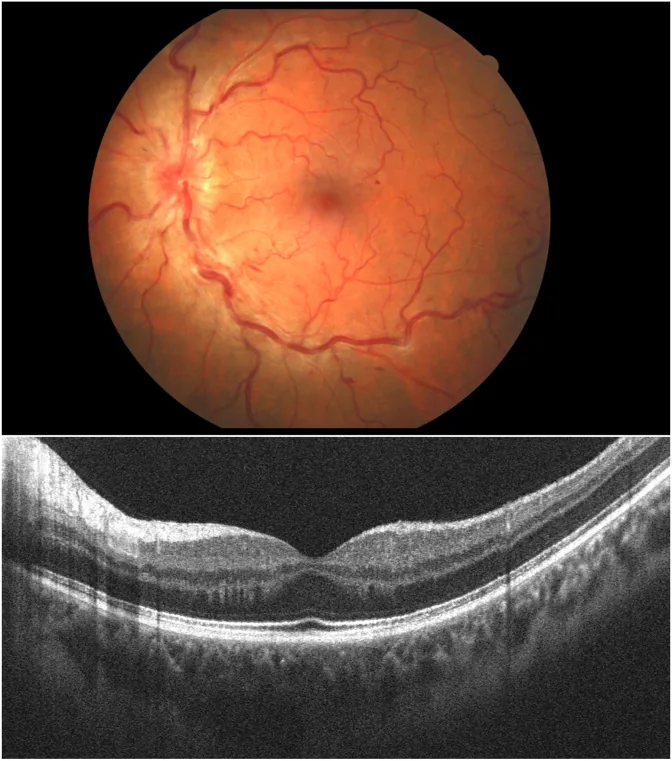
اتیولوژی اغلب ایدیوپاتیک فرض میشود، اما ارتباط با حالتهای انعقادپذیری بالا گزارش شده است.
جدول زیر عوامل خطر اصلی و میزان همراهی با بیماریهای سیستمیک را نشان میدهد.
| عوامل خطر / بیماریهای همراه | فراوانی / نکات ویژه |
|---|---|
| دیابت | ۳ تا ۹٪ |
| فشار خون بالا | ۲۳ تا ۴۲٪ |
| بیماری التهابی روده، پسوریازیس | مرتبط |
| بارداری، داروهای ضدبارداری خوراکی | مرتبط |
| ارتفاعات بالا، کمآبی بدن | مرتبط |
ارتباط با اختلالات انعقادی ارثی نیز مهم است. شایعترین اختلال انعقادی ارثی در اروپا، جهش فاکتور V لیدن (FVL) است که شیوع هتروزیگوت در یونان ۱۵٪ (بالاترین در اروپا) گزارش شده و مواردی از فلبیت پاپیلا در اثر ترکیب جهشهای هتروزیگوت FVL و MTHFR-C677T گزارش شده است 2).
ارتباط با کووید-۱۹ نیز مورد توجه قرار گرفته است. SARS-CoV-2 از طریق گیرنده ACE2 باعث آسیب اندوتلیال عروقی و فعالسازی سیستم انعقاد میشود. بیش از ۳۰٪ از بیماران مبتلا به کووید-۱۹ دچار رویدادهای ترومبوآمبولی وریدی و شریانی میشوند و مواردی از فلبیت پاپیلا شش هفته پس از ابتلا گزارش شده است 1).
بیشتر در زنان جوان ۲۰ تا ۳۵ سال دیده میشود. اختلالات انعقادی (مانند جهش فاکتور V لیدن)، ابتلا به کووید-۱۹، و مصرف قرصهای ضدبارداری خوراکی به عنوان عوامل خطر گزارش شدهاند. همچنین ممکن است با بیماریهای سیستمیک (فشار خون بالا، دیابت) همراه باشد.
فلبیت پاپی یک تشخیص افتراقی است و افتراق آن از بیماریهای شایع در همین گروه سنی مانند ادم پاپی و نوریت اپتیک مهم است.
برای تأیید تشخیص و جستجوی علت، آزمایشهای زیر انجام میشود.
بیماریهایی که باید افتراق داده شوند عبارتند از:
در حال حاضر، یک روش درمانی استاندارد مبتنی بر شواهد که به طور جهانی پذیرفته شده باشد، وجود ندارد.
کورتیکواستروئیدها درمان اصلی هستند و به دلیل احتمال درگیری واسکولیت استفاده میشوند. در نوع I مؤثر است، اما گزارشهایی از عدم تأثیر در نوع II وجود دارد. از آنجایی که این بیماری حتی بدون درمان نیز بهبود خودبهخودی نشان میدهد، شواهد واضحی مبنی بر برتری استروئیدها وجود ندارد. معمولاً درمان سیستمیک با استروئید فقط برای موارد شدید بالینی در نظر گرفته میشود.
Ntora و همکاران (2021) یک زن 22 ساله (با ترکیب هتروزیگوت FVL و هتروزیگوت MTHFR-C677T) را با متیلپردنیزولون خوراکی 50 میلیگرم در روز شروع و به تدریج کاهش دادند که پس از یک هفته بهبود یافته و پس از یک ماه کاملاً برطرف شد. بینایی و میدان بینایی پس از 6 ماه همچنان طبیعی باقی ماند2).
سایر درمانها مانند درمان ضد پلاکتی و ضد انعقادی نیز پیشنهاد شدهاند اما اثربخشی آنها ثابت نشده است.
در موارد ادم ماکولای شدید، تزریق داخل زجاجیهای داروهای ضد VEGF ممکن است در نظر گرفته شود (تأیید نشده توسط FDA).
Insausti-García و همکاران (2022) یک مرد 40 ساله را که پس از ابتلا به COVID-19 دچار فلبیت پاپیلای عصب بینایی شده بود، در ابتدا با آسپرین خوراکی 100 میلیگرم در روز و قطره چشمی برومفناک 0.9 میلیگرم/میلیلیتر (دو بار در روز) درمان کردند. سپس به دلیل کاهش بینایی (20/200) ناشی از ادم ماکولا، ایمپلنت دگزامتازون با رهش پایدار داخل زجاجیهای (Ozurdex) تزریق کردند که پس از دو هفته بینایی به 20/40 بهبود یافت1).
این بیماری بدون درمان نیز بهبود خودبهخودی نشان میدهد و پیشآگهی عموماً خوب است و انتظار میرود طی ۶ تا ۱۲ ماه به طور خودبهخود برطرف شود. با این حال، تا ۳۰٪ خطر پیشرفت به انسداد ورید ایسکمیک وجود دارد، بنابراین پیگیری منظم چشمپزشکی ضروری است. برای جزئیات به بخش «روشهای درمانی استاندارد» مراجعه کنید.
پاتوفیزیولوژی فلبیت پاپی واضح نیست و تصور میشود مکانیسم بروز آن واحد نباشد.
فرضیه اصلی این است که التهاب ایدیوپاتیک سر عصب بینایی، ورید مرکزی شبکیه را فشرده کرده و باعث نارسایی ثانویه وریدی و خونریزی داخل شبکیه میشود. در نوع I طبقهبندی هایره، التهاب غیراختصاصی عروق ناحیه پیشغربالی و در نوع II، التهاب ورید مرکزی شبکیه در ناحیه سر عصب بینایی یا پسغربالی به عنوان مکانیسم فرض شده است.
مکانیسم بروز مرتبط با کووید-۱۹ شامل آبشار زیر است که پیشنهاد شده است1).
الگوی اختلال انعقادی مرتبط با کووید-۱۹ (CAC) با افزایش D-دایمر و فیبرینوژن همزمان با نشانگرهای التهابی مشخص میشود1).
نقش اختلالات انعقادی ارثی نیز گزارش شده است. تصور میشود که ترکیب هتروزیگوت FVL و هتروزیگوت MTHFR-C677T میتواند باعث عدم تعادل انعقادی شده و به بروز فلبیت پاپیلاری کمک کند2). جهش MTHFR-C677T در حالت هموزیگوت میتواند باعث هیپرهموسیستئینمی و حالت انعقادپذیری بیش از حد شود، اما در حالت هتروزیگوت ممکن است هیپرهموسیستئینمی رخ ندهد.
مکانیسم بروز بیماری منفرد نیست، اما تصور میشود که التهاب سر عصب بینایی باعث فشردگی ورید مرکزی شبکیه میشود. در افراد جوان، از آنجایی که عوامل خطر CRVO در میانسالی مانند فشار خون بالا و تصلب شرایین وجود ندارد، اختلالات انعقادی (عوامل ارثی) و التهاب پس از عفونت (مانند COVID-19) به عنوان عوامل محرک نسبتاً مهم هستند.
اینشتاوستی-گارسیا و همکاران (۲۰۲۲) موردی از یک مرد ۴۰ ساله را گزارش کردند که ۶ هفته پس از ابتلا به کووید-۱۹ دچار فلبیت پاپیلاری شد1). آزمایشها افزایش نشانگرهای انعقادی و التهابی را نشان داد: D-دایمر ۶۷۲ میکروگرم در لیتر (طبیعی <۴۶۰)، فیبرینوژن ۴۵۱ میلیگرم در دسیلیتر (طبیعی ۲۰۰-۴۰۰)، و CRP ۰.۸۹۸ میلیگرم در دسیلیتر (طبیعی <۰.۵۰۰). تمام عوامل ترومبوفیلی ارثی طبیعی بودند. دو هفته پس از تزریق ایمپلنت داخل زجاجیهای دگزامتازون (Ozurdex)، بینایی از ۲۰/۲۰۰ به ۲۰/۴۰ بهبود یافت. بهبود سریع با دگزامتازون ممکن است از فرضیه التهابی حمایت کند.
نتورا و همکاران (۲۰۲۱) اولین گزارش جهانی از یک مورد فلبیت پاپیلاری را در یک زن ۲۲ ساله با ترکیب هتروزیگوت FVL و هتروزیگوت MTHFR-C677T ارائه کردند2). با متیلپردنیزولون خوراکی به تنهایی بهبودی کامل حاصل شد. غربالگری ژنتیکی به عنوان یک آیتم جستجوی مهم در تشخیص فلبیت پاپیلاری نشان داده شد. مشاوره هماتولوژی برای پیشگیری از عوارض آینده ضروری تلقی میشود.
Insausti-García A, Reche-Sainz JA, Ruiz-Arranz C, et al. Papillophlebitis in a COVID-19 patient: inflammation and hypercoagulable state. Eur J Ophthalmol. 2022;32(1):NP168-NP172.
Ntora E, Dalianis G, Terzidou C. Papillophlebitis associated with coexisting heterozygous mutations of Factor V Leiden and methylenetetrahydrofolate reductase enzyme (C677T). Cureus. 2021;13(5):e15081.
Abdel Jalil S, Amer R. The Spectrum of Papillophlebitis. Ocul Immunol Inflamm. 2024;32(10):2515-2520. PMID: 38842197.