پیگیری
خط اول: در بسیاری از موارد، ادم پاپیلا طی ۳ تا ۶ ماه پیگیری خودبهخود ناپدید میشود.
معاینات دورهای: پیگیری تغییرات ادم پاپیلا و ME با OCT و آنژیوگرافی فلورسئین.
کنترل قند خون: ادامه کنترل پایدار با اجتناب از نوسانات شدید قند خون.

پاپیلوپاتی دیابتی (Diabetic Papillopathy; DP) یک ادم نسبتاً نادر سر عصب بینایی است که در بیماران دیابتی رخ میدهد. اولین بار در سال 1971 توسط Lubow و Makley در بیماران جوان مبتلا به دیابت نوع 1 گزارش شد. میزان بروز حدود 0.5% پایین است، اما در تمام گروههای سنی، چه نوع 1 و چه نوع 2، رخ میدهد.
ماهیت DP ایسکمی خفیف و برگشتپذیر در ناحیه لایه پیشپاپیلاری سر عصب بینایی (ONH) در نظر گرفته میشود 2). به عنوان بخشی از طیف ایسکمی پاپیلاری، این دیدگاه نیز مطرح شده است که یک پیوستار پاتولوژیک از ادم پاپیلاری بدون اختلال عملکرد تا انفارکتوس واضح NA-AION وجود دارد 2).
ویژگی DP این است که با وجود ادم برجسته پاپیلاری، تأثیر بر بینایی و میدان بینایی حداقل است. نقص نسبی مردمک آوران (RAPD) خفیف است و معمولاً نقص شدید میدان بینایی مشاهده نمیشود 2). ادم پاپیلاری خودبهخود برطرف میشود و تقریباً هیچ آتروفی عصب بینایی باقی نمیگذارد 2).
برخی از نویسندگان DP را شکلی از NA-AION میدانند، اما موقعیت پاتولوژیک آن هنوز قطعی نیست. تشخیص یک تشخیص افتراقی است و نیاز به افتراق از سایر بیماریها دارد (به بخش «تشخیص و روشهای آزمایش» مراجعه کنید).
ارتباط واضحی وجود ندارد. DP میتواند بدون رتینوپاتی دیابتی (DR) رخ دهد. از سوی دیگر، گزارش شده است که در 63-80% موارد DR همزمان وجود دارد و همراهی این دو شایع است. همبستگی بین شدت DR و بروز DP مشاهده نشده است 1).
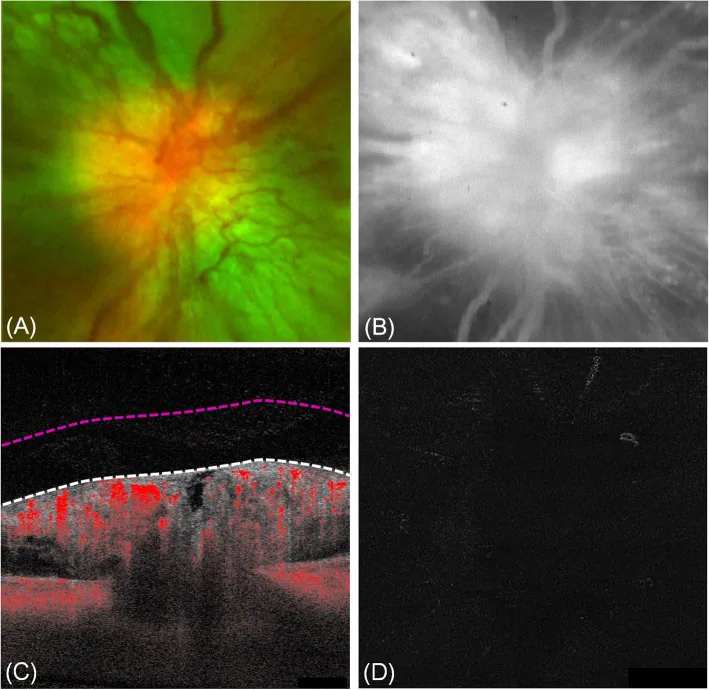
بسیاری از بیماران بدون علامت هستند و به طور تصادفی در معاینات دوره ای چشم برای دیابت کشف می شوند. حتی در صورت وجود علائم، خفیف هستند.
عدم تطابق بین شدت ادم پاپی و تأثیر بر بینایی و میدان بینایی از ویژگیهای DP است. در زیر یافتههای بالینی اصلی DP آورده شده است.
| مورد یافته | ویژگی |
|---|---|
| ادم پاپی | پر خون، گشاد شدن عروق سطحی |
| بینایی اولیه | 20/20 تا 20/200 |
| RAPD | فقط خفیف |
| ناهنجاری رنگبینی | معمولاً بدون علامت |
| میدان بینایی | فقط بزرگ شدن نقطه کور |
| ادم پایدار دیسک بینایی | حداکثر پس از ۱۲ ماه خودبهخود برطرف میشود |
در حدود ۵۰٪ موارد، عروق کوچک گشاد شده روی سطح دیسک بینایی دیده میشود. مهم است که این گشاد شدن عروق سطحی به داخل زجاجیه گسترش نمییابد و از عروق جدید در رتینوپاتی دیابتی پرولیفراتیو (NVD) متمایز میشود.
ادم ماکولا (ME) در بیش از ۵۰٪ موارد همراه است 1). همچنین، دیسک بینایی شلوغ (crowded optic disc) در چشم مقابل با فراوانی بالایی گزارش شده است 2). ادم دیسک بینایی اغلب حداکثر تا ۱۲ ماه ادامه یافته و سپس خودبهخود برطرف میشود و به ندرت آتروفی عصب بینایی باقی میگذارد 2).
در مورد ۱ گزارش شده توسط Arapi و همکاران (۲۰۲۱) (زن ۶۰ ساله، دیابت نوع ۲، HbA1c ۱۰.۹٪)، دید چشم راست ۶/۳۶۰ و ادم شدید دیسک بینایی همراه با خونریزی خطی (splinter hemorrhage) مشاهده شد. پس از ۷ هفته درمان، دید به ۲۰/۳۰ بهبود یافت 1).
علت دقیق DP به طور کامل شناخته نشده است، اما تصور میشود که میکروآنژیوپاتی دیابتی زمینهساز آن باشد. این عارضه در هر دو نوع دیابت نوع ۱ و ۲ رخ میدهد.
عوامل خطر اصلی به شرح زیر است:
دیابت به عنوان یک عامل خطر برای NA-AION ذکر شده است و DP و NA-AION ممکن است زمینه پاتوفیزیولوژیک مشترکی داشته باشند2).
کنترل سریع قند خون (مانند شروع جدید انسولین) ممکن است در بروز DP نقش داشته باشد. تصور میشود که کاهش ناگهانی قند خون باعث تجمع مایع در اطراف دیسک بینایی و ادم پاپی میشود. پیگیری چشم پزشکی در شروع درمان با انسولین مهم است.
DP یک تشخیص افتراقی است. لازم است با معیارهای تشخیصی زیر مطابقت داشته باشد و سایر بیماریها رد شوند2).
معیارهای تشخیصی DP (Salvetat et al. 2023)2):
نقاط افتراقی DP و NA-AION در زیر آورده شده است.
| نقطه افتراقی | پاپیلوپاتی دیابتی | NA-AION |
|---|---|---|
| RAPD | خفیف/ندارد | واضح |
| نقص میدان بینایی | فقط بزرگ شدن نقطه کور | همیانوپسی افقی |
| یافتههای FA | نشت زودرس | تأخیر در پرشدگی وجود دارد |
DP با RAPD منفی، حداقل نقص میدان بینایی و بهبود خودبهخودی مشخص میشود. در NA-AION، همیانوپسی افقی، RAPD واضح و آتروفی عصب بینایی رخ میدهد. در یافتههای FA، DP نشت بسیار زودرس از سطح پاپیلا و NA-AION تأخیر در پرشدگی را نشان میدهد2). هر دو به عنوان طیف پیوستهای از ایسکمی ONH در نظر گرفته میشوند2).
اساس درمان پیگیری است. DP اغلب طی ۳ تا ۶ ماه (حداکثر ۱۲ ماه) بهبود خودبهخودی مییابد و ادم پاپیلا با حفظ بینایی برطرف میشود.
پیگیری
خط اول: در بسیاری از موارد، ادم پاپیلا طی ۳ تا ۶ ماه پیگیری خودبهخود ناپدید میشود.
معاینات دورهای: پیگیری تغییرات ادم پاپیلا و ME با OCT و آنژیوگرافی فلورسئین.
کنترل قند خون: ادامه کنترل پایدار با اجتناب از نوسانات شدید قند خون.
درمان با استروئید
تزریق زیر تانون (STTAI): استفاده از تریامسینولون ۴۰ میلیگرم/میلیلیتر. خطر افزایش فشار چشم نسبت به IVTA کمتر است. گزارش شده است که تزریق سابتنون بتامتازون دوره ۵ ماهه طبیعی را به ۳ هفته کاهش میدهد1). IVTA (تزریق داخل زجاجیهای) در مقایسه با STTAI حدود ۳ برابر خطر افزایش فشار چشم (>۲۱ میلیمتر جیوه) دارد.
ترکیب ضد VEGF و استروئید
IAI (aflibercept 2mg/0.05mL) + STTAI (TA 40mg/mL): گزارش ترکیبی برای موارد شدید وجود دارد1).
اثر: ادم پاپی و بینایی در عرض ۵ تا ۷ هفته بهبود مییابد. با پیگیری ۱۲ ماهه ثبات حفظ میشود1).
سایر: گزارشهایی از درمان تکدارویی ضد VEGF با ranibizumab یا bevacizumab وجود دارد.
Arapi و همکاران (2021) در دو مورد DP شدید، درمان ترکیبی IAI (aflibercept 2mg) و STTAI (triamcinolone 40mg/mL) را انجام دادند1). مورد 1 (HbA1c 10.9%) از 6/360 در چشم راست به 20/30 پس از 7 هفته و از 6/60 در چشم چپ به 20/25 پس از 5 هفته بهبود یافت. مورد 2 (HbA1c 11.2%) از 6/120 در چشم چپ به 20/30 پس از 5 هفته بهبود یافت. هر دو در پیگیری 12 ماهه سیر پایدار نشان دادند.
بسیاری از موارد در عرض ۳ تا ۶ ماه (حداکثر ۱۲ ماه) بهبود خودبهخودی دارند و در ۹۲% موارد بینایی حفظ میشود. پیگیری اولین گزینه است. در موارد شدید یا همراه با ادم ماکولا显著، درمان با استروئید یا ضد VEGF ممکن است بهبود را تسریع کند1).
پاتولوژی DP بر پایه میکروآنژیوپاتی دیابتی است. مکانیسمهای اصلی مطرح شده به شرح زیر است:
درمان ترکیبی ضد VEGF (aflibercept، ranibizumab، bevacizumab) و استروئید برای DP در موارد شدید در سطح گزارش موردی مؤثر گزارش شده است. Arapi و همکاران نشان دادند که درمان ترکیبی بهبود بینایی و کاهش ادم پاپی را در DP شدید تسریع میکند 1). با این حال، در حال حاضر فقط گزارشهای موردی وجود دارد و برای استانداردسازی پروتکل درمان، مطالعات آیندهنگر در مقیاس بزرگ لازم است 1).
Salvetat و همکاران (2023) DP را به عنوان انتهای خفیف طیف ایسکمی ONH قرار داده و احتمال تشکیل یک گروه بیماری با تداوم پاتوفیزیولوژیک بین DP و NA-AION را مطرح میکنند 2). این دیدگاه برای شناسایی عوامل پیشآگهی DP و تعیین زمان مداخله درمانی اهمیت دارد. توسعه نشانگرهای زیستی و شاخصهای تصویربرداری که مرز بین این دو را مشخص کنند، چالش آینده است 2).