观察

糖尿病性视乳头病变
一目了然的要点
Section titled “一目了然的要点”1. 什么是糖尿病性视乳头病变?
Section titled “1. 什么是糖尿病性视乳头病变?”糖尿病性视乳头病变(Diabetic Papillopathy; DP)是糖尿病患者发生的相对罕见的视乳头水肿。1971年Lubow和Makley首次在1型糖尿病年轻患者中报道。发病率约0.5%,但1型和2型糖尿病各年龄层均可发病。
DP的本质被认为是视乳头前层(ONH)区域的轻度、可逆性缺血2)。也有观点认为,作为视乳头缺血谱系的一部分,存在从无功能障碍的视乳头水肿到NA-AION的明确梗死的一系列连续病理状态2)。
DP的特点是尽管有明显的视乳头水肿,但对视力和视野的影响极小。相对性传入性瞳孔障碍(RAPD)轻微,通常不出现严重的视野缺损2)。视乳头水肿可自行消退,几乎不留视神经萎缩2)。
一些作者将DP视为NA-AION的一种形式,但其病理定位尚无定论。诊断是排除性诊断,需要与其他疾病鉴别(参见“诊断和检查方法”一节)。
没有明确关联。即使没有糖尿病视网膜病变(DR),DP也可能发生。另一方面,有报道称63-80%的病例合并DR,两者常同时出现。DR的严重程度与DP的发生未见相关性1)。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”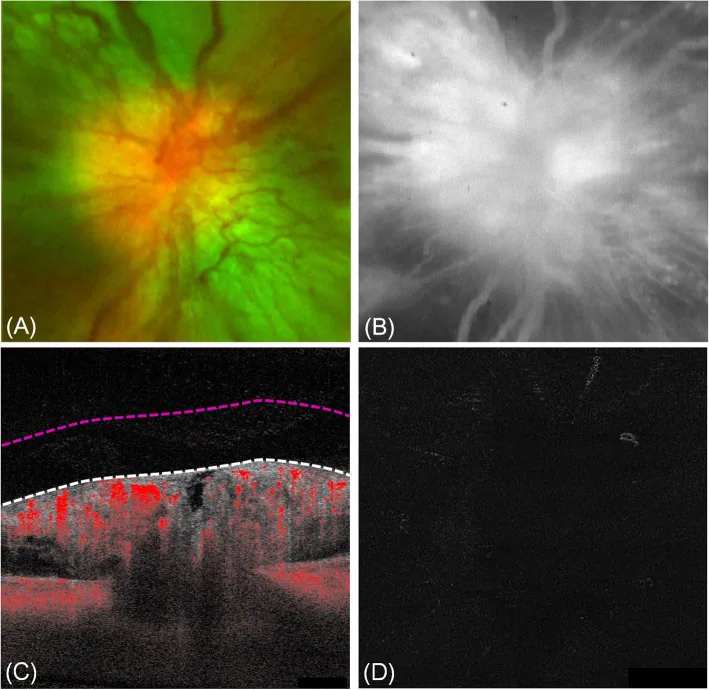
许多患者无症状,在糖尿病常规眼科检查中偶然发现。即使有症状,也较轻微。
- 无症状:大多数患者缺乏自觉症状。
- 视物模糊:部分患者可能出现。
- 视力下降(轻度):通常改善,不留明显视力损害。
DP的特征是视盘水肿程度与视力、视野影响之间的分离。以下为DP的主要临床所见。
| 所见项目 | 特征 |
|---|---|
| 视盘水肿 | 充血性、表面血管扩张 |
| 初诊视力 | 20/20~20/200 |
| RAPD | 仅轻微 |
| 色觉异常 | 通常无 |
| 视野 | 仅盲点扩大 |
| 视乳头水肿持续 | 最长12个月后自然消退 |
约50%的病例可见视乳头表面扩张的微血管。重要的是,这种视乳头表面血管扩张不会延伸至玻璃体,需与增殖性糖尿病视网膜病变中的视盘新生血管(NVD)相鉴别。
黄斑水肿(ME)见于超过50%的病例1)。此外,对侧眼常表现为拥挤视盘2)。视乳头水肿通常持续最长12个月后自然消退,几乎不留视神经萎缩2)。
Arapi等人(2021)报告的病例1(60岁女性,2型糖尿病,HbA1c 10.9%)中,右眼视力6/360,重度视乳头水肿伴线状出血。治疗后7周,视力恢复至20/301)。
3. 病因与风险因素
Section titled “3. 病因与风险因素”DP的发病机制尚未完全阐明,但认为糖尿病微血管病变是基础。1型和2型糖尿病均可发病。
主要风险因素如下:
- 血糖控制不良:多见于高HbA1c的病例(如HbA1c 10.9%、11.2%)1)。
- 血糖快速控制:如新开始胰岛素治疗等导致的血糖快速改善被认为与发病有关。
- 拥挤视盘:视盘内神经纤维密集增加血管受压风险2)。
- 视盘玻璃膜疣:视盘内的异常沉积物被认为是危险因素。
DM被认为是NA-AION的危险因素,DP和NA-AION可能具有共同的病理基础2)。
快速血糖控制(如新开始胰岛素治疗)被认为有助于DP的发生。推测血糖急剧下降会导致视盘周围水分积聚,引起视盘水肿。开始胰岛素治疗时,眼科随访很重要。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”DP是一种排除性诊断。需要符合以下诊断标准并排除其他疾病2)。
DP诊断标准(Salvetat et al. 2023)2):
主要检查方法
Section titled “主要检查方法”- 荧光素眼底血管造影(FA/FFA):DP的特征是极早期渗漏(早期视盘表面扩张血管的荧光素渗漏)2)。无充盈延迟有助于与NA-AION鉴别1)。视盘新生血管可见玻璃体内随机渗漏,而DP无玻璃体进展。
- 光学相干断层扫描(OCT):有助于确认视网膜神经纤维层(RNFL)增厚和黄斑水肿(ME)1)。
- 眼底自发荧光(FAF):可见视盘周围低自发荧光1)。
- 视野检查:典型表现为仅盲点扩大。若出现水平半盲,则怀疑NA-AION。
- MRI:对于双眼视盘水肿,考虑进行以排除颅内压增高。
DP与NA-AION的鉴别要点如下所示。
| 鉴别点 | 糖尿病性视乳头病变 | NA-AION |
|---|---|---|
| RAPD | 轻微/无 | 明显 |
| 视野缺损 | 仅盲点扩大 | 水平半盲 |
| FA所见 | 早期渗漏 | 充盈延迟 |
5. 标准治疗方法
Section titled “5. 标准治疗方法”以观察为主。DP常在3至6个月(最长12个月)内自然缓解,视盘水肿消退且视力得以维持。
类固醇疗法
Tenon囊下注射(STTAI):使用曲安奈德40 mg/mL。与IVTA相比,眼压升高风险较低。有报告称,球筋膜下注射倍他米松可将自然病程从5个月缩短至3周1)。IVTA(玻璃体内注射)的眼压升高风险(>21 mmHg)约为STTAI的3倍。
抗VEGF联合类固醇
IAI(阿柏西普2 mg/0.05 mL)+ STTAI(TA 40 mg/mL):有报告用于重症病例的联合治疗1)。
效果:5-7周内视乳头水肿和视力恢复。12个月随访期间保持稳定1)。
其他:也有使用雷珠单抗或贝伐珠单抗进行抗VEGF单药治疗的报道。
Arapi等人(2021)对2例重症DP患者实施了IAI(阿柏西普2mg)联合STTAI(曲安奈德40mg/mL)治疗1)。病例1(HbA1c 10.9%)右眼从6/360改善至7周后20/30,左眼从6/60改善至5周后20/25。病例2(HbA1c 11.2%)左眼从6/120恢复至5周后20/30。两者在12个月随访中均表现稳定。
许多病例在3-6个月(最长12个月)内自然缓解,92%的视力得以维持。观察是首选。对于重症或合并明显黄斑水肿的病例,类固醇或抗VEGF治疗可能促进恢复1)。
6. 病理生理学及详细发病机制
Section titled “6. 病理生理学及详细发病机制”DP的病理基础是糖尿病性微血管病变。目前提出的主要机制如下。
- 视乳头周围微血管病变:视乳头周围毛细血管损伤导致血管通透性增加,引起视乳头水肿1)。
- 深层筛板循环障碍及轴浆流中断:筛板水平的血流障碍阻碍轴浆运输,导致视神经纤维肿胀1)。
- 快速血糖控制导致的水分蓄积:血糖急剧下降改变组织渗透压,导致视乳头周围水分积聚。这被认为会压迫筛板,导致轴浆流减少。
- 视乳头前层ONH的轻度可逆性缺血:DP被认为是ONH缺血谱系的轻度端2)。有观点认为它是一种连续病变,重症化时可进展为NA-AION2)。
- 炎症细胞因子与VEGF的相互作用:糖尿病微血管病变中VEGF的过度产生导致血管通透性增加1)。
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”抗VEGF联合类固醇治疗的建立
Section titled “抗VEGF联合类固醇治疗的建立”抗VEGF药物(阿柏西普、雷珠单抗、贝伐珠单抗)与类固醇联合治疗DP在重症病例中的有效性已有病例报告。Arapi等人表明,联合治疗可促进重症DP的视力恢复和视盘水肿消退1)。但目前仅限于病例报告,治疗方案的标准化需要大规模前瞻性研究1)。
DP与NA-AION的病理连续性
Section titled “DP与NA-AION的病理连续性”Salvetat等人(2023)将DP定位为ONH缺血谱系的轻症端,并讨论了DP与NA-AION可能形成病理上连续的疾病群2)。这一观点对于确定DP的预后因素和治疗干预时机具有重要意义。界定两者边界的生物标志物和影像诊断指标的开发是未来的课题2)。
8. 参考文献
Section titled “8. 参考文献”- Arapi I, Neri P, Giovannini A, Grezda A. Combined therapy with intravitreal aflibercept and subtenon corticosteroids in eyes with severe diabetic papillopathy: two case reports. J Med Case Reports. 2021;15:518.
- Salvetat ML, et al. Non-Arteritic Anterior Ischemic Optic Neuropathy. Vision. 2023;7(4):72.
