Type I (œdème papillaire)
Lésion : vaisseaux de la lame criblée antérieure
Mécanisme : stase veineuse due à une inflammation non spécifique
Caractéristiques : œdème papillaire prédominant. Des rapports indiquent que les stéroïdes sont efficaces.

La papillophlébite (Papillophlebitis) est un sous-type clinique (forme incomplète) de l’occlusion de la veine centrale de la rétine (OVCR), une maladie rare survenant chez les jeunes adultes en bonne santé de moins de 45 ans1, 2). Elle est également appelée « vascularite du disque optique ».
Contrairement à l’OCR des personnes d’âge moyen, qui est liée au vieillissement, à l’hypertension et à l’artériosclérose, la papillophlébite se caractérise par sa fréquence chez les jeunes adultes en bonne santé âgés de 20 à 35 ans, en particulier les femmes. Hayreh (1972) a classé cette maladie en deux types suivants.
Type I (œdème papillaire)
Lésion : vaisseaux de la lame criblée antérieure
Mécanisme : stase veineuse due à une inflammation non spécifique
Caractéristiques : œdème papillaire prédominant. Des rapports indiquent que les stéroïdes sont efficaces.
Type II (occlusion veineuse centrale)
Lésion : Tête du nerf optique ou région de la lame criblée postérieure
Mécanisme : Inflammation de la veine centrale de la rétine
Caractéristiques : Dilatation veineuse, tortuosité et hémorragies rétiniennes. Certains rapports indiquent une inefficacité des stéroïdes
La CRVO survient souvent chez les personnes d’âge moyen ou âgées présentant des facteurs de risque tels que l’hypertension, le diabète et l’artériosclérose, et le type ischémique entraîne facilement une déficience visuelle sévère. En revanche, la papillophlébite survient chez des jeunes en bonne santé, la vision est souvent relativement préservée, et c’est une maladie de bon pronostic qui disparaît spontanément en 6 à 12 mois. Cependant, chez les jeunes atteints de CRVO, la distinction avec la papillophlébite est importante, et un traitement systémique par stéroïdes peut être nécessaire.
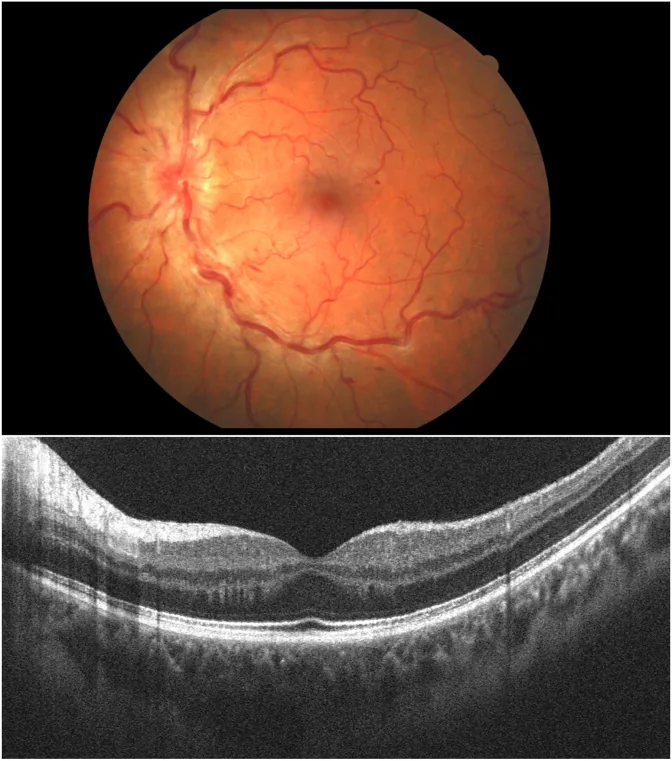
L’étiologie est souvent considérée comme idiopathique, mais une association avec des états d’hypercoagulabilité sanguine a été rapportée.
Le tableau ci-dessous présente les principaux facteurs de risque et les taux de comorbidités systémiques.
| Facteurs de risque / comorbidités | Fréquence / remarques |
|---|---|
| Diabète | 3 à 9 % |
| Hypertension | 23 à 42 % |
| Maladies inflammatoires de l’intestin, psoriasis | Associé |
| Grossesse, contraceptifs oraux | Associé |
| Altitude, déshydratation | Associé |
L’association avec des anomalies héréditaires de la coagulation est également importante. La mutation Factor V Leiden (FVL), le trouble d’hypercoagulabilité héréditaire le plus courant en Europe, a une prévalence hétérozygote élevée de 15 % en Grèce (la plus élevée d’Europe), et des cas de papillophlébite ont été rapportés en raison de la combinaison des mutations hétérozygotes FVL et MTHFR-C677T 2).
L’association avec la COVID-19 attire également l’attention. Le SARS-CoV-2 provoque des lésions endothéliales vasculaires via le récepteur ACE2 et active le système de coagulation. On rapporte que plus de 30 % des patients atteints de COVID-19 développent des événements thromboemboliques veineux et artériels, et des cas de papillophlébite survenus 6 semaines après l’infection ont été signalés 1).
Elle touche principalement les jeunes femmes âgées de 20 à 35 ans. Les troubles de la coagulation (comme la mutation du facteur V Leiden), les suites d’une infection au COVID-19 et l’utilisation de contraceptifs oraux sont rapportés comme facteurs de risque. Certains cas sont associés à des maladies systémiques (hypertension, diabète).
La papillite veineuse est un diagnostic d’exclusion, et il est important de la différencier des maladies courantes dans la même tranche d’âge, telles que la papille congestive et la névrite optique.
Les examens suivants sont effectués pour confirmer le diagnostic et rechercher la cause.
Les maladies à différencier comprennent les suivantes.
Il n’existe actuellement aucun traitement universellement accepté fondé sur des preuves.
Les corticostéroïdes sont le traitement principal, utilisés en raison de la suspicion d’une vascularite. Ils sont efficaces dans le type I mais pas dans le type II selon certains rapports. Comme la maladie peut régresser spontanément sans traitement, il n’existe pas de preuve claire de la supériorité des stéroïdes. En pratique clinique, la corticothérapie systémique n’est souvent envisagée que pour les cas graves.
Ntora et al. (2021) ont rapporté le cas d’une femme de 22 ans (hétérozygote pour FVL et MTHFR-C677T) traitée par méthylprednisolone orale à 50 mg/jour, avec réduction progressive. Une amélioration des signes a été observée en une semaine, et une régression complète en un mois. L’acuité visuelle et le champ visuel sont restés normaux après six mois2).
D’autres traitements, tels que l’antiagrégation plaquettaire et l’anticoagulation, ont été proposés mais leur efficacité n’est pas prouvée.
En cas d’œdème maculaire sévère, une injection intravitréenne d’anti-VEGF peut être envisagée (non approuvée par la FDA).
Insausti-García et al. (2022) ont traité un homme de 40 ans atteint de papillite veineuse après une infection au COVID-19 avec de l’aspirine 100 mg/jour par voie orale et du bromfénac 0,9 mg/mL en collyre (2 fois par jour) initialement. En raison d’une baisse de l’acuité visuelle (20/200) due à un œdème maculaire, un implant intravitréen de dexaméthasone à libération prolongée (Ozurdex) a été injecté, et l’acuité visuelle s’est améliorée à 20/40 après deux semaines1).
Il s’agit d’une maladie qui peut s’améliorer spontanément sans traitement, et le pronostic est généralement bon, avec une régression spontanée attendue en 6 à 12 mois. Cependant, jusqu’à 30 % des cas présentent un risque de progression vers une occlusion veineuse ischémique, un suivi ophtalmologique régulier est donc indispensable. Voir la section « Traitement standard » pour plus de détails.
La physiopathologie de la papillite veineuse n’est pas claire et le mécanisme de déclenchement n’est probablement pas unique.
L’hypothèse principale est qu’une inflammation idiopathique de la tête du nerf optique comprime la veine centrale de la rétine, entraînant une insuffisance veineuse secondaire et des hémorragies rétiniennes. Dans la classification de Hayreh, le type I implique une inflammation non spécifique des vaisseaux de la lame criblée antérieure, tandis que le type II implique une inflammation de la veine centrale de la rétine au niveau de la tête du nerf optique ou de la lame criblée postérieure.
Mécanismes liés au COVID-19 : la cascade suivante a été proposée 1).
Le schéma de la coagulopathie associée au COVID-19 (CAC) se caractérise par une augmentation du D-dimère et du fibrinogène parallèlement aux marqueurs inflammatoires1).
Implication des anomalies de la coagulation héréditaires a également été rapportée. La combinaison d’une hétérozygotie pour le FVL et d’une hétérozygotie pour le MTHFR-C677T pourrait entraîner un déséquilibre de la coagulation et contribuer au développement d’une papillite veineuse2). La mutation MTHFR-C677T, lorsqu’elle est homozygote, peut provoquer une hyperhomocystéinémie et favoriser un état d’hypercoagulabilité, mais une hétérozygotie seule peut ne pas entraîner d’hyperhomocystéinémie.
Le mécanisme n’est pas unique, mais on suppose que l’inflammation de la tête du nerf optique comprime la veine centrale de la rétine. Chez les jeunes, en l’absence de facteurs de risque d’OCVR comme l’hypertension et l’artériosclérose chez les personnes d’âge moyen, les anomalies de la coagulation (facteurs héréditaires) et l’inflammation post-infectieuse (comme la COVID-19) deviennent des déclencheurs relativement importants.
Insausti-García et al. (2022) ont rapporté le cas d’un homme de 40 ans ayant développé une papillophlébite 6 semaines après une infection par la COVID-191). Les examens ont montré une élévation des marqueurs de coagulation et d’inflammation : D-dimères 672 μg/L (normal <460), fibrinogène 451 mg/dL (normal 200-400), CRP 0,898 mg/dL (normal <0,500). Toutes les thrombophilies héréditaires étaient normales. Deux semaines après l’injection d’un implant intravitréen de dexaméthasone (Ozurdex), l’acuité visuelle est passée de 20/200 à 20/40. L’amélioration rapide sous dexaméthasone pourrait soutenir l’hypothèse inflammatoire.
Ntora et al. (2021) ont rapporté le premier cas mondial de papillophlébite chez une femme de 22 ans associée à une combinaison d’hétérozygotie pour le FVL et la mutation MTHFR-C677T2). Une rémission complète a été obtenue avec de la méthylprednisolone orale seule. Le dépistage génétique s’est révélé être un élément important dans le diagnostic de la papillophlébite. Une consultation en hématologie est considérée comme essentielle pour prévenir les complications futures.
Insausti-García A, Reche-Sainz JA, Ruiz-Arranz C, et al. Papillophlebitis in a COVID-19 patient: inflammation and hypercoagulable state. Eur J Ophthalmol. 2022;32(1):NP168-NP172.
Ntora E, Dalianis G, Terzidou C. Papillophlebitis associated with coexisting heterozygous mutations of Factor V Leiden and methylenetetrahydrofolate reductase enzyme (C677T). Cureus. 2021;13(5):e15081.
Abdel Jalil S, Amer R. The Spectrum of Papillophlebitis. Ocul Immunol Inflamm. 2024;32(10):2515-2520. PMID: 38842197.