感染性因素

Wessely免疫環
一目瞭然的要點
Section titled “一目瞭然的要點”1. 什麼是Wessely免疫環?
Section titled “1. 什麼是Wessely免疫環?”Wessely免疫環是角膜基質內對外來抗原的免疫反應形成的無菌性環狀浸潤。1911年,Wessely在暴露於牛或馬血清蛋白的兔角膜中記錄到可重複的免疫反應,首次報告為「Wessely現象」。
1956年,Morawiecki提出了免疫複合物介導的補體激活的作用。後來發現,其他抗原如細菌內毒素也可觸發抗體非依賴的備解素介導的補體替代途徑激活。
它可在感染性角膜炎病程中出現,或作為非感染性角膜反應發生。
2. 主要症狀和臨床所見
Section titled “2. 主要症狀和臨床所見”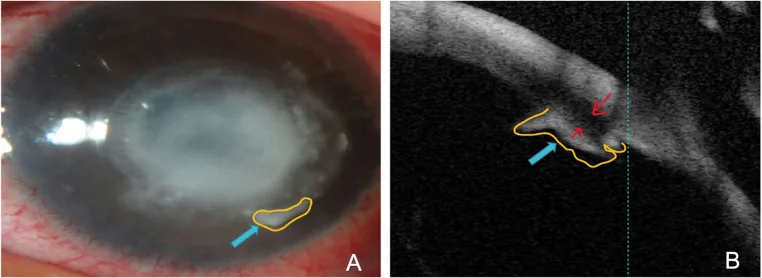
Wessely免疫環的自覺症狀與基礎疾病相關。免疫環本身通常不會對視力產生重大影響。
臨床所見(醫師檢查確認的所見)
Section titled “臨床所見(醫師檢查確認的所見)”典型的Wessely免疫環是在角膜緣附近形成的角膜基質內環狀浸潤。在遠離感染中心病灶、隔有透明部分的位置形成可見的環。
免疫環的出現時間因補體活化途徑而異。
| 活化途徑 | 出現時間 | 代表性病因 |
|---|---|---|
| 經典路徑 | 10~14天後 | 常見感染性角膜炎 |
| 替代路徑 | 1~5天內 | 綠膿桿菌、已致敏抗原 |
| 遲發型 | 進一步延遲 | 棘阿米巴、微孢子蟲 |
- 疱疹免疫性基質角膜炎:表現為基質中層的深層混濁環。通常位於中心或旁中心,有時可見圍繞盤狀角膜內皮炎區域。
- 棘阿米巴角膜炎:約15%的患者出現角膜基質環狀浸潤1)。環狀浸潤被定義為「重症炎症性併發症(SIC)」之一1)。
- 與假性老年環的相似性:卡他性角膜潰瘍可見與角膜緣平行的浸潤,浸潤病灶與角膜緣之間有1~2 mm的透明帶。由III型過敏反應(補體活化+嗜中性球浸潤)引起的無菌性浸潤,表現出與Wessely免疫環相似的病理狀態。
3. 原因與風險因素
Section titled “3. 原因與風險因素”非感染性因素
棘阿米巴角膜炎的危險因子
Section titled “棘阿米巴角膜炎的危險因子”在棘阿米巴角膜炎中,環狀浸潤和鞏膜炎被定義為「嚴重發炎併發症(SIC)」1)。已確定以下SIC的獨立危險因子1)。
- 年齡>34歲:OR 2.36(95% CI 1.21–4.57)1)
- 抗阿米巴治療(AAT)前使用類固醇:OR 2.56(95% CI 1.28–5.10)1)
- HSV角膜炎治療史:與SIC獨立相關1)
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”Wessely免疫環透過裂隙燈顯微鏡的臨床所見進行診斷。當觀察到角膜基質內的環狀浸潤時,與感染性環狀浸潤的鑑別最為重要。
環狀浸潤(ring infiltrate)在真菌性角膜炎和棘阿米巴角膜炎中也常見2),HSV、水痘-帶狀皰疹病毒、EB病毒也可引起免疫介導的角膜浸潤,可能類似於細菌性、真菌性或棘阿米巴角膜炎2)。
提示感染性浸潤的所見
Section titled “提示感染性浸潤的所見”提示感染性環狀浸潤(活微生物侵入角膜組織)的體徵如下:
另一方面,位於潰瘍邊界外側、對類固醇眼藥水有反應的輕度浸潤,提示為「純」Wessely免疫環區域。
5. 標準治療方法
Section titled “5. 標準治療方法”伴隨感染性角膜炎時
Section titled “伴隨感染性角膜炎時”優先根據病原微生物進行抗微生物治療。感染得到控制後,免疫環會消退。
無菌性免疫環
Section titled “無菌性免疫環”通常無需特殊治療。臨床上有時會使用類固醇眼藥水。如果是「真正無菌性」浸潤,通常迅速完全癒合。
卡他性角膜潰瘍(類似病變)
Section titled “卡他性角膜潰瘍(類似病變)”這是由葡萄球菌抗原引起的III型過敏反應(補體活化+嗜中性球浸潤)導致角膜周邊出現的無菌性浸潤,與Wessely免疫環表現相似。聯合使用抗生素和低濃度類固醇眼藥水有效,長期管理需注意眼瞼緣清潔和抗生素眼藥膏塗抹。
6. 病理生理學·詳細發病機制
Section titled “6. 病理生理學·詳細發病機制”免疫複合物與補體活化
Section titled “免疫複合物與補體活化”Wessely免疫環病理的核心是外來抗原與從角膜輪部血管系統擴散到基質內的抗體之間的相互作用。
- 外源性抗原(微生物抗原、內毒素等)存在於角膜基質中。
- 從角膜緣血管擴散的IgG抗體與抗原結合,形成免疫複合物。
- 免疫複合物激活補體系統。
- 產生趨化因子(C3a、C5a),將多形核白血球(主要是嗜中性球)募集到基質內。
- 嗜中性球的積聚在角膜緣周圍形成環狀浸潤。
補體激活的兩條途徑
Section titled “補體激活的兩條途徑”- 經典途徑:抗原-抗體複合物與C1q結合並激活。感染發病後10~14天出現免疫環。
- 替代途徑(備解素途徑):內毒素等不依賴抗體直接激活C3。在綠膿桿菌角膜炎或已致敏抗原的情況下,免疫環在1~5天內早期出現。
兩條途徑的參與可以解釋從症狀出現到免疫環出現的時間差異。
環狀形成的機制
Section titled “環狀形成的機制”免疫環在角膜緣周圍形成環狀的原因是,抗體從角膜緣血管向角膜中央擴散,與角膜基質中的抗原以等量比結合的部位(等價帶)出現在距角膜緣一定距離的位置。該反應與Arthus反應(局部III型過敏反應)機制類似。
抗體從角膜緣血管向角膜中央呈放射狀擴散。而抗原從角膜中央的感染灶或外來物質向周邊擴散。兩者以最佳比例(等價帶)結合的部位成為距角膜緣一定距離的環狀區域,免疫複合物在此集中沉積。補體激活和嗜中性球募集也集中於此,因此形成環狀浸潤。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”棘阿米巴角膜炎中環狀浸潤的預後意義
Section titled “棘阿米巴角膜炎中環狀浸潤的預後意義”Moorfields眼科醫院1991年至2012年棘阿米巴角膜炎隊列(培養或病理確診病例)的回顧性分析中,環狀浸潤和鞏膜炎被定義為「嚴重炎症併發症(SIC)」1)。SIC的獨立危險因子為年齡>34歲(OR 2.36)和AAT前使用類固醇(OR 2.56)1)。
分層分析顯示,在無鞏膜炎的患者中,環狀浸潤是預後不良的強獨立因子(OR 5.57;95% CI 2.02–15.39;P=0.001)1)。相反,當存在鞏膜炎時,無論有無環狀浸潤,預後不良風險均較高,環狀浸潤的額外影響較小1)。這些結果表明鞏膜炎和環狀浸潤相關但可能具有不同的病理生理學1)。
準分子雷射後的免疫環形成
Section titled “準分子雷射後的免疫環形成”PRK和PTK後曾有Wessely免疫環的報導。以前認為這是由於雷射切除區邊緣變性DNA蛋白的釋放所致,但近年提出假說認為,物理應激後產生的哺乳動物熱休克蛋白(HSP)與既往感染來源的細菌HSP的循環抗體發生交叉反應。
帕里毒素誘導的角膜炎
Section titled “帕里毒素誘導的角膜炎”這是一種與處理產帕里毒素(PTX)珊瑚相關的罕見眼表疾病。PTX作用於Na-K ATP酶泵,可能導致角膜上皮脫落、Wessely免疫環形成和角膜周邊變薄。嚴重程度從輕度眼表損傷到角膜融解和穿孔不等。
8. 參考文獻
Section titled “8. 參考文獻”- Carnt N, Robaei D, Watson SL, et al. Demographic and clinical risk factors associated with Acanthamoeba keratitis in a large UK case series of 221 patients. Br J Ophthalmol. 2018;102(10):1431-1435.
- American Academy of Ophthalmology Cornea/External Disease Preferred Practice Pattern Panel. Bacterial Keratitis Preferred Practice Pattern. Ophthalmology. 2024;131(2):P1-P47.
