特应性白内障

特应性皮炎的眼部并发症(白内障、视网膜脱离风险)(Atopic-Dermatitis-and-Ocular-Complications)
1. 特应性皮炎的眼并发症是什么?
Section titled “1. 特应性皮炎的眼并发症是什么?”特应性皮炎(AD)相关的眼部疾病统称为“特应性眼病”。白内障、视网膜脱离和圆锥角膜是主要并发症,长期的眼搔抓和拍打行为是发病的主要机制。
AD是一种以免疫学机制为背景的慢性炎症性皮肤病,当眼睑和面部皮肤病变严重时,眼部并发症的风险尤其高。根据文部科学省调查(2004-2006年),中小学生平均患病率为5.5%,成人中也有约2-3%患病。
| 眼部并发症 | 发病率 | 主要发病机制 |
|---|---|---|
| 特应性白内障 | 约10-25%的AD患者 | 揉眼造成的物理刺激及嗜酸性粒细胞颗粒蛋白进入眼内 |
| 视网膜脱离 | 约0.5-8%的AD患者(报告范围不一) | 揉眼导致Zinn小带断裂及视网膜裂孔 |
| 圆锥角膜 | 约7-30%的AD患者存在角膜形态异常 | 揉眼导致角膜实质的机械变形和脆弱化 |
诊断AD的重要发现包括:①瘙痒,②皮疹(湿疹病变的分布和性质),③病程(慢性复发性),④特应性素质(家族史和合并过敏性疾病)四项。
关于有揉眼或拍打习惯的患者白内障发病率,梅奥诊所对101例病例的研究(Brunsting报告)报道约为10%6)。其特征是年轻人(10多岁至30多岁)视力快速下降,临床表现与年龄相关性白内障不同。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”
视网膜脱离
圆锥角膜
眼睑炎 / 过敏性结膜炎
裂隙灯显微镜检查可确认前囊下混浊的形态(星状、星芒状、龟裂状)。这种形态与类固醇性白内障(后囊下混浊)明显不同,而与外伤性白内障非常相似,这是诊断的关键。散瞳眼底检查需仔细评估周边部视网膜裂孔和脱离。
它发生于年轻人(10多岁至30多岁),晶状体前囊下呈现星状或星芒状的特征性混浊。揉眼或拍打眼睛的习惯造成的物理刺激与发病有关,在形态、发病年龄和发病机制上与年龄相关的后囊下混浊不同。
3. 原因与风险因素
Section titled “3. 原因与风险因素”揉眼 / 拍打行为(最大风险因素)
Section titled “揉眼 / 拍打行为(最大风险因素)”揉眼和拍打行为是特应性眼病的最大修饰因素。眼睑炎引起的瘙痒是诱因,长期对眼球的物理刺激通过以下途径引起眼部并发症:
- 对晶状体的直接钝性外力 → 前囊下混浊(与外伤性白内障机制相同)
- 血-眼屏障破坏 → 血清中嗜酸性粒细胞颗粒蛋白(ECP、MBP等)流入眼内 → 晶状体蛋白变性
- 对Zinn小带的反复机械负荷 → 微小断裂 → 晶状体半脱位 / 震颤
- 玻璃体基底部的牵引 → 视网膜裂孔 → 孔源性视网膜脱离
- 反复机械刺激角膜基质 → 角膜脆弱化 → 圆锥角膜
与外用类固醇的关系
Section titled “与外用类固醇的关系”外用类固醇在特应性白内障发病中的作用被认为是否定的。在类固醇临床引入之前(1950年代以前)已有特应性白内障的报道6),类固醇引入前后白内障发病率没有显著变化。但需注意,类固醇眼膏进入结膜囊时可能引起眼压升高。
与AD严重程度的相关性
Section titled “与AD严重程度的相关性”面部和眼睑的皮炎越严重,搔抓眼部的冲动越强,眼部并发症风险越高。血清TARC值、血清LDH值、外周血嗜酸性粒细胞计数和血清总IgE值是AD严重程度的指标,也可作为眼部并发症风险的间接指标。
基于人群的队列研究表明,与非AD者相比,AD患者患白内障、青光眼和视网膜脱离的风险显著更高12)。
2型免疫应答(IL-4、IL-13、IL-31)增强导致的嗜酸性粒细胞活化也发生在眼部局部。结膜中也会引发过敏性炎症,可能导致杯状细胞增殖、巨大乳头形成和角膜上皮损伤2)3)。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”| 检查 | 评估项目 | 注意事项 |
|---|---|---|
| 裂隙灯显微镜检查 | 确认前囊下混浊形态(星状、星芒状、龟裂状) | 与类固醇性白内障(后囊下混浊)的鉴别 |
| 散瞳眼底检查 | 确认视网膜裂孔、脱离及周边部变性 | 建议所有有眼搔抓史的AD患者每年至少进行一次 |
| OCT | 详细评估视网膜层结构及确认黄斑异常 | 对术前和术后随访有用 |
| 角膜地形图 | 筛查圆锥角膜和球形角膜 | 对有不规则散光的年轻AD患者进行 |
| Zinn小带评估 | 术前评估断裂和脆弱性 | 白内障手术前必需。UBM和前段OCT有用 |
| 血液检查 | 外周血嗜酸性粒细胞计数、血清总IgE、LDH、TARC水平 | 评估AD严重程度和疾病活动性 |
白内障的诊断
Section titled “白内障的诊断”诊断的核心是通过裂隙灯显微镜确认前囊下混浊的形态。特征性表现为“星形”、“星状”或“地裂样线状混浊”,可与表现为后囊下混浊的类固醇性白内障进行形态学鉴别。此类白内障多见于核相对较软的年轻患者,术前核硬度评估也很重要。晶状体活动性和Zinn小带状态需在术前通过超声生物显微镜(UBM)或眼前节OCT评估。
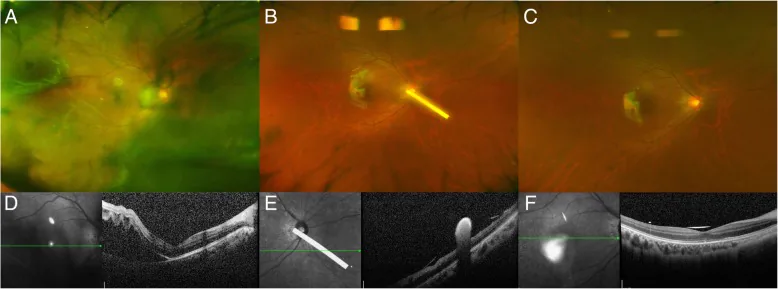
必须在散瞳下仔细检查眼底周边部。AD患者出现青少年型格子状变性和裂孔的频率高于非AD患者8)。出现急性飞蚊症或闪光感时需紧急进行眼底检查。
如果面部或眼睑有严重的皮炎,建议至少每年进行一次眼科检查。如果有揉眼或拍打眼睛的习惯,建议更频繁地检查。如果自觉视力下降、飞蚊症或闪光感,请及时就诊。
5. 标准治疗方法
Section titled “5. 标准治疗方法”| 并发症 | 严重程度 | 治疗方法 |
|---|---|---|
| 特应性白内障 | 视力下降 | 超声乳化吸除术(PEA)+ 人工晶状体植入。术前必须评估Zinn小带和视网膜。 |
| 视网膜脱离 | 仅裂孔 | 激光光凝(预防性治疗) |
| 视网膜脱离 | 有脱离 | 玻璃体手术 / 巩膜扣带术 |
| 圆锥角膜 | 轻度 | 硬性透气性角膜接触镜(RGP)光学矫正 |
| 圆锥角膜 | 进展期 | 角膜交联术(CXL)抑制进展 |
| 圆锥角膜 | 重症 | 角膜移植(穿透性或深板层角膜移植) |
| 眼睑炎/眼周AD | 轻度 | 涂抹保湿剂如Propet眼膏 |
| 眼睑炎/眼周AD | 中度至重度 | Predonin眼膏,每日2次,适量涂抹,根据症状适当增减 |
| 眼睑炎/眼周AD | 类固醇难治性病例 | 0.03%或0.1% Protopic软膏,每日1~2次涂抹 |
特应性白内障的手术
Section titled “特应性白内障的手术”进行超声乳化吸除术(PEA)并植入人工晶状体。手术方式基本与年龄相关性白内障相同,但需注意以下几点。
- Zinn小带断裂风险:术前评估怀疑断裂时,考虑使用囊袋张力环(CTR)。严重断裂病例考虑缝线固定型人工晶状体。
- 确认合并视网膜脱离或裂孔:术前散瞳眼底检查确认裂孔或变性,必要时术前进行激光光凝。
- 后发性白内障风险:年轻患者晶状体上皮细胞活性高,后发性白内障风险高。需准备术后YAG激光后囊切开术。
- 核的软度:年轻患者的晶状体核较软,超声乳化相对容易,但需注意囊袋处理。
眼周AD的药物治疗
Section titled “眼周AD的药物治疗”眼睑及眼周皮炎是直接导致眼搔抓的原因,因此与皮肤科协作进行积极控制非常重要。
轻度情况:涂抹保湿剂如白凡士林眼膏。维持皮肤屏障功能是长期管理的基础。
中重度情况:使用类固醇眼膏。
- 处方示例:泼尼松龙眼膏,每日2次,适量涂抹,根据症状适当增减。
- 类固醇眼膏均属于弱效药物。注意:若进入结膜囊可能导致眼压升高。
类固醇眼膏无效时:与皮肤科医生协商后,使用0.03%或0.1%普特彼软膏(他克莫司水合物)。
- 处方示例:普特彼软膏,每日1~2次涂抹。
- 改善后不要突然停药,采用每周约2天每日1次涂抹的主动疗法可减少复发频率1)。
预防(最重要)
Section titled “预防(最重要)”控制眼搔抓和拍打行为是所有眼并发症预防的根本。眼科医生需要与皮肤科医生合作,积极治疗面部AD和眼睑炎。随着他克莫司软膏的普及,眼睑炎的控制得到改善,有望降低特应性白内障的发病率。
眼科类固醇软膏(如泼尼松龙眼膏)可用于眼周,但药效属于弱效。若进入结膜囊可能导致眼压升高,涂抹时注意不要进入眼球侧。长期使用建议定期检查眼压。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”眼揉搓和拍打引起的物理损伤级联反应
Section titled “眼揉搓和拍打引起的物理损伤级联反应”AD合并眼病的发生源于以眼揉搓和拍打行为为起点的物理刺激,通过多条途径损伤眼组织。
白内障的发病机制:
- 反复钝性外力作用于眼球 → 晶状体前囊下直接损伤(与外伤性白内障机制相同)
- 血-眼屏障破坏 → 嗜酸性粒细胞颗粒蛋白(ECP、MBP等)流入眼内 → 诱导晶状体蛋白α-晶状体蛋白聚集和变性
- 这些综合作用导致前囊下混浊形成。类似外伤性白内障的形态(星状、星芒状、龟裂状)反映了这一机制4)7)
视网膜脱离的发病机制:
- 反复外力作用于眼球 → Zinn小带微小断裂 → 晶状体半脱位和晃动
- 玻璃体基底部的牵拉 → 在格子状变性区或周边部形成视网膜裂孔
- 通过裂孔的视网膜下液积聚 → 进展为孔源性视网膜脱离8)
圆锥角膜的发病机制:
- 反复机械刺激作用于眼球 → 角膜基质胶原纤维微小损伤
- 基质金属蛋白酶(MMP)激活 → 胶原降解增强 → 角膜基质脆弱化
- 眼内压与外部压力的不平衡 → 角膜前凸和变薄(圆锥角膜)9)
在AD中,2型免疫反应增强(IL-4、IL-13、IL-31过度产生)会激活嗜酸性粒细胞,并在眼部局部释放炎症介质。结膜也会发生Th2型过敏性炎症,导致杯状细胞增殖、巨大乳头形成和角膜上皮损伤3)。
否定与外用类固醇的关系
Section titled “否定与外用类固醇的关系”以下证据支持外用类固醇不是特应性白内障的主要原因:①在20世纪50年代类固醇临床引入之前已有白内障合并的报道6);②类固醇引入前后白内障发病率没有显著变化。这表明特应性白内障本质上是由眼揉搓和拍打等物理刺激以及免疫学机制引起的。
他克莫司的意义
Section titled “他克莫司的意义”随着他克莫司软膏(普特彼)的出现,眼睑炎和眼周AD的控制有望比传统外用类固醇疗法更好。预期形成良性循环:控制眼睑炎→减轻瘙痒→减少揉眼→降低特应性白内障、视网膜脱离和圆锥角膜的发病率1)。关于他克莫司外用治疗特应性眼睑炎的有效性和安全性已有多个报告积累1)。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”生物制剂的普及与眼部并发症
Section titled “生物制剂的普及与眼部并发症”度普利尤单抗(抗IL-4受体α抗体)已被批准并广泛用于中重度AD的一线生物制剂。然而,据报道约10-30%的患者在使用期间出现结膜炎5)10),也有前葡萄膜炎合并的病例报告。度普利尤单抗引起结膜炎的确切机制仍在研究中,许多病理细节尚未阐明。建议在使用度普利尤单抗期间进行眼科监测。
结膜炎的管理包括使用人工泪液、低浓度类固醇滴眼液和环孢素滴眼液,但某些情况下可能需要停用度普利尤单抗5)。
JAK抑制剂与AD治疗
Section titled “JAK抑制剂与AD治疗”巴瑞替尼、乌帕替尼和阿布昔替尼等JAK抑制剂已在日本获批用于中重度AD。眼部并发症(特别是疱疹性眼部感染风险增加)仍在持续研究中。
角膜交联术(CXL)的进展
Section titled “角膜交联术(CXL)的进展”关于角膜交联术(CXL)对AD相关圆锥角膜进展的抑制效果,已有越来越多的报告显示其对患有AD的年轻患者有效11)。在眼揉行为得到控制改善后进行CXL被认为有助于提高长期疗效,但关于长期疗效的证据仍在积累中。
眼部并发症风险的流行病学量化
Section titled “眼部并发症风险的流行病学量化”基于人群的队列研究已从统计学上量化了AD与眼部并发症(白内障、青光眼、视网膜脱离)之间的关联12)。未来的挑战包括通过更大规模的前瞻性研究细化风险因素,并阐明连接AD严重程度、眼揉行为和眼部并发症发病的因果路径。
8. 参考文献
Section titled “8. 参考文献”- Takahashi Y, Ichinose A, Kakizaki H. Topical tacrolimus (FK506) for atopic blepharitis: risk factors for corneal complications. Ophthalmology. 2012;119(11):2200-2203.
- Garrity JA, Liesegang TJ. Ocular complications of atopic dermatitis. Can J Ophthalmol. 1984;19(1):21-24.
- Rich LF, Hanifin JM. Ocular complications of atopic dermatitis and other eczemas. Int Ophthalmol Clin. 1985;25(1):61-76.
- Taniguchi H, Ohki M, Isogai N, et al. Atopic cataract: a morphological study. Graefes Arch Clin Exp Ophthalmol. 1999;237(7):559-566.
- Akinlade B, Guttman-Yassky E, de Bruin-Weller M, et al. Conjunctivitis in dupilumab clinical trials. Br J Dermatol. 2019;181(3):459-473.
- Brunsting LA, Reed WB, Bair HL. Occurrence of cataracts and keratoconus with atopic dermatitis. AMA Arch Derm. 1955;72(3):237-241.
- Matsuo T, Saito H, Matsuo N. Cataract and aqueous flare levels in patients with atopic dermatitis. Am J Ophthalmol. 1997;124(1):36-42.
- Hida T, Tano Y, Okinami S, et al. Multicenter retrospective study of retinal detachment associated with atopic dermatitis. Jpn J Ophthalmol. 2000;44(4):407-418.
- Rabinowitz YS. Keratoconus. Surv Ophthalmol. 1998;42(4):297-319.
- Merdler I, Hassidim A, Sorber-Goldfield R, et al. Dupilumab-associated conjunctivitis in patients with atopic dermatitis. Ophthalmology. 2020;127(2):236-238.
- Wollenberg A, Barbarot S, Bieber T, et al. Consensus-based European guidelines for treatment of atopic eczema (atopic dermatitis) in adults and children. J Eur Acad Dermatol Venereol. 2018;32(6):850-878.
- Nguyen KD, Lee EE, Yue H, et al. Atopic dermatitis and risk of cataract, glaucoma, and retinal detachment: a population-based cohort study. Am J Ophthalmol. 2022;236:245-253.
