细胞毒性化疗

抗癌药和分子靶向药物的眼部副作用
1. 什么是抗癌药和分子靶向药的眼部副作用?
Section titled “1. 什么是抗癌药和分子靶向药的眼部副作用?”抗癌药和分子靶向药的眼部副作用是指用于癌症治疗和免疫疾病治疗的药物对眼组织引起不良事件的总称。
涉及的药物类别非常广泛。
- 细胞毒性化疗(5-FU、顺铂、紫杉烷类等):溢泪、角膜上皮病变、视神经病变等1)
- 激素治疗(他莫昔芬等):结晶样黄斑沉积物、CME、角膜涡状混浊
- 免疫调节药(氯喹、羟氯喹、干扰素):视网膜病变、眼底出血、棉絮状白斑
- 分子靶向药物(MEK抑制剂、EGFR抑制剂、BRAF抑制剂、ALK抑制剂等):每种药物有特有的眼部副作用2)
- 免疫检查点抑制剂(ICI)(纳武利尤单抗、帕博利珠单抗等):作为irAE的葡萄膜炎、VKH样综合征3)
- 抗体药物偶联物(ADC)(德曲妥珠单抗等):角膜损伤10)
随着癌症治疗的发展,生存期延长,长期治疗中眼部副作用管理的重要性日益增加1)。眼部副作用从轻微不适到不可逆的视力障碍范围广泛,适当的筛查和早期干预直接关系到视力预后。
2. 按药物类别的症状和临床所见
Section titled “2. 按药物类别的症状和临床所见”不同药物类别的眼部副作用不同。以下列出主要药物及其眼部症状。
激素疗法和免疫调节剂
他莫昔芬:黄斑周围结晶样沉积物、角膜涡状混浊、CME。发生率:海外3~6%,国内0.2%
羟氯喹/氯喹:牛眼黄斑病变(环形萎缩)、视力下降、夜盲、色觉异常。使用5年以上约0.5%
干扰素:眼底后极部小出血、棉絮状白斑。给药后2~3个月内出现。多数无症状、自然消退。
分子靶向药物
免疫检查点抑制剂(ICI)
芬戈莫德引起的黄斑水肿
Section titled “芬戈莫德引起的黄斑水肿”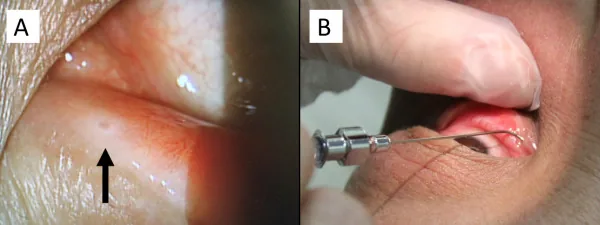
用于预防多发性硬化复发的芬戈莫德(伊姆塞拉/吉列尼亚)已知可引起黄斑水肿。黄斑水肿的发生率在芬戈莫德0.5 mg/天时为0.2%,1.25 mg/天时为1.4%,多数在开始治疗后3~4个月内出现。
3. 原因和风险因素
Section titled “3. 原因和风险因素”不同药物类别的眼部副作用风险因素不同。
| 药物类别 | 主要风险因素 |
|---|---|
| 羟氯喹/氯喹 | 用药时间超过5年、CQ >3.0 mg/kg/日或HCQ >6.5 mg/kg/日、高龄、肾/肝功能不全、合并视网膜疾病 |
| 他莫昔芬 | 高剂量和长期使用(累积剂量增加) |
| 干扰素 | 高初始剂量、高龄、糖尿病、高血压、贫血 |
| MEK抑制剂 | 剂量依赖性(高剂量时频率增加)2) |
| 免疫检查点抑制剂 | 合并全身irAE(如甲状腺炎、结肠炎)的患者更易发生眼部irAE 3) |
| 抗体药物偶联物 | 药物特异性角膜毒性机制 10) |
HCQ视网膜病变的具体危险因素包括以下内容。
- 用药时间:长期用药5年以上(累积剂量:CQ >460 g,HCQ >1,000 g)
- 每日剂量:CQ >3.0 mg/kg/日,HCQ >6.5 mg/kg/日
- 全身风险:高龄、肾功能下降(HCQ排泄延迟)、肝功能异常
- 眼部局部风险:合并已有的视网膜疾病或黄斑病变
干扰素视网膜病变在患有糖尿病、高血压、贫血等全身性疾病时更常见且更严重,也更容易发生在治疗抵抗或复发的病例中。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”HCQ筛查方案
Section titled “HCQ筛查方案”根据美国眼科学会(AAO)的建议9),进行以下筛查。
- 开始用药时(基线):视力、眼底和SD-OCT检查
- 用药5年后:如无高风险因素,开始每年一次筛查
- 有风险因素:不等5年,尽早开始筛查,并缩短间隔
- 推荐最大剂量:按实际体重不超过5 mg/kg/日9)
有用的检查包括Humphrey 10-2中心视野检查、SD-OCT、眼底自发荧光、多焦ERG和全视野ERG。牛眼状黄斑病变(轮状萎缩)是晚期HCQ视网膜病变的特征性眼底表现。
按药物的筛查建议
Section titled “按药物的筛查建议”| 药物 | 筛查时机与检查 |
|---|---|
| HCQ/氯喹 | 治疗开始时基线检查 + 5年后每年一次(SD-OCT、10-2视野、FAF)9) |
| 他莫昔芬 | 出现症状时及定期眼底检查、SD-OCT |
| 干扰素 | 开始治疗后2~3个月进行眼底检查。如有症状,立即就诊眼科 |
| MEK抑制剂 | 出现视力下降或视物变形时,通过OCT确认浆液性视网膜脱离2) |
| ICI | 出现视力下降、充血或眼痛时,立即就诊眼科3) |
| 芬戈莫德 | 治疗前基线眼底检查 + 治疗后3~4个月随访 |
使用ICI的患者出现视力下降、充血或眼痛时,应评估前房炎症细胞、玻璃体混浊和脉络膜病变,并考虑irAE引起的葡萄膜炎或VKH样综合征的可能性3)。
建议在开始用药时进行基线眼科检查,包括视力、眼底和SD-OCT。之后,如果没有危险因素(用药时间≥5年、高剂量、高龄、肾功能障碍等),从5年后开始每年筛查一次。如果有危险因素,则需要更早、更频繁的检查。主要检查项目包括SD-OCT、Humphrey 10-2视野检查和眼底自发荧光。
5. 标准治疗方法
Section titled “5. 标准治疗方法”羟氯喹/氯喹视网膜病变
Section titled “羟氯喹/氯喹视网膜病变”停药是唯一的治疗方法。由于药物从体内排出缓慢,停药后病变仍可能进展或恶化。因此,早期发现极为重要,在发生不可逆损伤之前决定停药对视力预后至关重要。
他莫昔芬眼部副作用
Section titled “他莫昔芬眼部副作用”干扰素视网膜病变
Section titled “干扰素视网膜病变”多数病例预后良好,无症状者基本等待IFN治疗结束。重症或视力下降者考虑减量或停用IFN。合并糖尿病或高血压者需早期处理。
MEK抑制剂引起的浆液性视网膜脱离
Section titled “MEK抑制剂引起的浆液性视网膜脱离”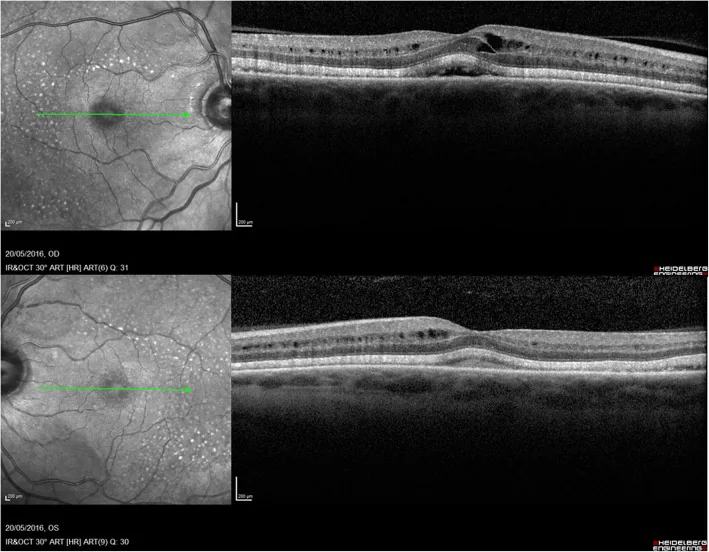
- 对于中度至重度浆液性视网膜脱离,应停药或减量2)
- 轻度病例可在观察下继续用药,多数可自然缓解2)
- 停药或减量后确认视网膜下液消退
EGFR抑制剂引起的眼部不良反应
Section titled “EGFR抑制剂引起的眼部不良反应”- 睫毛乱生(trichiasis):拔除变形的睫毛5)
- 眼睑炎:局部使用类固醇或抗生素软膏5)
- 角膜上皮损伤:使用不含防腐剂的人工泪液和角膜保护滴眼液
ICI相关葡萄膜炎
Section titled “ICI相关葡萄膜炎”根据CTCAE分级进行管理3)。
- 1级(轻度):使用类固醇滴眼液管理。可继续ICI治疗
- 2级(中度):全身使用类固醇(泼尼松龙)。考虑暂停ICI
- 3~4级(重度):大剂量全身类固醇。考虑暂停或永久停用ICI
- VKH样综合征:甲泼尼龙1克/日×3天冲击治疗,随后口服类固醇逐渐减量8)
芬戈莫德黄斑水肿
Section titled “芬戈莫德黄斑水肿”多数病例在停药后改善。必要时可联合使用NSAIDs滴眼液或类固醇滴眼液。
并非必须停药。根据眼部副作用的严重程度(CTCAE分级)和药物种类,处理方式不同。对于HCQ视网膜病变和他莫昔芬视网膜病变,停药是基本原则;而对于MEK抑制剂引起的轻度浆液性视网膜脱离或EGFR抑制剂引起的睫毛粗长,有时会选择对症治疗的同时继续用药。重要的是肿瘤内科主治医生与眼科医生协作,根据个体情况做出判断。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”不同药物类别对眼组织的损伤机制不同。
氯喹和HCQ的视网膜毒性
Section titled “氯喹和HCQ的视网膜毒性”CQ和HCQ对黑色素有高亲和力,与视网膜色素上皮(RPE)细胞的黑色素颗粒结合并在细胞内蓄积。蓄积的CQ/HCQ被溶酶体摄取,导致溶酶体pH升高,损害溶酶体酶活性。当RPE的酶代谢功能受损时,光感受器外节的降解和更新受阻,进而发展为光感受器变性。由于体内蓄积量大,停药后损伤仍可能进展。
他莫昔芬视网膜病变的机制
Section titled “他莫昔芬视网膜病变的机制”在神经纤维层和内丛状层形成球状病灶(神经纤维变性和轴索肿胀)。结晶样沉积物被认为是含有钙和复合糖类的变性产物沉积在神经纤维内。囊样黄斑水肿(CME)由Müller细胞功能障碍和液体潴留引起。
干扰素视网膜病变的机制
Section titled “干扰素视网膜病变的机制”IFN诱导血管痉挛、白细胞浸润和血管内皮损伤,免疫复合物沉积在毛细血管中,导致毛细血管闭塞。闭塞毛细血管的前方(动脉侧)出现棉絮斑(神经纤维层梗死),闭塞部位出血表现为小出血。多数为一过性,停药后消退。
MEK抑制剂引起的浆液性视网膜脱离
Section titled “MEK抑制剂引起的浆液性视网膜脱离”MEK抑制剂阻断MAPK/ERK通路(细胞增殖和生存信号)。由于RPE通过ERK信号维持主动转运(离子和水分),ERK抑制导致RPE的离子转运和泵功能受损。结果导致视网膜下液体积聚,表现为浆液性视网膜脱离和视网膜色素上皮脱离(PED)2)。
免疫检查点抑制剂(ICI)的眼部irAE
Section titled “免疫检查点抑制剂(ICI)的眼部irAE”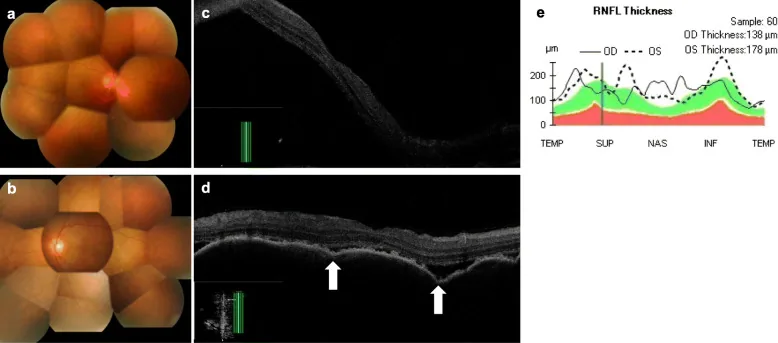
ICI(PD-1/PD-L1抑制剂、CTLA-4抑制剂)解除T细胞的免疫检查点,增强抗肿瘤免疫。然而,这一机制同时也解除了自身免疫抑制,引发眼组织(葡萄膜、巩膜、眼眶、泪腺)的自身免疫反应。在VKH样综合征中,针对黑色素细胞(脉络膜、睫状体、虹膜)的自身反应性T细胞被激活,导致全葡萄膜炎、浆液性视网膜脱离和脱色素病变3)。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”ICI相关眼部irAE的大规模注册研究
Section titled “ICI相关眼部irAE的大规模注册研究”为了全面了解ICI相关眼部irAE,国际多中心注册研究正在进行中3)。通过阐明葡萄膜炎、VKH样综合征、眼外肌炎等多种眼部irAE的谱系、频率和转归,有望实现风险分层和方案确立。
抗体药物偶联物(ADC)的角膜毒性
Section titled “抗体药物偶联物(ADC)的角膜毒性”以曲妥珠单抗德鲁替康(T-DXd)为代表的ADC作为下一代抗癌疗法正在普及,但角膜毒性(点状角膜病变、角膜基质混浊)已被确认为不良事件10)。通过药物警戒研究积累病例并建立角膜保护策略是当前的课题。
HCQ视网膜病变的超早期检测
Section titled “HCQ视网膜病变的超早期检测”自适应光学OCT和多光谱眼底成像正在尝试可视化传统方法无法检测的早期RPE结构变化11)。此外,利用人工智能(AI)分析OCT图像进行自动筛查的开发也在进行中,有望降低漏诊风险11)。
眼科与肿瘤内科协作方案的建立
Section titled “眼科与肿瘤内科协作方案的建立”随着ICI和分子靶向药物的普及,需要建立眼科与肿瘤内科之间的标准化协作方案8)。基于CTCAE分级的眼部副作用管理算法的指南化正在推进中。
8. 参考文献
Section titled “8. 参考文献”-
Omoti AE, Omoti CE. Ocular toxicity of systemic anticancer chemotherapy. Pharm Pract (Granada). 2006;4(2):55-59.
-
Francis JH, Habib LA, Abramson DH, et al. Clinical and morphologic characteristics of MEK inhibitor-associated retinopathy: differences from central serous chorioretinopathy. Ophthalmology. 2017;124(12):1788-1798.
-
Dalvin LA, Shields CL, Orloff M, et al. Checkpoint inhibitor immune therapy: systemic indications and ophthalmic side effects. Retina. 2018;38(6):1063-1078.
-
Joshi MM, Garretson BR. Paclitaxel maculopathy. Arch Ophthalmol. 2007;125(5):709-710.
-
Renouf DJ, Velazquez-Martin JP, Simpson R, et al. Ocular toxicity of targeted therapies. J Clin Oncol. 2012;30(26):3277-3286.
-
Choe CH, McArthur GA, Caro I, et al. Ocular toxicity in BRAF mutant cutaneous melanoma patients treated with vemurafenib. Am J Ophthalmol. 2014;158(4):831-837.
-
Camidge DR, Bang YJ, Kwak EL, et al. Activity and safety of crizotinib in patients with ALK-positive non-small-cell lung cancer: updated results from a phase 1 study. Lancet Oncol. 2012;13(10):1011-1019.
-
Sun MM, Levinson RD, Filipowicz A, et al. Uveitis in patients treated with CTLA-4 and PD-1 checkpoint blockade inhibition. Ocul Immunol Inflamm. 2020;28(7):1036-1040.
-
Marmor MF, Kellner U, Lai TY, et al. Recommendations on screening for chloroquine and hydroxychloroquine retinopathy (2016 revision). Ophthalmology. 2016;123(6):1386-1394.
-
Matsuoka H, Tanaka H, Nagai Y, et al. Corneal adverse events associated with trastuzumab deruxtecan: a pharmacovigilance study. Target Oncol. 2023;18(1):77-85.
-
Melles RB, Marmor MF. The risk of toxic retinopathy in patients on long-term hydroxychloroquine therapy. JAMA Ophthalmol. 2014;132(12):1453-1460.
