Hóa trị liệu diệt tế bào
5-FU: Chảy nước mắt (hẹp ống lệ), viêm kết mạc, rối loạn biểu mô giác mạc1)
Cisplatin: Bệnh thần kinh thị giác, rối loạn thị giác màu sắc (hiếm)1)
Taxan (docetaxel, paclitaxel): Chảy nước mắt, phù hoàng điểm dạng nang4)

Tác dụng phụ ở mắt do thuốc chống ung thư và thuốc nhắm trúng đích phân tử là thuật ngữ chung cho các tình trạng mà thuốc dùng trong điều trị ung thư và bệnh miễn dịch gây ra các tác dụng phụ trên mô mắt.
Các loại thuốc liên quan rất đa dạng.
Với sự phát triển của điều trị ung thư, thời gian sống thêm được kéo dài và việc quản lý các tác dụng phụ ở mắt trong quá trình điều trị dài hạn ngày càng trở nên quan trọng1). Các tác dụng phụ ở mắt dao động từ khó chịu nhẹ đến mất thị lực không hồi phục, và việc sàng lọc thích hợp cùng can thiệp sớm liên quan trực tiếp đến tiên lượng thị lực.
Nếu xuất hiện các triệu chứng như giảm thị lực, đỏ mắt, đau mắt, ruồi bay, chớp sáng, nhìn méo mó (vật thể bị biến dạng), hãy đến khám bác sĩ nhãn khoa ngay lập tức. Ngay cả khi triệu chứng nhẹ, việc bỏ qua có thể dẫn đến tổn thương không hồi phục, do đó cần báo cáo với bác sĩ điều trị (ung thư) và phối hợp với bác sĩ nhãn khoa.
Các tác dụng phụ ở mắt khác nhau tùy theo nhóm thuốc. Dưới đây là các thuốc chính và triệu chứng ở mắt của chúng.
Hóa trị liệu diệt tế bào
5-FU: Chảy nước mắt (hẹp ống lệ), viêm kết mạc, rối loạn biểu mô giác mạc1)
Cisplatin: Bệnh thần kinh thị giác, rối loạn thị giác màu sắc (hiếm)1)
Taxan (docetaxel, paclitaxel): Chảy nước mắt, phù hoàng điểm dạng nang4)
Liệu pháp hormone và thuốc điều hòa miễn dịch
Tamoxifen: Lắng đọng tinh thể quanh hoàng điểm, đục giác mạc hình xoắn ốc, phù hoàng điểm dạng nang. Tỷ lệ mắc: 3-6% ở nước ngoài, 0,2% trong nước
HCQ/chloroquine: Bệnh hoàng điểm hình mắt bò (teo vòng), giảm thị lực, quáng gà, bất thường thị giác màu sắc. Khoảng 0,5% sau 5 năm sử dụng
Interferon: Xuất huyết nhỏ và đốm trắng dạng bông ở cực sau đáy mắt. Xảy ra trong vòng 2-3 tháng sau khi dùng thuốc. Phần lớn không có triệu chứng và tự hồi phục.
Thuốc nhắm trúng đích phân tử
Thuốc ức chế MEK (ví dụ trametinib): Bong võng mạc dạng thanh dịch và bong biểu mô sắc tố. Tỷ lệ mắc khoảng 10-25%2)
Thuốc ức chế EGFR (ví dụ gefitinib): Lông mi mọc ngược, viêm bờ mi, tổn thương biểu mô giác mạc5)
Thuốc ức chế BRAF (ví dụ vemurafenib): Viêm màng bồ đào, bong võng mạc dạng thanh dịch6)
Thuốc ức chế ALK (ví dụ crizotinib): Ảo giác thị giác, nhìn mờ. Khoảng 60% bị rối loạn thị giác7)
Thuốc ức chế điểm kiểm soát miễn dịch (ICI)
Viêm màng bồ đào (trước, sau, toàn bộ): Tỷ lệ mắc khoảng 1%3)
Hội chứng giống VKH: Dạng nặng cần điều trị bằng steroid liều cao3)
Khô mắt, viêm kết mạc, bệnh viêm hốc mắt, viêm cơ ngoài nhãn cầu8)
ADC (ví dụ T-DXd): Tổn thương giác mạc (viêm giác mạc chấm nông, đục nhu mô giác mạc)10)
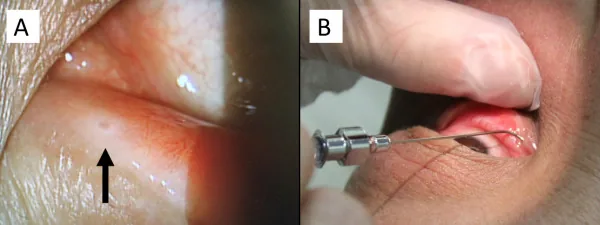
Fingolimod (Imusera/Gilenya) được sử dụng để ngăn ngừa tái phát bệnh đa xơ cứng được biết là gây phù hoàng điểm. Tỷ lệ phù hoàng điểm là 0,2% với fingolimod 0,5 mg/ngày và 1,4% với 1,25 mg/ngày, và hầu hết xảy ra trong vòng 3-4 tháng sau khi bắt đầu điều trị.
Các yếu tố nguy cơ của tác dụng phụ ở mắt khác nhau tùy theo nhóm thuốc.
| Nhóm thuốc | Yếu tố nguy cơ chính |
|---|---|
| HCQ/Chloroquine | Thời gian dùng >5 năm, CQ >3,0 mg/kg/ngày hoặc HCQ >6,5 mg/kg/ngày, tuổi cao, suy thận/gan, bệnh võng mạc kèm theo |
| Tamoxifen | Liều cao và sử dụng kéo dài (tăng liều tích lũy) |
| Interferon | Liều khởi đầu cao, tuổi cao, đái tháo đường, tăng huyết áp, thiếu máu |
| Thuốc ức chế MEK | Phụ thuộc liều (tần suất tăng ở liều cao) 2) |
| ICI | Bệnh nhân có irAE toàn thân (ví dụ viêm tuyến giáp, viêm đại tràng) dễ bị irAE ở mắt hơn 3) |
| ADC | Cơ chế độc tính giác mạc đặc hiệu thuốc 10) |
Các yếu tố nguy cơ cụ thể của bệnh võng mạc do HCQ bao gồm:
Bệnh võng mạc do interferon thường gặp và nặng hơn khi có các bệnh toàn thân như đái tháo đường, tăng huyết áp và thiếu máu, và cũng thường xảy ra ở các trường hợp kháng trị hoặc tái phát.
Dựa trên khuyến cáo của AAO (Học viện Nhãn khoa Hoa Kỳ)9), thực hiện tầm soát như sau:
Các xét nghiệm hữu ích bao gồm: thị trường trung tâm Humphrey 10-2, SD-OCT, tự huỳnh quang đáy mắt, điện võng mạc đa tiêu và điện võng mạc toàn trường. Hình ảnh mắt bò (teo vòng) là dấu hiệu đáy mắt đặc trưng của bệnh võng mạc do HCQ giai đoạn tiến triển.
| Thuốc | Thời điểm sàng lọc và xét nghiệm |
|---|---|
| HCQ/Chloroquine | Đo cơ bản khi bắt đầu dùng thuốc + hàng năm sau 5 năm (SD-OCT, thị trường 10-2, FAF) 9) |
| Tamoxifen | Khi xuất hiện triệu chứng và khám đáy mắt định kỳ cùng SD-OCT |
| Interferon | Khám đáy mắt sau 2-3 tháng kể từ khi bắt đầu dùng thuốc. Nếu có triệu chứng, hãy đến khám bác sĩ mắt ngay |
| Thuốc ức chế MEK | Khi xuất hiện giảm thị lực hoặc rối loạn thị giác, xác nhận bong võng mạc thanh dịch bằng OCT 2) |
| ICI | Khi xuất hiện giảm thị lực, đỏ mắt hoặc đau mắt, hãy đến khám bác sĩ mắt ngay 3) |
| Fingolimod | Khám đáy mắt cơ bản trước khi dùng thuốc + theo dõi sau 3-4 tháng dùng thuốc |
Ở bệnh nhân sử dụng ICI bị giảm thị lực, đỏ mắt hoặc đau mắt, cần đánh giá tế bào viêm tiền phòng, đục dịch kính và tổn thương hắc mạc, đồng thời xem xét khả năng viêm màng bồ đào hoặc hội chứng giống VKH như irAE 3).
Khuyến cáo thực hiện khám mắt bao gồm thị lực, đáy mắt và SD-OCT làm cơ sở ban đầu khi bắt đầu điều trị. Sau đó, nếu không có yếu tố nguy cơ (thời gian dùng thuốc >5 năm, liều cao, tuổi cao, suy thận, v.v.), bắt đầu tầm soát hàng năm từ năm thứ 5. Nếu có yếu tố nguy cơ, cần khám sớm hơn và thường xuyên hơn. Các xét nghiệm chính bao gồm SD-OCT, thị trường Humphrey 10-2 và tự huỳnh quang đáy mắt.
Phương pháp điều trị duy nhất là ngừng thuốc. Do thuốc đào thải chậm khỏi cơ thể, tổn thương có thể tiến triển và xấu đi ngay cả sau khi ngừng thuốc. Vì vậy, phát hiện sớm là cực kỳ quan trọng, và quyết định ngừng thuốc trước khi tổn thương không hồi phục quyết định tiên lượng thị lực.
Hầu hết các trường hợp có tiên lượng tốt, và nếu không triệu chứng, về cơ bản chờ kết thúc liệu pháp IFN. Trường hợp nặng hoặc giảm thị lực, cân nhắc giảm liều hoặc ngừng IFN. Trường hợp có kèm đái tháo đường hoặc tăng huyết áp, cần can thiệp sớm.
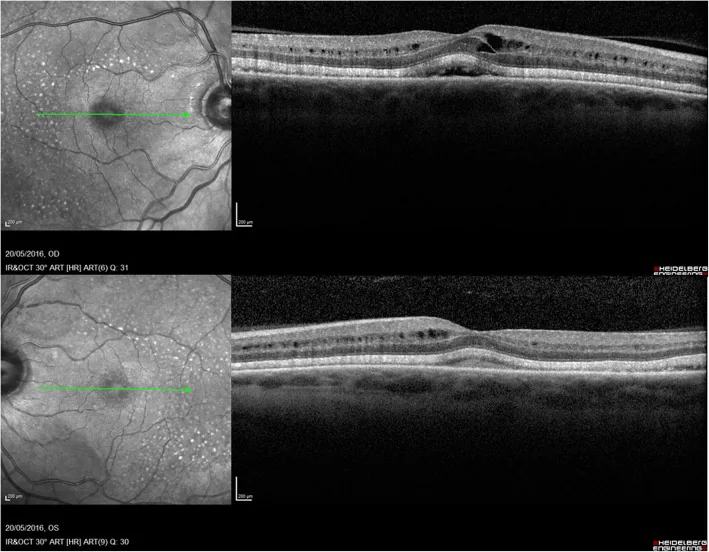
Quản lý dựa trên phân độ CTCAE 3).
Hầu hết các trường hợp đều cải thiện khi ngừng thuốc. Nếu cần, có thể kết hợp nhỏ mắt NSAID hoặc steroid.
Không nhất thiết phải ngừng. Cách xử trí khác nhau tùy theo mức độ nghiêm trọng của tác dụng phụ ở mắt (độ CTCAE) và loại thuốc. Trong một số trường hợp như bệnh võng mạc do HCQ hoặc tamoxifen, ngừng thuốc là cơ bản, trong khi ở các trường hợp khác như bong võng mạc thanh dịch nhẹ do thuốc ức chế MEK hoặc lông mi mọc lệch do thuốc ức chế EGFR, có thể tiếp tục điều trị kết hợp với điều trị triệu chứng. Điều quan trọng là bác sĩ ung thư nội khoa và bác sĩ nhãn khoa phối hợp để đưa ra quyết định phù hợp với từng tình huống.
Cơ chế tổn thương mô mắt khác nhau theo từng nhóm thuốc.
CQ và HCQ có ái lực cao với melanin, liên kết với các hạt melanin trong tế bào biểu mô sắc tố võng mạc (RPE) và tích tụ trong tế bào. Sự tích tụ CQ/HCQ làm tăng pH lysosome, gây rối loạn hoạt động của enzyme lysosome. Khi chức năng chuyển hóa enzyme của RPE bị tổn thương, quá trình phân hủy và tái tạo các đoạn ngoài của tế bào cảm thụ ánh sáng bị ảnh hưởng, dẫn đến thoái hóa tế bào cảm thụ. Do lượng tích tụ trong cơ thể lớn, tổn thương có thể tiến triển ngay cả sau khi ngừng thuốc.
Hình thành các tổn thương dạng cầu (thoái hóa sợi thần kinh và phình sợi trục) ở lớp sợi thần kinh và lớp đám rối trong. Các lắng đọng tinh thể được cho là sản phẩm thoái hóa chứa canxi và carbohydrate phức tạp lắng đọng trong các sợi thần kinh. Phù hoàng điểm dạng nang (CME) xảy ra do rối loạn chức năng tế bào Müller và ứ đọng dịch.
IFN gây co thắt mạch, thâm nhập bạch cầu và tổn thương nội mô mạch máu, dẫn đến lắng đọng phức hợp miễn dịch trong mao mạch gây tắc mao mạch. Phía trước mao mạch bị tắc (phía động mạch) xuất hiện các đốm trắng dạng bông (nhồi máu lớp sợi thần kinh), và chảy máu nhỏ được quan sát dưới dạng xuất huyết chấm. Hầu hết là tạm thời và biến mất sau khi ngừng IFN.
Thuốc ức chế MEK chặn con đường MAPK/ERK (tín hiệu tăng sinh và sống sót của tế bào). RPE duy trì vận chuyển tích cực (ion và nước) thông qua tín hiệu ERK, do đó ức chế ERK làm rối loạn chức năng vận chuyển ion và bơm của RPE. Kết quả là tích tụ dịch dưới võng mạc, biểu hiện dưới dạng bong võng mạc thanh dịch và bong biểu mô sắc tố võng mạc (PED)2).
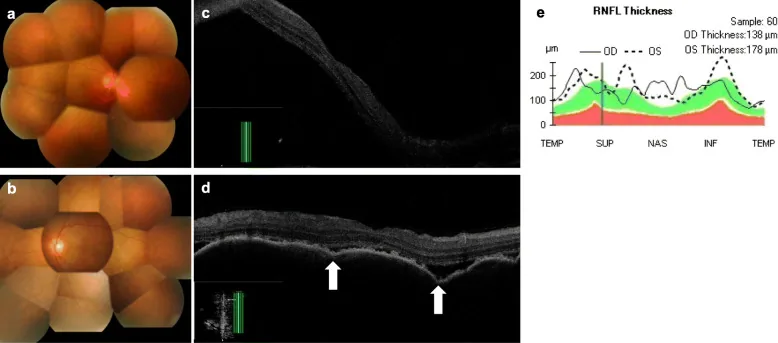
ICI (thuốc ức chế PD-1/PD-L1, thuốc ức chế CTLA-4) giải phóng các điểm kiểm soát miễn dịch của tế bào T và tăng cường miễn dịch chống khối u. Tuy nhiên, cơ chế này đồng thời giải phóng các cơ chế ức chế tự miễn, gây ra phản ứng tự miễn ở các mô mắt (màng bồ đào, củng mạc, hốc mắt, tuyến lệ). Trong hội chứng giống VKH, các tế bào T tự phản ứng với tế bào hắc tố (hắc mạc, thể mi, mống mắt) được kích hoạt, gây viêm màng bồ đào toàn bộ, bong võng mạc thanh dịch và tổn thương mất sắc tố 3).
Để hiểu bức tranh toàn cảnh về các tác dụng phụ ở mắt liên quan đến miễn dịch của ICI, các nghiên cứu đăng ký đa trung tâm quốc tế đang được tiến hành 3). Bằng cách làm rõ phổ, tần suất và kết quả của các tác dụng phụ ở mắt đa dạng như viêm màng bồ đào, hội chứng giống VKH và viêm cơ ngoài nhãn cầu, việc phân tầng nguy cơ và thiết lập quy trình được kỳ vọng.
Các ADC như trastuzumab deruxtecan (T-DXd) đang trở nên phổ biến như liệu pháp chống ung thư thế hệ tiếp theo, nhưng rối loạn giác mạc (viêm giác mạc biểu mô chấm nông, đục nhu mô giác mạc) được công nhận là tác dụng phụ 10). Việc tích lũy ca bệnh thông qua các nghiên cứu giám sát thuốc và thiết lập chiến lược bảo vệ giác mạc là thách thức.
Với OCT thích ứng và chụp ảnh đáy mắt đa phổ, các nỗ lực đang được thực hiện để hình dung các thay đổi cấu trúc RPE sớm mà không thể phát hiện bằng phương pháp thông thường 11). Ngoài ra, việc phát triển sàng lọc tự động sử dụng AI để phân tích hình ảnh OCT cũng đang tiến triển, hy vọng giảm nguy cơ bỏ sót 11).
Với sự phổ biến của ICI và thuốc nhắm mục tiêu phân tử, việc thiết lập quy trình hợp tác chuẩn hóa giữa nhãn khoa và ung thư nội khoa là cần thiết 8). Các hướng dẫn về thuật toán quản lý tác dụng phụ ở mắt dựa trên phân loại CTCAE đang được phát triển.
Omoti AE, Omoti CE. Ocular toxicity of systemic anticancer chemotherapy. Pharm Pract (Granada). 2006;4(2):55-59.
Francis JH, Habib LA, Abramson DH, et al. Clinical and morphologic characteristics of MEK inhibitor-associated retinopathy: differences from central serous chorioretinopathy. Ophthalmology. 2017;124(12):1788-1798.
Dalvin LA, Shields CL, Orloff M, et al. Checkpoint inhibitor immune therapy: systemic indications and ophthalmic side effects. Retina. 2018;38(6):1063-1078.
Joshi MM, Garretson BR. Paclitaxel maculopathy. Arch Ophthalmol. 2007;125(5):709-710.
Renouf DJ, Velazquez-Martin JP, Simpson R, et al. Ocular toxicity of targeted therapies. J Clin Oncol. 2012;30(26):3277-3286.
Choe CH, McArthur GA, Caro I, et al. Ocular toxicity in BRAF mutant cutaneous melanoma patients treated with vemurafenib. Am J Ophthalmol. 2014;158(4):831-837.
Camidge DR, Bang YJ, Kwak EL, et al. Activity and safety of crizotinib in patients with ALK-positive non-small-cell lung cancer: updated results from a phase 1 study. Lancet Oncol. 2012;13(10):1011-1019.
Sun MM, Levinson RD, Filipowicz A, et al. Uveitis in patients treated with CTLA-4 and PD-1 checkpoint blockade inhibition. Ocul Immunol Inflamm. 2020;28(7):1036-1040.
Marmor MF, Kellner U, Lai TY, et al. Recommendations on screening for chloroquine and hydroxychloroquine retinopathy (2016 revision). Ophthalmology. 2016;123(6):1386-1394.
Matsuoka H, Tanaka H, Nagai Y, et al. Corneal adverse events associated with trastuzumab deruxtecan: a pharmacovigilance study. Target Oncol. 2023;18(1):77-85.
Melles RB, Marmor MF. The risk of toxic retinopathy in patients on long-term hydroxychloroquine therapy. JAMA Ophthalmol. 2014;132(12):1453-1460.