شیمیدرمانی سیتوتوکسیک
5-FU: اشکریزش (تنگی مجرای اشکی)، ورم ملتحمه، آسیب اپیتلیوم قرنیه1)
سیسپلاتین: نوروپاتی بینایی، اختلال دید رنگی (نادر)1)
تاکسانها (دوکتاکسل، پاکلیتاکسل): اشکریزش، ادم ماکولار کیستیک4)

عوارض چشمی ناشی از داروهای ضد سرطان و داروهای هدفمند مولکولی، اصطلاحی کلی برای شرایطی است که در آن داروهای مورد استفاده در درمان سرطان و بیماریهای ایمنی باعث ایجاد عوارض جانبی در بافت چشم میشوند.
دستههای دارویی درگیر بسیار گسترده هستند.
با پیشرفت درمان سرطان، طول عمر بیماران افزایش یافته و اهمیت مدیریت عوارض چشمی در طول درمان طولانیمدت بیشتر شده است1). عوارض چشمی از ناراحتی خفیف تا اختلال بینایی غیرقابل برگشت متغیر است و غربالگری مناسب و مداخله زودهنگام مستقیماً بر پیشآگهی بینایی تأثیر میگذارد.
در صورت بروز علائمی مانند کاهش بینایی، قرمزی چشم، درد چشم، مگسپران، فوتوپسی (دیدن جرقههای نور)، یا متامورفوپسی (دیدن اشیاء به صورت کج و معوج)، سریعاً به چشمپزشک مراجعه کنید. حتی اگر علائم خفیف باشند، نادیده گرفتن آنها میتواند منجر به آسیب غیرقابل برگشت شود. بنابراین، به پزشک معالج (انکولوژیست) نیز اطلاع داده و همکاری با چشمپزشک ضروری است.
عوارض چشمی بسته به دسته دارویی متفاوت است. در زیر داروهای اصلی و علائم چشمی آنها آورده شده است.
شیمیدرمانی سیتوتوکسیک
5-FU: اشکریزش (تنگی مجرای اشکی)، ورم ملتحمه، آسیب اپیتلیوم قرنیه1)
سیسپلاتین: نوروپاتی بینایی، اختلال دید رنگی (نادر)1)
تاکسانها (دوکتاکسل، پاکلیتاکسل): اشکریزش، ادم ماکولار کیستیک4)
هورموندرمانی و داروهای تعدیلکننده ایمنی
تاموکسیفن: رسوبات کریستالین اطراف ماکولا، کدورت قرنیه به شکل گرداب، CME. میزان بروز: 3-6٪ در خارج از ژاپن، 0.2٪ در ژاپن
HCQ/کلروکین: ماکولوپاتی bull’s eye (آتروفی حلقوی)، کاهش بینایی، شبکوری، اختلال دید رنگی. حدود 0.5٪ پس از 5 سال مصرف
اینترفرون: خونریزیهای کوچک و لکههای پنبهای در قطب خلفی شبکیه. معمولاً ۲ تا ۳ ماه پس از مصرف رخ میدهد. اغلب بدون علامت و خودبهخود برطرف میشود.
داروهای هدفمند مولکولی
مهارکنندههای MEK (مانند ترامتینیب): جداشدگی سروزی شبکیه و PED. میزان بروز حدود ۱۰ تا ۲۵٪2)
مهارکنندههای EGFR (مانند گفیتینیب): رشد غیرطبیعی مژهها، بلفاریت و آسیب اپیتلیوم قرنیه5)
مهارکنندههای BRAF (مانند وموارفنیب): یووئیت و جداشدگی سروزی شبکیه6)
مهارکنندههای ALK (مانند کریزوتینیب): فتوپسی و تاری دید. حدود ۶۰٪ دچار اختلال بینایی میشوند7)
مهارکنندههای ایست بازرسی ایمنی (ICI)
یووئیت (قدامی، خلفی، پانیووئیت): میزان بروز حدود ۱٪3)
سندرم شبه VKH: شکل شدید که نیاز به استروئید با دوز بالا دارد3)
خشکی چشم، ورم ملتحمه، بیماری التهابی اربیت و میوزیت خارج چشمی8)
ADC (مانند T-DXd): آسیب قرنیه (کراتوپاتی نقطهای سطحی و کدورت استرومای قرنیه)10)
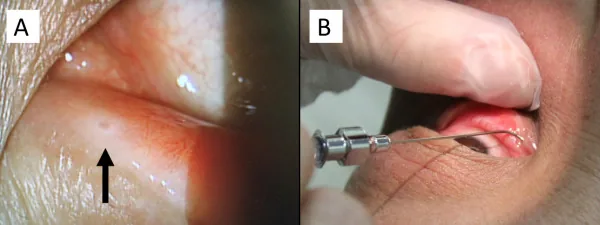
فینگولیمود (ایموسرا/گیلنیا) که برای پیشگیری از عود مولتیپل اسکلروزیس استفاده میشود، میتواند باعث ادم ماکولا شود. میزان بروز ادم ماکولا با دوز ۰.۵ میلیگرم در روز ۰.۲٪ و با دوز ۱.۲۵ میلیگرم در روز ۱.۴٪ است و بیشتر موارد در ۳ تا ۴ ماه اول پس از شروع درمان رخ میدهد.
عوامل خطر عوارض جانبی چشمی برای هر دسته دارویی متفاوت است.
| دسته دارویی | عوامل خطر اصلی |
|---|---|
| HCQ/کلروکین | مدت مصرف بیش از 5 سال، CQ >3.0 mg/kg/day یا HCQ >6.5 mg/kg/day، سن بالا، اختلال عملکرد کلیه/کبد، بیماری شبکیه همزمان |
| تاموکسیفن | دوز بالا و مصرف طولانی مدت (افزایش دوز تجمعی) |
| اینترفرون | دوز اولیه بالا، سن بالا، دیابت، فشار خون بالا، کم خونی |
| مهارکنندههای MEK | وابسته به دوز (با دوز بالا فراوانی افزایش مییابد) 2) |
| ICI | در بیماران با irAE سیستمیک (مانند تیروئیدیت، کولیت) irAE چشمی نیز شایعتر است 3) |
| ADC | مکانیسم سمیت قرنیه اختصاصی دارو 10) |
عوامل خطر خاص برای رتینوپاتی HCQ عبارتند از:
رتینوپاتی ناشی از اینترفرون در صورت وجود بیماریهای سیستمیک مانند دیابت، فشار خون بالا و کمخونی، با فراوانی بیشتر و شدت بیشتری بروز میکند و در موارد مقاوم به درمان یا عودکننده نیز شایعتر است.
بر اساس توصیه آکادمی چشمپزشکی آمریکا (AAO)9)، غربالگری زیر انجام میشود:
آزمایشهای مفید شامل Humphrey 10-2 میدان بینایی مرکزی، SD-OCT، خودفلورسانس فوندوس، ERG چندکانونی و ERG تمام میدان است. نمای bull’s eye (آتروفی حلقوی) یک یافته فوندوسکوپی مشخص در رتینوپاتی پیشرفته HCQ است.
| دارو | زمان غربالگری و آزمایش |
|---|---|
| HCQ/کلروکین | پایه در شروع درمان + سالانه از سال ۵ به بعد (SD-OCT، میدان بینایی 10-2، FAF) 9) |
| تاموکسیفن | در زمان بروز علائم و معاینه منظم فوندوس و SD-OCT |
| اینترفرون | معاینه فوندوس ۲ تا ۳ ماه پس از شروع درمان. در صورت وجود علائم، مراجعه فوری به چشمپزشک |
| مهارکنندههای MEK | در صورت کاهش بینایی یا دگرنمایی، تأیید جداشدگی سروزی شبکیه با OCT 2) |
| ICI | در صورت کاهش بینایی، قرمزی یا درد چشم، مراجعه فوری به چشمپزشک 3) |
| فینگولیمود | معاینه فوندوس پایه قبل از درمان + پیگیری ۳ تا ۴ ماه پس از درمان |
در بیماران مصرفکننده ICI که دچار کاهش بینایی، قرمزی یا درد چشم میشوند، باید سلولهای التهابی اتاق قدامی، کدورت زجاجیه و ضایعات مشیمیه ارزیابی شود و احتمال یووئیت یا سندرم شبه VKH به عنوان irAE در نظر گرفته شود 3).
توصیه میشود در شروع درمان، معاینه چشمی شامل اندازهگیری حدت بینایی، معاینه فوندوس و SD-OCT به عنوان پایه انجام شود. پس از آن، در صورت عدم وجود عوامل خطر (مدت درمان بیش از ۵ سال، دوز بالا، سن بالا، نارسایی کلیه و غیره)، غربالگری سالانه از سال پنجم به بعد آغاز میشود. در صورت وجود عوامل خطر، معاینات زودتر و مکررتر لازم است. SD-OCT، پریمتری Humphrey 10-2 و خودفلورسانس فوندوس از جمله معاینات اصلی هستند.
تنها درمان، قطع مصرف دارو است. از آنجایی که دفع دارو از بدن کند است، ممکن است ضایعات پس از قطع دارو نیز پیشرفت و بدتر شوند. بنابراین تشخیص زودهنگام بسیار مهم است و تصمیم به قطع دارو قبل از ایجاد آسیب غیرقابل برگشت، پیشآگهی بینایی را تعیین میکند.
پیشآگهی در بسیاری از موارد خوب است و در صورت بدون علامت بودن، اساساً منتظر پایان درمان IFN میمانیم. در موارد شدید یا کاهش بینایی، کاهش دوز یا قطع IFN بررسی میشود. در موارد همراه با دیابت یا فشار خون بالا، مداخله زودهنگام لازم است.
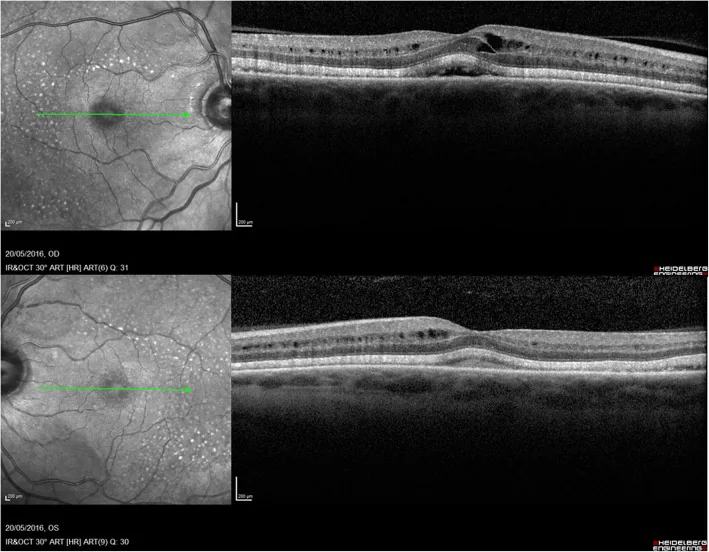
بر اساس درجه CTCAE مدیریت میشود 3).
در بسیاری از موارد با قطع مصرف بهبود مییابد. در صورت نیاز، قطرههای NSAIDs و استروئید نیز تجویز میشود.
قطع درمان همیشه ضروری نیست. اقدامات بر اساس شدت عارضه چشمی (گرید CTCAE) و نوع دارو متفاوت است. در مواردی مانند رتینوپاتی ناشی از HCQ یا تاموکسیفن، قطع دارو اساس درمان است، در حالی که در موارد جداشدگی خفیف سروزی شبکیه ناشی از مهارکنندههای MEK یا مژههای نابجا ناشی از مهارکنندههای EGFR، ممکن است درمان علامتی همراه با ادامه مصرف دارو انتخاب شود. همکاری بین انکولوژیست و چشمپزشک برای تصمیمگیری بر اساس شرایط فردی ضروری است.
مکانیسم آسیب به بافت چشم برای هر دسته دارویی متفاوت است.
کلروکین و هیدروکسی کلروکین میل ترکیبی بالایی با ملانین دارند و به گرانولهای ملانین در سلولهای اپیتلیوم رنگدانهای شبکیه (RPE) متصل شده و در داخل سلول تجمع مییابند. CQ/HCQ تجمعیافته وارد لیزوزومها شده و باعث افزایش pH لیزوزوم و اختلال در فعالیت آنزیمهای لیزوزومی میشود. اختلال در عملکرد متابولیک آنزیمهای RPE منجر به اختلال در تجزیه و بازسازی بخش خارجی گیرندههای نوری و در نهایت تخریب گیرندههای نوری میشود. به دلیل تجمع بالای دارو در بدن، آسیب ممکن است حتی پس از قطع مصرف نیز پیشرفت کند.
ضایعات کروی (دژنراسیون فیبرهای عصبی و تورم آکسون) در لایه فیبرهای عصبی و لایه پلکسیفرم داخلی تشکیل میشود. رسوبات کریستالوئید احتمالاً محصولات دژنراتیو حاوی کلسیم و گلیکوکونژوگهها هستند که در داخل فیبرهای عصبی رسوب میکنند. ادم ماکولای کیستیک (CME) ناشی از اختلال عملکرد سلولهای مولر و تجمع مایع است.
IFN باعث اسپاسم عروقی، نفوذ لکوسیتها و آسیب اندوتلیال عروق میشود و رسوب کمپلکسهای ایمنی در مویرگها منجر به انسداد مویرگی میگردد. در جلوی مویرگ مسدود شده (سمت شریانی)، لکههای پنبهای (انفارکتوس لایه فیبرهای عصبی) ایجاد میشود و خونریزی ناشی از انسداد به صورت خونریزیهای کوچک مشاهده میگردد. این تغییرات اغلب گذرا هستند و پس از قطع IFN برطرف میشوند.
مهارکنندههای MEK مسیر MAPK/ERK (سیگنال رشد و بقای سلولی) را مسدود میکنند. RPE برای انتقال فعال (یونها و آب) به سیگنال ERK وابسته است، بنابراین مهار ERK باعث اختلال در انتقال یون و عملکرد پمپ RPE میشود. در نتیجه، تجمع مایع زیر شبکیه رخ میدهد که به صورت جداشدگی سروزی شبکیه و جداشدگی اپیتلیوم رنگدانهای (PED) ظاهر میشود 2).
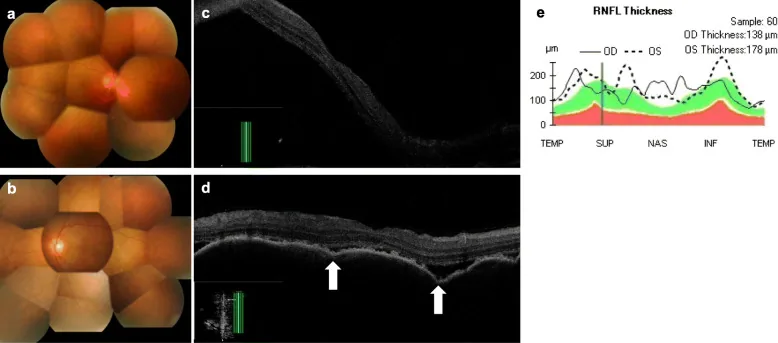
مهارکنندههای ایست بازرسی ایمنی (ICI) (مهارکنندههای PD-1/PD-L1 و CTLA-4) با برداشتن ایست بازرسی ایمنی سلولهای T، ایمنی ضد توموری را تقویت میکنند. با این حال، این مکانیسم همزمان مکانیسمهای سرکوب خودایمنی را نیز لغو کرده و واکنش خودایمنی علیه بافتهای چشمی (یووه آ، صلبیه، حدقه، غدد اشکی) را برمیانگیزد. در سندرم شبه VKH، سلولهای T خودواکنشی علیه ملانوسیتها (در مشیمیه، جسم مژگانی و عنبیه) فعال شده و باعث پانیووئیت، جداشدگی سروز شبکیه و ضایعات دپیگمانتاسیون میشوند 3).
برای درک تصویر کلی عوارض جانبی چشمی مرتبط با ICI، یک مطالعه رجیستری بینالمللی چندمرکزی در حال انجام است 3). با روشنسازی طیف، فراوانی و پیامدهای عوارض جانبی چشمی متنوع مانند یووئیت، سندرم شبه VKH و میوزیت خارج چشمی، انتظار میرود که طبقهبندی خطر و ایجاد پروتکلها امکانپذیر شود.
ADCها مانند تراستوزوماب دروکستکان (T-DXd) به عنوان درمانهای نسل بعدی سرطان در حال گسترش هستند، اما آسیب قرنیه (کراتوپاتی نقطهای سطحی، کدورت استرومای قرنیه) به عنوان یک عارضه جانبی شناخته شده است 10). جمعآوری موارد از طریق مطالعات نظارت دارویی و ایجاد استراتژیهای محافظت از قرنیه از چالشها است.
با استفاده از OCT تطبیقی (adaptive optics OCT) و عکسبرداری فوندوس چندطیفی، تلاش برای تجسم تغییرات اولیه ساختار RPE که با روشهای معمول قابل تشخیص نیستند، در حال انجام است 11). همچنین توسعه غربالگری خودکار با استفاده از تحلیل تصاویر OCT توسط هوش مصنوعی (AI) در حال پیشرفت است که انتظار میرود خطر نادیدهگرفته شدن موارد را کاهش دهد 11).
با گسترش استفاده از ICI و داروهای هدفمند مولکولی، نیاز به ایجاد پروتکلهای همکاری استاندارد بین چشمپزشکی و انکولوژی احساس میشود 8). تدوین دستورالعملهای الگوریتم مدیریت عوارض جانبی چشمی بر اساس درجهبندی CTCAE در حال پیشرفت است.
Omoti AE, Omoti CE. Ocular toxicity of systemic anticancer chemotherapy. Pharm Pract (Granada). 2006;4(2):55-59.
Francis JH, Habib LA, Abramson DH, et al. Clinical and morphologic characteristics of MEK inhibitor-associated retinopathy: differences from central serous chorioretinopathy. Ophthalmology. 2017;124(12):1788-1798.
Dalvin LA, Shields CL, Orloff M, et al. Checkpoint inhibitor immune therapy: systemic indications and ophthalmic side effects. Retina. 2018;38(6):1063-1078.
Joshi MM, Garretson BR. Paclitaxel maculopathy. Arch Ophthalmol. 2007;125(5):709-710.
Renouf DJ, Velazquez-Martin JP, Simpson R, et al. Ocular toxicity of targeted therapies. J Clin Oncol. 2012;30(26):3277-3286.
Choe CH, McArthur GA, Caro I, et al. Ocular toxicity in BRAF mutant cutaneous melanoma patients treated with vemurafenib. Am J Ophthalmol. 2014;158(4):831-837.
Camidge DR, Bang YJ, Kwak EL, et al. Activity and safety of crizotinib in patients with ALK-positive non-small-cell lung cancer: updated results from a phase 1 study. Lancet Oncol. 2012;13(10):1011-1019.
Sun MM, Levinson RD, Filipowicz A, et al. Uveitis in patients treated with CTLA-4 and PD-1 checkpoint blockade inhibition. Ocul Immunol Inflamm. 2020;28(7):1036-1040.
Marmor MF, Kellner U, Lai TY, et al. Recommendations on screening for chloroquine and hydroxychloroquine retinopathy (2016 revision). Ophthalmology. 2016;123(6):1386-1394.
Matsuoka H, Tanaka H, Nagai Y, et al. Corneal adverse events associated with trastuzumab deruxtecan: a pharmacovigilance study. Target Oncol. 2023;18(1):77-85.
Melles RB, Marmor MF. The risk of toxic retinopathy in patients on long-term hydroxychloroquine therapy. JAMA Ophthalmol. 2014;132(12):1453-1460.